维药降糖孜亚比提片定性定量方法研究
2017-02-14蒋子鸿康雨彤贺金华
严 欢 蒋子鸿 康雨彤 贺金华*
1.新疆维吾尔自治区药物研究所,新疆 乌鲁木齐 830004;2.新疆维吾尔药业有限责任公司,新疆 乌鲁木齐 830026
维药降糖孜亚比提片定性定量方法研究
严 欢1蒋子鸿2康雨彤1贺金华1*
1.新疆维吾尔自治区药物研究所,新疆 乌鲁木齐 830004;2.新疆维吾尔药业有限责任公司,新疆 乌鲁木齐 830026
目的:建立维药降糖孜亚比提片的定性定量方法。方法:采用薄层色谱法对鹿茸、人参和石榴皮进行薄层鉴别。采用高效液相色谱法对人参中特征成分人参皂苷Rg1、人参皂苷Re和人参皂苷Rb1进行含量测定。结果:薄层色谱中,定性鉴别斑点清晰,且阴性无干扰,方法稳定可靠。人参皂苷Rg1对照品在0.0151~0.4840 mg/mL范围内,线性关系良好(r=0.9996),平均回收率(n=6)为96.20%,RSD为1.58%;人参皂苷Re对照品在0.0584~0.9340 mg/mL范围内,线性关系良好(r=1),平均回收率(n=6)为102.14%,RSD为1.64%;人参皂苷Rb1对照品在0.0689~1.1020 mg/mL范围内,线性关系良好(r=1),平均回收率(n=6)为97.15%,RSD为1.36%。结论:采用该方法专属性好,灵敏度高,结果稳定可靠,可用于维药降糖孜亚比提片的质量控制。
降糖孜亚比提片;薄层色谱法;高效液相色谱法;人参;人参皂苷
降糖孜亚比提片由欧玉竹、鹿茸、人参、石榴皮、香茅等共10味药组成。方中香茅、石榴皮为水提取;鹿茸为70%醇提取后再用水提取;其余7味粉碎成细粉与上述2种浸膏粉及辅料混匀、压片。处方来源于《中华人民共和国卫生部药品标准——维吾尔药分册》(1999年版)[1],标准号:WS3-BW-0159-98,是按照维吾尔医理论组方的维药复方制剂,具有益肾健身,收敛固涩的作用,临床用于自然力摄住力下降引起的尿多、烦渴、疲乏、消瘦等糖尿病病症。为了保证制剂的质量,现对该方中的主要药味进行了薄层鉴别和含量测定研究。
人参为五加科植物人参PanaxginsengC.A.Mey.的干燥根和根茎。人参味甘、微苦,微温。归脾、肺、心、肾经。功效为大补元气、复脉固脱、补脾益肺、生津养血、安神益智。用于体虚欲脱、肢冷脉微、脾虚食少、肺虚喘咳、津伤口渴、内热消渴、气血亏虚、久病虚赢、惊悸失眠、阳痿宫冷的病症[2]。人参既为主药又为贵重药材,其主要活性成分是人参皂苷,故以人参对照药材及人参皂苷Rg1,Re,Rf和Rb1进行薄层鉴别,以人参皂苷Rg1、人参皂苷Re及人参皂苷Rb1对照品为指标,采用HPLC法测定制剂中三种人参皂苷的含量,以控制药品质量。鹿茸中含有多种化学成分,其中总氨基酸含量达50%以上,有甘氨酸、赖氨酸等10余种,本制剂中所用药材为马鹿茸,故本实验主要鉴别马鹿茸对照药材及甘氨酸。石榴皮中含鞣质10.4%~21.3%,没食子酸4.0%,故本实验主要鉴别石榴皮对照药材及没食子酸对照品[3-5]。
1 仪器与材料
1.1 仪器 AS20500BDT超声波清洗器(上海科导仪器设备有限公司);HHS21-NI4电热恒温水浴锅(北京长安科学仪器厂);Agilent 1260高效液相色谱仪(安捷伦公司);色谱柱:Cosmosil ODS C18(4.6mm×250mm,5μm)、Cosmosil ODS C18(pH1-7)(4.6mm×250mm,5μm)、Agilent TC C18(4.6mm×250mm,5μm);BP-211D电子天平(Sartorias公司)。
1.2 试药 降糖孜亚比提片(中试产品批号:20121101,20121102,20121103,和田维吾尔药业有限责任公司);全部药材购自新疆和田,经质检科鉴定,质量符合《中国药典》2010年版一部、《中华人民共和国卫生部药品标准--维吾尔药分册》1999年版和《维吾尔药材标准 上册》的有关规定,其中欧玉竹和西黄蓍胶无药材标准。
甘氨酸(批号:110735-200102)、人参皂苷Re(批号:110754-201123)、人参皂苷Rf(批号:111719-201104)、人参皂苷Rb1(批号:110704-200420)、人参皂苷Rg1(批号:0703-200119)、没食子酸(批号:110831-200302)均购于中国食品药品检定研究院;马鹿茸(批号:121570-021001)、人参(批号:120917-201110)、石榴皮(批号:121043-200403),均购于中国食品药品检定研究院。硅胶G薄层板(青岛海洋化工厂),聚酰胺薄膜(薄层层析,浙江省台州市路桥四甲生化塑料厂),乙腈为色谱级(Fisher公司),其余化学试剂均为分析纯。
2 方法与结果
2.1 定性鉴别
2.1.1 鹿茸 取本品8片,研细,加70%乙醇5mL,超声处理15min,滤过,取滤液作为供试品溶液。另取鹿茸对照药材0.4g,同法制成对照药材溶液。再取甘氨酸对照品,加70%乙醇制成每1mL含2mg的溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取供试品溶液和对照药材溶液各8μL、对照品溶液1μL,分别点于同一硅胶G薄层板上,以正丁醇-冰醋酸-水(3:1:1)为展开剂,展开、取出、晾干,喷以2%茚三酮丙酮溶液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的主斑点;在与对照品色谱相应的位置上,显相同颜色的斑点,且阴性无干扰。见图1。

2.1.2 人参 取本品20片,研细,加三氯甲烷100mL,加热回流1h,弃去三氯甲烷液,药渣挥干溶剂,加水5mL搅拌湿润,加水饱和正丁醇50mL,超声处理30min,吸取上清液加3倍量氨试液,摇匀,放置分层,取上层液蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。另取人参对照药材1g,同法制成对照药材溶液。再取人参皂苷Rb1对照品、人参皂苷Re对照品、人参皂苷Rf对照品及人参皂苷Rg1对照品,加甲醇制成每1mL各含2mg的混合溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各1~2μL,分别点于同一硅胶G薄层板上,以三氯甲烷-乙酸乙酯-甲醇-水(15:40:22:10)10℃以下放置的下层溶液为展开剂,展开、取出、晾干,喷以10%硫酸乙醇溶液,在105℃加热至斑点显色清晰,分别置日光和紫外光灯(365nm)下检视[6]。结果:供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的主斑点;在与对照品色谱相应的位置上,显相同颜色的斑点,且阴性无干扰,故列入正文。见图2。

2.1.3 石榴皮 取本品20片,研细,加无水乙醇30mL,加热回流1h,滤过,滤液蒸干,残渣加水20mL使溶解,滤过,滤液用石油醚(60℃~90℃)振摇提取2次,每次20 mL,弃去石油醚液,水液再用乙酸乙酯振摇提取2次,每次20mL,合并乙酸乙酯液,蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。另取石榴皮对照药材1g,同法制成对照药材溶液。再取没食子酸对照品,加甲醇制成每1mL含1mg的溶液,作为对照品溶液。照薄层色谱法(附录ⅥB)试验,吸取上述三种溶液各5μL,分别点于同一聚酰胺薄膜上,以乙酸乙酯-丁酮-甲酸-水(10:1:1:1)为展开剂,展开、取出、晾干,喷以1%三氯化铁乙醇溶液。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点;在与对照品色谱相应的位置上,显相同颜色的斑点,且阴性无干扰。见图3。

2.2 含量测定
2.2.1 对照品溶液的制备 精密称取人参皂苷Rg1对照品、人参皂苷Re对照品和人参皂苷Rb1对照品,加甲醇制成每1mL各含0.2mg的混合溶液,摇匀,即得。
2.2.2 供试品溶液的制备 取本品50片,研细,取约20g,精密称定,置具塞锥形瓶中,精密加入甲醇200mL,称定重量,超声(功率220 W,频率40 kHz)提取30min,放冷,再次称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液100 mL,蒸去甲醇,残渣加水40mL使溶解,用三氯甲烷提取2次,每次30mL,合并三氯甲烷液,三氯甲烷液用水30mL洗涤,弃去三氯甲烷液,水液与上述水液合并;用水饱和的正丁醇提取3次,每次30mL,合并正丁醇液,用氨试液洗涤3次,每次30mL,合并碱液层,再用水饱和的正丁醇30mL提取,与上述正丁醇液合并;用正丁醇饱和的水洗涤3次,每次30mL,正丁醇饱和的水的洗涤液依次用同一水饱和的正丁醇30mL提取,合并正丁醇液,蒸干,残渣以甲醇溶解并定容至5mL量瓶中,摇匀,滤过,取续滤液,即得[7-13]。
2.2.3 阴性样品溶液的制备 依照处方工艺,制备缺人参的阴性样品,并按照“2.2.2”项下供试品溶液的制备方法制备阴性样品溶液。
2.2.4 色谱条件 以十八烷基硅烷键合硅胶为填充剂;流动相:乙腈(A)-水(B),梯度洗脱(0~35 min,19%A;35~55 min,19%A→29%A;55~70 min,29%A;70~100 min,29%A→40%A;100~105 min,40%A→90%A;105~110 min,90%A→19%A;110~120 min,19%A);检测波长:203 nm;流速:1mL/min,柱温:30℃;进样量:10μL。结果见图4。
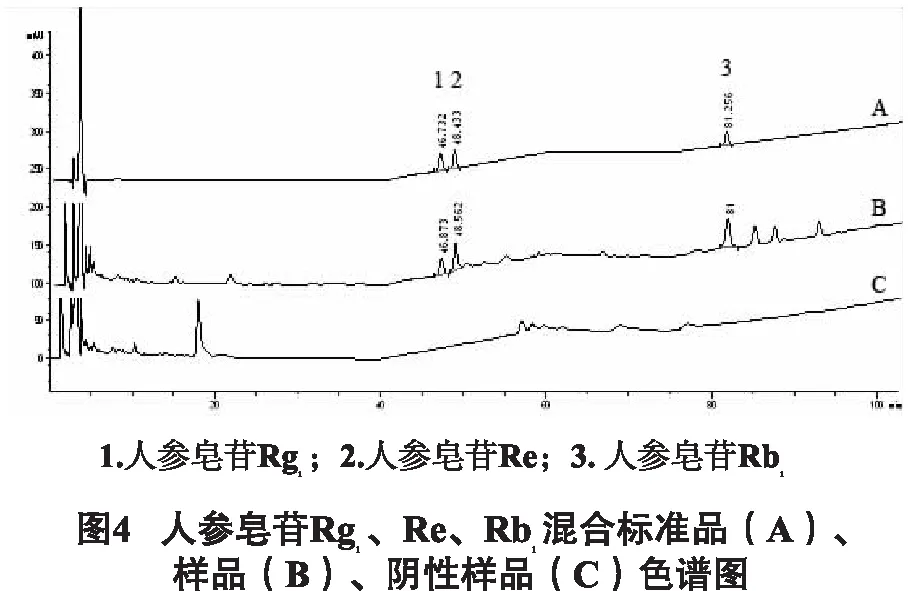
2.2.5 线性范围的考察 分别精密吸取人参皂苷Rg1对照品(0.6050mg/mL)溶液、人参皂苷Re对照品(0.9340mg/mL)溶液、人参皂苷Rb1对照品(1.1020mg/mL)溶液各0.1、0.3、0.5、1.0、2.0、5.0 mL至5 mL量瓶中,加流动相至刻度,摇匀。分别精密吸取上述溶液各10 μL注入液相色谱仪,以对照品浓度(X)为横坐标,峰面积(Y)为纵坐标进行线性回归,绘制标准曲线。结果人参皂苷Rg1、Re和Rb1线性关系均良好。见表1。

表1 线性关系结果(n=5)
2.2.6 仪器精密度 分别精密吸取对照品溶液10μL,重复进样6次,以测定人参皂苷Rg1、Re、Rb1的峰面积值,计算相对标准偏差。测定结果人参皂苷Rg1的面积平均值(n=6)为703.1,RSD=1.60%;人参皂苷Re的面积平均值(n=6)为573.2,RSD=1.11%;人参皂苷Rb1的面积平均值(n=6)为445.4,RSD=1.53%。RSD值均小于2%,表明仪器进样精密度良好。
2.2.7 供试品溶液稳定性 精密称取复方制剂粉末20g,依供制备试品溶液制备方法制备1份供试品溶液。分别在0、2、4、6、8、10、24、48、72、96、120h分别进样10μL,测定人参皂苷Rg1、Re、Rb1的峰面积,计算含量(平均片重0.4942g)。由测定结果可知人参皂苷Rg1的平均质量分数日内0.0183mg/片,日间0.0183mg/片,RSD值日内为0.77%,日间为0.84%,人参皂苷Re的平均质量分数日内0.0395mg/片,日间0.0391mg/片,RSD值日内为0.77%,日间为1.83%,人参皂苷Rb1的平均质量分数日内0.0722mg/片,日间0.0725mg/片,RSD值日内为1.03%,日间为1.40%。表明供试品溶液在制备120h内稳定。
2.2.8 重复性 取同一批次样品6份,按供试品溶液制备方法平行制备供试品溶液,分别进行测定。由测定结果可知人参皂苷Rg1+Re的平均质量分数为0.0578mg/片,RSD值为0.60%;人参皂苷Rb1的平均质量分数为0.0721mg/片,RSD值为1.04%。表明重复性良好。
2.2.9 准确度 称取已知含量的供试品10g,精密称定,共6份,分别精密加入人参皂苷Rg1对照品溶液(每1mL含人参皂苷Rg10.0605mg)、人参皂苷Re对照品溶液(每1mL含人参皂苷Re 0.1168mg)、人参皂苷Re对照品溶液(每1mL含人参皂苷Re 0.1168mg)5mL,依供试品溶液制备方法同法操作,分别进样10μL,记录峰面积,计算准确度,结果见表2。

表2 回收率实验结果 (n=6)
2.2.10 耐用性考察 取同一供试品溶液,分别采用三种不同品牌的色谱柱Cosmosil ODS C18(4.6mm×250mm,5μm)、Cosmosil ODS C18(pH1-7)(4.6mm×250mm,5μm)、Agilent TC C18(4.6mm×250mm,5μm)进样测定。结果见表3。

表3 耐用性考察结果(n=3)
由表3可知,三种品牌色谱柱对人参皂苷含量的影响不大,均能准确的对人参皂苷含量进行测定。通过对色谱系统适用性中色谱理论塔板数、分离度、拖尾因子的综合分析,最终决定选择色谱柱:Cosmosil ODS C18(250mm×4.6mm,5μm)。
2.2.11 样品测定 分别精密称取不同批次的复方制剂粉末20g,按照正文供试品溶液按制备方法处理,在上述色谱条件下分别进样10μL,注入高效液相色谱仪,计算降糖孜亚比提片中人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1的含量,所测样品中人参皂苷含量均符合要求。结果见表4。

表4 样品含量测定结果(mg/片,n=3)
3 讨论
3.1 薄层鉴别 鹿茸、人参和石榴皮薄层鉴别均参考中国药典2010年版一部各自项下的薄层鉴别方法,结果斑点均较清晰,且阴性样品无干扰。
3.2 人参的HPLC含量测定 供试品溶液的制备采用了药典方法(方法1)和改进后方法(方法2)。方法1:取本品内容物约20g,精密称定,加甲醇100mL,超声提取30min,过滤,提取液水浴蒸干,残渣加水适量溶解,至分液漏斗中,用水饱和的正丁醇萃取3次,每次50mL,合并正丁醇液,加氨试液振摇提取3次,每次50mL,弃去氨试液,正丁醇层继用正丁醇饱和的水洗涤2次,每次50mL,弃去水液,正丁醇层蒸干。残渣加甲醇5mL使溶解,作为供试品溶液。①方法2:取本品20片,研细,加三氯甲烷100mL,加热回流1h,弃去三氯甲烷液,药渣挥干溶剂,加水5mL搅拌湿润,加水饱和正丁醇50mL,超声处理15min,吸取上清液加3倍量氨试液,摇匀,放置分层,取上层液蒸干,残渣加甲醇1mL使溶解,作为供试品溶液。②结果显示:方法1杂质峰含量高,人参皂苷Rb1分离效果差;方法2色谱图杂质含量低,分离度较好,故采用方法2制备供试品溶液。
综上,该方法专属性好,灵敏度高,结果稳定可靠,可用于维药降糖孜亚比提片的质量控制。
[1]卫生部药典委员会.中华人民共和国卫生部药品标准(维吾尔药分册)[S].乌鲁木齐:新疆科技卫生出版社,1999.
[2]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010.
[3]新疆维吾尔自治区卫生厅.维吾尔药材标准[M].乌鲁木齐:新疆科技出版社,1999.
[4]刘勇民.维吾尔药志(上册)[M].乌鲁木齐:新疆科技卫生出版社,1999.
[5]中华本草编委会.中华本草(维吾尔药卷)[M].上海:上海科学技术出版社,2005.
[6]郑耀东.薄层色谱扫描法测定三七伤药胶囊中人参皂苷Rb1、Rg1的含量[J].江西中医学院学报, 2004,16 (3): 53-54.
[7]CAO Shuping,NIE Lixing,WANG Gangli,et al.Simultaneous determination of 9 ginsenosides in Shenmai injection by HPLC[J].Chin J Pharm Anal, 2011,31(3):476.
[8]郑友兰,杨春花,鲍建才,等.RP-HPLC测定西洋生晒参和西洋红参中人参皂苷含量[J].中国药学杂志,2006,(19):1494-1496.
[9]张旭,王丽娜,宋凤瑞,等.液质联用测定人参与五灵脂、莱菔子配伍的人参皂苷[J].分析化学,2007,(4):559-563.
[10]宿延丽,宿艳霞,宿武林.人参有效成分及其复方研究进展[J].人参研究,2008,(02):7-11.
[11]乔雪,李月茹.黑参中7种人参皂苷含量测定[J].人参研究,2012,(1):10-12.
[12]张斌,唐伟中复方降糖宁颗粒的质量标准的研究[J].江西科学,2006,24(2):153-154.
[13]熊学敏,石扬,康明,等.复方降糖宁颗粒剂的质量标准研究[J].江西中医学院学报, 2001,13 (l): 91-93.
(编辑:陶希睿)
Study on Qualitative and Quantitative Methods of Jiangtangziyabiti Tablets
YAN Huan1JIANG Zihong2KANG Yutong1HE Jinhua1*
1.Xinjiang Institute of Material Medica, Urmuqi 830004, China; 2.Xinjiang Uygur Pharmaceutical Co.,Ltd, Urmuqi 830026, China
Objective To establish the qualitative and quantitative methods of Jiangtangziyabiti tablets.Methods Cervi Cornu Pantotrichum, Ginseng Radix et Rhizoma and Granati Pericarpium were identified by TLC.To establish the HPLC methods to determine the content of three ginsenosides: Rg1, Re and Rb1in Jiangtangziyabiti tablets.Results Identification spots were clear, and this methods was stable and reliable.The ginsenoside Rg1control in 0.0151 ~ 0.4840 mg/mL range, good linear relationship,r=0.9996, average recovery=96.20%,RSD=1.58%; ginsenoside Re control in 0.0584 ~ 0.9340 mg/mL range, good linear relationship,r=1, the average recovery rate-102.41%,RSD=1.64%.ginsenoside Rb1control in 0.0689 ~ 1.1020 mg/mL range, good linear relationship,r=1, the average recovery rate=97.15%,RSD=1.36%.Conclusion This method is simple, reliable, stable and can control the quality of ginseng in compound preparation.
Jiangtangziyabiti Tablets; TLC; HPLC; Ginseng; Ginsenoside
2016-11-07
严欢(1981-),女,汉族,副研究员,硕士,研究方向为维吾尔药分析及质量标准研究。E-mail:19835500@qq.com
贺金华(1981-),女,汉族,研究员,硕士生导师,研究方向为维吾尔药分析及质量标准研究。E-mail:3482410@qq.com
R283
A
1007-8517(2017)02-0028-05
