以吞咽困难为首发症状的皮肌炎一例并文献回顾
2017-02-09章正祥王晓杭
黄 宜 章正祥 王 珏 王晓杭 陈 强 侯 群*
皮肌炎(DM)是一种主要累及皮肤和横纹肌的以慢性非化脓性炎症为特征的系统性自身免疫性疾病[1]。临床上多表现为肌无力、肌肉疼痛、肌萎缩等肌肉损害,和以眼睑为中心的水肿性紫红斑为特征性的皮肤损害[2]。其中以眼睑为中心的水肿性紫红色斑及肌无力是核心症状,但在临床中伴随吞咽功能障碍DM也越来越多见,约为15%~20%[3]。本文主要报道1例以吞咽困难为首发症状的DM并随访,系统回顾类似文献,对DM所致的吞咽困难临床特点进行概括。
1 检索方法
(1)万方数据库,以“皮肌炎、吞咽”为关键词,共检索到10篇文献,通过阅读标题及摘要剔除7篇,剩余3篇通过下载并阅读全文,剔除未描述医技结果的文献1篇,剩余2篇(共4个病例)。(2)CNKI数据库,以“皮肌炎、吞咽”为关键词,共检索到13篇文献,通过阅读标题及摘要剔除7篇,剩余6篇通过下载并阅读全文,剔除未描述医技结果的文献1篇,剩余5篇(共21个病例)。在2个数据库检索后,比较剔除重复者及无法获取全文者,剩余5篇(共9个病例)。
2 结果
2.1 病案 患者女性,73岁,患者无明显诱因下自感咽部有异物感,不易咳出,并出现吞咽困难,进食不畅,饮水有呛咳,伴左上肢明显水肿、疼痛,有高血压、糖尿病、脑梗死病史。于某县医院内分泌科住院治疗,肌酐131.5μmol/L,葡萄糖23.90mmol/L。诊断为“2型糖尿病”和“糖尿病肾病”。发病1周后来本院就诊。入院专科检查:神清,精神软,查体合作。皮肤巩膜无黄染,无皮疹及出血点,颜面眼睑无明显浮肿,双侧扁桃体无肿大,全身浅表淋巴结未及肿大,甲状腺未及肿大。左上肢重度非凹陷性水肿,双肺呼吸音清,未闻及明显干湿性罗音。腹平软,无压痛、反跳痛,肝脾肋下未及,肾区无叩击痛,双下肢无水肿,NS(-)。检验:肌酸激酶(CK酶)最高至1976U/L,肌酸激酶MB同工酶72.3U/L,乳酸脱氢酶(LDH)578U/L,血沉(ESR)36mm/h, 肿 瘤 类 :CA199 42.82U/ml、CA242 20.35IU/ml、CA50 31.85IU/ml,神经元特异性烯醇化酶 21.26ng/ml,ANA谱、ANCA谱未见明显异常。辅助检查:胸部CT提示两肺下叶斑片状炎性病灶可能。食管吞钡造影:食管吞钡后,见钡流通畅,无明显狭窄和梗阻,未见龛影和充盈缺损形成;食管黏膜无增粗、紊乱和破坏,管腔边缘光整。主支气管显影伴部分钡剂涂布。考虑会厌功能障碍(图1、2)。肌电图示:四肢部分周围神经病损(运动支);右肱二头肌、三角肌呈肌源性损害,左正中神经F波引出频率降低;右胫神经H反射未引出。胃镜示慢性萎缩性胃炎。胃镜病理诊断:“胃窦”轻度慢性萎缩性胃炎伴轻度肠化,HP(-)。喉镜示左侧声带肿物,咽部黏膜充血,左侧声带稍肿胀,前中1/3交界边缘白色新生物,右侧声带光,梨状窝大量分泌物,双声带活动可。入院10d后,患者前胸部、腹部、后背、颈部逐渐出现红色皮疹,伴瘙痒,最后双侧眼眶周围出现紫红色水肿。PET-CT(外院)示全身多处肌肉FDG代谢增高,诊断为DM。治疗上予甲强龙40mg抗炎,1次/d,1d后患者吞咽功能改善,出现右上肢无力伴感觉消失,头颅MRI+DWI显示左侧顶脑局部急性脑梗死。予抗炎5d后患者吞咽功能恢复正常,同时抗血小板、降脂、降压、抗自由基,胰岛素降糖等治疗2周后,双上肢肌力、水肿、皮损等症状明显好转,复查肌电图示肌肉传导未见明显异常,左侧胸锁乳突肌及舌肌未见明显肌电损害,患者于2015年11月16日出院。后期回访,患者出院后未规律服甲强龙,于2016年8月去世,具体死因不详。

图1 喉镜下见白色新生物
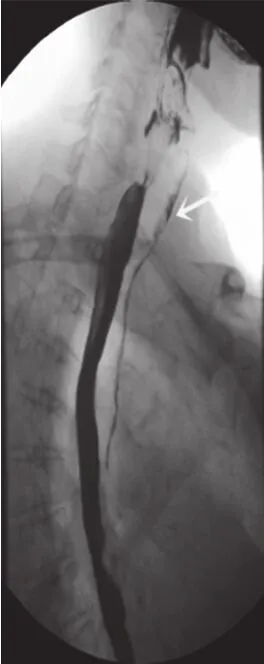
图2 主支气管显影伴部分钡剂涂布
2.2 以吞咽困难为首发症状的DM临床特点及文献回顾 纳入的10个DM病例,结合相关辅助检查结果,对其在皮肤表面、喉镜、肌电图及肌肉活检处的表现进行归纳总结。10个病例中患者均有不同程度皮肤损害表现,多分布于头面部及前胸,呈紫红色水肿性红斑改变,少数除了1篇未描述肌力外,其余9篇DM报道均有四肢肌力的下降,其中病例3、病例4、病例5及病例6均伴有肌肉压痛或酸痛感,此外,病例1中出现肌肉萎缩和腱反射减弱,病例3和10中肢体出现凹陷性水肿。除病例7肌电图未见明显异常、病例8未描述外,8例肌电图均显示有肌源性的损害。6个病例中患者均做了喉镜检查,梨状窝中均可见有粘液或食物残渣潴留,声带运动未受明显影响,但其中2例患者出现声带闭合不严等情况。3例行食管吞钡造影患者均有钡剂滞留现象,其中1例主气管钡剂显影。入选文献中,5例患者住院期间进行了肌肉活检,均有阳性表现,具体表现为肌肉组织中有淋巴细胞和浆细胞等浸润。在10个病例里有记载的血清酶谱中的肌酸激酶(CK)均有明显升高。
3 讨论
DM属于特发性炎症性肌病的一种,随着数十年对特发性炎性肌病的了解不断深入,临床诊断标准经历过多次修改。其中获得公认并流传至今的是1975年Bohan和Peter诊断标准[4](简称B/P标准),此标准简单、操作性强且敏感度高,但特异度不够,会将IBM和部分肌营养不良纳入;1995年,Tanimoto等[5]建议在DM的诊断中加入血清抗Jo-1抗体;2004年,欧洲神经肌肉病中心(ENMC)在制定特发性炎性肌病诊断标准时将DM的诊断更为细化,分为确诊DM、拟诊DM、无肌病性DM、无皮损的可疑DM共4种亚类[6]。但MSAs以及部分病理染色并未在全国广泛开展[7]。目前我国最新DM诊断标准为《2010年的多发性肌炎和皮肌炎诊断及治疗指南》。
DM除了眼睑为中心的水肿性紫红色斑及Gottron征外,临床中伴随吞咽功能障碍的DM也越来越多见。吞咽是一种复杂的神经肌肉反射性协同运动,正常吞咽的神经控制包括3个部分:(1)传入传出系统,包括脑神经的感觉传入和运动传出。(2)脑干吞咽中枢反射性协调吞咽。(3)皮质高级中枢,启动和调节自主吞咽[8]。吞咽困难是指食物通过咽部或食管时感到费力,有梗阻、障碍、咽不下的感觉[9]。目前电视透视检查是检测吞咽困难的金标准[10],根据吞咽困难发生的不同阶段,可将吞咽困难分为口腔期、咽期、食管期三期。
以吞咽困难为首发的患者入院后首先需排除食管、食管周围组织、喉返神经是否有疾患和结构的异常,因此,应进行喉镜或电视透视、钡餐等检查。其次通过肺部CT、胃镜检查喉返神经是否有压迫,尤其是食管癌,其他纵膈内肿瘤、以及肿瘤或炎症所致纵膈淋巴结肿大所致压迫。对于胸部CT、胃镜、钡餐检查未见明显异常的患者,应考虑神经系统疾病。当有关临床症状不能用神经系统病变圆满解释时,应考虑到肌源性病变。DM所致的吞咽困难在肌源性疾病中较为常见。
通过相关文献的系统回顾,作者发现DM的吞咽困难主要表现为梨状窝中均可见有粘液或食物残渣潴留,黏膜充血、声带闭合不全、声带上白色斑样或膜样改变、会厌功能障碍等情况,属于咽期吞咽困难。据Ro-drigues[11]研究,DM患者中喉部表现为室带对称性苍白病变的最终多因纵隔气肿呼吸衰竭而死亡,由此可以推测,DM患者喉部黏膜损伤的表现在一定程度上可以体现肺部病变的严重性。因此,DM患者出现吞咽困难、声嘶、喉部黏膜损伤应为患者预后不良的一项指标[12]。此外有研究表明[13],伴有吞咽困难的DM患者病情进展快,病情较重,本例患者诊断DM后10月去世。此外需注意的是,在一些有吞咽困难表现的DM确诊病例中,常合并硬皮病,故仍需排除患者的吞咽困难是否由硬皮病导致,临床上可通过是否出现皮肤硬化表现、雷诺现象、RNP抗体、抗着丝点抗体指标进行鉴别[14]。由于10%~50%DM患者常伴有恶性肿瘤,其中肺癌更为常见[15],故DM确诊后需排查肿瘤等相关指标,有条件可行PET CT排除肿瘤的可能。
因此,以吞咽困难为首发症状的患者入院后应该积极早期行喉镜检查,若咽喉部出现如梨状窝中见有粘液或食物残渣潴留、黏膜充血、声带闭合不全、声带上白色斑样或膜样改变等阳性表现,应该注意DM的筛查,且对于确诊DM患者行喉镜检查,可在一定程度上对预估患者的预后有重要意义。
[1] Ramos-E-Silva M,Pinto AP,Pirmez R,et al.Dermatomyositis-Part 1:Definition,Epidemiology,Etiology and Pathogenesis,and Clinics.Skinmed,2016,14(4):273.
[2] Findlay AR,Goyal NA,Mozaffar T.An overview of polymyositis and dermatomyositis.Muscle & nerve,2015,51(5):638-656.
[3] Espinoza-Cobos JC, Pérez-Figueroa J, Zúñiga-Ahuet G, et al.Oropharyngeal dysphagia as a first manifestation of dermatomyositis associated with colon cancer.Revista de gastroenterologia de Mexico, 2009,75(4):522-527.
[4] Bohan A,Peter JB.Polymyositis and dermatomyositis(second of two parts).N Engl J Med,1975,292:403-407.
[5] Tanimoto K,Nakano K,Kano S,et al.Classification criteria for polymyositis and dermatomyositis.J Rheumatol,1995,22:668-674.
[6] Hoogendijk JE, Amato AA, Lecky BR, et al. 119th ENMC International Workshop:trial design in adult idiopathic inflammatory myopathies, with the exception of inclusion body myositis. Neuromuscul Disord,2004,14(5):337-345.
[7] 张巍.特发性炎性肌病诊断发展历程.中国现代神经疾病杂志,2016,16(10):651-655.
[8] 张婧,王拥军.卒中后吞咽困难的发生机制.国外医学(脑血管疾病分册),2004,12(4):274-277.
[9] 高尚谦,王芳,郭海玲,等.基于指南的脑卒中患者吞咽困难识别与管理循证实践方案的构建.中国护理管理,2016,16(12): 1623-1627.
[10] 杜丽洁,刘婷婷,王娇,等.电视透视吞咽功能检查在吞咽障碍型颈椎病中的诊断价值.中国药物与临床,2015,15(10):1431-1433.
[11] Rodrigues AJ,Jacomelli M,Scordamaglio PR,et al.Spontaneous pneumomediastinum associated with laryngeal lesions and tracheal ulcer in dermatomyositis.Revista brasileira de reumatologia, 2012,52(5): 798-799.
[12] 王辉,史旭华,张文静,等.喉部病变对皮肌炎纵隔气肿患者预后影响的研究.临床耳鼻咽喉头颈外科杂志,2016,30(23):1870-1872.
[13] 陈其奎,黄志清,曾志勇,等.合并吞咽困难皮肌炎患者的临床和实验室特点.Arthritis Rheum,2003,4(9):2555-2566.
[14] 门月华,曹源,王琨,等.皮肌炎并发食管癌1例.临床皮肤科杂志,2016,45(1):45-46.
[15] Sunderkötter C, Nast A, Worm M, et al. Guidelines on dermatomyositis excerpt from the interdisciplinary S2k guidelines on myositis syndromes by the German Society of Neurology.JDDG: Journal der Deutschen Dermatologischen Gesellschaft,2016, 14(3):321-338.
