新型氮杂环卡宾银(I)配合物的合成及其晶体结构
2017-02-07李山山周明东
李山山, 孙 京, 吴 爽, 王 欣, 周明东
(辽宁石油化工大学 化学化工与环境学部,辽宁 抚顺 113001)
·研究论文·
新型氮杂环卡宾银(I)配合物的合成及其晶体结构
李山山, 孙 京, 吴 爽, 王 欣, 周明东*
(辽宁石油化工大学 化学化工与环境学部,辽宁 抚顺 113001)
以取代苄氯(1a~1c)为起始原料,与咪唑经氮烷基化反应制得苄基咪唑氯盐(2a~2c); 2a~2c与氧化银经原位去质子化反应合成了3种新型的氮杂环卡宾银配合物——(NHC)AgCl[NHC: 1,3-二(4-甲氧基苄基)咪唑-2-亚基(3a), 1,3-二(3-甲氧基苄基)咪唑-2-亚基(3b)]和[(NHC)AgCl]2[NHC=1,3-二(4-氯苄基)咪唑-2-亚基(3c)],其结构经1H NMR,13C NMR, IR,元素分析和X-射线单晶衍射表征。3a~3c单晶结构均属单斜晶系,3a为P21/n空间群,3b和3c为P21/c空间群,3a和3b为单核银配合物,3c为双核银配合物。
苄基咪唑氯盐; 氮杂环卡宾; 银配合物; 合成; 晶体结构
氮杂环卡宾(NHC)及其金属配合物是一类极具价值的催化剂。氮杂环卡宾金属配合物不仅在聚合[1]、氢甲酰化、氢转移[2]和环加成等反应中被广泛应用,而且在抗菌和抗癌[3]等生物医学领域、光学材料及电子材料[4]等方面展现了广阔的应用前景。1968年Öfele和Wanzlick等[5-6]首次报道了NHC金属配合物的结构和制备方法。1991年Arduengo[7]首次成功分离出稳定的自由卡宾,使卡宾化合物的研究得到迅猛发展[8-11]。NHC具有强的σ给电子能力[12-13]和配位能力、结构易于调变、易于合成等优点,对NHC及其金属配合物的结构与性质研究具有重要意义,其研究也取得了诸多成果[14-23]。
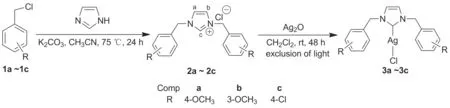
Scheme 1
本文以取代苄氯(1a~1c)为起始原料,与咪唑经氮烷基化反应制得苄基咪唑氯盐(2a~2c); 2a~2c分别与氧化银经原位去质子化反应合成了三种新型的氮杂环卡宾银配合物——(NHC)AgCl [NHC: 1,3-二(4-甲氧基苄基)咪唑-2-亚基(3a), 1,3-二(3-甲氧基苄基)咪唑-2-亚基(3b)]和[(NHC)AgCl]2[NHC=1,3-二(4-氯苄基)咪唑-2-亚基(3c)](Scheme 1),其结构经1H NMR,13C NMR, IR,元素分析和X-射线单晶衍射表征。并对其晶体结构进行了研究。
1 实验部分
1.1 仪器与试剂
AVANCE DPX-500型核磁共振仪(DMSO-d6为溶剂,TMS为内标);Spectrum GX型红外光谱仪(KBr压片);Perkin-Elemer PE 2400型元素分析仪;Bruker XRDR3M/ESYSTCM型X-射线单晶衍射仪。
4-甲氧基苄氯(1a), 3-甲氧基苄氯(1b)和4-氯苄氯(1c), 98%,安耐吉化学有限公司;其余所用试剂均为分析纯,其中二氯甲烷和乙腈经CaH2回流6 h后蒸出。
1.2 合成
(1) 2a~2c的合成(以2a为例)[24-25]
在无水无氧条件下,向100 mL Schlenk瓶中依次加入咪唑0.43 g(6.4 mmol), 1a 2.00 g(12.8 mmol)和无水乙腈25 mL,搅拌使其溶解,加入K2CO30.88 g(6.4 mmol),搅拌下于75 ℃反应24 h。过滤,滤液蒸干得白色固体2a。
用类似的方法合成白色固体2b和2c。
2a: 产率81%;1H NMRδ: 9.54(s, 1H, c-H), 7.83(d,J=1.5 Hz, 2H, a,b-H), 7.42(d,J=9.0 Hz, 4H, ArH), 6.98(d,J=9.0 Hz, 4H, ArH), 5.36(s, 4H, CH2), 3.76(s, 6H, OCH3);13C NMRδ: 160.05, 136.25, 130.66, 127.19, 123.05, 114.83, 55.69, 51.98。
2b: 产率76%;1H NMRδ: 9.64(s, 1H, c-H), 7.89(d,J=1.5 Hz, 2H, a,b-H), 7.34(t,J=8.0 Hz, 2H, ArH), 7.06(s, 2H, ArH), 7.00(d,J=7.5 Hz, 2H, ArH), 6.96(d,J=8.0 Hz, 2H, ArH), 5.42(s, 4H, CH2), 3.76(s, 6H, OCH3);13C NMRδ: 160.05, 136.86, 136.78, 130.66, 123.33, 120.87, 114.66, 114.61, 55.68, 52.38。
2c: 产率70%;1H NMRδ: 9.50(s, 1H, c-H), 7.86(s, 2H, a,b-H), 7.50(q,J=8.5 Hz, 8H, ArH), 5.45(s, 4H, CH2);13C NMRδ: 137.02, 134.22, 134.03, 130.99, 129.47, 123.34, 51.64。
(2) 3a~3c的合成(以3a为例)
在无水无氧条件下,向100 mL Schlenk瓶中加入新制2a 0.69 g(2 mmol)、氧化银0.26 g(1.1 mmol)和二氯甲烷20 mL,搅拌下于室温避光反应48 h。过滤,滤液浓缩后用乙醚重结晶得白色固体3a。
用类似的方法合成白色固体3b和3c。
3a: 产率75%;1H NMRδ: 7.50(s, 2H, a, b-H), 7.27(d,J=8.0 Hz, 4H, ArH), 6.90(d,J=8.5 Hz, 4H, ArH), 5.23(s, 4H, CH2), 3.72(s, 6H, OCH3);13C NMRδ: 178.80(Ag—C), 159.51, 129.63, 122.72, 114.63, 55.59, 54.31; IRν: 3 423(N—H), 3 129, 2 829(CH2), 1 615(C=C), 1 449(C=N), 1 252, 725 cm-1; Anal. calcd for C19H20N2O2ClAg: C 50.52, H 4.46, N 6.20; found C 50.50, H 4.43, N 6.22。
3b: 产率79%;1H NMRδ: 7.57(s, 2H, a, b-H), 7.25(t,J=8.0 Hz, 2H, ArH), 6.90~6.82(m, 6H, ArH), 5.28(s, 4H, CH2), 3.71(s, 6H, OCH3);13C NMRδ: 178.92(Ag—C), 159.33, 138.60, 129.81, 122.44, 119.50, 113.32, 113.14, 54.93, 54.08; IRν: 3 437(N—H), 2 837(CH2), 1 598(C=C), 1 473(C=N), 1 267, 737 cm-1; Anal.calcd for C19H20N2O2ClAg: C 50.52, H 4.46, N 6.20; found C 50.50, H 4.42, N 6.21。
3c: 产率62%;1H NMRδ: 7.57(s, 4H, a, b-H), 7.44(d,J=8.0 Hz, 8H, ArH), 7.31(d,J=8.5 Hz, 8H, ArH), 5.34(s, 8H, CH2);13C NMRδ: 179.85(Ag—C), 136.64, 133.16, 129.88, 129.22, 123.17, 53.91; IRν: 3 424(N—H), 2 855(CH2), 1 586(C=C), 1 456(C=N), 1 223, 739 cm-1; Anal.calcd for C34H28N4Cl6Ag2: C 44.34, H 3.06, N 6.08; found C 44.30, H 3.05, N 6.05。
1.3 晶体结构测定
将配合物单晶置衍射仪上,用石墨单色器单色化的MoKα射线(λ=0.71073 Å),以ω-φ扫描方式收集衍射数据,对衍射强度数据进行了LP因子和经验吸收校正。晶体结构由直接法解出[26],非氢原子坐标采用直接法和差值傅立叶合成法获得。对非氢原子坐标及各向异性热参数采用全矩阵最小二乘法对初结构进行精修,所有计算用SHELXS-97和SHELXS-97程序包完成。3a~3c的CCDC分别为1432048, 1413847和1413845,晶体学参数见表1。
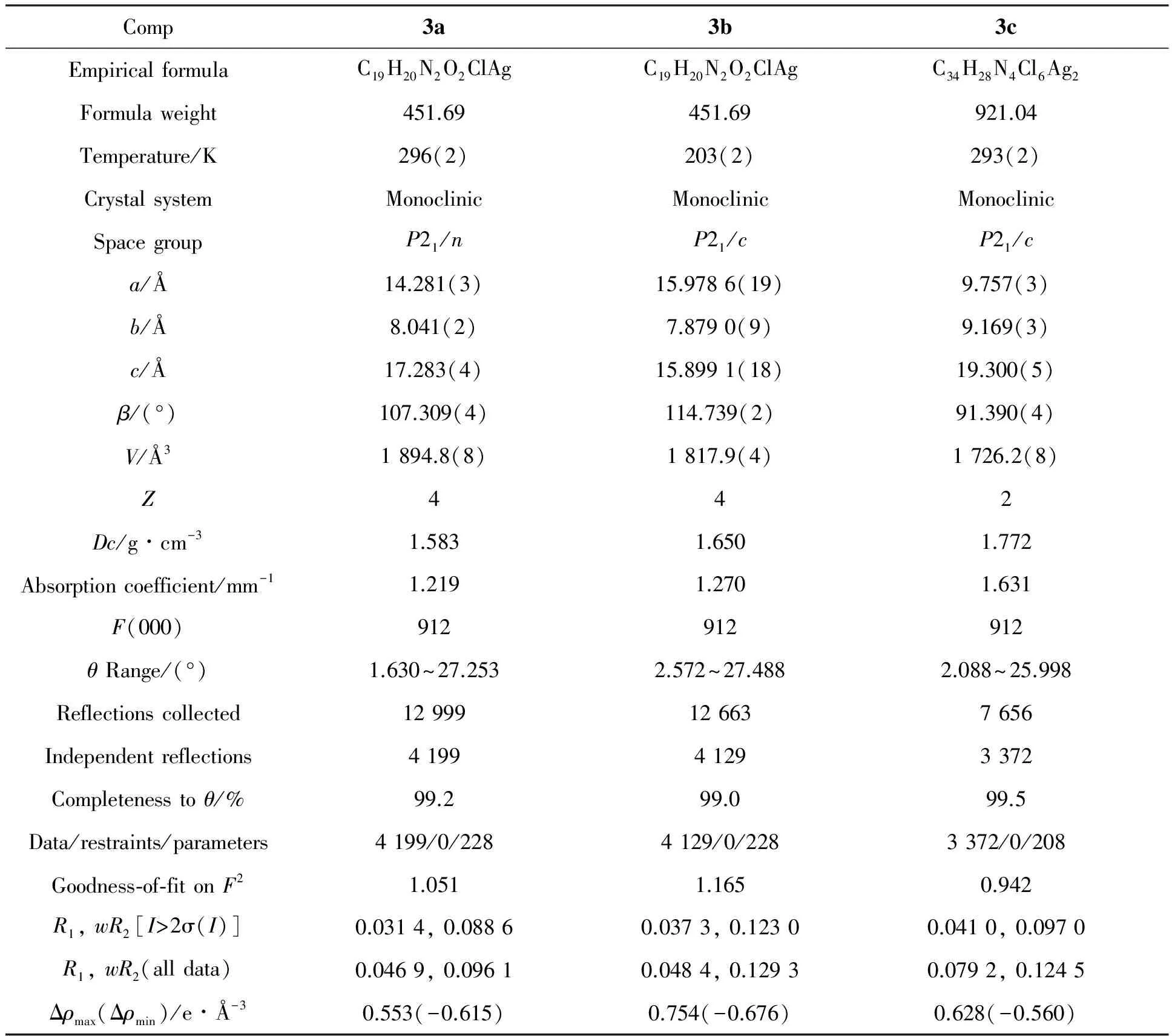
表1 3a~3c的晶体学数据
2 结果与讨论
2.1 表征
苄基咪唑氯化物与氧化银反应是制备氮杂环卡宾银配合物的通用方法[27-28]。三种新型的银卡宾配合物均为白色晶体,可溶于二氯甲烷、DMSO和DMF等有机溶剂,在空气中稳定存在,不发生分解或变质。苄基咪唑氯化物2a~2c与对应的银配合物3a~3c的1H NMR分析表明,咪唑环1-位质子吸收峰消失,表明该位置的碳原子与银原子发生了配位,同时,金属原子与配体结合,使分子的共轭体系进一步增强,π电子活动范围更广,咪唑环上电子云密度有所降低,这使得3a~3c的氢质子吸收峰向高场区偏移。另外,与2a~2c的13C NMR相比,3a~3c的卡宾碳的吸收峰位置发生了显著变化,分别位于δ178.80,δ178.92和δ179.85,与文献[29]报道一致,表明形成了银配合物。
3a的IR分析表明,3 423 cm-1处吸收峰为N—H伸缩振动吸收峰,1 615 cm-1和1 449 cm-1处的吸收峰分别为咪唑环上C=C和C=N的伸缩振动峰。另外,3a~3c在725 cm-1, 737 cm-1和739 cm-1处出现的吸收峰,归属Ag—C吸收峰,表明金属原子与分子中碳原子形成了配位。
2.2 晶体结构
3a~3c的部分键长和键角数据见表2,晶体结构分别见图1~图3。
晶体结构解析表明,3a和3b属于单核配合物,两种配合物均通过卡宾碳原子与中心银原子直接配位形成配合物。3a属单斜晶系,P21/n空间群,Ag1—C1和Ag1—Cl1的键长分别为2.093(3) Å和2.357 2(9) Å, C1—Ag1—Cl1的键角为169.00(7)°,该键长键角与其它类似结构的氮杂环卡宾银配合物的键长键角一致[30-31]。3b的结构与3a相似,仅在键长和键角上有微小差别,Ag1—C1和Ag1—Cl1的键长分别为2.101(4) Å和2.338 1(12) Å, C1—Ag1—Cl1的键角为165.55(12)°。 3c的结构与3a和3b不同,3c属单斜晶系,P21/c空间群,为双核配合物,在结构中存在着(NHC)AgCl的二聚体,两个单体通过Ag…Cl桥联的方式形成一个Ag2Cl2四元环。两个桥键上的氯离子是非对称的,其中Ag1—Cl1和Ag1—Cl1#1的键长分别为2.414 6(16) Å和2.851 3(17) Å, C1—Ag1—Cl1, C1—Ag1—Cl1#1, Cl1—Ag1—Cl1#1和Ag1—Cl1—Ag1#1的键角分别为153.95(15)°, 110.89(15)°, 95.09(5)°和84.91(5)°,这些键长键角与文献[32]报道的类似结构的银配合物键长键角一致。

表2 3a~3c的部分键长和键角

图1 3a的晶体结构
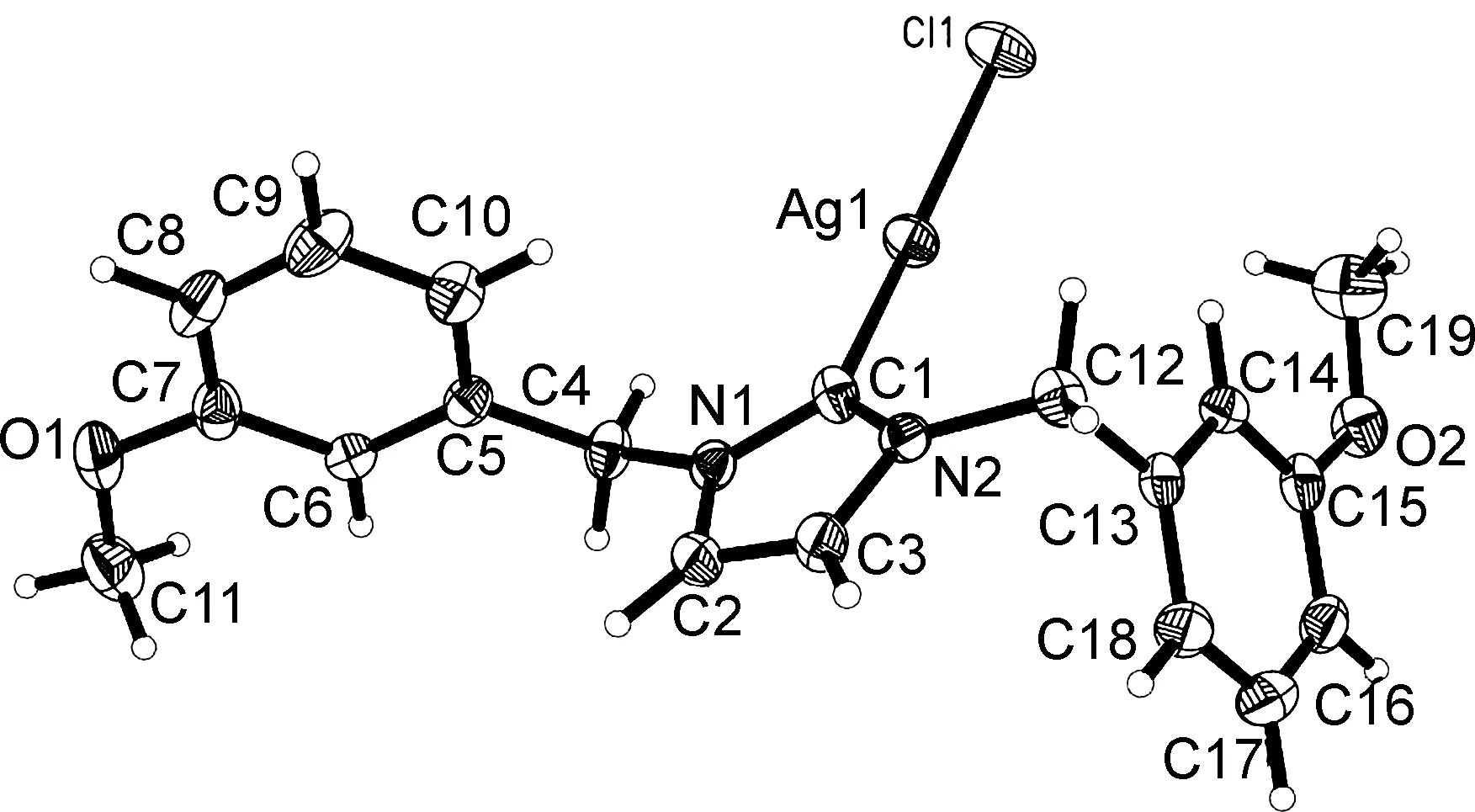
图2 3b的晶体结构

图3 3c的晶体结构
合成了三种新型的氮杂环卡宾银配合物(3a~3c)。 3a~3c不仅可以在空气中稳定存在,而且对于大多数有机溶剂具有良好的溶解性。该合成方法原料廉价易得,实验过程简单,反应条件温和,该类卡宾银配合物具有良好的催化活性,有望在C—H键活化反应体系中得到应用。晶体结构研究结果表明:3a~3c晶体均属单斜晶系,3a和3b为单核银配合物,3c为双核银配合物。三种配合物结构相似,由于配体取代基团不同而略有差异,可能与配体的结构和体积不同有关。
[1] Kong Y, Ren H, Xu S,etal. Synthesis,structures,and norbornene polymerization behavior of bis(aryloxide-N-heterocyclic carbene) palladium complexes[J].Organometallics,2009,28(20):5934-5940.
[2] Zuo W, Braunstein P.N-heterocyclic dicarbene iridium(Ⅲ) pincer complexes featuring mixed NHC/abnormal NHC ligands and their applications in the transfer dehydrogenation of cyclooctane[J].Organometallics,2011, 31(7):2606-2615.
[3] Ray S, Mohan R, Singh J K,etal. Anticancer and antimicrobial metallopharmaceutical agents based on palladium,gold,and silverN-heterocyclic carbene complexes[J].J Am Chem Soc,2007,129(48):15042-15053.
[4] Albrecht M, Maji P, Häusl C,etal.N-Heterocyclic carbene bonding to cobalt porphyrin complexes[J].Inorg Chim Acta,2012, 380:90-95.
[5] Öfele K. 1,3-Dimethyl-4-imidazolinyliden-(2)-pentacarbonylchrom ein neuer übergangsmetall-carben-komplex[J].J Organomet Chem,1968,12(3):42-43.
[6] Wanzlick H W, Schönherr H J. Direct synthesis of a mercury salt-carbene complex[J].Angew Chem In Ed Engl,1968,7(2):141-142.
[7] Arduengo III A J, Harlow R L, Kline M. A stable crystalline carbene[J].J Am Chem Soc,1991,113(1):361-363.
[8] Weskamp T, Böhm V P W, Herrmann W A.N-Heterocyclic carbenes:State of the art in transition-metal-complex synthesis[J].J Organomet Chem,2000,600(1):12-22.
[9] Zhang C, Huang J, Trudell M L,etal. Palladium-imidazol-2-ylidene complexes as catalysts for facile and efficient Suzuki cross-coupling reactions of aryl chlorides with arylboronic acids[J].J Org Chem,1999,64(11):3804-3805.
[10] Scholl M, Ding S, Lee C W,etal. Synthesis and activity of a new generation of ruthenium-based olefin metathesis catalysts coordinated with 1,3-dimesityl-4,5-dihydroimidazol-2-ylidene ligands[J].Org Lett,1999,1(6):953-956.
[11] Trnka T M, Grubbs R H. The development of L2X2Ru CHR olefin metathesis catalysts:An organometallic success story[J].Acc Chem Res,2001,34(1):18-29.
[12] Díez-González S, Nolan S P. Stereoelectronic parameters associated withN-heterocyclic carbene(NHC) ligands:A quest for understanding[J].Coordin Chem Rev,2007,251(5):874-883.
[13] Cavallo L, Correa A, Costabile C,etal. Steric and electronic effects in the bonding ofN-heterocyclic ligands to transition metals[J].J Organomet Chem,2005,690(24):5407-5413.
[14] Hahn F E, Radloff C, Pape T,etal. Synthesis of silver(I) and gold(I) complexes with cyclic tetra-and hexacarbene ligands[J].Chem-Eur J,2008,14(35):10900-10904.
[15] Würtz S, Lohre C, Froöhlich R,etal. IBiox [(-)-menthyl]:A sterically demanding chiral NHC ligand[J].J Am Chem Soc,2009,131(24):8344-8345.
[16] Peris E, Crabtree R H. Recent homogeneous catalytic applications of chelate and pincerN-heterocyclic carbenes[J].Coordin Chem Rev,2004,248(21):2239-2246.
[17] Nolan S P. The development and catalytic uses ofN-heterocyclic carbene gold complexes[J].Acc Chem Res,2010,44(2):91-100.
[18] Marion N, Navarro O, Mei J,etal. Modified(NHC) Pd(allyl)Cl(NHC=N-heterocyclic carbene) complexes for room-temperature Suzuki-Miyaura and Buchwald-Hartwig reactions[J].J Am Chem Soc,2006,128(12):4101-4111.
[19] de Frémont P, Scott N M, Stevens E D,etal. Synthesis and structural characterization ofN-heterocyclic carbene gold(I) complexes[J].Organometallics,2005,24(10):2411-2418.
[20] 刘鸿,李创海,廖亚四. 7-{2-[1-(8-羟基喹啉-7-亚甲基)]苯并咪唑基}-8-羟基喹啉及其金属配合物的合成与荧光性能[J].合成化学,2015,23(12):1120-1123.
[21] 李家明,史忠丰. 具有(4,4)-连接(44· 62)拓扑结构的新型一维钴配合物的合成及其表面光电性能[J].合成化学,2015,23(12):1143-1146.
[22] Zhang W Z, Li W J, Zhang X,etal. Cu(I)-catalyzed carboxylative coupling of terminal alkynes,allylic chlorides,and CO2[J].Org Lett,2010,12(21):4748-4751.
[23] Yu D Y, Tan M X, Zhang Y G. Carboxylation of terminal alkynes with carbon dioxide catalyzed by poly (N-heterocyclic carbene)-supported silver nanoparticles[J].Adv Synth Catal,2012,354(6):969-974.
[24] Liu X, Braunstein P. Complexes with hybrid phosphorus-NHC ligands:Pincer-type Ir hydrides,dinuclear Ag and Ir and tetranuclear Cu and Ag complexes[J]. Inorg Chem,2013,52(13):7367-7379.
[25] Li F, Hu J J, Koh L L,etal. Substituent-dependent structures and catalysis of benzimidazole-tetheredN-heterocyclic carbene complexes of Ag(I),Ni(II) and Pd(II)[J].Dalton Trans,2010,39(22):5231-5241.
[26] Sheldrick G M. SHELXS 97,Program for X-ray Crystal Structure Solution and Refinement[K].University of Göttingen,Germany,1997.
[27] Cheng C H, Chen D F, Song H B,etal. Synthesis and catalytic activity ofN-heterocyclic carbene silver complexes derived from 1-[2-(pyrazol-1-yl) phenyl] imidazole[J].J Organomet Chem,2013,726:1-8.
[28] Lin J C Y, Huang R T W, Lee C S,etal. Coinage metal-N-heterocyclic carbene complexes[J].Chem Rev,2009,109(8):3561-3598.
[29] Herrmann W A, Elison M, Fischer J,etal. Metal complexes ofN-heterocyclic carbenes——A new structural principle for catalysts in homogeneous catalysis[J].Angew Chem Int Ed Eng,1995,34(21):2371-2374.
[30] Garrison J C, Youngs W J. Ag (I)N-heterocyclic carbene complexes:Synthesis,structure,and application[J].Chem Rev,2005,105(11):3978-4008.
[31] Li Y, Chen X, Song Y,etal. Well-definedN-heterocyclic carbene silver halides of 1-cyclohexyl-3-arylmethylimidazolylidenes:Synthesis,structure and catalysis in A3-reaction of aldehydes,amines and alkynes[J].Dalton Trans,2011,40(9):2046-2052.
[32] Su H L, Peérez L M, Lee S J,etal. Studies of ligand exchange inN-heterocyclic carbene silver(Ⅰ) complexes[J].Organometallics,2012,31(10):4063-4071.
Synthesis and Crystal Structures of Novel Silver(I) N-Heterocyclic Carbene Complexes
LI Shan-shan, SUN Jing, WU Shuang, WANG Xin, ZHOU Ming-dong*
(College of Chemistry, Chemical Engineering and Enviromental Engineering, Liaoning Shihua University, Fushun 113001, China)
Benzyl imidazolium chlorides(2a~2c) were prepared byN-alkylation reaction of substituted benzyl chloride with imidazole. Three novel silverN-heterocyclic carbene complexes, (NHC)AgCl [NHC: 1,3-bis(4-methoxybenzyl)imidazol-2-ylidene(3a), 1,3-bis(3-methoxybenzyl) imidazol-2-ylidene(3b)] and [(NHC)AgCl]2[NHC=1,3-bis(4-chlorobenzyl)imidazol-2-ylidene(3c)], were synthesized by theinsitudeprotonation reaction of 2a~2c with Ag2O. The structures were characterized by1H NMR,13C NMR, IR, elemental analysis and X-ray single crystal diffraction analysis. 3a~3c belong to monoclinic crystal system, space groups areP21/nfor 3a,P21/cfor 3b and 3c. 3a and 3b are mononuclear Ag(I) complexes, where as 3c is a di-nuclear Ag(I) complex.
benzyl imidazolium chloride;N-heterocyclic carbene; silver complex; synthesis; crystal structure
2016-04-06;
2016-11-09
国家自然科学基金资助项目(21201095)
李山山(1988-),女,汉族,山东东营人,硕士研究生,主要从事金属有机化合物的合成及应用研究。 E-mail: 835367481@qq.com
周明东,教授, E-mail: mingdong.zhou@hotmail.com
O614.122; O641.4; O76
DOI: 10.15952/j.cnki.cjsc.1005-1511.2017.01.16093
