胆道镜引导下胰管切开取石加T管引流术治疗胰管结石
2017-02-06刘金阳李全福刘现立
刘金阳,李全福,刘现立
胰管结石是一种少见的胰腺疾病,传统的治疗方法存在着诸多不足。因此,探索一种简便易行、并发症少,且术后尽可能保留功能性胰腺组织,且符合消化道生理结构的治疗方法具有重要的临床意义。本研究回顾分析了2006年至2016年共18例胰管结石患者的临床资料,其中有8例胰管切开胆道镜取石术后用T管引流术,而未再行胰肠吻合或胰体尾切除手术,效果良好。其余患者5例行胰管空肠吻合手术,3例行胰体尾+脾脏切除,2例行胰保留脾脏的胰体尾切除。现对前8例总结报道如下。
1 资料与方法
1.1病例资料8例患者中,男6例,女2例;年龄(47±21)岁;病程(2.5±1.3) a。其中合并糖尿病3例,有经常饮酒史者3例。所有患者均表现为不同程度的上腹部疼痛,部位为上腹部或左上腹,伴向左侧腰背部放射,性质为持续或间断性,多可忍受。进食油腻食物或饮酒后,可诱发疼痛加重。伴有明显消瘦6例,慢性腹泻2例,伴有血/尿淀粉酶升高3例,伴有谷丙转氨酶/谷草转氨酶不同程度升高6例。所有病例均经常规彩超检查,确诊有胰管结石,检出率100%。随后,经CT或磁共振胰胆管成像(magnetic resonance cholangiopancreatography,MRCP)进一步检查,了解胰管结石的大小、数量、分布范围以及胰管的扩张情况。影像学显示结石均为多发,位于胰头或胰颈部位者5例,胰体部2例,胰体+胰尾部位者1例。结石部位及近端胰管均显示不同程度扩张,直径0.6~1.5 cm不等,见图1。

图1 示胰体部胰管内多发结石 (粗白箭头示胰管结石,细白箭头示胰管扩张)
1.2设备日本产Olympus P20型纤维胆道镜或Olympus OTV-S7电子胆道镜,FG-24SX-1取石网篮,国产TCS普东光电液电碎石机。
1.3治疗方法
1.3.1胰管切开取石与T管引流术8例均进行开放手术。根据术前CT和/或MRCP所显示的胰管结石位置,经术中扪诊,多可最终确定结石的位置和胰管扩张处。先以7#针头穿刺,证实为胰管后,尽可能靠近胰头部位,沿胰管长轴切开约1~2 cm。胆道镜经胰管切口进入,对胰管全程进行探查,观察有无胰管狭窄,寻找并取石。表面光滑的小结石,可经冲洗后自行排出。较大结石,以取石钳夹碎后分次取出。部分嵌入胰腺组织的结石,以冲击波碎石后取出或冲出。经胆道镜检查证实胰管结石取净后,在胰管切开部位置入T型管(短臂修剪为半管)。经T型内注入生理盐水,让T管长臂直立,若T型管内水柱能自行下降,或术中胆道镜能够经胰管进入胆总管(图2)或十二指肠者,则说明胰管—胆管汇合处通畅,放置T管。
若术中不能证实胰—胆管汇合处通畅,或胰管结石嵌入胰腺钩突部位实在难以取出者,则行常规胰管空肠吻合手术。若结石相对集中于胰腺远端,或结石细碎,难以取净者,则行胰体尾+脾脏切除或保留脾脏的胰体尾切除。

图2 示胆道镜经胰管进入胆总管末端见到壶腹部(可见壶腹部黏膜走向及下方的Oddis括约肌开口)
1.3.2术后处理T管的术后处理等同于胆总管探查术后的处理。即术后7~10 d开始,间断闭管并逐渐延长闭管时间。术后6~8周行经T管胰管造影,若证实无结石残留且胰—胆管汇合处通畅,拔除T管。
2 结果
胰管切开胆道镜取石、T管引流术后胰管扩张改善8例,腹痛完全缓解6例,大部缓解2例。本组有3例胆道镜经胰头部胰管进入胆总管或十二指肠。采用冲击波碎石6例,用管道类器械,捣烂结石或使其松动后取出8例,见图3。
术中胆道镜检查,可以发现很细小的胰管分支内有结石,而术前影像检查难以发现。如图1患者,并未见胰头部位胰管内有结石,但术中胆道镜却可以看到在胰头部胰管分支内,散在很多小结石,见图4。
术后随访到4例,1.5~2 a内未发现胰管结石复发。另10例行胰管空肠吻合手术或胰体尾切除的患者,2例出现术后胰漏,经保守治疗后痊愈。胰管切开胆道镜取石术后用T管引流术后胰管扩张改善情况,见图5。

图3 示用导管松动或捣碎结石(黑白相间管道为输尿管导管,胰管内白色物为胰管结石)
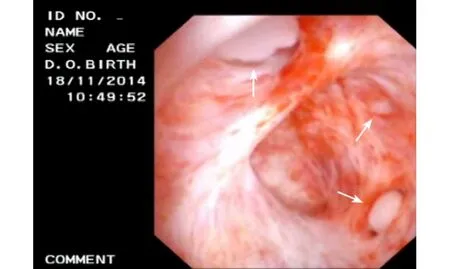
图4 示胰头部小胰管内散在有很多小结石(白色箭头所指处为胰管内小结石)
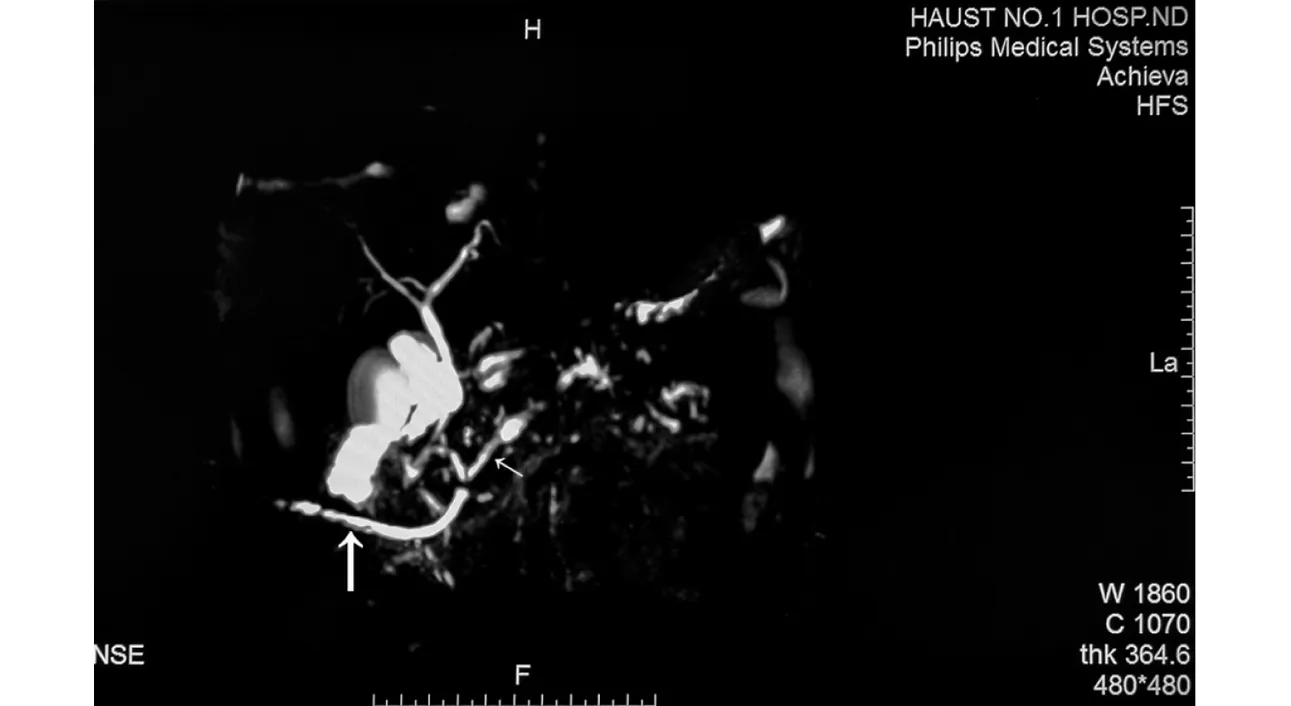
图5 示术后胰管内结石影消失(粗白箭头所指为T形管,细白箭头所指为变细的胰管)
3 讨论
胰管结石的主要症状为不同程度的腹痛,胰腺内、外分泌功能不全以及各种并发症。外科治疗的目的,多强调在尽量保留胰腺内外分泌功能的前提下,取净胰管结石,胰管引流通畅,以最大限度地改善症状并提高生活质量[1-4]。
现有的治疗手段,包括经开放手术的十二指肠切开副乳头成形胆道镜胰管取石[5]、内镜治疗[6-8]、体外冲击波碎石(extracorporeal shock wave lithotripsy, ESWL)[9-11]、液电/激光碎石[12-14]、内窥镜逆行胰胆管造影(endoscopic retrograde cholangiopancreatography,ERCP)+ESWL[3,15-16]、胰腺部分切除及胰肠吻合术[4,6,8,12,17-18]、胰头十二指肠切除术[4,6,8,18]、保留十二指肠的胰头切除[8, 17-18]等。对部分胰管结石,胆道镜可以经胰管进入胆总管,说明胰胆汇合处是通畅的,因此认为取出胰管结石,解除胰管梗阻后,并无必要再行胰肠吻合引流手术。本研究结果使用胰管切开胆道镜取石术后用T管引流治疗胰管结石是可行的。
3.1胰管切开胆道镜取石+T管引流的可行性近年来,以ERCP为主导的内镜下治疗及ESWL治疗胰管结石已在临床上得到了广泛的应用[6-7,9-10]。这些治疗取出胰管结石后,主胰管的引流仍经过原来的解剖结构,说明胰管结石的患者不一定都需要在术后重新建立新的胰液引流通道,只要保证原正常解剖通道畅通即可。因此,在手术取出胰管结石后,只要能证实胰胆管汇合处通畅,即可以施行单纯放置T型管的手术。
3.2胰管切开胆道镜取石+T管引流的适应证对拟行该术式的患者,作者目前掌握的指征是:①胰管结石能够取净,需要有胆道镜及多种取石手段,如胆道取石钳、止血钳、取石网、冲击波碎石机等的支持。②胆道镜能够经胰头部胰管进入胆总管末端,见到壶腹部(图2)或进入十二指肠。胆胰管汇合处的解剖及术中实践证实,部分伴有胰管扩张的胰管结石,胆道镜是可以经胰头部胰管进入胆总管或十二指肠的[12,19-20]。本组有3例这样的患者,占37.5%。③T管长臂内注入生理盐水后直立,其水柱能够因重力作用自然下降至较低的位置。
3.3胰管切开胆道镜取石+T管引流术的优点①手术简便,术后吻合口漏的风险小;②手术不改变消化道的解剖结构,符合人体生理;③术后胰腺外分泌液能通过正常的途径进入消化道;④能最大限度地保留胰腺组织,有利于胰腺功能的恢复;⑤对于术后胰管造影有结石残留的患者,保留有再次进入胆道镜的通道。
3.4胰管切开胆道镜取石的缺点①胰管结石时,结石远端部位的主胰管扩张,往往足够胆道镜的进入,但在胰头及胰尾部位,胰管分支很多,且扩张程度有限,普通胆道镜(Olympus P20型)往往难以进入,有胰管分支内小结石残留的可能。②因胰管分支直径所限,普通的取石网往往难以张开,即使能看到的结石也难以取出。本组的处理方式是用冲击波碎石或其他管道类器械,捣烂结石或使其松动后取出(图4)。尽管如此,仍有手术后胰管结石残留的可能,但常规取石术后残留结石的可能更多、更大[8,21]。
3.5术中注意事项因胰管结石多表面粗糙,在取石过程中常因结石或器械损伤,造成胰管表面黏膜出血。一定要用足量的生理盐水冲洗,待出血停止后,取出胆道镜下可见的血凝块,再放置T管。防止术后血凝块堵塞胰管出口或堵塞胆道末端引起阻塞性黄疸。对胰头或钩突部的结石,尽量避免在胰头部实质处切开,因此处组织较厚、血供丰富,胰管位置往往偏后,视野深、易出血。可在邻近的胰颈处切开。同时需要预先游离胰头部,左手把持后,用胆道取石钳或止血钳小心夹碎或用冲击波碎石后,再分次逐一取出。尽量不用胆道探子试图经胰管进入胆道,防止穿透胰腺组织或胆管,形成术后胰漏或胆漏。
术中胆道镜检查,可以发现很细小的胰管分支内有结石,但术前影像检查却难以发现。尽管MRCP对诊断胰管结石的准确率约78.25%~93.23%[6,8,18],但对于更细小的胰管分支内的结石,往往需要术中用胆道镜才能发现。如图1患者,术前MRCP并未见胰头部位胰管内有结石,但术中胆道镜却可以看到在胰头部胰管分支内,散在很多小结石(图4)。文献报道中的术后胰管结石“复发”[6],是否就是这部分残留结石的继续增大,还有待商榷。尽管已有文献报道,可用直径更细的输尿管软镜代替胆道镜治疗胰管结石,但期待更精细胆道镜及取石网的出现,对细小胰管分支内的小结石的发现与治疗,无疑将提供了一个更好的选择。
本研究结果显示,胰管切开胆道镜取石并T管引流术相比内镜取石,有更好的彻底性和简便性;相比开放的胰肠吻合或胰腺切除,有更少的并发症;能最大限度地保留功能性的胰腺组织,对胰—胆管汇合处通畅的患者而言,具有不可比拟的优势。
[1] 刘续宝,谭春路.慢性胰腺炎合并胰管结石的外科治疗策略[J].中国普外基础与临床杂志,2016,23(6):641-643.
[2] 仵正,周灿灿.慢性胰腺炎合并胰管结石的规范化治疗[J].中国普外基础与临床杂志,2016,23(6):650-653.
[3] Hayes JM,Ding SL.Pancreatic stone and treatment using ERCP and ESWL procedures:a case study and review[J].N Z Med J,2012,125(1361):89-97.
[4]Bachmann K,Izbicki JR,Yekebas EF.Chronic pancreatitis: modern surgical management[J].Langenbecks Arch Surg,2011,396(2):139-149.
[5] 张丽玉,吴烨,朱峰.1例经十二指肠切开副乳头成形胆道镜胰管取石的手术配合[J].实用临床医药杂志,2013,17(22):208-209.
[6] 曾锦生,赵慧,李勇,等.15例胰管结石的诊断及治疗[J].南昌大学学报(医学版),2012,52(11):40-42.
[7] 黄涛,刘勇,王震宇.慢性胰腺炎合并胰管结石临床特点及治疗的探讨[J].临床肝胆病杂志,2012,28(8):584-586.
[8] 何义仁,黄强,王成,等.胰管结石40例诊治体会[J].肝胆外科杂志,2014,22(6):456-458.
[9]Milovic V,Wehrmann T,Dietrich CF,et al.Extracorporeal shock wave lithotripsy with a transportable mini-lithotripter and subsequent endoscopic treatment improves clinical outcome in obstructive calcific chronic pancreatitis[J].Gastrointest Endosc,2011,74(6): 1294-1299.
[10]Hu LH,Liu MH,Liao Z,et al.Steinstrasse formation after extracorporeal shock wave lithotripsy for pancreatic stones[J].Am J Gastroenterol,2012,107:1762-1764.
[11]Tandan M, Reddy DN. Extracorporeal shock wave lithotripsy for pancreatic and large common bile duct stones[J].World J Gastroenterol,2011,17(39):4365-4371.
[12]魏晓平,田大广,胡明道,等.胆道镜结合液电碎石治疗胰管结石5例临床分析[J].中国普通外科杂志,2012,21(9):1164-1165.
[13]Papachristou GI,Baron TH.Endoscopic treatment of an impacted pancreatic duct stone using a balloon catheter for eletrohydraulic lithotripsy without pancreatoscopy[J].J Clin Gastroenterol,2006,40(8):753-756.
[14]Li BR,Pan Jun,Hu LH,et al.Laser lithotripsy as a supplementary approach for the treatment of main pancreatic duct stones[J].Gastrointest Endosc,2016,83(6):1300-1301.
[15]杨晶,张筱凤.体外冲击波碎石联合经内窥镜逆行胰胆管造影术治疗胰管结石的研究[J].中国内镜杂志,2017,23(5):83-87.
[16]胡良,李兆申.慢性胰腺炎胰管结石的微创治疗[J].肝胆外科杂志,2014,22(1):9-11.
[17]Mihaljevic AL,Kleeff J,Friess H.Beger’s operation and the Berne modification: origin and current results [J].J Hepatobiliary Pancreat Sci,2010,17(6):735-744.
[18]杨骥,黄强,林先盛,等.慢性胰腺炎合并胰管结石的诊断及治疗分析[J].中国普通外科杂志,2014,23(3):379-382.
[19]陈风,汤琳,蒋晓飞,等.MRCP观察胰胆管合流解剖及意义[J].中国临床解剖学杂志,2013,31(5):539-542.
[20]邱志胜,赵海鹰,刘金钢,等.胰管结石手术治疗中胆道镜应用价值研究[J].中国实用外科杂志,2012,32(7):576-578.
[21]杨诏旭,宋文杰,何勇,等.胰管结石的诊断与外科治疗:附43例报告[J].中国普通外科杂志,2012,21(3):340-344.
