两性霉素B聚乳酸普鲁兰纳米胶束的制备及评价
2017-01-16唐晓娇
黄 俊, 唐晓娇, 马 悦, 宋 娟, 杨 丽
两性霉素B聚乳酸普鲁兰纳米胶束的制备及评价
黄 俊, 唐晓娇, 马 悦, 宋 娟, 杨 丽*
(沈阳药科大学药学院,辽宁沈阳 110016)
目的制备两性霉素B聚乳酸普鲁兰(PLA-pullulan)纳米胶束,并进行体外评价。方法以新型两亲性高分子PLA-pullulan为载体材料,采用薄膜水化法制备两性霉素B纳米胶束,并分别采用透射电镜、激光粒径仪和zeta电位分析仪对胶束的形态、粒径和表面电位进行表征,测定其包封率、载药量和体外释放动力学,考察其药物分散状态和溶血毒性。结果所制备的两性霉素B聚乳酸普鲁兰纳米胶束溶液外观透明,电镜下呈圆整的球形,平均粒径为152.1 nm,包封率为71.1%,载药量达10.9%,24 h的累积释放量为10.01%,溶血毒性低于两性霉素B去氧胆酸钠胶束。结论聚乳酸普鲁兰胶束是两性霉素B潜在的优良纳米载体,具有良好的应用价值。
药剂学;胶束;薄膜水化法;两性霉素B;聚乳酸普鲁兰;体外评价
近年来,深部真菌感染的发病率在侵入性诊断、免疫缺陷和器官移稙的患者身上呈增长趋势[1-3]。由于这类疾病早期临床诊断困难以及常见的抗真菌药治疗起效慢而导致死亡率较高[4]。尽管真菌的种类在不断地增加,但注射用两性霉素B依然是临床上治疗真菌感染的一线用药[5]。然而,其较大的毒性及不良反应限制了它的应用[6],其中,80%以上的患者出现了肾功能不全[7]。20世纪90年代,两性霉素B的三种脂质制剂相继上市,虽然大大降低了其肾毒性,但是同等剂量下的药物抗菌活性下降[8],临床上通常使用比注射用两性霉素B 高4到10倍的剂量[9]。另外对于发展中国家来说,其价格较昂贵[10]。因此更加迫切地需要发现新的、更价廉的药物传递系统。
聚合物胶束是近年来作为一种新的传递BCS IV类药物(如两性霉素B)的载体而被广泛研究。聚合物胶束具有热力学和动力学稳定;粒度较小,对于存在渗漏的脉管具有更强的渗透能力;疏水性内核可以增加难溶性药物的溶解性,而亲水性外壳可以将药物与体内环境更好地隔离,改变药动学和药物在体内的分布等优点。目前,国内外已有大量关于两性霉素B(amphotericin B, AmB)聚合物胶束的报道,杨卓理等采用透析法制备了两性霉素B的聚乙二醇-聚乳酸胶束[11]。朱丽君等利用透析法制备了两性霉素B聚乙二醇-聚谷氨酸苄酯胶束[12]。然而,采用透析法备胶束时,DMSO不易除尽,且药物易在透析袋DMSO与水交换处析出。Glen S. Kwon等制备了聚乙氧基聚已基天冬氨酸[13]、聚乙氧基聚苄基天冬氨酸[14]和聚乙氧基聚已基天冬氨酸系列烷基衍生物用以装载两性霉素B,然而其聚乙氧基聚已基天冬氨酸和聚乙氧基聚苄基天冬氨酸胶束仍然具有较强的溶血毒性。虽然聚乙氧基聚已基天冬氨酸系列烷基衍生物溶血性降低,但是材料需要多步合成,较为复杂。
普鲁兰是一种新型的微生物水溶性多糖,具有良好的安全性、生物相容性和肝靶向性,而且还具有长循环特性,是良好的载体材料[15]。聚乳酸安全、可降解、具有温敏性,被广泛用于接枝多糖,构建两亲性载体。因此,作者通过微波辅助的开环聚合反应合成了两亲性材料聚乳酸普鲁兰(poly(-lactide)-pullulan, PLA-pullulan)[16],通过控制投料比,合成了最佳比例的聚乳酸普鲁兰,在水中可自组装形成核-壳型的纳米胶束。亲水性的普鲁兰外壳可以将两性霉素B与体内环境有效地隔离,影响药物的体内分布,减少两性霉素B在肾脏的聚集。疏水性的内核成为药物的临时储库,在具有很好的增溶能力的同时,减缓了两性霉素B的释放,使体内的两性霉素B以单体的形式存在,而单体形态的两性霉素B对真菌细胞具有更大的亲和力[17],从而降低两性霉素B的毒性。目前,有关两性霉素B聚乳酸普鲁兰纳米胶束的研究未见文献报道。
作者以两亲性材料聚乳酸普鲁兰,利用薄膜水化法制备两性霉素B胶束,并对其制剂学特性进行评价,为后期研究奠定基础。
1 仪器与材料
UV-2000紫外可见分光光度计、4802H UV/VIS 紫外扫描仪(上海 Unico仪器有限公司),NanoZS90 粒度分析仪(英国Malvern仪器公司),RE5298A旋转蒸发仪(上海亚荣生化仪器厂),JY92-2D超声波细胞粉碎仪(宁波新芝生物科技股份有限公司),JEM 2100 透射电子显微镜(日本JEOL 公司)。
两性霉素B(华北制药集团华胜有限公司),透析袋(上海绿鸟公司,截留分子质量 1.2×104~ 1. 5×104u),聚乳酸普鲁兰(自制)。
新西兰大耳兔,雌性,体质量2.5 kg,沈阳药科大学动物实验中心提供。
2 方法与结果
2.1 两性霉素B聚乳酸普鲁兰载药胶束的制备
采用薄膜水化法制备两性霉素B胶束,具体过程如下:称取处方量的两性霉素B和聚乳酸普鲁兰加入适量的甲醇使其溶解后,减压旋转蒸发除去有机溶剂,直至在瓶底形成一层透明的薄膜,继续旋蒸除去残留的有机溶剂。加入适量水化介质水化,探头超声,将得到的制剂以5 000 r·min-1离心10 min,过0.22 μm微孔滤膜,即得。
2.1.1 有机溶剂的选择
按照有机试剂即能溶解药物,又具有较低沸点的要求,选择了甲醇、乙腈、二氯甲烷、氯仿等有机溶剂进行实验,结果显示两性霉素B仅在甲醇中微溶,在其他有机溶剂中不溶。因此选择甲醇为成膜溶剂。
2.1.2 成膜温度的选择
实验中考察了成膜温度对胶束外观及包封率的影响。当成膜温度分别为30、40和50 ℃时,按“2.1”条方法制备胶束,并按“2.4”条方法测定包封率,结果见表1。
结果表明,30 ℃时制得的制剂透明,包封率最高,为65.5%。所以选择30 ℃为成膜温度。

Table1 Effect of film forming temperature on appearance, entrapment efficiency of micelle
2.1.3 水化介质的选择
实验中考察了水化介质对胶束外观及包封率的影响。分别用去离子水、质量分数5%葡萄糖水溶液和质量分数0.9%氯化钠水溶液为水化介质,按“2.1”条方法制备胶束,并按“2.4”条方法测定包封率,结果见表2。
结果表明,以水为水化介质时包封率最高,为71.1%,所以选择水作为水化介质。

Table 2 Effect of water phase on appearance, entrapment efficiency of micelle
2.1.4 水化温度的选择
实验中考察了不同的水化温度对胶束的外观及包封率的影响。当水化温度分别为0、25和37 ℃时,按“2.1”条方法制备胶束,并按“2.4”条方法测定胶束的包封率,结果见表3。
结果表明,当水化温度为25 ℃即室温时,所制得的胶束的包封率最高,为71.1%。所以水化温度选择25 ℃。
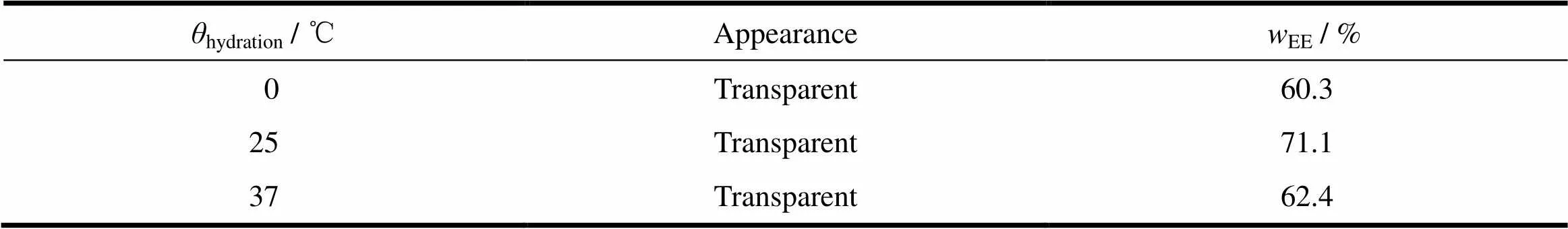
Table 3 Effect of hydration temperature on appearance, entrapment efficiency of micelle
2.1.5 超声时间的选择
实验中考察了超声时间对胶束外观、粒度、粒度分布和包封率的影响。当以超声功率为200 W、超声时间分别为2、6和12 min时,按“2.1”条方法制备胶束,并按“2.3”条方法测定胶束的粒度及粒度分布,按“2.4”条方法测定包封率,结果见表4。
结果表明,当以超声功率为200 W、超声12 min时,所制备的胶束粒度最小为152.1 nm,粒度分布较窄,PDI为0.207,包封率为71.1%。所以超声时间确定为12 min。

Table 4 Effect of ultrasound time on appearance, size, entrapment efficiency of micelle
2.1.6 药脂质量比的选择
实验中考察了药脂质量比对胶束的外观、粒度、粒度分布和包封率的影响。固定加入材料的量,以药脂质量比分别为0.077∶1、0.154∶1和0.231∶1时,按“2.1”条方法制备胶束,并按“2.3”条方法测定胶束的粒度及粒度分布,按“2.4”条方法测定包封率,结果见表5。
结果表明:药脂质量比为0.154∶1时,胶束的外观、粒度和包封率较好;药脂质量比为0.231∶1时,制剂外观浑浊,粒度明显增大。所以药脂质量比选择0.154∶1。

Table 5 Effect of weight ratio of drug to polymer on appearance, size, entrapment efficiency of micelle
2.1.7 材料质量浓度的选择
实验中考察了材料的质量浓度对外观、粒度、粒度分布和包封率的影响。固定药物的量,材料质量浓度分别为16、26和46 g·L-1时,按“2.1”条方法制备胶束,按“2.3”条方法测定胶束的粒度及粒度分布,按“2.4”条方法测定包封率,结果见表6。
结果表明:材料的质量浓度为16 g·L-1时,制得的制剂出现双峰,粒度较不均匀;而材料的质量浓度为46 g·L-1时,制得的制剂外观浑浊。综合考虑选择材料的质量浓度为26g·L-1,其胶束的外观、粒度和包封率较好。

Table 6 Effect of polymer concentration on appearance, size, PDI and entrapment efficiency of micelle
Note: *—Means double peaks appeared in the particle size spectrum
2.1.8 最优处方和工艺
经过筛选,得到的最优处方和工艺为:称取两性霉素B 20 mg、聚乳酸普鲁兰130 mg加入适量甲醇使其溶解后,30 ℃减压旋转蒸发除去有机溶剂,直至在瓶底形成一层透明的薄膜,继续旋蒸10 min除去残留的有机溶剂。加入5 mL蒸馏水25 ℃水化30 min,200 W探头超声12 min,将得到的制剂以5 000 r·min-1离心10 min,过0.22 μm的微孔滤膜,即得。
2.2 形态观察
采用透射电镜观察两性霉素B PLA-pullulan胶束的形态。方法如下:室温条件下用蒸馏水将载药胶束稀释至适当浓度,滴加到覆有支持膜的铜网上,用质量浓度10 g·L-1磷钨酸进行负染,室温下自然晾干,透射电镜进行观察。由图1可知,制备的载药胶束呈球形,粒度圆整,分散性较好。

Fig. 1 TEM photograph of AmB loaded micelles
2.3 胶束粒度和zeta电位测定
采用马尔文粒度仪测定两性霉素B胶束的粒径,测定条件为:测定温度25 ℃,检测器角度为90°,检测池平衡时间3 min,结果见图2。由图2可知,测得两性霉素B胶束的平均粒径为152.1 nm,多分散指数为0.207,粒度分布较均匀。

Fig. 2 The size distribution of AmB loaded micelles
Zeta电位是微粒表面荷电大小和荷电性质的标志,是影响微粒分散制剂稳定性和体内分布的重要因素。作者采用马尔文粒度仪对胶束的zeta电位进行测定。结果表明两性霉素B胶束的zeta电位为-0.167 mV。
2.4 包封率和载药量的测定
由于两性霉素B在水中的溶解度很低,因此采用过膜法测定载药胶束的包封率和载药量。取过0.22 μm滤膜的制剂适量,按“2.5”条方法测定胶束的含量。按下面的公式计算包封率(entrapment efficiency,EE)和载药量(loading content,LC):
EE=1/2Î100%;LC=1/3Î100%。
其中,EE表示载药胶束的包封率,LC表示胶束的载药量,1为胶束内包封的药物质量,2为投药量;3为载体材料质量。测得的最优处方和工艺的包封率和载药量分别为71.1%和10.9%。
2.5 含量测定方法的建立
由紫外扫描结果可知,AmB在体积分数50% DMSO的甲醇溶液中于411 nm处有吸收峰,而聚合物在此位置无吸收,确定411 nm为AmB的特征吸收波长。配制质量浓度分别为:1.2、2.4、3.6、4.8和6.0 g·L-1AmB的体积分数50%DMSO的甲醇溶液,在波长411 nm处分别测定吸光度值(),以对质量浓度()进行回归得标准曲线方程= 1.750Î10-2+0.126 8(=0.999),两性霉素B质量浓度在1.2~6.0 g·L-1内与吸光度呈良好的线性关系。测得最优处方和工艺制备的两性霉素B载药胶束的药物含量为2.84 g·L-1。
2.6 体外释放试验
取两性霉素B胶束溶液置于透析袋内,将其放置于盛有100 mL释放介质(pH值7.4、质量分数2%的十二烷基硫酸钠磷酸盐缓冲液)的容器中,然后置于(37±0.5) ℃、100 r·min-1的恒温震荡器中,分别于0.5、1、2、4、 8、12、18和24 h取样,每次取出5 mL释放介质,并同时补加同体积的新鲜释放介质。将所取的样品按“2. 5”条方法测定其含量,并计算其累积释放百分率。由图3可知,胶束24 h的累积释放量为10.01%。

Fig. 3 Drug release profile in vitro from micelle
2.7 两性霉素B紫外-可见吸收光谱的测定
文献报道,两性霉素B在胶束内的聚集状态可以用紫外-可见吸收光谱中320~330和410~420 nm处吸收峰的比值来衡量。当比值小于0.25时,两性霉素B以单体的形式存在,此时药物与材料有很强的相互作用,药物很好地分散在胶束的内核中;高于2.0时,主要以聚集体的形式存在[18],此时药物与材料的相互作用较弱,药物在材料内聚集。
将所制备两性霉素B普鲁兰胶束和两性霉素B脱氧胆酸钠胶束用纯化水稀释适宜倍数,采用紫外扫描仪进行扫描,记录在波长300~500 nm内的色谱图,结果见图4。
结果表明,两性霉素B脱氧胆酸钠胶束在320~330 nm时峰形较宽,Ⅰ/Ⅳ的比值为1.95。而所制备两性霉素B普鲁兰胶束Ⅰ/AⅣ的比值为1.59。表明药物在胶束中以部分聚集的状态存在,药物聚集程度低于两性霉素B脱氧胆酸钠胶束。

Fig. 4 Absorption spectra of AmB in sodium deoxycholate(A)and PLA-pullulan(B)
2. 8 溶血实验
取兔血数毫升,放入含玻璃珠的三角烧瓶中振摇10 min,除去纤维蛋白,使成脱纤血液。加入约10倍量的生理盐水,1 000 r·min-1离心15 min,除去上清液。沉淀的红细胞再用生理盐水按上述方法重新洗涤2、3次,直至上清液不显红色。将所得的红细胞用生理盐水配成体积分数为2%的红细胞混悬液,备用。将所制备的聚乳酸普鲁兰空白胶束、两性霉素B聚乳酸普鲁兰胶束和两性霉素B脱氧胆酸钠胶束分别与红细胞悬液37 ℃孵育,测定其溶血百分率。
结果表明,质量浓度为2~10 mg·L-1的两性霉素B脱氧胆酸钠胶束溶液37 ℃孵育2 h,100%溶血,而聚乳酸普鲁兰空白胶束和两性霉素B聚乳酸普鲁兰胶束未发生溶血。
3 讨论
3.1 制备方法的选择
目前,胶束制备常用的方法有透析法、乳化溶剂挥发法、反溶剂沉淀法和薄膜水化法。透析法是将药物和材料同时溶解于与水相溶的有机溶剂中,然后透析除去有机溶剂。由于两性霉素B仅在DMSO中有较好的溶解性,所以选择DMSO作为溶剂。然而在透析袋的水和DMSO交换处,两性霉素B易析出沉淀,且DMSO不易除尽。乳化溶剂挥发法需要药物溶解于与水不互溶且沸点低的有机试剂中(如乙醚、氯仿、二氯甲烷等),但两性霉素B在这些溶剂中不溶。使用反溶剂法制备的胶束载药量较低。因此,结合药物与材料的性质,最终选用薄膜水化法作为两性霉素B胶束的制备方法。
3.2 处方和制备工艺的考察
不同的水化介质对胶束形成具有重要影响,其中用质量分数5%葡萄糖水和纯化水制得的胶束外观较好,而用生理盐水进行水化时,制得的胶束浑浊,可能是因为NaCl与药物相互作用,使药物沉淀析出。超声时间对药物粒度有很大的影响,当超声时间为12 min时,粒度和粒度分布明显降低,较小的粒度可以影响药物的体内分布,而较小的粒度分布对胶束的稳定性有很大的影响。
药脂质量比对包封率和载药量均有影响。当药脂质量比为0.077∶1和0.154∶1时,包封率和粒度没有发生太大的变化。当药脂质量比增加到0.231∶1时,包封率和载药量略有增加,然而制得的制剂浑浊,粒度增加了一倍,可能是胶束之间发生了聚集。
3.3 载药胶束的体外释放、紫外扫描和溶血性
AmB胶束在pH值7.4、质量分数2%SDS的PBS缓冲液中释放缓慢。可能原因是AmB被材料包埋于胶束内部,需要克服与材料聚乳酸酯链的相互作用力,透过亲水性的外壳才能释放。紫外扫描图谱中,Ⅰ/Ⅳ的比值为1.59,药物以部分聚集状态的形式存在,两性霉素B的峰位从408 nm红移至414 nm,表明药物分子与材料产生了较强的相互作用。
脱氧胆酸钠是阴离子表面活性剂,其本身就具有溶血毒性。而且它的临界胶束浓度较高,大量稀释后可迅速解离,使得两性霉素B快速的释放和聚集,产生较强的溶血毒性,这也是市售两性霉素B注射剂毒性较大的原因之一。而作者所制备聚乳酸普鲁兰载药胶束,因材料本身无溶血性,且临界胶束质量浓度较低(1.02 g·L-1),具有良好的稳定性和耐稀释性,可使药物更缓慢地释放,浓度低于溶血域值,所以未产生溶血。从而降低了药物毒性,提高了制剂的安全性。
4 结论
作者通过薄膜水化法制备了两性霉素B聚乳酸普鲁兰胶束,并对其处方和工艺进行了筛选。所制得的载药胶束粒度小,分布均匀,包封率为71.1%,载药量高达10.9%。药物在胶束中以部分聚集的状态存在,载药胶束释药缓慢,溶血毒性低于两性霉素B脱氧胆酸钠胶束,是两性霉素B的优良的载体,具有良好的应用价值。
[1] KUMAR L, VERMA S, BHARDWAJ A, et al. Eradication of superficial fungal infections by conventional and novel approaches: a comprehensive review[J]. Artificial Cells Nanomedicine and Biotechnology, 2014, 42(1): 32-46.
[2] VIRAGH M, VOROS D, KELE Z, et al. Production of a defensin-like antifungal protein NFAP from Neosartorya fischeri in pichia pastoris and its antifungal activity against filamentous fungal isolates from human infections[J]. Protein Expression and Purification, 2014, 94: 79-84.
[3] WASAN K M, SIVAK O, ROSLAND M, et al. Assessing the antifungal activity, pharmacokinetics, and tissue distribution of amphotericin B following the administration of Abelcet (R) and AmBisome (R) in combination with caspofungin to rats infected with[J]. Journal of Pharmaceutical Sciences, 2007, 96(7): 1737-1747.
[4] MOZAFFARPUR S A, NASERI M, ESMAEILIDOOKI M R, et al. The effect of cassia fistula emulsion on pediatric functional constipation in comparison with mineral oil: a randomized, clinical trial[J]. Daru-Journal of Pharmaceutical Sciences, 2012, 20(12): 1-9.
[5] GIRMENIA P, MARTINO P. New antifungal drugs and new clinical trials: Interpreting results may be difficult [J].
Curr Opin Oncol, 2003, 15(4): 283–288.
[6] HARBARTH S, PESTOTNIK S L, LLOYD J F, et al. The epidemiology of nephrotoxicity associated with conventional amphotericin B therapy [J]. Am J Med, 2001, 111: 528–534.
[7] SABRA R, BRANCH R A. Amphotericin-B nephrotoxicity[J]. Drug Safety, 1990, 5: 94–108.
[8] GALLIS H A, DREW R H, PICKARD W W. Amphotericin B: 30 years of clinical experience[J]. Rev Infect Dis, 1990, 12: 308–329.
[9] DIEZI T A, TAKEMOTO J K, DAVIES N M, et al. Pharmacokinetics and nephrotoxicity of amphotericin B-incorporated poly(ethylene glycol)-block-poly(-hexyl stearate l-aspartamide) micelles[J]. Journal of Pharmaceu- tical Sciences, 2011, 100(6): 2064-2070.
[10] TOLLEMAR J, ANDERSSON S, RINGDEN O, et al. A retrospective clinical comparison between antifungal treatment with liposomal amphotericin B (AmBisome) and conventional amphotericin B in transplant recipients[J]. Mycoses, 1992, 35: 215-220.
[11] JAIN J P, KUMAR N. Development of amphotericin B loaded polymersomes based on (PEG)(3)-PLA co-polymers: factors affecting size andevaluation[J]. European Journal of Pharmaceutical Sciences, 2010, 40(5): 456-465.
[12] 朱丽君,潘仕荣. 两性霉素B/聚乙二醇-聚天冬氨酸苄酯嵌段共聚物纳米粒胶束的制备与性能[J]. 中国药学杂志, 2010, 45(5): 359-365.
[13] 杨卓理,杨可伟,李馨儒, 等. 两性霉素B的聚乙二醇一聚乳酸胶束的制备及其体外释放动力学[J]. 中国药学杂志, 2007, 42(7): 519-526.
[14] LAVASANIFAR A, SAMUEL J, GLEN S, et al. self-assembled from poly(ethylene oxide)-block-poly(-hexyl stearate-aspartamide) by a solvent evaporation method: effect on the solubilization and haemolytic activity of amphotericin B[J]. Journal of Controlled Release, 2001, 77: 155–160.
[15] YAN Wang, LIU Yuanyuan, LIU Yang, et al. A polymeric prodrug of cisplatin based on pullulan for the targeted therapy against hepatocellular carcinoma[J].International Journal of Pharmaceutics, 2015, 483(1/2): 89-100.
[16] TANG Xiaojiao, HUANG Jun, XU Liangyu, et al. Microwave-assisted rapid synthesis, characterization and application of poly(-lactide)-graft-pullulan[J]. Carbohydrate Polymers, 2014, 107: 7–15.
[17] LEGRAND P, ROMERO E A, COHEN B E, et al. Effects of aggregation and solvent on the toxicity of amphotericin B to human erythrocytes[J]. Antimicrob Agents Chemother, 1992, 36: 2518–2522.
[18] BARWICZ J,CHRISTIAN S,GRUDA I.Effects of the aggregation state of amphotericin B on its toxicity to mice[J]. Antimicrobial Agents and Chemotherapy, 1992, 36(10): 2310-2315.
(本篇责任编辑:赵桂芝)
Preparation andcharacterization of amphotericin B poly(-lactide)-pullulan micelles
HUANG Jun, TANG Xiaojiao, MA Yue, SONG Juan, YANG LiPPPPPPP*
(,,110016,)
Objective To prepare and characterize the amphotericin B(AmB) loaded poly(-lactide) pullulan(PLA-pullulan) nanomicelles.Methods PLA-pullulan, a new amphiphilic polymer, was used for loading AmB with thin film dispersion method. The morphology, diameter and surface potential of the micelles were characterized by transmission electron microscopy, size and zeta potential analyzer. The drug loading content, entrapment efficiency andrelease of AmB loaded micelles were determined. The relative aggregation state of the encapsulated AmB and hemolytic toxicity were studied. Results The micelle was clear and transparent, globular shaped. The average particle size, drug loading content and entrapment efficiency were 152.1 nm with narrow distribution, 71.1% and 10.9%, respectively. The cumulative release amount of micelle within 24 h is 10.01%. AmB loaded micelles showed lower hemolysis than AmB solutions. Conclusions PLA-pullulan micelles, used as nanocarrier of amphotericin B, has a very good application prospect.
pharmaceutics; micelles; thin film dispersion method; amphotericin B; poly(-lactide)-pullulan;characterization
(2016)02–0033–10
10.14146/j.cnki.cjp.2016.02.001
R 94
A
2015-03-31
黄俊(1990-), 男(汉族), 湖北随州人, 硕士研究生, E-mail 834861227@ qq.com;
杨丽(1966-), 女(汉族), 吉林集安人, 教授, 博士, 博士生导师, 主要从事生物技术药物制剂学研究, Tel. 024-23986349, E-mail pharm305@126.com。
