一种特殊用途婴幼儿配方奶粉的理化性及蛋白质功效比分析
2017-01-14孙义玄邓杰郭明若王利王青云包怡红
孙义玄,邓杰,郭明若,王利,王青云,包怡红
(1.东北林业大学林学院,哈尔滨150040;2.吉林大学食品科学与工程学院,长春130062;3.黑龙江省完达山乳业股份有限公司,哈尔滨150060)
一种特殊用途婴幼儿配方奶粉的理化性及蛋白质功效比分析
孙义玄1,邓杰2,郭明若2,王利3,王青云3,包怡红1
(1.东北林业大学林学院,哈尔滨150040;2.吉林大学食品科学与工程学院,长春130062;3.黑龙江省完达山乳业股份有限公司,哈尔滨150060)
研制了一种特殊用途婴幼儿配方奶粉,并对其理化性及功能性进行研究。通过大鼠生长实验,测定蛋白质功效比值(Protein Efficiency Ratio,PER)。结果表明:研制出的配方奶粉化学成分与设计值相符。渗透压734.08 kPa,符合婴幼儿体液平衡的需求。奶粉的流动性评价和溶解度良好。研制奶粉组动物的体重增长率是酪蛋白组动物体重增长率的2.19倍,与进口市售同类奶粉组动物增重率无显著性差异。研制奶粉的PER为4.2,与进口市售婴幼儿奶粉相同,是酪蛋白组PER的1.69倍。研制奶粉具有较好的促进生长能力,为研制具有特殊功效的婴幼儿配方奶粉奠定了基础。
配方奶粉;理化性;功能性;蛋白质功效比值
0 引 言
婴幼儿配方奶粉是指以牛乳羊乳及其加工制品为主要原料,加入适量的维生素、矿物质和其他辅料加工而成的[1-2]。而母乳化配方奶粉则是以母乳为标准,使其最大限度地接近母乳,符合婴儿消化吸收的特性并达到其营养需求[3-5]。
模拟人乳的母乳化婴儿配方奶粉需要多个步骤才能逐步实现[6-7]。蛋白质功效比值(protein efficiency ratio,PER)是测定蛋白质生物利用率最常用的方法[8]。任何蛋白质的PER都可以用参比酪蛋白的PER值2.5校正测得的PER值来表示[9-10]本研究设计了一款适合于婴幼儿甚至早产和低出生体重儿食用的配方奶粉,进行功能性分析研究,应用GB10767-1997[11]和 AOAC 960.48[12]标准开展大鼠生长动物实验,测定特殊用途婴幼儿配方奶粉的PER。为系列婴幼儿奶粉的研究提供理论基础。
1 实 验
1.1 材料与仪器
特殊用途婴幼儿配方奶粉(由吉林大学功能乳品研究室提供),进口市售婴幼儿奶粉。
实验鼠清洁级初断乳的SPF级雄性Wistar大鼠36只,体质量60 g左右,鼠龄21 d。
无水脂肪、浓硫酸、盐酸、硼酸、硫酸铜、硫酸钾、氢氧化钠、无水乙醇、甲基红、溴甲酚绿、过氧化氢、无水乙醚、石油醚、氨水、碘溶液、活性炭、乙酸镁。
消化装置,滴定装置,天平,水分分析仪,万用电磁炉,送风干燥箱。
1.2 方法
1.2.1 配方奶粉工艺流程
鲜乳验收→净乳→降温暂存→配料→预热→均质→冷却暂存→杀菌→浓缩→喷雾干燥→接粉→冷却→包装→检验→入库→出厂
1.2.2 奶粉的设计配方
特殊用途婴幼儿配方奶粉研制依据的国家标准,GB 14880-2012,即《食品营养强化剂使用标准》;GB 2760-2011,即《食品添加剂使用标准;GB 10765-2010,即《婴儿配方食品》;GB 25596-2010,即《特殊医学用途婴儿配方食品通则》;
其中,对促进婴幼儿生长配方产品要求如下:1.能量、蛋白质及某些矿物质和维生素的含量应高于本标准第4.4项必需成分的相关规定;2.促进婴幼儿生长配方应采用容易消化吸收的中链脂肪酸作为脂肪的部分来源,但中链脂肪酸不应超过总脂肪的40%。检测相应指标时,应符合2010版的GB 5413系列婴幼儿食品和乳品中成分的测定标准。根据此原则分别得到实验室小试产品和中试产品,作为后期实验原料。
1.2.3 奶粉理化成分分析
按照GB 10765-2010《婴儿配方食品》的要求,对婴儿配方奶粉各项指标进行检测。
1.2.4 奶粉渗透压测定
测渗透压时,用50 ℃新制的蒸馏水按照设计的冲调比例溶解一定量的自制奶粉,恒温50 ℃磁力搅拌1 h,使奶粉充分溶解,得到比较稳定的渗透压。仪器用室温25℃的蒸馏水调零后,对样品进行测定,至少做3次平行实验[13]。
1.2.5 粉体物性分析方法
将自制特殊用途婴幼儿配方奶粉混合均匀后取样,按照相应操作要求进行粉体流动性评价检测。
粉体的流动性是固体制剂制备过程中必须考虑的重要性质,流动性不仅影响正常的生产过程,而且影响制剂质量,如重量差异和含量均匀度等。
(1)休止角。本次研究使用英国Copley公司的粉末流动性测试仪BEP2以固定圆锥法进行测定。
(2)压缩度。将待测奶粉样品精密称定后,轻缓地加入量筒中,测量体积,记算松装密度;然后按照GB/ T 21354-2008/ISO 3953:1993《粉末产品振实密度测定通用方法》的要求测量振实密度。压缩度为
C=(ρf-ρ0)/ρf,
式中:C为压缩度;ρf为振实密度;ρ0为松装密度。
1.2.6 溶解性评价
根据GB 5413.29-2010,即《婴幼儿食品和乳品溶解性的测定》方法对自制特殊用途婴幼儿配方奶粉和市售婴幼儿奶粉分别进行检测[14]。
1.2.7 动物实验
1.2.7.1 动物选择
清洁级初断乳的SPF级雄性Wistar大鼠36只,体质量60 g左右,鼠龄21 d。
1.2.7.2 动物分组
将动物按照体质量随机分为3组,每组12只,分别喂食不同饲料。组1为参比组,饲料中蛋白质来源仅为ANRC参比酪蛋白;组2为目标实验组,饲料中蛋白质来源仅为自制婴幼儿配方奶粉;组3为对比实验组,饲料中蛋白质来源仅为市售婴幼儿奶粉。
各组饲料中蛋白质质量分数均为8.0%,脂肪质量分数均为16.4%,总碳水化合物质量分数均为64.6%,其中乳糖质量分数均为43.5%。
1.2.7.3 实验期
适应期:开始实验前,动物需先经过7 d的适应环境阶段。所有动物均在不锈钢大鼠笼内单独饲养,自由进食普通饲料、自由饮水。
实验期:实验期28 d,在此期间,动物单笼饲养,分别喂各组实验饲料。动物自由摄食及饮水。在实验期间尽可能保持实验组动物与参考(标准)酪蛋白组动物的全部环境条件一致。
实验期间记录内容:①实验开始时每只大鼠的体质量(精确至0.1g);②每天各只大鼠的体重和饲料摄取量;③实验最后一天记录大鼠的体重和摄食量[15-16]。
2 结果与分析
2.1 理化成分
成分分析包括蛋白质、脂肪、碳水化合物、灰分、各种维生素与矿物质等项目的含量测定,结果如表1所示。
由表1可以看出,各项指标均与设计值相近,尤其是蛋白质、脂肪、碳水化合物无论是小试还是中试产品均与设计值非常接近;而水分、灰分、胆碱、亚油酸、亚麻酸和牛磺酸中试比小试略有提高;矿物质质量分数和维生素质量分数普遍小试较高而中试接近,高于设计值;钙、镁、硒、碘和维生素B1小试质量分数比设计值略低,可能是由于小试中产量小,添加的成分太少导致混合不均匀而致。
2.2 渗压测定
小试和中试生产的自制特殊用途婴幼儿配方奶粉与进口市售婴幼儿奶粉按照同样的比例12.9 g粉:90 mL温开水分别冲调,测定的渗透压值结果如表2所示。
小试产品渗透压低于进口市售产品,经过调整后,中试生产的自制特殊用途婴幼儿配方奶粉的渗透压检测值与进口市售婴幼儿奶粉相同。渗透压与溶液中离子含量具有直接的关系,由于婴幼儿的肾脏发育不完全,较高渗透压的产品不易消化吸收,并且影响到肾脏等相关泌尿系统的发育,因此在国外同类产品中往往要测定产品的渗透压,但此项指标在我国文献中少有报道。
2.3 奶粉流动性评价
2.3.1 休止角分析
对自制特殊用途婴幼儿配方奶粉和进口市售婴幼儿奶粉分别进行休止角的测定,结果如表3所示。
在测定粉体流动性时休止角是指粉体堆积体形成的坡面与水平面所成的最大角。休止角的大小说明粒子与水平表面或者粒子之间相互摩擦力的大小,休止角越小表明流动性越好,反之,则流动性越差。休止角受到多种因素的综合影响,包括物料混合程度、颗粒大小、表面性质、荷电、湿度、堆积体的颗粒位置分布等[17]。休止角的测定是检验粉体流动性好坏的最简便的方法[18]。有研究表明,在一定的冲击高度下,角度测定数值与冲击高度基本符合线性关系[19]。

表1 自制婴幼儿配方粉成分检测结果

表2 渗透压测定结果

表3 奶粉休止角的测定结果
当粉末从75 mm高度落下时,将自制特殊用途婴幼儿配方奶粉与对照奶粉的休止角作比较,P=0.145,因为P>0.05,故二者方差为齐性。“单因素ANOVA”分析结果,P为0,故二者在75 mm时休止角差异极显著。当粉末从80 mm高度落下时,方差齐性检验结果中P为0.055,由于P>0.05,故二者方差为齐性。“单因素ANOVA”分析结果中P为0.002,由于P小于0.01,故二者在80 mm时休止角差异极显著。当粉末从85 mm高度落下时,方差齐性检验结果中P为0.656,由于P>0.05,故二者方差为齐性。“单因素ANOVA”分析结果显示P=0,故二者在85 mm时休止角差异极显著。从分析结果可以看出无论受试奶粉从75,80 mm还是85 mm下落,自制特殊用途婴幼儿配方奶粉的休止角总是显著小于对照的进口奶粉,说明研制奶粉的流动性更好。检测时,自制奶粉的水分质量分数在1%左右,低水分质量分数使得粉粒间作用力较小,从而获得较低的粘度,体现出更好的流动性。
2.3.2 压缩度分析
对自制特殊用途婴幼儿配方奶粉和进口市售婴幼儿奶粉分别进行压缩度的测定,结果如表4所示。

表4 奶粉压缩度的测定结果
压缩度表示振动流动时粉体的流动性,可评价振动加料、振动筛振动填充与振动流动等。粉末的振实密度对于粉末产品的包装、贮存和运输用容器的设计具有指导作用。实践证明,压缩度在20%以下时流动性较好,当压缩度达到40%~50%时粉体很难从容器中流出[20]。
研制奶粉与进口市售婴幼儿奶粉比较,P=0.630,因为P>0.05,故二者方差为齐性。“单因素ANOVA”分析结果,P为0.113,由于P大于0.05,故二者压缩度无显著性差异。从实验结果可以看出,自制特殊用途婴幼儿配方奶粉与进口市售婴幼儿奶粉的压缩度相近。
2.4 奶粉溶解性分析
对自制特殊用途婴幼儿配方奶粉和进口市售婴幼儿奶粉分别进行溶解性的测定,结果如表5所示。

表5 奶粉溶解性和pH值的测定结果 %
从实验结果可以看出,对于溶解性,自制奶粉P= 0.468(P>0.05),故二者方差为齐性。“单因素ANOVA”分析结果,P=0.078(P>0.05),故二者溶解性无显著差异;对于pH值,自制奶粉P=0.561(P>0.05),故二者方差为齐性。“单因素ANOVA”分析结果,P=0.005(P小于0.01),故二者pH值具有极显著性差异。综上,这款自制奶粉的溶解性较对照的进口市售奶粉略低,而pH值略高,二者溶解性差异不显著,pH值差异极显著,但是二者均在人体可摄入的pH值范围之内。
2.5 动物饲料配方及日粮制作
参照《中华人民共和国国家标准GB10767-1997婴幼儿配方粉及婴幼儿补充谷粉通用技术条件》饲料标准配制。各组饲料制作时的配料如表6所示,各原料混合后成品饲料中各种成分质量分数如表7所示。向南通特洛菲饲料科技有限公司定制3种混合均匀的实验用饲料各8 kg,真空密封包装邮寄到动物饲养室,置于4℃冷藏。

表6 实验动物饲料的配料 %

表7 实际测得饲料中成分质量分数 %
2.6 动物实验结果分析
2.6.1 大鼠体质量变化情况
实验期开始时,参比酪蛋白组,自制特殊用途婴幼儿配方奶粉组和进口市售婴幼儿奶粉组实验动物的体质量经统计分析表明,差异无统计学意义(P>0.05)。

图1 大鼠体质量随时间变化
图1为实验期实验大鼠的体重随喂养时间变化。图1中,L代表酪蛋白组,Z代表自制特殊用途婴幼儿配方奶粉组,H代表对照市售婴幼儿奶粉组。由图1可以看出,三组大鼠实验期间体重均稳步增长,自制奶粉组和对照奶粉组动物体重增加趋势明显超过酪蛋白组。经SPSS检验,三组实验鼠体质量之间P=0.872(>0.05),故三组试验鼠体质量随时间的变化之间方差齐性。将研制奶粉组与酪蛋白组大鼠体质量相比较,P=0(<0.01),差异极显著,将自制奶粉组与对照奶粉组相比较,P=0.750(>0.05),无显著性差异。

表8 实验大鼠体质量增长情况
表8中,L代表酪蛋白组,Z代表自制促进婴幼儿生长配方奶粉组,H代表对照进口市售婴幼儿奶粉组。此表列出实验期间大鼠的初始体质量、结束体质量、增质量和增重率,可以看出研制奶粉组和对照奶粉组的体质量增重率均明显高于酪蛋白组,但是研制奶粉组与对照进口市售奶粉组增重率的差异并不显著。研制奶粉组动物的体质量增长率约是酪蛋白组动物体质量增长率的2.19倍。
2.6.2 大鼠日摄食量变化情况
实验期间,每天早上在相同时间点记录大鼠的摄食量,实验结果如图2所示。
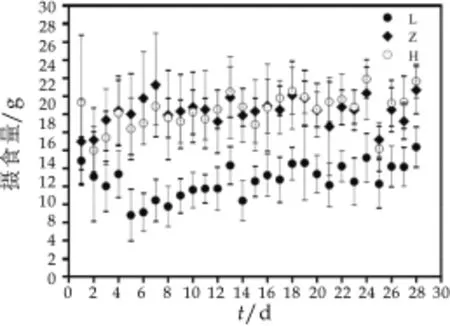
图2 大鼠摄食量随时间变化
由图2可以看出,三组大鼠实验期中每日的摄食量随喂养时间变化的情况。实验期28天中,三组试验鼠日摄食量之间方差齐性P=0.412(>0.05),故三组实验鼠日摄食量随时间的变化之间方差齐性。进一步分析组间日摄食量得到,自制奶粉组与酪蛋白组相比较,P= 0(<0.01),差异极显著,但是自制奶粉组与对照奶粉组相比较P=0.652(>0.05),差异不显著。
2.6.3 PER值的比较分析
表9中所示为实验期间三组大鼠的体质量总增质量、总摄食量和PER值,可以看出研制奶粉组和对照奶粉组的PER均明显高于酪蛋白组,但是研制奶粉与对照进口市售奶粉差异不大。经SPSS检验,三组受试蛋白PER之P=0.187(>0.05),故三组受试蛋白PER随喂养时间的变化之间方差齐性。进一步分析得到,研制奶粉组与酪蛋白组相比较,P=0(<0.01),差异极显著,自制奶粉组与对照奶粉组相比较,P=0.936(>0.05),差异不显著。研制奶粉组的PER约是参比酪蛋白组PER的1.69倍。
国际AOAC规定,受试蛋白质质量与酪蛋白对照组相比较,PER大于2.0的蛋白质通常认为是高质量,1.5~2.0为中等质量,而小于1.5则认为质量较低。

表9 实验大鼠PER计算结果
实验结果显示,参比酪蛋白的PER为1.61,校正后,自制促进婴幼儿生长配方奶粉的PER为4.2,与作为对照的进口市售婴幼儿奶粉PER相同,具有很好的促进生长能力,说明受试奶粉含有高质量的蛋白质,受试奶粉的蛋白质营养价值较高。
3 结 论
本研究对研制出的特殊用途婴幼儿配方奶粉进行化学成分分析,结果与设计值相符,研制奶粉的渗透压为734.08 kPa,与对照市售奶粉的渗透压相同,符合婴幼儿体液平衡的需求。无论受试奶粉从75,80 mm还是85 mm下落,自制促进婴幼儿生长配方奶粉的休止角总是显著小于对照的进口奶粉。研制奶粉与对照进口奶粉的压缩度无显著性差异。两款奶粉的溶解性无显著差异。
大鼠生长实验结果显示,研制奶粉组动物的体质量增长率约是酪蛋白组动物体质量增长率的2.19倍,研制与进口市售奶粉组动物增重率无显著性差异。研制奶粉的PER为4.2,与进口市售婴幼儿奶粉相同,是参比酪蛋白组PER的1.69倍,研制奶粉和对照的进口奶粉都具有很好的促进生长能力。
[1]李晓东,蒋琛.我国婴幼儿配方奶粉生产技术的现状及展望[J].乳业科学与技术,2013,36(2):34-38.
[2]HOVI P,ANDERSON S,ER IKSSON J G,et al.Glucose regulation in young adults with very low birth weight[J].New England Journal of Medicine,2007,356(20):2053-2063.
[3]HAY WW JR,LUCAS A,HEIRD W C,et al.Workshop summary:nutrition of the extremely low birthweighr infant[J]..Pediatrics,1999,104 (6):1360-1368.
[4]LOU IA,RAAB A,OBLADEN M,et al.Nutritional zinc balance in extremely low-birth-weight infants[J].Journal of Pediatric Gastroenterology and Nutrition,2001,32(4):438-442.
[5]CATHERINE J.Nutrient requirements for preterminfant formulas[J]. Journal of Nutrition,2002,132(6):l395s-1577s.
[6]PLAZA-ZAMORA J,SABATER-MOLINA M,Rodriguez-Palmero M,et al.Polyamines in human breast milk for preterm and terminfants [J].British Journal of Nutrition,2013,110(3):524-528.
[7]JUN W,XIAN-WEIC,JUN Z,et al.Peptidome analysis of human skim milk in term and preterm milk[J].Biochemical and Biophysical Research Communications,2013,438(1):236-241.
[8]郭明若.功能性食品学[M].北京:中国轻工业出版社,2011:207.
[9]KREISSL A,ZWIAUER V,REPA A,et al.Effect of fortifiers and additional protein on the osmolarity of human milk:Is it still safe for the premature infant[J].Journal of Pediatric Gastroenterology and Nutrition, 2013,57(4):432-437.
[10]刘晓娜.极低出生体重早产儿肠道内喂养新进展[J].护理实践与研究,2012(1):134-135.
[11]GB10767-1997《婴幼儿配方粉及婴幼儿补充谷粉通用技术条件》.
[12]RAITEN D J,Talbot JM,W aters JH.Assessment of nutrient requirements for infant formulas[R].Prepared by the Life Sciences Research O ffice,9650 Rockville Pike,Bethesda MD.The Journal of Nutrition, 1998,128(Supplement11S):2059s-2294s.
[13]RAGHAVENDRA R,GEORGIEFF M K.Iron therapy for preterminfants[J].Clinics in Perinatology,2009,36(1):27-42
[14]GB5413.29-2010,婴幼儿食品和乳品溶解性的测定[S].北京:中华人民共和国卫生部,2010.
[15]JIMENEZ MAR IA J,ESTEBAN L,ROBLESA.Production of triacylglycerols rich in palmitic acid at position 2 as intermediates for the synthesis of humanmilk fat substitutes by enzymatic acidolysis[J].PROCESS,2010,45(3):407-414.
[16]LUCAS A,FEWTRELL M S,MORLEY R,et al.Randomized trial of nutrient-enriched formula versus standard formula for postdischarge preterminfants[J].Pediatrics,2001,108(3):703-711.
[17]李艳洁,徐泳.用离散元模拟颗粒堆积问题[J].农机化研究,2005,(2): 57-58.
[18]董玉秀,宋珍鹏,崔素娟.对休止角测定方法的讨论[J].中国药科大学报,2008,39(4):317-320.
[19]於海明,龚红菊,韩英.谷物休止角圆盘式快速测试仪的设计GN试验[J].粮油加工与食品机械,2005,(12):75-76.
[20]GB/T 21354-2008/ISO 3953:1993,粉末产品振实密度测定通用方法[S].北京:中华人民共和国国家质量监督检验检疫总局与中国国家标准化管理委员会,2008.
Physical,chemical and functional analysis of a special infant formula
SUN Yi-xuan1,DENG Jie2,GUO Ming-ruo2,WANG Li3,WANG Qing-yun3,BAO Yi-hong1
(1.College of Forestry Nurtheast Forestry University,Harbin 150040,China;2.College of Food science and Engineering,Jilin University,Changchun 130062,China;3.Heilongjiang Wondersun Dairy Co.,Ltd,Harbin 150060,China)
A special infant formula(SIF)was developed and analyzed for physicochemical properties and protein efficiency ratio(PER).Results showed that chemical composition of SIF fitted the designed values and osmolality met the needs of infant isohydria with a value of 734.08kPa.The new SIF exhibited better fluidity and solubility.Growth rate of rats in the SIF group was 2.19 times of casein group,and there was no significant difference in PER between the SIF group and commercial control group.SIF showed a similar value of PER to commercial control group with the value of 4.2,compared with the value of casein group 2.5.Results indicated that the new product may enhance infants’growth effectively and provide theory basis for development of special infant formula.
special infant formula;physicochemical properties;PER
TS252.51
A
1001-2230(2016)05-0004-05
2016-01-16
孙义玄(1990-),男,博士研究生,研究方向为功能性食品。
包怡红
