双霉菌混合发酵腐乳前发酵条件优化及酶活研究
2017-01-13顾永忠陈小举吴学凤姜绍通李兴江
李 顺,顾永忠,郑 志,陈小举,吴学凤,姜绍通,李兴江,*
(1.合肥工业大学食品科学与工程学院,农产品精深加工安徽省重点实验室,安徽合肥 230009;2.安徽八公山豆制品有限公司,安徽寿县 232200;3.巢湖学院化学化工与生命科学学院,安徽巢湖 238000)
双霉菌混合发酵腐乳前发酵条件优化及酶活研究
李 顺1,顾永忠2,郑 志1,陈小举3,吴学凤1,姜绍通1,李兴江1,*
(1.合肥工业大学食品科学与工程学院,农产品精深加工安徽省重点实验室,安徽合肥 230009;2.安徽八公山豆制品有限公司,安徽寿县 232200;3.巢湖学院化学化工与生命科学学院,安徽巢湖 238000)
八公山腐乳前发酵工艺对其总体风味具有重要影响,在总状毛霉和米根霉单独发酵腐乳的基础上,探索总状毛霉(Mucorracemosus)和米根霉(Rhizopusoryzae)混合发酵腐乳的发酵工艺。在单因素的基础上,以蛋白酶活力和糖化酶活力为评价指标,选取发酵时间、发酵温度和混合比例为影响因子,采用响应面法优化总状毛霉和米根霉混合发酵腐乳的前发酵条件,比较最优条件下混合发酵和总状毛霉与米根霉单独发酵的前发酵情况。研究结果表明总状毛霉和米根霉混合发酵的前发酵条件为:发酵时间56 h、发酵温度28 ℃、混合比例(总状毛霉和米根霉)1∶1,此时分泌产蛋白酶活力50.51 U/mL,糖化酶活力为15.15 U/mL。通过对比双菌和单菌发酵腐乳前发酵情况可知:总状毛霉和米根霉混合发酵较总状毛霉更能耐高温,且在菌丝的生长和酶系的分泌积累较单独发酵都更有优势,为后期发酵的一系列生化反应奠定了良好的基础,有利于改善腐乳的发酵周期,提高腐乳的品质。
腐乳,总状毛霉,米根霉,混合发酵,前发酵
腐乳是在豆腐的基础上利用微生物发酵的大豆制品,因其具有良好的感官性能且营养丰富,而深受我国百姓喜爱[1-3]。工业发酵腐乳常用菌为毛霉菌属和根霉菌属,少量利用细菌发酵(克东腐乳)[4-5]。我国各地所产的腐乳在口感风味、理化性质、感官性质和功能活性方面各有差异,这可能是由于毛霉菌属、根霉菌属以及各种发酵腐乳的微生物在发酵分泌的酶不尽相同[6-7]。腐乳酿造过程中,主要的生化变化就是蛋白酶将豆腐中的蛋白质分解成多肽、氨基酸等小分子化合物并形成风味物质[8-12]。毛霉菌属分泌蛋白酶量较大,但是不耐高温;根霉菌属虽然分泌蛋白酶能力较弱,但是其耐高温且可以分泌较多的其他糖化酶、脂肪酶等酶系[13-15]。
目前我国腐乳的生产主要利用单一菌种发酵,然而采用单一菌种发酵或自然发酵,存在酶系不全,风味单一等问题[16-17]。本研究主要结合安徽地方特色食品――八公山腐乳,研究总状毛霉和米根霉混合发酵腐乳的前发酵工艺优化,以期丰富前发酵的酶类,改善理化性质,丰富风味物质的同时优化腐乳的发酵条件和发酵周期,为腐乳的研究和生产提供理论和实践基础。
1 材料与方法
1.1 材料与设备
豆腐 安徽八公山豆制品有限公;总状毛霉(MucorracemosusCICC 40481) 中国工业微生物菌种保藏中心;米根霉(Rhizopusoryzae) 合肥工业大学农产品加工研究院保藏菌种;福林酚试剂 生物试剂纯,上海振企化学试剂有限公司;磷酸氢二钠 分析纯,天津市四友精细化学品公司;氯化钠、磷酸二氢钠、干酪素、碳酸钠、三氯乙酸、乙酸钠、氢氧化钠 均为分析纯,国药集团;PDA培养基 实验室配制。
HH.B11420-BS型电热恒温培养 上海跃进医疗器械厂;SWO-CJ-1F超净工作台 苏静集团泰安公司;721G紫外分光光度计 上海精密科学仪器有限公司;HC-3018R高速冷冻离心机 安徽中科中佳科学仪器公司;手提式压力蒸汽灭菌器 宁波开普电子仪表有限公司;BST-801放大镜 贝斯特科技有限公司;B203LD生物显微镜 重庆奥特光学仪器有限公司。
1.2 实验方法
1.2.1 菌种活化及孢子悬液的制备 将总状毛霉和米根霉分别接种于PDA斜面,分别置于26 ℃和30 ℃条件下培养5 d,置于4 ℃冰箱保存,使用前向斜面加入20 mL无菌水冲洗,并用接种环刮划,充分振荡,用双层擦镜纸过滤至三角瓶中,通过血球计数板计数并调节孢子悬液浓度为1×105CFU/mL[18]。孢子悬液现配现用。
1.2.2 腐乳坯的制备 豆腐切块摆放好,通过高压喷壶喷洒接种一定比例的总状毛霉和米根霉混合孢子悬液,接种量每三块豆腐接种1 mL混合孢子悬液,置于霉菌培养箱中,控制培养箱湿度在80%以上,在一定温度条件下培养一定时间,制得腐乳坯。
1.2.3 腐乳样品前处理 将1.2.2中制备的腐乳毛坯充分研磨,准确称取5 g,加20 mL 0.15 mol/mL的氯化钠溶液,在40 ℃水浴中加热不断搅拌,浸提1.5 h后离心取上清液。
1.2.4 腐乳毛坯感官属性评价 用放大镜观察不同发酵方式发酵的腐乳坯上霉菌生长情况,由8名同课题组同学组成评定小组,对霉菌的密度、菌丝的粗壮程度以及霉菌产孢子量对腐乳坯体上霉菌生长情况进行综合评分,取其平均数[18-19]。评分标准见表1。
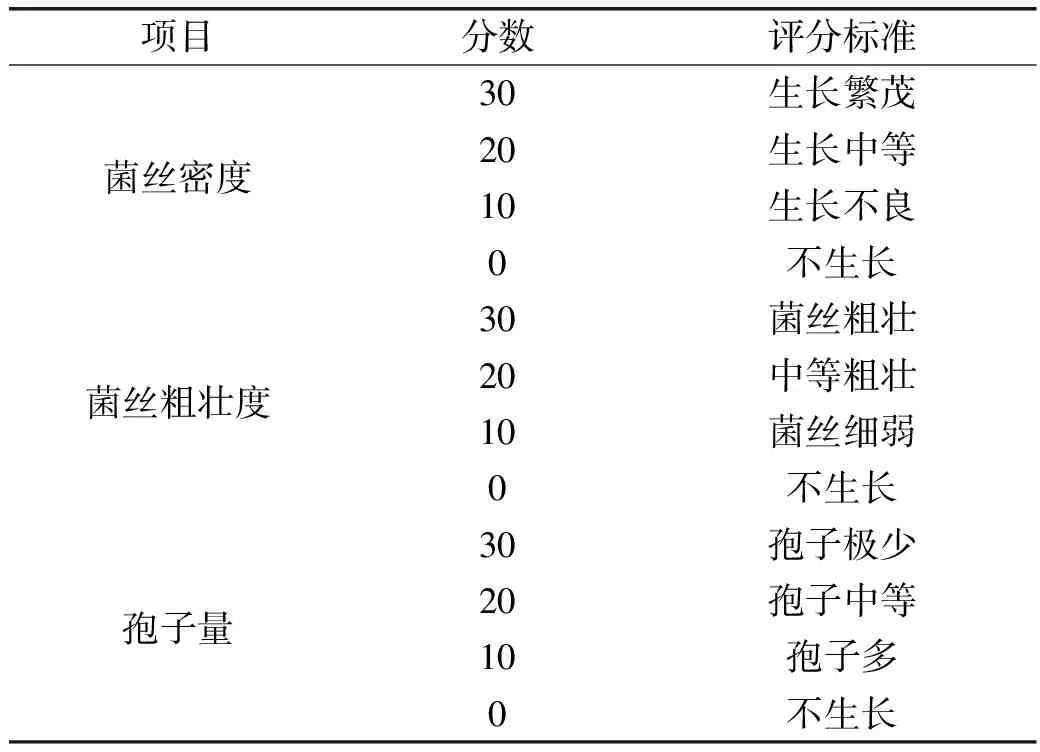
表1 霉菌生长情况评分标准
1.3 测定方法
1.3.1 蛋白酶活力 采用福林酚法测定,40 ℃、pH7.2条件下,1 min水解酪蛋白产1 μg酪氨酸所需要的酶量,定义为1个酶活力单位[20]。
1.3.2 糖化酶活力 采用碘量法测定,40 ℃、pH4.6条件下,1 h水解可溶性淀粉产生1 mg葡萄糖所需的酶量,定义为1个酶活力单位[21]。
1.3.3α-淀粉酶活力 采用3,5-二硝基水杨酸(DNS)法进行测定,在40 ℃、pH5.6条件下,1 min水解淀粉产1 μg麦芽糖所需要的酶量,定义为1个酶活力单位[22]。
1.3.4 脂肪酶活力 采用PVA-橄榄油乳化液水解滴定法进行测定,将在40 ℃、pH7.5条件下,1 min水解底物产生1 μmol可滴定的脂肪酸所需要的酶量,定义为1个酶活力单位[23]。
1.4 前发酵条件优化的单因素实验
通过对总状毛霉和米根霉单独发酵腐乳前发酵条件优化得到二者的接种量均为每三块豆腐接种1 mL浓度为1×105CFU/mL的孢子悬液。在总状毛霉和米根霉单独发酵的基础上选取发酵时间、发酵温度、混合菌种比例为单因素考察混合霉菌发酵腐乳的前发酵情况。
1.4.1 发酵时间对前发酵的影响 选取发酵温度28 ℃,总状毛霉和米根霉的混合比例1∶1,选取发酵时间分别为50、52、54、56、58、60 h,考察发酵时间对总状毛霉和米根霉混合发酵的影响。
1.4.2 发酵温度对前发酵的影响 选取发酵时间56 h,总状毛霉和米根霉的混合比例1∶1,选取发酵温度分别为24、26、28、30、32 ℃,考察发酵温度对总状毛霉和米根霉混合发酵的影响。
1.4.3 总状毛霉和米根霉的混合比例对前发酵的影响 选取发酵时间56 h,发酵温度28 ℃,选取总状毛霉和米根霉的混合比例分别为3∶1、2∶1、1∶1、1∶2、1∶3,考察混合比例对前发酵的影响。
1.4.4 前发酵条件的响应面优化实验 在单因素实验结果的基础上,以前发酵分泌蛋白酶活力和糖化酶活力为响应值,采用Design Expert软件中的Box Behnken实验,优化总状毛霉和米根霉混合发酵的前发酵条件[24-25],响应面设计见表2。

表2 前发酵条件Box-Benhnken设计实验因素水平及编码
1.5 数据处理
所有实验重复三次,应用Origin 9.1软件作图,采用Design-Expert V8.0.6处理数据。
2 结果与分析
2.1 前发酵单因素实验
2.1.1 发酵时间对前发酵蛋白酶及糖化酶活力的影响 考察不同发酵时间对前发酵蛋白酶及糖化酶活力的影响,结果如图1所示。

图1 发酵时间对前发酵蛋白酶及糖化酶活力的影响Fig.1 Effect of fermentation time on the pre-fermentation of the protease and glucoamylase
随着培养时间的增加,霉菌开始生长繁殖,蛋白酶和糖化酶活力呈现先增加后下降的趋势。发酵时间56 h时蛋白酶和糖化酶的酶活力都达到最大值,酶活力分别为50.67 U/mL和14.21 U/mL。随着发酵时间的继续增加,蛋白酶和糖化酶的活力均呈现下降的趋势。这是由于随着发酵时间的增加,总状毛霉和米根霉菌丝出现老化,同时代谢副产物的增加,从而减慢了酶的分泌。因此选择发酵时间56 h。
2.1.2 发酵温度对前发酵蛋白酶及糖化酶活力的影响 考察不同发酵温度对前发酵蛋白酶及糖化酶活力的影响,结果如图2所示。

图2 发酵温度对前发酵蛋白酶及糖化酶活力的影响Fig.2 Effects of fermention temperature on the pr-fermentation of the protease and glucoamylase
发酵温度过低不利于总状毛霉和米根霉的菌丝生长从而影响了酶量的分泌,随着发酵温度的增加蛋白酶活力和糖化酶活力由于菌种的生长繁殖而逐渐递增。在28 ℃时两者都达到一个峰值,随着温度的继续增加蛋白酶活力和米根霉活力都呈现下降的趋势,可能是因为温度超过28 ℃后总状毛霉的生长繁殖会受到抑制,酶活受到影响;温度过高致使水分散失过快,加快菌丝老化,蛋白酶和糖化酶活力受到影响呈现下降趋势[26]。由图2也可以看出在28 ℃之后随着温度的增加,蛋白酶活力的降低趋势明显大于糖化酶的下降趋势,这可能是由于总状毛霉最适发酵温度比米根霉低,而在发酵过程中总状毛霉主要产蛋白酶,米根霉主要产糖化酶,所以温度增加对蛋白酶活力影响要大于糖化酶。
2.1.3 混合比例对前发酵蛋白酶及糖化酶活力的影响 考察总状毛霉和米根霉混合的比例对前发酵蛋白酶及糖化酶活力的影响,结果如图3所示。

图3 混合比例对前发酵蛋白酶及糖化酶活力的影响Fig.3 Effects mix ratio of mould on the pr-fermentation of the protease and glucoamylase
由图3可知总状毛霉和米根霉的比例从3∶1~1∶1,发酵分泌糖化酶的活力随着米根霉的比例增大而逐渐增加;这期间虽然总状毛霉的比例在降低,然而蛋白酶活力也依然呈现上升的趋势,一方面米根霉也有不错的分泌蛋白酶的活力,其次可能是两者协同作用促进了酶的分泌。总状毛霉和米根霉的混合比例在1∶1时蛋白酶活力和糖化酶活力均到达峰值。随着米根霉的比例增加,蛋白酶活力和糖化酶活力都呈现下降的趋势。
2.2 响应面优化前发酵

表3 前发酵条件响应面设计及结果
2.2.1 回归模型的建立 以发酵时间(X1)、发酵温度(X2)和混合比例(X3)为自变量,总状毛霉和米根霉混合发酵产蛋白酶活力(Y1)和混合发酵产糖化酶活力(Y2)为因变量,建立回归模型方程分别为:

表4 蛋白酶活力回归模型方差分析表

式(1)
Y2=-1418.94503+40.75204X1+20.95967X2+4.57278X3-9.37500×10-3X1X2-3.3333×10-3X1X3+0.071667X2X3-0.36237X12-0.36675X22-2.69244X32
式(2)



表5 糖化酶活力回归模型方差分析
注:**表示差异极显著(p<0.01);*表示差异显著(p<0.05)。2.2.3 双因子效应分析 前期发酵分泌蛋白酶活力的双因子效应分析:根据回归方程及回归模型方差分析表绘出双因子效应图见图4~图6。

图4 时间和温度对蛋白酶活力影响的响应面图Fig.4 Three-dimensional plot and corresponding contour plot of the effect of time and temperature on activity of protease

图5 混合比例和时间对蛋白酶活力影响的响应面图Fig.5 Three-dimensional plot of the effect of mix ratio of mould and time on activity of protease
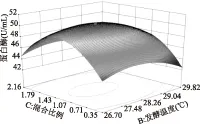
图6 混合比例和温度对蛋白酶活力影响的响应面图Fig.6 Three-dimensional plot of the effect of mix ratio of mould and temperature on activity of protease
由图4~图6所示,两两因素之间的影响基本呈抛物线型关系,均有极大点,变化趋势都是呈现先增大后减小的趋势;等高线主要说明两因素之间的交互作用,如果等高线呈圆形说明两因素之间的交互作用不显著,等高线呈椭圆或者马鞍形则说明因素之间交互作用显著,上图4~图6的等高线均呈椭圆形,结果均与模型方差分析一致。
前期发酵分泌糖化酶活力的双因子效应分析:根据回归方程及回归模型方差分析表绘出双因子效应图见图7~图9。

图7 时间和温度对糖化酶活力影响的响应面图Fig.7 Three-dimensional plot of the effect of time and temperature on activity of glucoamylase

图8 混合比例和时间对糖化酶活力影响的响应面图Fig.8 Three-dimensional plot of the effect of mix ratio of mould and time on activity of glucoamylase
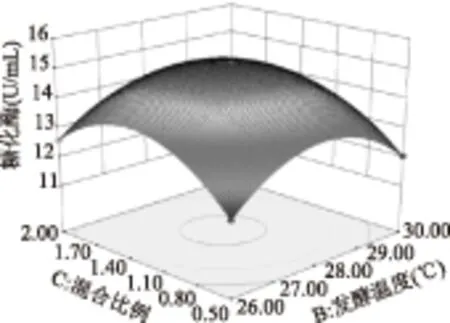
图9 混合比例和温度对糖化酶活力影响的响应面图Fig.9 Three-dimensional plot of the effect of mix ratio of mould and temperature on activity of glucoamylase
由图7~图9所示,两两因素之间的影响基本呈抛物线型关系,均有极大点,变化趋势都是呈现先增大后减小的趋势;等高线主要说明两因素之间的交互作用,如果等高线呈圆形说明两因素之间的交互作用不显著,等高线呈椭圆或者马鞍形则说明因素之间交互作用显著,图7、图9的等高线呈椭圆形,而图8的等高线则较圆,结果均与模型方差分析一致。
综上所述,通过结果分析和综合考虑得到总状毛霉和米根霉协同发酵腐乳的前发酵最优条件为:发酵时间55.78 h、发酵温度27.97 ℃、混合比例总状毛霉和米根霉1.19∶1,此时分泌产蛋白酶活力为50.57 U/mL,糖化酶活力为15.209 U/mL。
2.2.4 验证实验 为检验实验结果与真实情况的一致性,对上述最优条件进行验证实验。对最优结果进行修正为发酵时间56 h、发酵温度28 ℃、混合比例总状毛霉和米根霉1∶1,此条件下进行三次平行实验,测得蛋白酶活力的平均值为50.51 U/mL,糖化酶活力为15.15 U/mL。
2.3 混合发酵与单独发酵前发酵比较
前期对总状毛霉和米根霉单独发酵腐乳的前发酵条件进行优化,得到的最优条件:总状毛霉的前发酵条件为发酵时间60 h、发酵温度24 ℃、接种量为1×105CFU/mL,此时分泌产蛋白酶活力为42.70 U/mL,糖化酶活力为11.62 U/mL;米根霉的前发酵条件为发酵时间50 h、发酵温度32 ℃、接种量为1×105CFU/mL,此时分泌产蛋白酶活力为33.53 U/mL,糖化酶活力为13.72 U/mL。在此条件下制得腐乳坯,对比总状毛霉和米根霉混合发酵前期情况与单独发酵的前发酵情况,包括前发酵腐乳坯的霉菌生长情况即为腐乳坯的感官属性和前发酵产酶(蛋白酶活力、糖化酶活力、脂肪酶活力和α-淀粉酶活力)的比较,腐乳前发酵的好坏,直接影响到腐乳的品质和风味。
2.3.1 发酵腐乳坯的感官属性 腐乳坯是腐乳前发酵产物,腐乳的前发酵就是在腐乳上接种微生物(霉菌或者细菌),使微生物在豆腐坯上生长繁殖,菌丝得到充分生长后会在豆腐坯上形成一层坚韧细致的菌膜且能积累大量的酶类,为后期发酵奠定基础。霉菌的生长情况也直接反应了腐乳坯的品质,用放大镜观察霉菌生长情况及孢子量结果见表6,显微镜四倍镜下三种方法发酵腐乳坯霉菌的生长情况见图10。

图10 四倍镜下霉菌的形态Fig.10 Four times times the microscopic mould shape注:(a)为混合霉菌、(b)为米根霉、(c)为总状毛霉。

霉菌生长情况发酵方式总状毛霉米根霉混合菌种菌丝密度202030菌丝粗壮度203030孢子量203020
由图10和表6可知,由于总状毛霉和米根霉的协同作用混合菌种发酵的腐乳坯上霉菌的菌丝密度要比总状毛霉和米根霉单独发酵的密度大;混合菌种发酵和米根霉发酵的腐乳坯的菌丝粗壮度差异不大,比总状毛霉的更为粗壮;在产孢子量上混合菌种和总状毛霉发酵的腐乳坯要比米根霉少,更有利于酶的分泌。综合考虑霉菌的菌丝密度、菌丝粗壮度和产孢子量,混合菌种发酵的腐乳坯体霉菌生长情况更好,有利于分泌和累积酶类。
在相应的最佳前发酵条件发酵产的腐乳坯,总状毛霉和米根霉混合发酵的腐乳坯上的菌丝生长旺盛,菌丝浓密,并且在腐乳坯上形成一层致密的菌膜,而总状毛霉和米根霉各自单独发酵的腐乳坯体上的菌丝较为短小稀疏,不利于腐乳坯体外层菌膜的形成,同时也不利用酶系的累积。协同发酵菌丝生长更有优势,有利于酶类的积累,为后期发酵的生化反应提供基础,保证后期发酵腐乳坯体具有完整的块形和丰富的风味。
2.4 前发酵分泌酶系的比较
在验证实验过程中检测协同发酵腐乳前发酵的蛋白酶活力、糖化酶活力、脂肪酶活力和α-淀粉酶活力。与前期实验中测得的总状毛霉和米根霉单独发酵产腐乳坯的各种酶的活力的比较,如图11所示。

图11 混合发酵与单独发酵分泌酶系比较Fig.11 Comparison of enzyme activity withco-fermentation and separate fermentation
腐乳发酵过程中起主要作用的是蛋白酶,在蛋白酶作用下蛋白质被分解生产多肽和氨基酸,改变腐乳坯的内部结构,并且生产风味物质。由图11可知,总状毛霉和米根霉混合发酵腐乳前发酵的蛋白酶活力比二者单独发酵的要高,且比米根霉要高出很多。混合发酵分泌的糖化酶活力、脂肪酶活力和α-淀粉酶活力比总状毛霉发酵的活力要高。虽然混合发酵分泌的糖化酶活力、脂肪酶活力和α-淀粉酶活力没有米根霉发酵的酶活力高,但是也具有较高的活力。综合考虑三种发酵方式前发酵分泌各种酶活力可知,总状毛霉和米根霉混合发酵分泌的各种酶活都有较高的积累和活力,混合发酵不仅发挥二者单独发酵的优势,而且弥补了二者发酵的某些不足,比二者单独发酵更为全面。为后期发酵过程中的一系列生化反应奠定了良好的基础。
3 结论
以蛋白酶活力和糖化酶活力为指标,通过单因素和响应面实验优化总状毛霉和米根霉混合发酵腐乳的前发酵条件,得到混合发酵腐乳的前发酵最佳条件为:发酵时间56 h、发酵温度28 ℃、混合比例总状毛霉和米根霉1∶1,此条件下测得蛋白酶活力为50.51 U/mL,糖化酶活力为15.15 U/mL。
在此条件发酵的腐乳坯与总状毛霉和米根霉最优条件下单独发酵的腐乳坯比,混合发酵的腐乳坯上霉菌的菌丝密度和粗壮度要更好一点,同时产孢子量也少,有利于腐乳坯体外层菌膜的形成和酶系的积累,混合发酵分泌的酶系比总状毛霉和米根霉单独发酵更为全面丰富。
通过对比三种发酵方式,总状毛霉和米根霉混合发酵前发酵温度比总状毛霉前发酵温度高,且在菌丝的生长和酶系的分泌积累较单独发酵都更有优势。混合发酵腐乳在丰富了酶类积累的同时也提高了发酵的温度,弥补了单独发酵不足,也突出了单独发酵的优势,为后期发酵的一系列生化反应奠定了良好的基础,有利于提高腐乳的品质,丰富腐乳的风味。
[1]李幼筠,周逦.中国独具特色的发酵豆制品[J].中国酿造,2010,217(4):12-15.
[2]王瑞芝. 中国腐乳酿造[M]. 第二版.北京:中国轻工业出版社,2009:100-142.
[3]刘亚,杨光影,吴悦,等. 腐乳进展研究[J]. 农产品加工(学刊),2013,337(12):64-66.
[4]孙冰玉,邹丽宏,刘颖,等. 克东腐乳生产过程中酶活力的变化[J]. 中国食品学报,2015,15(6):227-230.
[5]李璘佼,车振明,汪彬彬. 腐乳中毛霉菌株的初步筛选及其培菌期的生化变化[J]. 中国调味品,2010,35(9):56-60.
[6]周锦秀,林奇,唐卿燕. 我国腐乳生产用菌研究现状[J].食品科技,2007,11(10):19-21.
[7]徐海帝,程永强,徐永伟,等. 发酵菌种对低盐白腐乳感官品质的影响[J].食品与发酵工业,2007,33(10):16-22.
[8]LI YY,YU RC,CHOU CC. Some Biochemical and Physical Changes during the Preparation of the Enzyme-Ripening Sufu,a Fermented Product of Soybean Curd[J]. Journal of Agricultural and Food Chemistry,2010,58(8):4888-4893.
[9]HANB Z,Rombouts F M,Nout M J R.A Chinese fermented soybean food[J]. International Journal of Food Microbiology,2001,65:1-10.
[10]ANDUIC S,GENCCELEP H,KOSE S.Determination of biogenic amines in herby cheese[J]. International Journal of Food Properties,2010,13(6):1300-1314.
[11]GUAN R F,LIU Z F,ZHANG J J,et al. Investigation of biogenic amines in sufu(furu):A Chinese traditional fermented soybean food product[J]. Food Control,2013,31:345-352.
[12]冉春霞,陈光静,阚建全. 响应面法优化全豆腐乳前发酵条件的研究[J]. 食品工业科技,2012,33(18):227-231.
[13]HUANG Y H,LU T J,CHOU C C. Ripening temperature affects the content and distribution of isoflavones in sufu,a fermented soybean curd[J]. International Journal of Food Science and Technology,2011,46(2):257-262.
[14]蒋芳芳,刘嘉,蒋立文. 腐乳品质改善的研究进展[J]. 中国酿造,2011,236(11):1-5.
[15]哈尔乐哈西·布勒斯别克.改善腐乳品质的加工工艺技术研究[D]. 杭州:浙江大学,2015:1-12.
[16]冉春霞,阚建全,全腐乳发酵菌种选择的实验研究[J]. 中国调味品,2015,18(40):1-4.
[17]陈治霖,和七一,陈斌.腐乳毛坯双菌制曲工艺的研究[J].中国调味品,2015,2(40):91-95.
[18]叶明.微生物学实验技术[M].第一版.合肥:合肥工业大学出版社,2009:61-63.
[19]侯美珍,宋德贵,韦平英.时间及温度对腐乳毛霉生长及产蛋白酶的影响[J].广西师范大学学报,2004,40(2):97-99.
[20]诺维信(中国)生物技术有限公司,张家港市金源生物化工有限公司,中国食品发酵工业研究院,等. GB/T 23527-2009 蛋白酶活力测定法[S]. 中国标准出版社,2009.
[21]山东沂水隆达生物工程有限公司,江阴市星达生化工程有限公司,湖南鸿鹰祥生物工程有限公司,等. GB/T 8276-2007糖化酶制剂[S]. 中国标准出版社,2007.
[22]曾东方,杨帆,聂欢欢. DNS法对食用菌发酵液淀粉酶活力的测定[J]. 现代农业科技,2011,6(11):16-18.
[23]中国食品发酵工业研究院,诺维信中国生物技术有限公司. GB/T 23535-2009脂肪酶制剂[S]. 中国标准出版社,2009.
[24]刘威,曹蕾蕾,陈春雨,等.少孢根霉发酵腐乳前酵条件优化及发酵全程质构的研究[J]. 食品工业科技,2014,35(18):228-231.
[25]樊巧,陈厚荣,徐晓萍,等.响应面实验优化酪蛋白-魔芋葡甘聚糖共混溶胶制备工艺及其稳定性[J]. 食品科学,2015,36(24):10-15.
[26]于艳琴,李璘佼,车振明.响应面法优化腐乳生产中的培菌条件[J]. 中国食品学报,2010,5(10):184-188.
Study on the optimization and enzyme activity of co-fermentation sufu pr-fermentation with double moulds
LI Shun1,GU Yong-zhong2,ZHENG Zhi1,CHEN Xiao-ju3,WU Xue-feng1,JIANG Shao-tong1,LI Xing-jiang1,*
(1.Key Laboratory for Agriculture Products Processing of Anhui Province,School of Biotechnology and Food Engineering Hefei University of Technology,Hefei 230009,China; 2.Anhui Bagongshan LTD,Shouxian 232200,China; 3.School of Chemistry and Biology Science Chaohu University,Chaohu 238000,China)
The pre-fermentation of bagongshan sufu had an important influence in the overall nutrition flavor.Based on the single fermentation ofMucorracemosusandRhizopusoryzae,the exploration for its fermentation process surrounding both common strain(MucorracemosusandRhizopusoryzae)was needed. According to the basic fermentation conditions,the fermentation time,fermentation temperature and ratio of strain were investigated through single factor experiment. On the basis of single factor experiment,the activities of protease and glucoamylase were as response value and the prophase fermentation of co-fermentation of sufu byMucorracemosusandRhizopusoryzaewas identifed using response surface methodology. The pr-fermentation was considered by comparing of co-fermentation and separate fermentation. The conditions of the multi-fermentation were found that the fermenting time was 56 h,fermenting temperature was 28 ℃,ratio of strain was 1∶1,and the activity of protease was 50.51 U/mL,the activity of glucoamylase was 15.15 U/mL. Through the comparison of both strains,the result indicated that the enzyme system and sensory attributes of sufu pehtez in co-fermentation was better than separate fermentation,which laid a theoretical foundation for later fermentation,improved the fermented sufu fermentation period and improved the quality of sufu.
sufu;Mucorracemosus;Rhizopusoryzae;co-fermentation;prophase fermentation
2016-04-14
李顺(1991-),男,硕士研究生,研究方向:食品科学,E-mail:lishun@mail.hfut.edu.cn。
*通讯作者:李兴江(1978-),男,博士,副教授,研究方向:发酵工程代谢调控,E-mail:lixingjiang1978@hfut.edu.cn。
国家863计划项目(2013AA102201);安徽省重大科技专项(15czz03096);合肥工业大学应用科技成果培育计划项目(JZ2016YYPY0041);国家自然科学基金(31601465/31470002)。
TS214
A
1002-0306(2016)22-0205-08
10.13386/j.issn1002-0306.2016.22.032
