伊曲康唑的特性鉴定
2017-01-12董晓亚雷勇胜傅琳杨忠峰
董晓亚++雷勇胜+ 傅琳 杨忠峰
[摘 要] 目的:采用分析仪器对伊曲康唑进行特性鉴定,验证方法的准确性及可行性。方法:通过元素分析仪分析伊曲康唑的元素组成,利用紫外(UV)、红外(FTIR)、质谱(MS)、核磁共振碳谱(13C-NMR)、核磁共振氢谱(1H-NMR)、氢氢相关谱(1H-1HCOSY)、碳氢相关谱(HMQC)、碳氢远程相关谱(HMBC)等对伊曲康唑进行结构分析,并结合热重-差热分析(TGA/DSC)和X射线粉末衍射进行晶型鉴定。结果:通过紫外、红外、质谱和核磁等实验证实了伊曲康唑的结构,并通过熔点、X射线粉末衍射和DSC等实验结果证实了伊曲康唑的晶型。结论:该方法准确可行,可对伊曲康唑进行特性鉴定,可为生产过程控制提供理论依据。
[关键词] 伊曲康唑;结构确证;晶型鉴定;特性鉴定
中图分类号:O657 文献标识码:A 文章编号:2095-5200(2016)06-087-04
DOI:10.11876/mimt201606033
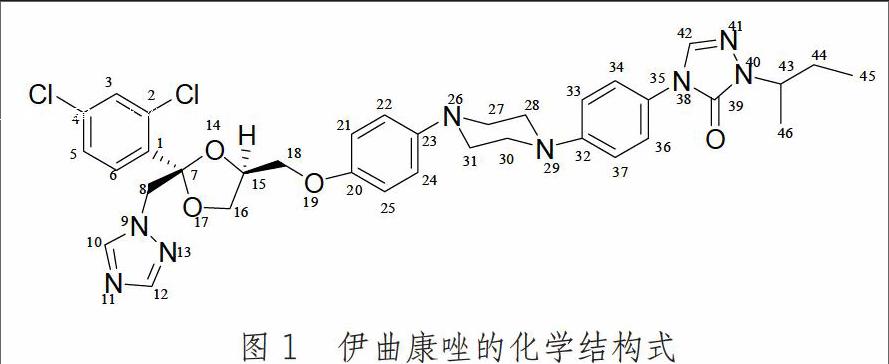
伊曲康唑(itraconazole)由美国强生公司研制,主要通过抑制细胞色素P450氧化酶介导的麦角甾醇的合成,从而对抗深部真菌和浅表真菌[1]。伊曲康唑是一个由两对对映异构体组成的外消旋混合物,分子式为C35H38Cl2N8O4,分子量为705.64,结构式见图1。
图1 伊曲康唑的化学结构式
关于伊曲康唑的新剂型制备和药理作用方面的研究文献较多[2-3],而关于其结构确证方面的文献资料尚不够完整[4-5]。该研究通过对伊曲康唑进行元素分析、紫外吸收光谱(UV)、红外吸收光谱(FTIR)、高分辨质谱(HR-MS)、核磁共振碳谱(13C-NMR)、核磁共振氢谱(1H-NMR)、核磁共振DEPT135°试验、氢氢相关谱(1H-1HCOSY)、碳氢相关谱(HMQC)、碳氢远程相关谱(HMBC)、热重-差热分析(TGA/DSC)和X射线粉末衍射分析,综合各分析结果对伊曲康唑进行特性鉴定。
1 仪器与试药
1.1 仪器
德国elementar vario EL元素分析仪、HP 8453紫外分光光度计、美国Nicolet公司ThermoNicolet is5红外光谱仪、Agilent Technologies6520型 Accurate-Mass-Q-TOF LC/MS质谱仪、BRUKER AV-400超导核磁共振仪、D/max-2500 X射线粉末衍射仪、METTLER LOLEDO TGA-DSCI分析仪。
1.2 试药
所有核磁共振实验均以CDCl3为溶剂,TMS(四甲基硅烷)为内标。所有试剂均为分析纯。
1.3 样品
伊曲康唑样品[6]为某制药企业提供,批号Y1012026,经高效液相色谱法测定,符合结构确证所需纯度要求。对照品购自中国药品生物制品检定所(含量为99.93%),批号10631-200401。
2 测定方法与结果分析
2.1 理化性质
2.1.1 伊曲康唑为淡黄色粉末,按照中国药典第二部附录溶解度测定法测得,伊曲康唑不溶于水,在乙醇中微溶,二氯甲烷中易溶。
2.1.2 旋光度测定 取伊曲康唑供试品和对照品适量,加二氯甲烷溶解并定容量稀释成每1mL含0.1g的溶液,测得旋光度均为0.1°。
2.1.3 熔点测定 取伊曲康唑供试品和对照品适量,分别按照中国药典第二部附录VI C熔点测定方法第一法对伊曲康唑的熔点进行测定,结果表明伊曲康唑Y1012026样品和伊曲康唑对照品的熔点均为166℃。
2.2 有机元素分析
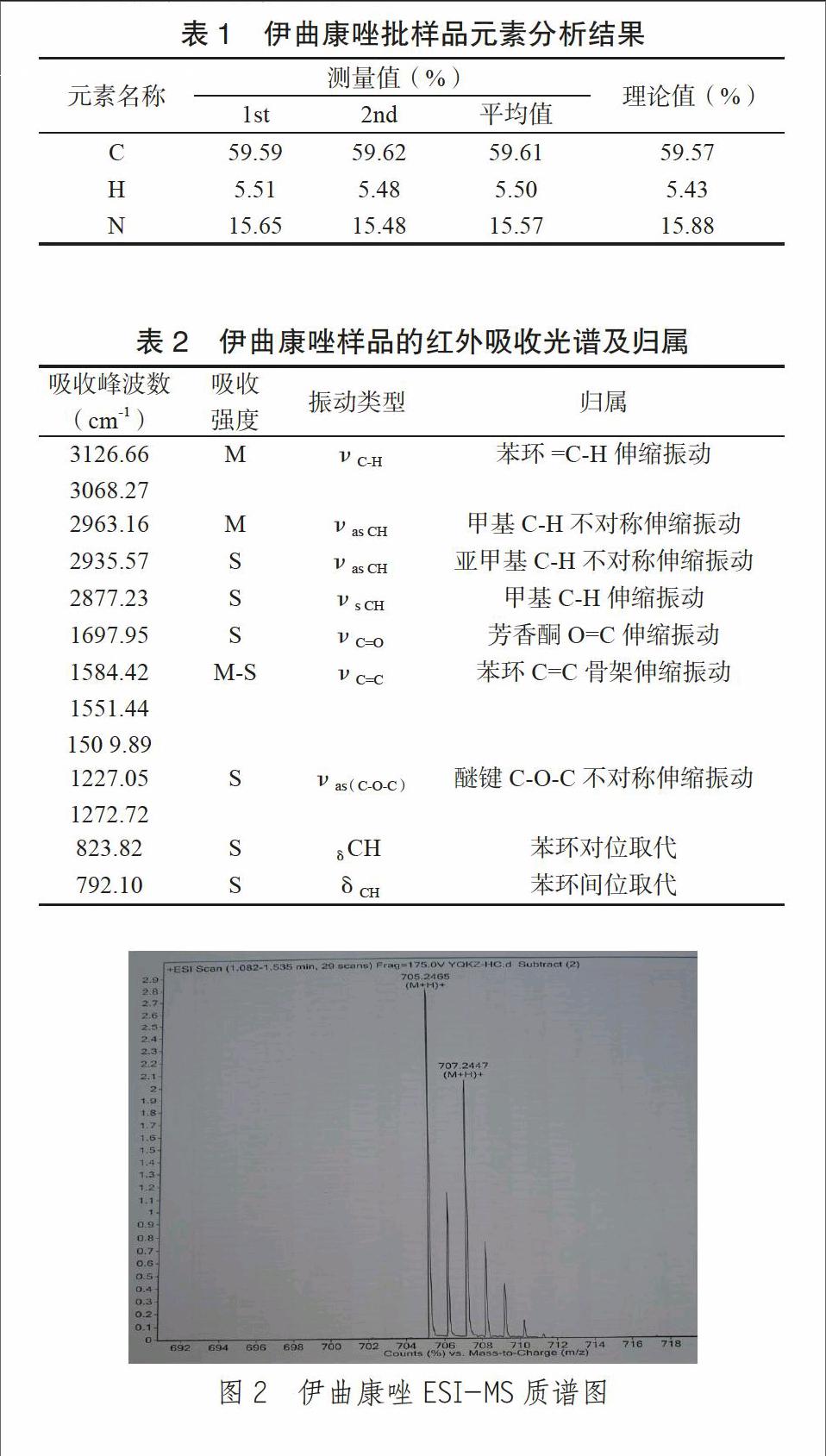
取伊曲康唑样品进行C、H、N元素分析,与理论基本计算值相符,见表1。
2.3 紫外吸收光谱
伊曲康唑样品在甲醇中的紫外吸收光谱显示,在262nm处有最大吸收(K带),236nm处有最小吸收。与中性溶液相比,伊曲康唑在0.1 mol/L的盐酸甲醇溶液中的最大吸收峰为259nm,最小吸收峰为238nm,并出现222nm的吸收峰;在0.1 mol/L的氢氧化钠甲醇溶液中的最大吸收峰为262nm,最小吸收峰为239nm。
2.4 红外光谱
按照中国药典2010年二部对仪器进行校正,符合规定。采取KBr压片制样。
伊曲康唑的红外光谱表明,化合物含有苯环、甲基、亚甲基、芳香酮、醚键和苯环的间位、对位取代,具体的红外数据与归属见表2。
2.5 高分辨质谱
采用高分辨质谱(ESI源)进行分析。伊曲康唑质谱的m/z为分子离子峰[M+H]+,m/z为705.2462,与分子量705.2465一致。伊曲康唑的ESI-MS质谱图见图2。
2.6 核磁共振谱
1H-NMR观测频率为400.13M Hz,1H90°脉冲宽度为13.6μs;13C-NMR观测频率为100.62M Hz,13C90°脉冲宽度为6.5μs。
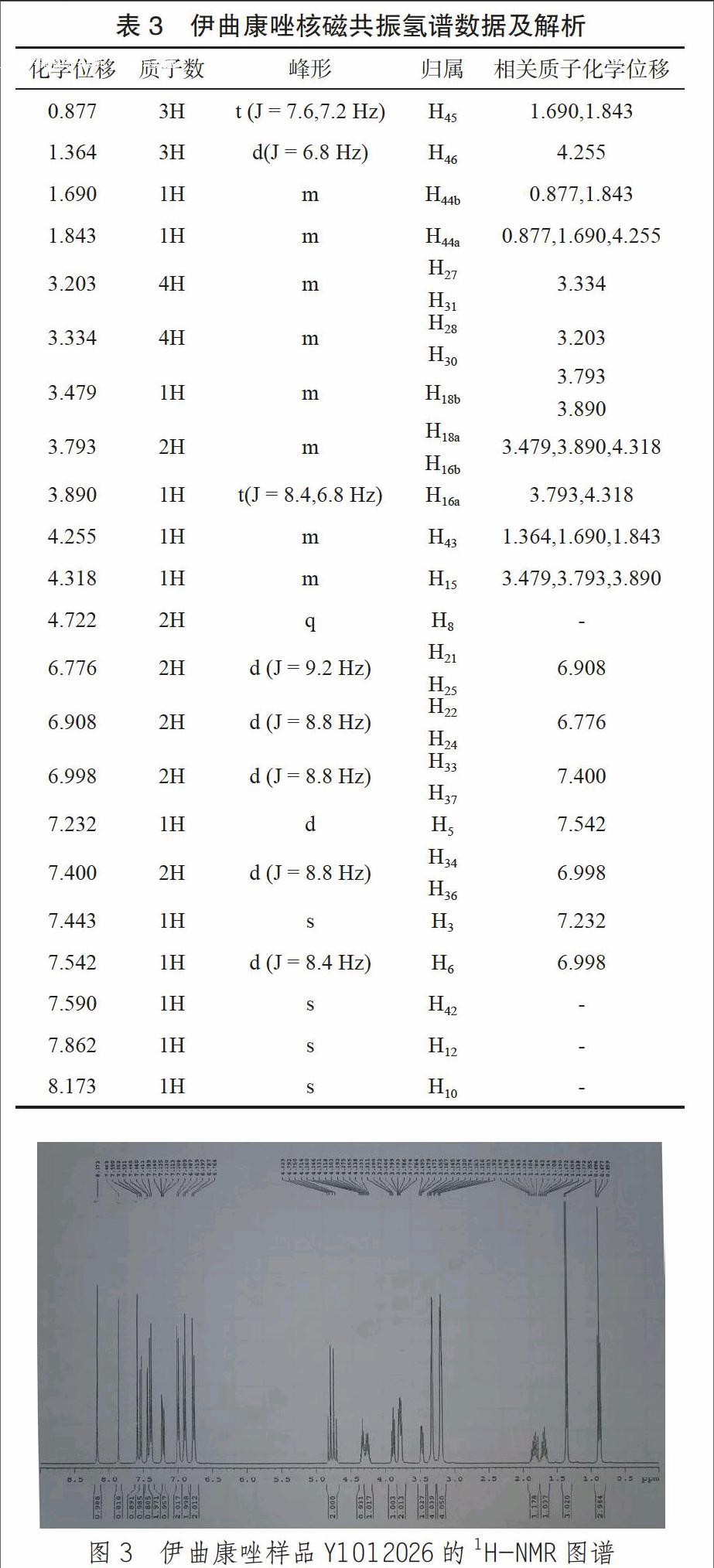
2.6.1 1H核磁共振谱 伊曲康唑样品的具体1H-NMR数据见表3,1H-NMR图谱见图3。结合1H-1HCOSY图谱、HSQC图谱和HMBC图谱,对1H核磁共振谱进行归属。
伊曲康唑样品的1H谱显示有38个质子,共有22组氢,从高场到低场各氢的积分比为3:3:1:1:4:4:1:2:1:1:1:2:2:2:2:1:2:1:1:1:1:1,与伊曲康唑结构相符,且与对照品一致。
2.6.2 13C核磁共振谱 伊曲康唑样品的具体13C-NMR数据见表4,核磁共振碳谱DEPT θ=135°见图4,13C-NMR谱见图5。
伊曲康唑13C图谱图谱上除溶剂峰(δ 76.68-77.31ppm)外共有29个峰,其中6个碳信号重合,实际有35个碳;由DEPT135°谱可知,分子中有8个仲碳和9个季碳,与伊曲康唑结构式相符。
2.7 X-射线粉末衍射及热分析
通过对伊曲康唑进行X-射线粉末衍射分析和热分析,伊曲康唑样品与对照品的衍射图中各衍射峰和强度一致。DSC分析结果显示,伊曲康唑的DSC曲线有一个吸收峰,样品与对照品的吸热峰峰顶温度均为167.86℃。TGA曲线中,在室温到150℃范围内,未见热失重峰,表明本品不含吸附水或结晶水/结晶溶剂。X-射线粉末衍射测定结果如表5。
2.8 晶型分析
根据伊曲康唑样品与对照品的熔点测定, X射线粉末衍射结果和DSC曲线,伊曲康唑样品Y1012026与对照品晶型一致。伊曲康唑样品Y1012026的X-粉末衍射结果中,其特征峰的衍射角2θ值为14.42°,17.4°,17.9°,20.36°,23.44°和25.3°;DSC曲线有一个吸收峰,吸热峰峰顶温度均为167.86℃。伊曲康唑样品的X射线粉末衍射图谱和DSC曲线对比结果如图6、7。
2.9 综合解析
经过对伊曲康唑的核磁共振一维、二维图谱的测定,可进一步确定目标化合物与伊曲康唑的分子结构式一致[7-8],并通过对其进行紫外、红外光谱测定,质谱测定,确定目标化合物与伊曲康唑的结构式一致,旋光度为0.1°,表明为消旋体,其结构为(士)-1-仲丁基-4-[4-[4-[4-[[(2R* , 4 S * )2-(2,4-二氯苯基)-2-(lH-l,2,4-三氮唑基-1-甲基)-1,3-二氧环戊-4-基]甲氧基]苯基]-1-哌嗪基]苯基]-△2 –l,2,4-三氮唑-5-酮。再通过对其进行X-射线粉末衍射和DSC的测定,确定其晶型与对照品一致,进一步为伊曲康唑的合成和质量控制提供了重要的参考依据。
3 讨论
3.1 伊曲康唑化合物中H15是受邻位H16、H18影响,氢谱峰应裂分为三重峰,但δ 4.318处为一组包含1个质子的多重峰,与δ 3.479,δ 3.793和δ 3.890处质子相关,且与δ 74.60处的叔碳相关,推断可能原因是由于C15为手性碳,影响H15的裂分,关于伊曲康唑化合物手性碳的研究还需进一步深入。
3.2 通过对比红外,DSC曲线和X-射线粉末衍射,伊曲康唑原料药的晶型与对照品一致。与Shankar等[9]对伊曲康唑原料药的晶型的研究相比,其DSC曲线、IR和X-射线粉末衍射结果一致,表明该伊曲康唑Y1012026样品晶型与对照品及文献资料一致。
3.3 试验证实该方法准确可行,可作为伊曲康唑的特性鉴定方法,为以后伊曲康唑的生产过程控制提供理论依据。
参 考 文 献
[1] 陈江飞,苗彩云,朱素燕.抗真菌药伊曲康唑的临床药理学研究进展[J].中国临床药理学杂志,2009,25(2):153-156.
[2] OGAWA T, MATSUMOTO K, TSUJIMOTO K, et al. Chronic invasive sinus and intracerebral aspergillosis controlled by combination therapy with micafungin and a daily dose of 400 mg itraconazole oral solution[J]. J Infect Chemother, 2015, 21(2): 134-137.
[3] GILANI K, DAMAN Z, MOAZENI E, et al. Preparation and characterization of various solid dispersion formulations of itraconazole to enhance the drug dissolution profile[J]. Drug Deliv Sci Tech, 2014, 24(6): 659-664.
[4] INKMANN E, HOLZGRABE U. 1H and 13C nuclear magnetic resonance studies of the sites of protonation in itraconazole and fluconazole[J]. J Pharm Biomed Anal, 1999, 20(1-2): 297-307.
[5] Shevchenko A, Miroshnyk I, Pietil? L O, et al. Diversity in Itraconazole Cocrystals with Aliphatic Dicarboxylic Acids of Varying Chain Length[J]. Crystal Growth & Design, 2013, 13(11):4877-4884.
[6] KANDA N, KANO R, ISHIKAWA T, et al. The antimycotic drugs itraconazole and terbinafine hydrochloride induce the production of human β-defensin-3 in human keratinocytes[J]. Immunobiology, 2011, 216(4): 497-504.
[7] 朱淮武.有机分子结构波谱解析[M].北京:化学工业出版社,2005:91.
[8] 陈合兵.核磁共振技术在药物定量分析和混合物结构鉴定中的应用[D].北京:军事医学科学院,2010.
[9] SWAMINATHAN S, SANGWAI M, WAWDHANE S, et al. Soluble itraconazole in tablet form using disordered drug delivery approach: critical scale-up considerations and bio-equivalence studies[J]. AAPS PharmSciTech, 2013, 14(1): 360-374.