原子荧光法测定浙江近岸养殖海水中的微量元素硒
2017-01-11朱敬萍梅光明张小军顾蓓乔李佩佩
朱敬萍,梅光明,张小军,金 雷,陈 瑜,顾蓓乔,李佩佩
(浙江海洋大学海洋与渔业研究所,浙江省海洋水产研究所,浙江省海洋渔业资源可持续利用技术研究重点实验室,浙江舟山 316021)
原子荧光法测定浙江近岸养殖海水中的微量元素硒
朱敬萍,梅光明,张小军,金 雷,陈 瑜,顾蓓乔,李佩佩
(浙江海洋大学海洋与渔业研究所,浙江省海洋水产研究所,浙江省海洋渔业资源可持续利用技术研究重点实验室,浙江舟山 316021)
采用氢化物发生-原子荧光法定养殖海水中硒含量。通过实验条件选择,对消解样品的酸浓度和硒还原方式等条件进行了优化。在优化后的最佳测定方法下,硒测定的标准曲线线性范围为0~10.0 μg/L,养殖海水样品加标回收率在84.4%~102%,相对标准偏差在0.13%~5.27%之间(n=6),方法检出限为0.15 μg/L。该方法简便快速、结果准确、灵敏度高、易于普及,适用于养殖海水中硒的快速检测。
硒;养殖海水;原子荧光法
硒是生物体内必要的微量元素之一,人体中约有2/3的硒以硒蛋白形式存在,其余1/3参与合成谷胱甘肽过氧化物酶[1-2]。硒是生物体内多种蛋白质的必要组成成分,具有催化和结构功能,在生物体的生长、发育、繁殖,特别是免疫的维持中扮演着十分重要的角色。硒元素的缺乏会使生物体产生机体营养失调、对疾病的抵抗力下降以及死亡率增加[3-4]等的氧化应激反应。目前认为硒最重要的生物学功效就是它的抗氧化能力。除此之外,硒又能构成在人体肌肉细胞生物氧化过程中起到电子传递作用的硒蛋白,它是含硒酶和硒蛋白的必要组成部分。人类的多种疾病就是由于人体内硒的摄入量不足而引发的。例如,在世界范围内蔓延的克山病、高血压、大骨节病、白内障、关节炎、心血管疾病免疫缺失都与所处环境中硒元素的缺乏有着密不可分的联系[5]。另外我们也不能忽视硒的毒性,若硒的摄入量过多,则会对人体的组织器官造成危害。若日均摄入量达到750-950 μg,就会引起硒中毒,甚至死亡[6]。硒是自然界环境中的重要生命元素,它在环境中的含量直接影响人类和动植物的健康。目前测定硒的方法有很多,主要有比色法[7-8]、原子吸收法[9-11]和氢化物发生-原子荧光光谱法[12-15]等。原子荧光法是一种定量分析方法,快速、灵敏、简便、线性好等优点,具有成熟的分析技术和仪器。本文采用原子荧光法对浙江近岸养殖海水中硒元素的测定进行探讨。
1 材料与方法
1.1 样品采集与预处理
于2015年6-11月间,在浙江省舟山和温州等近岸养殖海域(养殖塘、网箱养殖和筏式养殖)各进行一次海水样品的采集,见表1。将采集的样品经0.45 μm滤膜过滤,过滤水样用酸酸化至pH值小于2后贮于洁净的聚乙烯瓶中保存待检测。
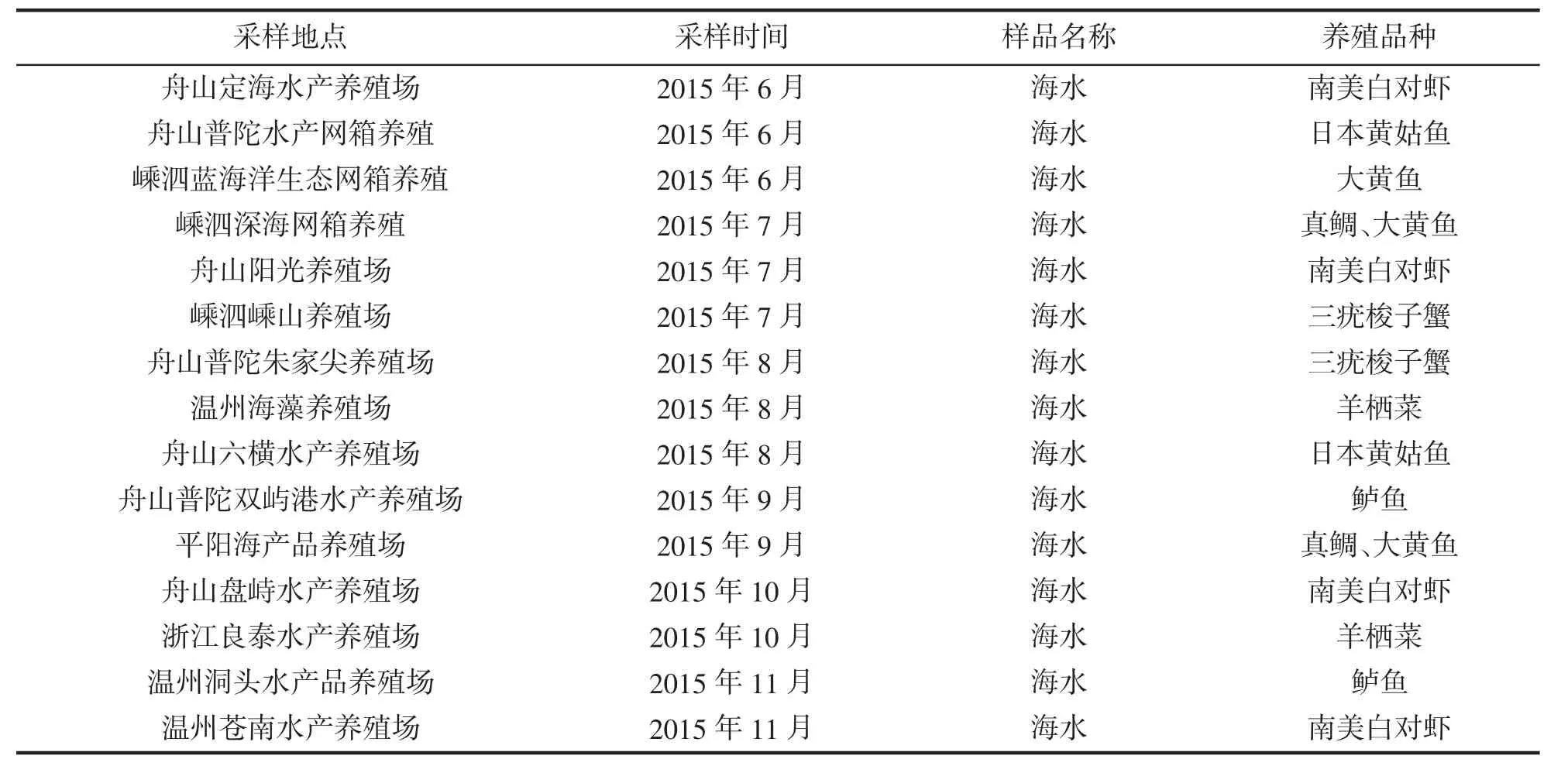
表1 浙江近岸养殖海域水质监测采集点Tab.1 Sample collecting points of mariculture seawater in Zhejiang coastal area
1.2 方法与原理
在盐酸介质中,以硼氢化钾作为还原剂,使硒生成硒化氢。然后用载气(氩气)将硒化氢导入石英炉原子化器,对硒化氢进行原子化。该方法的激发光源为硒特种空芯阴极灯,当硒原子受光辐射激发后,产生电子跃迁。利用处于激发态的电子反回基态时会发出荧光的现象来反应硒含量。该荧光强度在一定浓度范围内与硒的含量成正比。
1.3 主要仪器与试剂
AFS-9230原子荧光光度计(配特种硒空芯阴极灯和自动进样器),京吉天仪器公司;SB-3.6-4型控温电热板,上海隆拓仪器设备有限公司;盐酸、硝酸和高氯酸均为优级纯,其它试剂为分析纯,国药集团化学试剂公司生产;实验用水为去离子水。
所有玻璃器皿均用15%HNO3溶液浸泡24 h,并在洗净后再用去离子水冲洗干净方可使用。
混合液:将硝酸(ρ20=1.42 g/mL,优级纯)与高氯酸(ρ20=1.68 g/mL,优级纯)等体积混给。
还原剂:称取3.00 g KOH溶于200 ml去离子水中,溶解后加入6.00 g KBH4继续溶解,用去离子水稀释至600 mL,若有沉淀过滤后使用,用时现配。
硒标准溶液(100 μg/mL):国家标准物质研究中心。
硒标准使用溶液(0.10 μg/mL):准确移取硒标准溶液1.00 mL于100 mL容量瓶中,用(1+4)盐酸定容,混匀;再移取10 mL于100 mL容量瓶中,用(1+4)盐酸定容,混匀。
1.4 仪器工作条件
实验选定最佳工作条件见表2。测量条件:氩气气压:0.025~0.03 MPa;读数时间:9 s,读数延迟时间:0.5 s;读数方式:峰面积;标液或样液进入体积:0.5 mL。

表2 原子荧光仪器工作条件Tab.2 Instrument working conditions of AFS
1.5 样品的测定
取25.0 mL养殖海水样,于50 mL锥形瓶中,并各加数粒玻璃珠,沿瓶壁加入2 mL混合酸,放上小漏斗,在电热板上缓慢加热浓缩至冒尽白烟,(注意不可烧干),取下锥形烧杯稍冷,加入8 mL纯水和5 mL浓盐酸,加热微沸保持3~5 min。冷却至室温,将试样全量转入50 mL容量瓶或比色管中,加去离子水至刻度,摇匀等测。
2 结果与分析
2.1 盐酸和硼氢化钾溶液浓度的选择
结果表明当盐酸浓度在5%时,有较大的荧光强度,当盐酸浓度过低或超过5%时,荧光强度较弱,因此本实验选择5%的盐酸作为载流液。
还原剂浓度的大小直接影响氢化物生成的速率和氩氢火焰的质量。还原剂一般采用硼氢化钾或硼氢化钠。在还原剂中加入一定量的氢氧化钠或氢氧化钾,可以使溶液趋于稳定性。本试验选择硼氢化钾作为还原剂,氢氧化钾做为稳定剂。硼氢化钾浓度的大小直接影响到荧光强度,试验表明当硼氢化钾质量分数为3%时,有较大的荧光强度,硼氢化钾质量分数大于或小于3%时,荧光强度都有所降低。氢氧化钾浓度为1.5%时,一方面可以较好地提高硼氢化钾作还原剂稳定性,同时避免过多的氢氧化钾会中和盐酸载流液。因此试验确定硼氢化钾溶液质量分数为3%,氢氧化钾溶液质量分数为1.5%。
2.2 样品消解液的选择
加标水样分别采用不同体积比的硝酸、高氯酸、盐酸进行消解处理后进行测定。试验表明当硝酸和高氯酸的混合液(v/v,1:1)加入量大于2 mL、盐酸加入量大于5 mL时,存在酸耗量大、加热时间长、待测元素易挥发损失,回收率降低,达不到检测效果;当硝酸和高氯酸的混合液(v/v,1:1)加入量小于2 mL、盐酸加入量小于5 mL时,待测元素不能完全消解、易烧干,荧光强度明显降低,同样达不到最佳的检测效果。因此采用硝酸和高氯酸的混合液(v/v,1:1)混合液2 mL、盐酸5 mL时,样品消解完全,待测元素荧光强度值达到最大,添加回收率最高。
2.3 标准曲线及方法检出限
准确移取5.00 mL硒标准使用液(0.10 μg/mL)于50mL容量瓶中,加入25.0 mL 6 mol/L盐酸,用纯水稀释至50.00 mL。采用自动进样稀释配制0、0.20、0.50、1.00、2.00、4.00、8.00、10.0 μg/L的系列标准曲线浓度。按选定的仪器工作条件,分别自动吸取2.00 mL标准溶液进行测定,以浓度为横坐标,荧光强度为纵坐标,仪器工作站将自动绘制工作曲线。结果表明硒在0~10 μg/L范围内呈良好的线性关系,线性回归方程A=328.7 C+10.64,相关系数为R=0.999 8;根据3倍信噪比计算方法检出限为0.15 μg/L。
2.4准确度和精确度
对国家标准物质样品GSBZ50031-94进行测定,根据优化的检测条件,利用标准物质对硒的测定方法进行验证,6次平行测定结果见表3。

表3 标准参考物测定值Tab.3 Tested value of standard reference
由上表可知,6次平行测定,测定值均在标准值范围内,相对偏差4.29%~5.07%之间。由此可见该方法具有较好的精密度和准确度,能满足检测养殖海水中微量元素硒的分析要求。
2.5 养殖海水样品的分析及加标回收率实验
本实验对浙江近岸养殖水域采集的样品,按照上述方法进行前处理后进行测定。同时对各站位样品进行加标回收率实验,分析结果见表4。
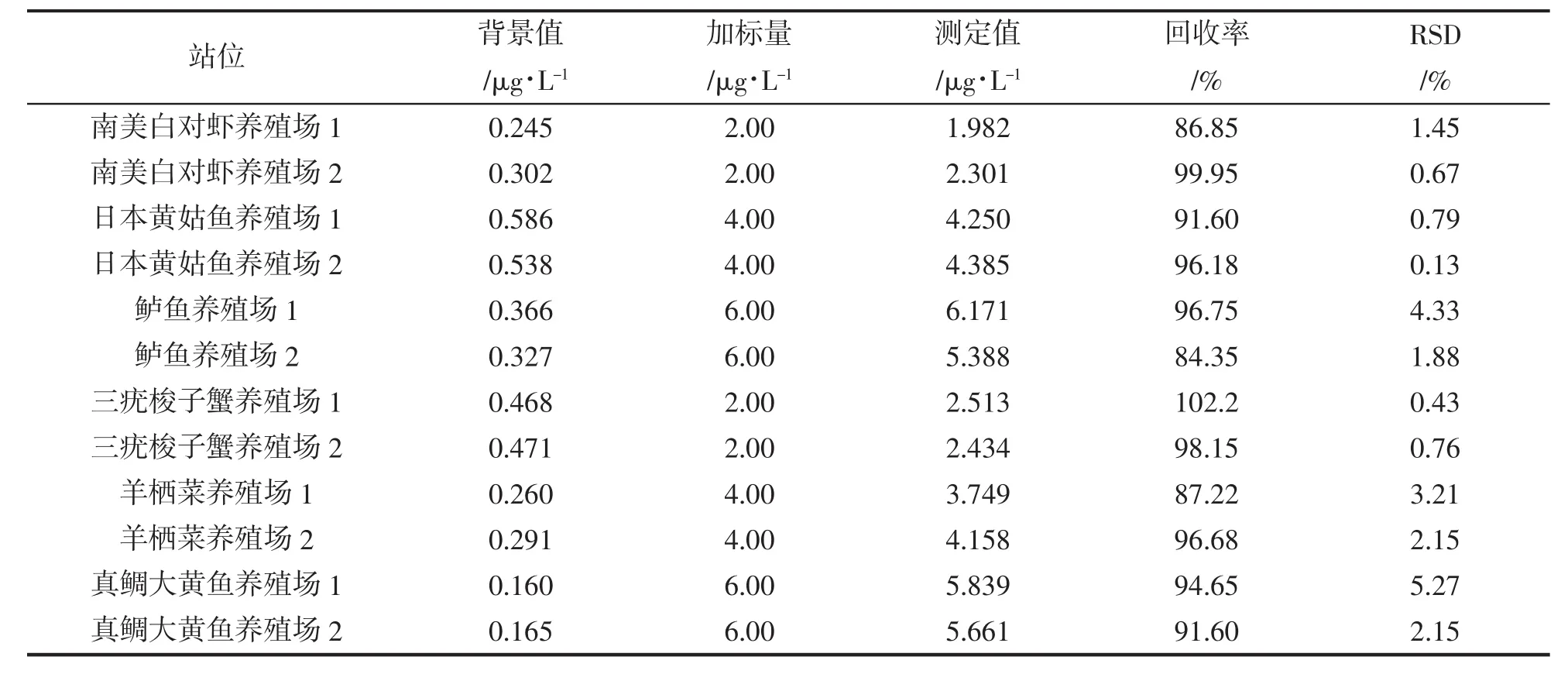
表4 样品分析结果(n=6)Tab.4 Sample results
由上表可见,对浙江近岸养殖水域采集的样品进行检测,检测结果均未超过无公害海水检测标准硒元素≤20 μg/L的限量标准。当在各样品中分别加入浓度为2.00 μg/L、4.00 μg/L、6.00 μg/L的硒标准溶液时,样品的加标回收率在84.4%~102%之间,相对偏差0.13%~5.27%之间。以上结果表明,该方法准确度高,重复性好,能满足养殖海水中硒的检测。
3 小结
本试验通过对样品消解条件和原子荧光仪器工作条件进行优化,建立了养殖海水中硒含量的原子荧光测定方法。实验结果表明,样品加标回收率在84.4%~102.2%之间,相对偏差0.13%~5.27%之间。该方法灵敏度高、线性范围宽、检出限低、准确度高、重复性好,方法具有操作简单和快捷等优点,适合于养殖海水中微量元素硒的分析。
[1]杜 莹,刘晓丹.微量元素硒的研究进展[J].微量元素与健康研究,2007,24(3):56-58.
[2]姚 昭,李红艳,张云龙,等.有机硒,无机硒,VE单独使用及有机硒与VE联用对大鼠体内抗氧化能力的影响[J].食品科学,2013,34(15):272-276.
[3]葛 阳,侯桂革,高雨霖.有机硒与人类健康[J].山东化工,2013,42(7):47-50.
[4]梁光裕.硒的保健功能[J].世界元素医学,2008,15(3):24-28.
[5]陈历程,张 勇.微量元素硒的研究现状及其食品强化[J].食品科学,2002,23(10):134-137.
[6]卿 艳,张立实.硒毒性研究进展[J].预防医学情报杂志,2012,28(3):216-218.
[7]刘媛媛,周焕英,周志江,等.比色法快速检测食品中硒含量[J].营养学报,2012,34(1):79-81.
[8]周华生,张连龙,戴舒春,等.钼蓝比色法测定保健食品中微量硒[J].食品工业科技,2011(8):412-414.
[9]刘礼武,涂高发.石墨炉原子吸收分光光度法测定水中硒的不确定度评定[J].福建分析测试,2013,22(3):26-29.
[10]刘 红,陈燕芹.微波消解样品-氢化物发生-原子吸收光谱法测定苦荞中微量硒[J].理化检验:化学分册,2011,47(1):76-77.
[11]金华丽,王晓君,邢智鑫.氢化物发生-原子吸收分光光度法测定鸡肝中硒的含量[J].食品科技,2009,34(1):245-247.
[12]周晓庆,张无敌.氢化-原子荧光法分析水质砷、汞、硒的实验研究[J].云南师范大学学报:自然科学版,2013,33(6):54-58.
[13]高向阳,韩 帅,王莹莹,等.微波消解-氢化物原子荧光光谱法同时测定贼小豆中的砷、硒、锑[J].食品科学,2013,34(10): 215-218.
[14]张美琴,季华曼,杨洪生,等.氢化物发生原子荧光光谱法测定水产品中有机硒和无机硒[J].中国水产科学,2012,19(5):900-905.
[15]朱敬萍,郭远明.氢化物发生原子荧光法测定海水中的微量元素硒[J].浙江海洋学院学报:自然科学版,2002,21(3):247-251.
Determination of Trace Element Selenium in Zhejiang Coastal Mariculture Seawater by Atomic Fluorescence Spectrometry
ZHU Jing-ping,MEI Guang-ming,ZHANG Xiao-jun,et al
(Institute of Marine and Fisheries of Zhejiang Ocean University,Marine Fishery Research Institute of Zhejiang Province,Key Laboratory of Sustainable Utilization of Technology research for Fishery Resource of Zhejiang Province,Zhoushan 316021,China)
Determination of selenium in mariculture seawater was conducted by hydride generation atomic fluorescence spectrometry.The conditions including acid concentration and selenium’s reduction method were optimized by the experimental conditions.In the optimized condition,the linear range of standard curve is 0-10.0 μg/L,recovery rates in spiked mariculture samples is 84.4%-102%,the relative standard deviation is between 0.13%-5.27%(n=6),and the detection limit is 0.15 μg/L.The method is simple,rapid,accurate,sensitive and easy to be popularized for the rapid detection of selenium in maricultured sea water.
selenium;mariculture seawater;atomic fluorescence spectrometry
TS207.3
A
1008-830X(2016)03-0228-05
2016-6
浙江省科技计划项目(2016C32074,2016F30020,2016F30022,2015C37065)
朱敬萍(1960-),女,山东滕州人,高级工程师,研究方向:水域环境及食品安全研究.E-mail:ZJP669888@163.com
顾蓓乔(1963-),男,上海市人,研究方向:水域环境及食品加工.E-mail:gbq@zjou.edu.cn
