谷氨酸脱羧酶基因工程改造研究进展
2017-01-09靳春鹏杨套伟徐美娟张显饶志明
靳春鹏,杨套伟,徐美娟,张显,饶志明*
1(国家知识产权局专利局专利审查协作北京中心, 北京, 100081) 2(江南大学 生物工程学院,工业生物技术教育部重点实验室,江苏 无锡,214122) 3(江南大学(如皋)食品生物技术研究所,江苏 如皋,226500)
谷氨酸脱羧酶基因工程改造研究进展
靳春鹏1,杨套伟2,3,徐美娟2,张显2,饶志明2,3*
1(国家知识产权局专利局专利审查协作北京中心, 北京, 100081) 2(江南大学 生物工程学院,工业生物技术教育部重点实验室,江苏 无锡,214122) 3(江南大学(如皋)食品生物技术研究所,江苏 如皋,226500)
γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种具有重要生理功能的天然氨基酸,广泛应用在医药、食品、化工等行业。利用谷氨酸脱羧酶催化法合成GABA因其反应条件温、对环境友好和原料易得已成为当前研究的热点。该研究论述了催化合成GABA关键酶谷氨酸脱羧酶的分子改造、基因工程菌构建等研究进展。
谷氨酸脱羧酶;γ-氨基丁酸;分子改造;重组菌构建
γ-氨基丁酸(γ-aminobutyric acid,GABA)是一种具有重要生理功能的天然氨基酸,具有降低血压、镇静安神、增进脑活力、增强记忆等功能,在医药、食品保健、化工等行业具有广泛应用前景[1-2]。其合成方法主要包括:化学合成法[3]、植物富集法[4]和生物合成法[5-6]。化学合成法因其反应条件较为剧烈,且常用到有毒催化剂等,限制了其应用范围。植物富集法因植物生长周期长,受资源和环境限制等因素,因此,该方法并不能应用于GABA大量合成。微生物法因反应条件温和、对环境友好等具有显著的优点,因此,利用微生物生产GABA具有广阔的应用前景。
谷氨酸脱羧酶(glutamate decarboxylase, GAD,EC4.1.1.15)的主要功能是催化L-谷氨酸的α-羧基脱羧合成GABA,广泛分布于微生物和动植物等各种有机体活细胞中[7]。微生物具有分布广、生长速度快、以及不受资源、环境等限制,是生物酶的重要来源。为了提高GABA合成效率,研究者对GAD进行了大量研究,包括筛选获得了不同来源的GAD,并对GAD进行分子改造和修饰研究。
本文首先概述了不同来源的GAD,并比较了其部分酶学性质;继而综述了目前对GAD的分子改造,即提高GAD催化活力、热稳定性,和拓展GAD在偏中性环境中的催化活力和催化效率方面的研究状况;随后,概述以谷氨酸为底物合成GABA基因工程菌构建及应用的研究进展。最后,讨论了在棒杆菌中构建以廉价底物葡萄糖为底物发酵生产GABA的重组菌株,以便为工业化生产GABA提供了新的方向。
1 谷氨酸脱羧酶
1.1 不同来源的谷氨酸脱羧酶
本文概述了不同来源的GAD,并对其部分酶学性质进行了比较。由表1可知,GAD来源比较广泛,人们不但对微生物中的GAD进行研究,在谷物、甚至水果中的GAD也有大量研究。不同来源的GAD在酶学性质上存在一定的差异。大部分的GAD最适作用pH偏酸性环境,一般在4.0~6.0之间,而当环境pH>6时,GAD活力急剧下降,甚至完全丧失催化活性。极少数来源的GAD最适作用pH偏碱性环境,如P.horikoshii来源的GAD最适作用pH为8.0。大部分的GAD最适作用温度在37~50 ℃,很少来源GAD最适作用温度在50 ℃以上,目前报道的最耐热的GAD来源于P.horikoshii,其最适作用温度可以达到97 ℃。另外,由表1可以看出,不同来源的GAD对底物谷氨酸/谷氨酸盐的亲和力存在较大差别,甚至同一属来源的GAD对底物谷氨酸/谷氨酸盐的亲和力也存在比较大的差别。总体而言,微生物来源的GAD比植物来源的GAD对底物谷氨酸/谷氨酸盐具有更好的亲和力。
一般来说,激活剂能够显著提高酶的活力以及催化效率。因此,大量研究者对GAD的激活剂进行了筛选研究。如表1所示,磷酸吡哆醛(PLP)是谷氨酸脱羧酶一个辅助因子,但是并不是所有来源的GAD都需要PLP参与,这无疑可以降低生产成本。另外,研究发现,Ca2+是GAD最通用的激活剂,其能激活大部分来源的GAD活力。Mg2+, Mn2+甚至 Li+和Ba2+也可以作为GAD的激活剂。而在生产研究过程中,则要求尽可能少地加入额外的物质,以便降低生产成本,因此,对PLP、金属离子等激活剂依赖较低的GAD将是工业生产中首选的对象。

表1 不同来源的谷氨酸脱羧酶及其部分酶学性质
1.2 谷氨酸脱羧酶分子改造研究
一般情况下,在酶催化工业中,要求酶具有较高的催化效率,同时最适作用pH为中性环境,以便减少酸碱加入量,降低生产成本。因此,研究者对GAD的分子改造一般集中在2个方面,1是提高GAD催化活力或热稳定性,2是拓展GAD在偏中性环境中的催化活力和催化效率。
1.2.1 基于提高GAD催化活力或热稳定性的研究
目前,关于提高GAD酶活力的研究报道较少。LIN等[34]通过易错PCR对短乳杆菌来源的GAD进行随机突变,筛选获得1个酶活力比原始GAD提高1.2倍的突变体Q51H;在此基础上对51位进行饱和突变,并为获得比突变体Q51H活力更高的突变体。而在进行N端缺失的试验中,他们发现第88位的天冬氨酸和N端区域对GAD的活力和正确折叠起到决定性作用。为了GAD 的催化活力或热稳定性,柯丕余等通过分析短乳杆菌GAD1407三维模拟结构的拉氏图,确定K413为GAD1407不稳定氨基酸残基位点,并对该位点进行定点突变获得2个突变体K413A 在50℃的半衰期是原始酶的2.1倍,而突变酶K413I 热稳定性没有明显的提高,但其酶活力是野生酶的1.6倍。
1.2.2 基于拓宽GAD酶催化pH作用范围的研究
据大多数文献报道(表1),GAD作用pH一般在4.0~6.0之间,而当环境pH>6时,GAD活力急剧下降,甚至完全丧失催化活性。较低的pH,在酶催化过程中需要加入无机盐作为缓冲剂,这无疑增加生产成本和下游提取费用;而催化底物谷氨酸和谷氨酸钠在酸性环境中的溶解度都较低,不利于GAD的催化反应进行和GABA的高效合成。因此,大部分学者就如何拓宽GAD的pH作用范围开展了大量研究。
PENNACCHIETTI等[35]发现,当对465位的His进行突变时,GadBH465A和GadBΔHT活性位点的“锁”不能形成,而突变体pH作用范围明显向碱性拓展,因此,他们推测His465并非GAD的活性位点,对该位点进行突变,并没有使其失活而是改变了酶的构型,该位点对整个构型的协调性是必须的。
KANG等[36]构建了大肠杆菌来源的GAD△466突变体,改突变体催化活力和pH作用范围均得到大幅提升。
THU等[37]发现,E.coli来源的GAD在pH6.0时基本完全丧失活力,而删除该GAD的C末端15个氨基酸残基 (Δ452~466) 时,突变体GAD(Δ452~466)的pH作用范围向碱性偏移的1个pH,该突变体在pH7.0时基本完全丧失活力。突变体 Glu89Gln/Δ452~466的pH作用范围继续向碱性偏移的0.5个pH,其在pH7.5时基本完全丧失活力。Glu89Gln/His465Ala在pH8.5时基本完全丧失活力,但是其pH4催化活力比原始酶降低了25%。
林玲等[38]发现来自短乳杆菌CGMCC NO.1306的谷氨酸脱羧酶(GADl407)催化pH范围较窄(4.2~5.2),当pH大于5.0以后,随着pH的增大酶活性急剧下降。与拟南芥GADl的氨基酸序列进行比对,发现了一个影响GAD1407催化pH特性的关键位点:S307。通过对这个位点进行饱和突变并筛选,最终确定S307N拓宽了该酶催化的最适pH范围。
De BIASE等[39]对改变GAD的pH作用范围进行了总结,他们发现,GAD有3个区域与pH作用范围有关,1是N端前15位氨基酸,2是C端347~466位氨基酸,3是300~313位点,这些位点位在PLP主要结合区域组成了一个-发夹结构。
2 以谷氨酸为底物合成GABA基因工程菌构建及应用研究
在酶催化工业中,人们通常希望酶的生产者具有高效合成具有优良工业属性的酶催化剂,而对于GAD的合成也是如此。而自然界中的天然GAD生产者,要么所产天然GAD特性不适合工业化生产要求,要么GAD产量和生产效率比较低等问题。对于酶的特性改造,我们已经在前一部分进行了综述,而在这一部分我们将概述以谷氨酸为底物合成GABA基因工程菌构建及应用的研究进展,具体研究情况如表2所示。
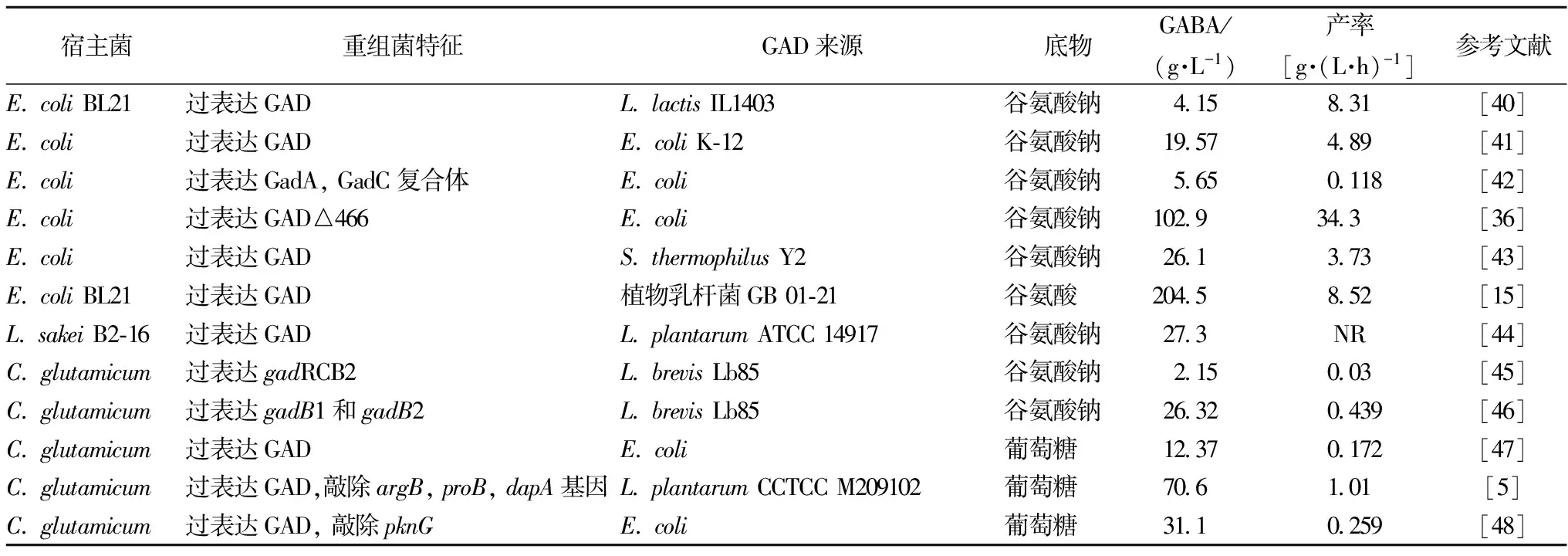
表2 利用基因工程菌合成GABA
2.1 大肠杆菌
大肠杆菌因其生长速度快,遗传背景清晰以及分子操作技术成熟等优点,在基因工程领域已被广泛应用。研究者构建了GAD过表达的大肠杆菌基因工程菌,并开展了GABA合成研究。
张天萌等[40]将来源于Lactococcuslactissubsp.lactisIL1403的GAD基因通过pET-22b(+)质粒为载体克隆至E.coliBL21(DE3)中,构建了基因重组。重组菌GAD的活力比原始菌株有明显提高;原始菌转化5 h,底物转化率为55.8%,而重组菌0.5 h时的底物转化率就达到了98.3%。
王期等[41]将E.coliBL21(DE3)来源的GAD通过pET-28a(+)质粒为载体自身中过量表达,重组菌E.coliK. 12中GAD活力比原始菌提高了60倍。工程菌1.15 U粗酶液以31 g/L的L-谷氨酸钠为底物,反应4 h,L-谷氨酸钠的转化率为93%。
田灵芝等[15]将来源于植物乳杆菌GB 01-21的GAD基因通过pET-22b(+)质粒为载体克隆至E.coliBL21(DE3)中,GAD成功在大肠杆菌E.coliBL21 (DE3) 中高效诱导表达,为植物乳杆菌GB 01-21中GAD 酶活的4.24倍。将该重组菌应用于转化L-谷氨酸生产GABA,最终5 L 发酵罐上进行转化实验,批次添加底物L-谷氨酸共600 g,转化24 h,GABA 累计浓度可达204.5 g/L,摩尔转化率为97.92%,为其工业化应用打下了良好的基础。
LE VO等[42]将谷氨酸脱羧酶GadA和GadB分别与谷氨酸/GABA反向转运体GadC进行不同形式的融合表达,发现GadA和GadC融合体催化活性最高,以10 g/L谷氨酸钠为底物,可以获得5.65 g/L的GABA,转化率达到93%。
KANG等[36]构建了大肠杆菌来源的GAD进行突变获得突变体GADΔ466,该突变体催化活力和pH作用范围均得到大幅提升,在无缓冲液体系中,利用改突变体进行催化合成GABA,3 h获得1 mol的GABA,合成效率达到34.3 g/(L·h)。该方法反应体系中无需添加无机盐作为缓冲试剂,有利于降低下游操作工序和成本。
2.2 枯草芽孢杆菌
芽孢杆菌遗传背景清楚,蛋白质分泌机制健全,生长迅速,培养简单,不产内毒素,适用于原核生物基因的克隆、表达以及重组蛋白多肽的有效分泌。莫征杰等[49]将LactobacillusplantarumZJ3443来源的GAD编码基因lapgad通过质粒pMA5导入到BacillussubtilisWB600系统中,实现了GAD基因在的B.subtilis异源重组表达,其胞内酶活达到0.35 U/mg。并考察了重组菌全细胞转化谷氨酸生产γ-氨基丁酸的最佳转化条件:温度为37 ℃,pH为4.5,添加1 mmol/L Ca2+作为激活剂。
丁伟等[50]从大肠杆菌来源的GAD基因gadB导入枯草芽孢杆菌168,构建了1株高表达GAD 的枯草杆菌,然后通过发酵条件的优化,使得发酵酶活提高了188.8%,确定了最佳发酵参数,为利用枯草芽孢杆菌生产GABA 奠定了基础。
2.3 乳酸菌
乳酸菌是GAD主要生产菌株,但其天然GAD活力较低。为了提高乳酸菌催化合成GABA能力,KOOK等[44]将L.plantarumATCC 14917 GAD基因通过穿梭载体pTRKH2导入到L.sakeiB2-16中。重组菌L.sakeiB2-16的GABA产量265.3 mmol/L,比原始菌提高了1.42倍。虽然乳酸菌催化生产安全性高,但发酵培养困难、成本高、GABA产量低。
2.4 酿酒酵母
酵母菌具有真核生物的特征,遗传背景清楚,生长迅速,培养简单,外源基因表达系统完善,遗传稳定,且生产安全性较高。乌云达来等[51]将酿酒酵母28的GAD1基因通过质粒pUG6在自身体系中进行过表达研究,结果发现,重组菌GAD酶活力比菌株28提高73.8%。通过以上实验结果得出结论,GAD基因高表达菌株DL28具有更高的G418抗性和GAD酶活性,但并未用于催化合成GABA研究。
2.5 谷氨酸棒杆菌
谷氨酸棒杆菌是氨基酸工业常用生产菌株,尤其在谷氨酸生产中被广泛利用。SHI等[45]将L.brevisLb85来源的GAD基因gadB2、L-谷氨酸/GABA逆向转运体基因gadC和上游调控基因gadR在谷氨酸棒杆菌中成功共表达,以谷氨酸为底物,重组谷氨酸棒杆菌pDXW-8/gadRCB2发酵72 h,GABA浓度仅为2.15 g/L。为了提高重组谷氨酸棒杆菌合成GABA效率,SHI等[46]随后将L. brevis Lb85来源的GAD基因gadB1和gadB2在谷氨酸棒杆菌中进行共表达,相比于单表达一个GAD基因,共表达2个GAD基因的重组菌GABA产量提高了1倍,最终,摇瓶发酵120 h,GABA产量达到27.13 ± 0.54 g/L,发酵罐培养60 h,GABA产量达到26.32 g/L, GABA产率为0.60~0.74 mol/mol。
3 廉价底物合成GABA研究
谷氨酸是GABA合成常用的底物,而谷氨酸发酵一般是以棒杆菌为生产菌株发酵代谢葡萄糖实现,因此,为降低生产成本,研究者尝试在棒杆菌中构建以葡萄糖为底物发酵生产GABA的重组菌株。
TAKAHASHI等[47]将E.coliW3110来源的GAD导入谷氨酸棒杆菌中,获得一种能以葡萄糖为底物直接发酵法合成GABA的重组菌,该菌株能在72 h内以葡萄糖为底物生产12.37±0.88 g/L的GABA,生产强度达到0.172 g/(L·h)。丝氨酸/苏氨酸蛋白激酶G调控三羧酸循环进入谷氨酸合成途径的关键酶2-酮戊二酸脱氢酶活力,因此,OKAI等[48]在上述基础上,为了提高谷氨酸合成途径中2-酮戊二酸脱氢酶活力活力,他们敲除了丝氨酸/苏氨酸蛋白激酶G的编码基因pknG,获得1株重组谷氨酸棒杆菌GADΔpknG;在发酵培养基中添加0.1 mmol磷酸吡哆醛(PLP),该菌株可以在120 h内以100 g/L葡萄糖为底物发酵合成31.1 ± 0.41 g/L的GABA,生产强度达到0.259 g/(L·h),GABA产率达到0.893 mol/mol葡萄糖。
孙红梅等[52]将来自于植物乳杆菌γ-氨基丁酸合成途径的关键酶谷氨酸脱羧酶基因(lpgad)在产谷氨酸菌株钝齿棒杆菌中进行整合表达,通过重叠PCR 的方法获得钝齿棒杆菌精氨酸合成途径关键酶N-乙酰谷氨酸激酶( NAGK) 基因内部缺失型基因ΔargB,获得1株能以葡萄糖为底物发酵合成γ-氨基丁酸的重组钝齿棒杆菌;发酵96 h,重组菌可合成约8.28 g/L 的GABA,且发酵液无精氨酸积累。
ZHANG等[5]通过系统代谢工程技术改造谷氨酸棒杆菌,首先通过插入突变技术,将带tac启动子的GAD编码基因tacgad导入谷氨酸棒杆菌argB和proB基因内部,在引入GAD的同时阻断L-精氨酸和L-脯氨酸合成途径。随后将带tac启动子的PLP合成关键酶基因tacplk插入dapA内部,在引入PLP合成关键酶的同时阻断L-赖氨酸合成途径,最终获得1株无需添加PLP既能高效合成GABA的重组谷氨酸棒杆菌。通过发酵流加实验,该菌株能够在70 h内以葡萄糖为底物发酵合成70.6 g/L的GABA,这是目前报道的利用葡萄糖一步法合成GABA的最高产量。
4 结论与展望
目前,生物法合成GABA主要包括酶转化法和微生物发酵法。酶催化法合成GABA通常以谷氨酸为底物,通过GAD一步催化合成GABA,相对于发酵法,步骤单一,反应体系成分简单。不足之处是酶需要分离获得、且反应过程不能持久,采用固定化细胞可以提高批次使用效率[53],但是其催化效率偏低,有待进一步筛选固定化材料和方法。另外,GAD作用pH偏酸性,需要加入无机盐维持最适催化环境,增加了生产附加成分。本文重点概述了拓展GAD在偏中性环境中的催化活力和催化效率方面的研究状况,GAD有3个区域与pH作用范围有关,1是N端前15位氨基酸,2是C端347~466位氨基酸,3是300~313位点,这些位点位在PLP主要结合区域组成了一个-发夹结构,对这些位点进行分子改造,有利于拓宽GAD在偏中性环境中的催化效率。
微生物发酵法合成GABA通常采用谷氨酸为底物,本文概述以谷氨酸为底物合成GABA基因工程菌构建及应用的研究进展,覆盖了大肠杆菌、枯草芽孢杆菌、乳酸菌、酵母菌和谷氨酸棒杆菌。接着讨论了在棒杆菌中构建以葡萄糖为底物发酵生产GABA的重组菌株,避免了谷氨酸为原料的附加成本,更加廉价,为工业化生产GABA的研究目标提供了新方向。但是,GABA前体谷氨酸生产条件一般控制在偏中性环境,而GAD催化的pH范围在4~6之间,这就会因前后两个途径所需环境不同而导致GABA合成效率较低。为解决这一矛盾,YANG等[7]C.glutamicum和L.plantarum双阶段发酵葡萄糖合成GABA,并取得了良好的结果,但是GABA产量还无法和酶催化法相媲美。另外,发酵法由于其发酵液中成分复杂,对下游分离提取造成不小的负担。因此,结合GAD分子改造策略,开发能在偏中性环境中高效利用葡萄糖生产GABA的生产菌株,和开发GABA简单、有效的分离提取策略和装置,将有望成为今后重点研究的方向。
[1] HAYAKAWA K, KIMURA M, KASAHA K, et al. Effect of a γ-aminobutyric acid-enriched dairy product on the blood pressure of spontaneously hypertensive and normotensive Wistar-Kyoto rats[J]. British Journal of Nutrition, 2004, 92(3): 411-417.
[2] YOSHIMURA M, TOYOSHI T, SANO A, et al. Antihypertensive effect of a gamma-aminobutyric acid rich tomato cultivar ′DG03-9′ in spontaneously hypertensive rats[J]. Journal of Agricultural and Food Chemistry, 2010, 58(1): 615-619.
[3] 王金玲,袁军,刘登才.γ-氨基丁酸的合成[J].化学与生物工程,2010,27(3):40-41.
[4] 何秋云, 杨志伟. 马铃薯中γ-氨基丁酸富集技术研究[J].湖北农业科学,2015(8): 1 957-1 960.
[5] ZHANG Rong-zheng,YANG Tao-wei, RAO Zhi-ming, et al. Efficient one-step preparation of γ-aminobutyric acid from glucose without an exogenous cofactor by the designedCorynebacteriumglutamicum[J]. Green Chemistry, 2014, 16(9): 4 190-4 197.
[6] 刘婷婷,杨套伟,张术聪,等.高效转化L-谷氨酸为γ-氨基丁酸菌株的筛选、鉴定及初步优化[J].食品与生物技术学报,2010,29(5): 742-747.
[7] YANG Tao-wei, RAO Zhi-ming, KIMANI BG, et al. Two-step production of gamma-aminobutyric acid from cassava powder usingCorynebacteriumglutamicumandLactobacillusplantarum[J]. Journal of Industrial Microbiology & Biotechnology,2015,42: 1 157-1 165.
[8] TSUCHIYA K, NISHIMURA K, IWAHARA M. Purification and characterization of glutamate decarboxylase fromAspergillusoryzae[J]. Food Science and Technology Research, 2003, 9(3): 283-287.
[9] 杨胜远, 陆兆新, 孙力军等.爬山虎内生菌的鉴定及其谷氨酸脱羧酶酶学特性[J].南京农业大学学报,2007(2):122-127.
[10] SEO MJ,NAM YD,LEE SY,et al.Expression and characterization of a glutamate decarboxylase fromLactobacillusbrevis877G producing gamma-aminobutyric acid[J].Bioscience, Biotechnology, and Biochemistry,2013,77(4):853-856.
[11] UENO Y, HAYAKAWA K, TAKAHASHI S, et al.Purification and characterization of gutamate decarboxylase fromLactobacillusbrevisIFO 12005[J]. Bioscience, Biotechnology,and Biochemistry,1997,61(7):1 168-1 171.
[12] FAN En-yu,HUANG Jun,HU Sheng,et al.Cloning, sequencing and expression of a glutamate decarboxylase gene from the GABA-producing strainLactobacillusbrevisCGMCC 1306[J]. Annals of Microbiology,2011,62(2):689-698.
[13] 许建军,江波,许时婴.Lactococcuslactis谷氨酸脱羧酶的分离纯化及部分酶学性质[J].无锡轻工大学学报,2004(3):79-84.
[14] 韩江雪,丁筑红.不同乳酸菌产谷氨酸脱羧酶特性研究[J].中国酿造,2012(9): 56-59.
[15] 田灵芝,徐美娟,饶志明.1株重组大肠杆菌/pET-28a-lpgad的构建及其高效生产γ-氨基丁酸转化条件的优化[J].生物工程学报, 2012(1): 65-75.
[16] KOMATSUZAKI N,NAKAMURA T,KIMURA T,et al.Characterization of glutamate decarboxylase from a high gamma-aminobutyric acid (GABA)-producer,Lactobacillusparacasei[J].Bioscience, Biotechnology, and Biochemistry,2008,72(2): 278-285.
[17] 刘清,姚惠源,张晖.乳酸菌谷氨酸脱羧酶的酶学性质研究[J].食品科学,2005,26(4): 100-104.
[18] 侯远策,李秀凉,贺强.乳酸片球菌产谷氨酸脱羧酶的相关酶学性质研究[J].黑龙江农业科学,2011(10): 10-13.
[19] 李云,杨胜远,陈郁娜,等.产谷氨酸脱羧酶片球菌的鉴定及其酶学性质[J].食品科学,2010,31(9): 187-191.
[20] KIM H-W,KASHIMA Y,ISHIKAWA K, et al.Purification and characterization of the first archaeal glutamate decarboxylase fromPyrococcushorikoshii[J].Bioscience,Biotechnology, and Biochemistry,2009,73(1):224-227.
[21] YANG Sheng-yuan,LIN Qian,LU Zhao-xin, et al.Characterization of a novel glutamate decarboxylase from Streptococcus salivarius ssp. thermophilus Y2[J]. Journal of Chemical Technology & Biotechnology,2008,83(6):855-861.
[22] 杨胜远,陆兆新,吕凤霞等.1株产谷氨酸脱羧酶乳酸菌的鉴定及其酶学性质[J].工业微生物,2007(6): 25-30.
[23] JOHNSON BS,SINGH NK,CHERRY JH,et al. Purification and characterization of glutamate decarboxylase from cowpea[J]. Phytochemistry,1997,46(1):39-44.
[24] 姚琪, 张永忠. 大豆谷氨酸脱羧酶分离纯化及酶学性质研究[J]. 中国油脂, 2011,36(11): 26-30.
[25] 龚福明, 张忠华, 宋园亮等.豆豉中高产γ-氨基丁酸乳酸菌的筛选及其谷氨酸脱羧酶酶学特性研究[J]. 中国微生态学杂志, 2012(5): 394-399.
[26] 白青云,曾波,顾振新.发芽粟谷中谷氨酸脱羧酶的主要酶学性质初探[J].安徽农业科学,2011(3): 1 268-1 270;1272.
[27] 穆小民,沈黎明,吴显荣.林生山黧豆谷氨酸脱羧酶的分离纯化及部分性质的研究[J].生物化学杂志,1997(2):181-186.
[28] ZHANG Hui,YAI Hui-yuan,CHEN Feng, et al. Purification and characterization of glutamate decarboxylase from rice germ[J]. Food Chemistry, 2007,101(4):1 670-1 676.
[29] 徐冬霞,王立,吕莹果,等.米糠谷氨酸脱羧酶的分离纯化及酶学性质研究[J].食品工业科技,2009,30(12):193-196,296.
[30] 吕莹果,张晖,徐冬霞,等.米糠谷氨酸脱羧酶的酶学性质研究[J].食品与发酵工业,2008,34(5):24-28.
[31] 范军,李纯,朱苏文,等.小麦谷氨酸脱羧酶的纯化及部分性质研究[J].中国生物化学与分子生物学报, 1998(5): 175-178.
[32] 李楠,王玲玲,吴子健,等.玉米胚谷氨酸脱羧酶的性质[J].食品与发酵工业,2011,37(7):34-38.
[33] 徐财凤,苏颖丽,黄芳,等.高活性果蔬谷氨酸脱羧酶的筛选及其酶学性质研究[J].食品工业,2015(9):180-184.
[34] LIN Ling,HU Sheng,YU Kai, et al. Enhancing the activity of glutamate decarboxylase fromLactobacillusbrevisby directed evolution[J].Chinese Journal of Chemical Engineering,2014(22):1 322- 1 327.
[35] PENNACCHIETTI E,LAMMENS TM, CAPITANI G, et al. Mutation of His465 alters the pH-dependent spectroscopic properties ofEscherichiacoliglutamate decarboxylase and broadens the range of its activity toward more alkaline pH[J].Journal of Biological Chemistry,2009, 284(46):3 1 587-31 596.
[36] KANG TJ,HO NAT, PACK SP. Buffer-free production of gamma-aminobutyric acid using an engineered glutamate decarboxylase fromEscherichiacoli[J].Enzyme and Microbial Technology,2013,53(3):200-205.
[37] THU HO NA, HOU CY, KIM WH, et al. Expanding the active pH range ofEscherichiacoliglutamate decarboxylase by breaking the cooperativeness[J].Journal of Bioscience and Bioengineering,2013,115(2):154-158.
[38] 林玲, 胡升, 郁凯等.饱和定点突变拓宽谷氨酸脱羧酶催化pH范围的研究[J]. 高校化学工程学报, 2014, 28(6): 1 410-1 414.
[39] DE BIASE D,PENNACCHIETTI E.Glutamate decarboxylase-dependent acid resistance in orally acquired bacteria: function, distribution and biomedical implications of thegadBCoperon[J].Molecular Microbiology,2012,86(4):770-786.
[40] 张天萌,沐万孟,江波,等. Lactococcus lactis subsp.lactis IL1403谷氨酸脱羧酶的克隆表达、分离纯化及活性研究[J].食品与生物技术学报,2012,31(3):302-306.
[41] 王期,抗晶晶,忻寅强,等.生物转化法重组谷氨酸脱羧酶合成γ-氨基丁酸[J].南京师大学报(自然科学版),2010(3):85-90.
[42] LE VO TD, KO JS, PARK SJ, et al. Efficient gamma-aminobutyric acid bioconversion by employing synthetic complex between glutamate decarboxylase and glutamate/GABA antiporter in engineeredEscherichiacoli[J].Journal of Industrial Microbiology & Biotechnology,2013,40(8):927-933.
[43] 陈琳,张充,吕凤霞,等.重组谷氨酸脱羧酶大肠杆菌合成γ-氨基丁酸条件的优化[J].食品科学,2015,36(1):158-163.
[44] KOOK MC,SEO M-J,CHEIGH CI,et al. Enhancement of γ-amminobutyric acid production byLactobacillussakeiB2-16 expressing glutamate decarboxylase fromLactobacillusplantarumATCC 14917[J].Journal of the Korean Society for Applied Biological Chemistry,2010,53(6):816-820.
[45] SHI Feng,LI You-xin.Synthesis of γ-aminobutyric acid by expressingLactobacillusbrevis-derived glutamate decarboxylase in theCorynebacteriumglutamicumstrain ATCC 13032[J]. Biotechnology Letter,2011,33(12):2 469-2 474.
[46] SHI Feng,JIANG Jun-jun,LI Yong-fu, et al. Enhancement of gamma-aminobutyric acid production in recombinantCorynebacteriumglutamicumby co-expressing two glutamate decarboxylase genes fromLactobacillusbrevis[J].Journal of Industrial Microbiology & Biotechnology,2013,40(11):1 285-1 296.
[47] TAKAHASHI C, SHIRAKAWA J, TSUCHIDATE T, et al. Robust production of gamma-amino butyric acid using recombinantCorynebacteriumglutamicumexpressing glutamate decarboxylase fromEscherichiacoli[J]. Enzyme and Microbial Technology, 2012, 51(3): 171-176.
[48] OKAI N,TAKAHASHI C,HATADA K,et al.Disruption ofpknGenhances production of gamma-aminobutyric acid byCorynebacteriumglutamicumexpressing glutamate decarboxylase[J].AMB Express,2014,4:20.
[49] 莫征杰,冯凤琴,叶慧.重组Bacillussubitilis(pMA5/lapgad)的构建及其在γ-氨基丁酸合成中的应用[J].食品科技,2014,35(9): 26-31.
[50] 丁伟, 张明俐, 史吉平等.表达谷氨酸脱羧酶重组枯草芽孢杆菌的构建及其发酵条件的优化[J]. 食品工业科技, 2015,36(23): 194-198.
[51] 乌云达来,张博润,郭雪娜,等.生物合成γ-氨基丁酸酿酒酵母谷氨酸脱羧酶基因的克隆与表达[J].食品科学,2015,36(13):131-136.
[52] 孙红梅,饶志明,李秀鹏,等.以葡萄糖为底物一步法合成γ-氨基丁酸整合型重组钝齿棒杆菌的构建[J].微生物学报,2013,43(8): 817-824.
[53] 张术聪.固定化植物乳杆菌合成γ-氨基丁酸及分离纯化的初步研究[D].无锡:江南大学;2010.
Genetically engineered modification of glutamate decarboxylase
JIN Chun-peng1, YANG Tao-wei2,3, XU Mei-juan2, ZHANG Xian2, RAO Zhi-ming2,3
1 (Patent Examination Cooperation Center of the Patent Office, SIPO, Beijing 100190, China) 2 (The Key Laboratory of Industrial Biotechnology, Ministry of Education, School of Biotechnology, Jiangnan University, Wuxi 214122, China) 3 (Jiangnan University (Rugao) Food Biotechnology Research Institute, Rugao 226500, China)
γ-Aminobutyric acid (GABA) is a kind of important non-protein amino acid. GABA can be used as a bioactive component in pharmaceutical, food, and chemical fields. The advantages of enzymatic synthesis of GABA are mild reaction conditions, simple operational procedure and easily available raw material. So, enzymatic synthesis of GABA by glutamate decarboxylase (GAD) has attracted growing attention in recent years. This review summarizes various strategies for molecular modification of GAD and construction of genetic engineered strain.
glutamate decarboxylase; γ-aminobutyric acid; molecular modification; construction of recombinant strain
10.13995/j.cnki.11-1802/ts.201612039
硕士,助理研究员(杨套伟为共同第一作者,饶志明教授为通讯作者,E-mail: raozhm@jiangnan.edu.cn)。
国家高技术研究发展计划(863计划) (2015AA021004);江苏省杰出青年科学基金(BK20150002);江苏省自然科学基金(BK20161292);江苏高校优势学科建设工程
2016-06-15,改回日期:2016-07-28
