GeneQuence试剂盒与国家标准法检测食品中沙门菌的比较
2017-01-07聂蓬勃刘炎艳莫仁湘康宝莱蕾硕湖南天然产物有限公司
□ 聂蓬勃 刘炎艳 莫仁湘 李 凡 康宝莱蕾硕(湖南)天然产物有限公司
GeneQuence试剂盒与国家标准法检测食品中沙门菌的比较
□ 聂蓬勃 刘炎艳 莫仁湘 李 凡 康宝莱蕾硕(湖南)天然产物有限公司
本文采用美国Neogen公司生产的沙门检测试剂盒GeneQuence结合DS2全自动酶标免疫分析仪对植物提取物进行沙门菌的检测,与传统检测的国家标准法进行对比。结果表明,该方法进行沙门菌的检测,与传统检测方法所得结果一致性达到99%。且该方法操作较传统方法简便,检测时间比传统方法缩短了2 f。
沙门菌;快速检测;GeneQuence
沙门菌(Salmonella spp.)是一种常见的食源性致病菌,引发人和动物的疾病,出现腹泻,急性肠胃炎等疾病。因此控制食品及其原料中的沙门氏菌尤为重要[1]。目前食品中沙门菌的检测主要采用GB4789.4-2010,该方法需经过五个步骤:①预增菌;②选择性增菌;③选择性平板分离;④生化鉴定;⑤血清学鉴定。该方法工作量大,检测时间长(需4~7天),易受检测人员的专业、经验等多种因素的影响,出现误判。因此,需寻求一种快速、有效、准确、简便的检测技术。
Neogen公司生产的沙门试剂盒GeneQuence是基于DNA分子杂交技术设计的。该法针对沙门菌核糖体RNA设计一段寡核苷酸探针,该探针用于与目标rRNA结合,结合后有显色反应,再经过Dynex设备的光路系统进行读数判定结果[2]。
Dynex DS2®全自动酶标免疫吸附(ELISA)分析仪是一款由电脑控制的微孔板处理系统[3],本文使用该分析仪配套Neogen®沙门菌检测试剂盒用于沙门菌的快速检测,该方法具有操作简单,灵敏度高,检测时间短的特点,与国家标准方法进行平行比对,结果显示,该方法与GB方法检测结果一致。
1 材料与方法
1.1 样品与试剂
1.1.1 样品
样品共100批,涵盖康宝莱蕾硕公司大部分类型的产品,测试样品及分类清单如下。
样品类型:绿茶提取物、红茶提取物、玉米须提取物、生姜提取物、瓜拉那果粉、洋葱粉、迷迭香提取物和苹果纤维粉各提取10份的数量;薄荷叶粉、葛根提取物、小茴香粉和人参提取物各提取5份的数量;样品编号分别为1-10、11-20、21-30、31-40、41-50、51-60、61-70、71-80、81-85、86-90、91-95、96-100。
1.1.2 标准菌株
阿伯尼沙门菌(Salmonella abony, NCTC 6017)
1.1.3 试剂与培养基
BPW缓冲蛋白胨水(陆桥);SC增菌液(陆桥);TTB增菌液(陆桥);XLDA平板(BD);HE平板(陆桥);BS平板(陆桥);TSI斜面(陆桥)。
1.2 仪器设备
二级生物安全柜:美国Labconco公司;恒温水浴锅:德国Julabo公司;Dynex系统:美国Dynex公司;恒温培养箱:德国Memmert公司。
1.3 实验方法
1.3.1 国家标准方法(GB 4789.4-2010)
以无菌操作称取25 g(或25 mL)样品,置于225 mL的缓冲蛋白胨水中,于(36±1)℃培养8~18 h。轻轻摇动培养过的样品混合物,移取1 mL,转种于10 mLTTB内,于(42±1)℃培养18~24 h。同时,另取1 mL,转种于10 mL SC内,于36±1℃培养18 h~24 h。分别用接种环取增菌液1 环, 划线接种于一个BS 琼脂平板和一个 XLD 琼脂平板。于36±1 ℃分别培养18 h~24 h,观察各个平板上菌落生长情况,疑似菌落用API鉴定试剂条进行进一步鉴定[4]。
1.3.2 Dynex方法
第一步:以无菌操作称取25 g(或25 mL)样品,置于225 mL的缓冲蛋白胨水中,于(36±1)℃培养24 h,为待测增菌液。
第二步:按照沙门试剂盒的说明书,分别配制:①裂解试剂:用于目标致病菌的裂解,释放出目标待测物rRNA(核糖体RNA)。②杂交溶液:用于目标的rRNA捕获或结合。③探针溶液:用于与目标rRNA结合与检测。④洗液:用于清洗微孔。⑤底物溶液,用于显色反应(加入微孔后,与溶液3中标记的HRP反应显色)。⑥终止液。
第三步:分别加入100 μL裂解溶液和400 μL待测增菌液至小试管中,混匀后置于(65±2.5)℃水浴中裂解5 min。
第四步:将第二步中配置的溶液和第三步配置的待测样品裂解液放置在Dynex仪器指定的位置上。
第五步:开启软件,按照软件提示进行自检,仪器自检完成后,将自动执行加样,加试剂,孵化,测定等操作,最终自动形成检测报告。
1.3.3 自然样品的检测
对以上共100个自然样品,分别使用国家标准方法和Dynex方法进行检测。
1.3.4 人工污染样品的检测
在经1.3.3步骤检测沙门氏菌为阴性的样品中,选择12个(每种类型样品1个),在其增菌液中添加阿伯尼沙门氏菌(Salmonella abony, NCTC 6017)标准菌株,加入量为10~100 CFU/mL。分别使用国家标准方法和Dynex方法进行检测。

表1 国家标准方法和Dynex方法检测结果
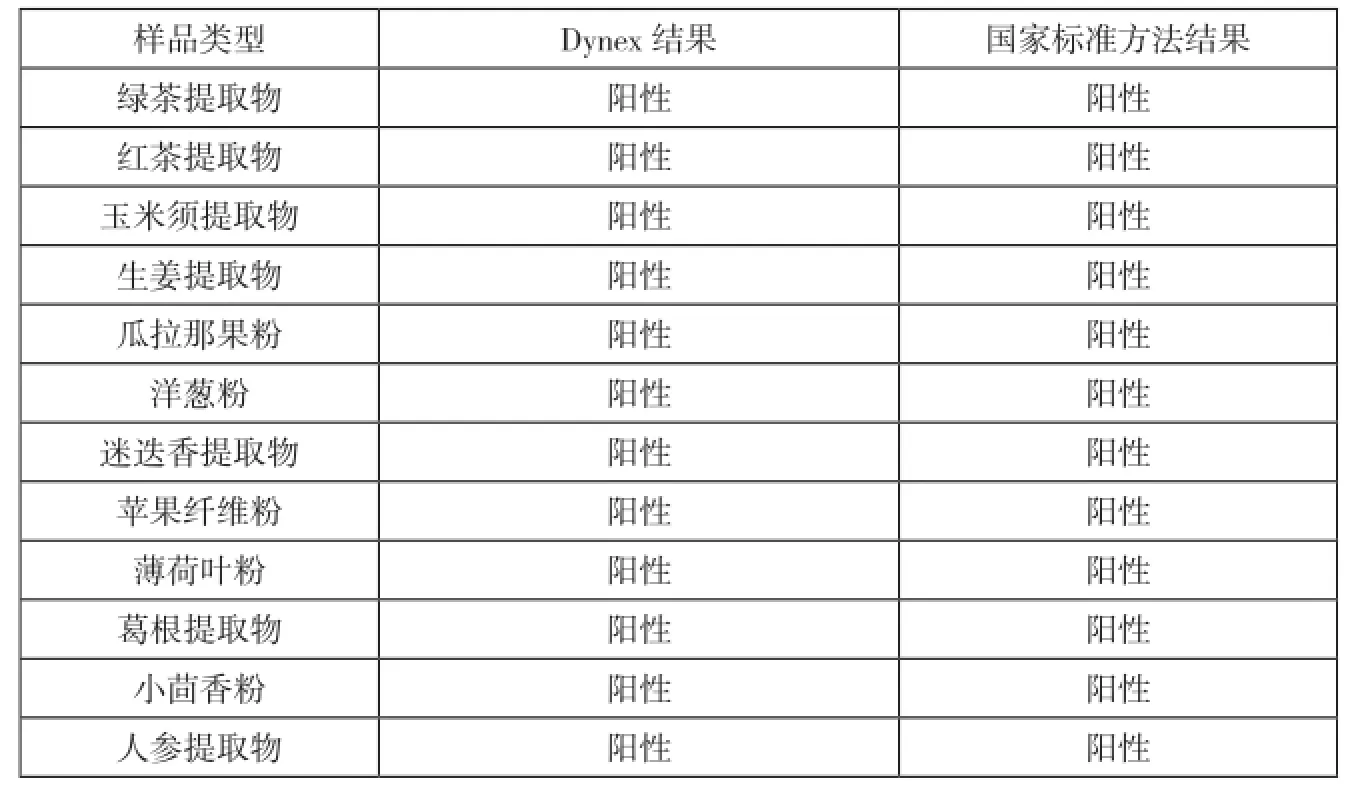
表2 两种方法对阿伯尼沙门菌的检测结果
2 结果与分析
2.1 自然样品的检测分析
对100批样品中12个品种分别使用国家标准方法和Dynex方法进行检测,结果见表1。
由表1可知,100个样品中,只有72号样品用Dynex检测为阳性,而经国家标准方法确认后,为阴性。因此可得知,用Dynex方法和GB方法对比,一致性可达99%。
2.2 污染样品的检测分析
对12个(每种类型样品1个)添加阿伯尼沙门菌(Salmonella abony, NCTC 6017)标准菌株的污染样品,分别使用国家标准方法和Dynex方法进行检测,结果见表2。试验结果表明,Dynex方法和国家标准方法都能够有效检出经浓度为10~100 CFU/mL阿伯尼沙门氏菌污染的样品。两种方法一致性达100%,且无假阴性结果。
3 结果与讨论
Dynex方法比国家标准方法操作简便,只需要配置一种培养基—缓冲蛋白胨水。而国家标准方法则需要配制很多种培养基。Dynex方法只需30 h左右即可出结果,而国家标准方法至少需要4 d。因此Dynex至少可缩短2 d的检测时间。Dynex方法结果判读由机器完成,而国家标准方法需有经验的人员进行判读。因此Dynex方法可减少由人员造成的误差。通过对112个样品进行检测方法比对,发现两种方法的符合率超过99%,因此可证实用Dynex方法进行沙门氏菌的检测是可靠的。
[1]SG Wilson, S Chan, M Deroo, et al. Development of a Colorimetric, Second Generation Nucleic Acid Hybridization Method for Detection of Salmonella in Foods and a Comparison with Conventional Culture procedure[J].Journal of food science, 1990, 55(5):1394-1398.
[2]袁辰刚,韩伟,谢小钰,等.沙门氏菌快速测试片在食品检测中的初步应用研究[J].食品安全质量检测学报,2015,6(1):293-298.
[3]田银芳,王翌明.ELISA方法与国标法在检测鲜奶中沙门氏菌的比较研究[J].中国乳品工业,1998,26(5):32-33.
[4]文其乙,焦新安,刘秀梵.酶免疫方法快速检测沙门氏菌的研究进展[J].肉品卫生,1995(7):27-29.
