胃粒细胞肉瘤误诊为非霍奇金淋巴瘤1例
2017-01-06朴文花
李 芳,柴 华,白 洁,朴文花
(宁夏回族自治区人民医院临床医学检验诊断中心,银川 750002)
·个案与短篇·
胃粒细胞肉瘤误诊为非霍奇金淋巴瘤1例
李 芳,柴 华,白 洁,朴文花△
(宁夏回族自治区人民医院临床医学检验诊断中心,银川 750002)
粒细胞肉瘤; 急性髓细胞白血病; 淋巴瘤
髓系肉瘤(GS)是指髓系原始细胞在髓外增殖,可同时发生于骨髓的髓系肿瘤,但也可单独发生[1]。其特点是在骨或髓外局部大量浸润形成实质性肿瘤。GS不是白血病的一种类型,而是急性髓细胞白血病的一种表现,就像骨髓急性髓细胞白血病(AML)一样,应尽一切努力对髓系肉瘤细胞遗传学和免疫表型进行分析。发病部位不确定,临床表现多样,误诊率较高[2]。为提高对该类疾病的认识,现将我院收治1例胃粒细胞肉瘤患者资料报道如下。
1 病例资料
患者,男,44岁,回族,主因“间断上腹疼痛2月”于2015年11月25日就诊本院急诊科,急诊查血常规:白细胞7.78×109/L,中性粒细胞44.2%,红细胞4.2×1012/L血红蛋白127 g/L,血小板230×109/L。肝功能:丙氨酸氨基转移酶(ALT)181 U/L,天门冬氨酸氨基转移酶(AST)122 U/L,总胆红素25.3 μmol/L。腹部彩超:胰腺炎并假性囊肿形成,肝内外胆管扩张,胆囊肿大,胆汁淤积。经本院肝胆外科会诊后以“急性胰腺炎、胰腺假性囊肿”急诊入院。2015年11月26日上午患者感到腹部疼痛难忍,较前加重。急诊腹部CT考虑患者上腹部包块破裂出血,急诊行“剖腹探查,胃大部切除术”。术中诊断“胃后壁间质瘤破裂出血,小肠及后腹膜广泛转移”。术后抗炎对症治疗,送重症监护室监护。2015年12月2日复查血常规:白细胞18.33×109/L,中性粒细胞未分类,血红蛋白127 g/L,血小板41×1012/L。肝功能:ALT 25 U/L,AST 20 U/L。外周血涂片:中性杆状核粒细胞1.0%,中性分叶核粒细胞22%,嗜酸粒细胞1%,嗜碱粒细胞2%,幼稚细胞20%,血小板散在分布少见。病理活检回报:胃窦溃疡伴出血穿孔,周围炎性肉芽肿形成伴淋巴组织高度反应性增生,其中可见弥漫中等偏大的转化淋巴细胞呈片状增生,较多浆细胞、中性粒细胞、嗜酸粒细胞及组织细胞浸润,局部可见核碎屑。免疫组织化学染色显示:淋巴细胞呈现非特异性表达,不完全排除黏膜免疫系统淋巴瘤可能。请血液内科会诊后建议行骨髓穿刺和骨髓活检。免疫组织化学染色结果显示瘤细胞:CD20(-),CD79a(-),CD3(-),ki-67(index 80%),CD10(-),Bcl-2(++),Bcl-6(-),MUM-1(-),CK-pan(-),MPO(++),CD34(+),CD117(+),ALK(-),CD30(-),EMA(-),CD38(-),CD138(-)。2015年12月15日患者突然出现恶心、呕吐并呕出较多新鲜血液,于胃镜予以止血治疗。2015年12月22日血常规:白细胞61.84×109/L,中性粒细胞未分类。宁夏医科大学总院病理科会诊意见考虑:T淋巴母细胞淋巴瘤可能性大。2015年12月24日转入血液内科专科治疗恶性淋巴瘤。2015年12月25日血常规:白细胞93.08×109/L,白细胞未分类,血小板26×1012/L。血液内科当日积极完善骨髓穿刺和活检,送检流式、染色体、融合基因等检查,向患者及家属交代病情后,暂予以VP方案诱导缓解治疗。复查外周血涂片:可见62%幼稚细胞。2015年12月29日淋巴瘤分期CT:双侧颈部、腋窝、腹股沟、腹腔内多发淋巴结肿大,考虑转移。流式结果考虑急性髓细胞白血病可能性大。首都医科大学附属北京友谊医院会诊意见:(胃切除)粒细胞肉瘤。结合上述实验室相关检查和临床,修正患者诊断为急性髓细胞白血病,分析患者入院时大出血为“急性髓细胞白血病所致为细胞肉瘤侵犯胃后壁肌层血管致破裂出血”。予以HA方案诱导化疗,并及时补充电解质、保肝、抑酸、水化等治疗。2015年12月31日血常规:白细胞29.23×109/L,白细胞未分类,红细胞2.83×1012/L,血红蛋白85 g/L,血小板10×1012/L。2016年1月12日复查外周血涂片:已无原始细胞,患者处于粒缺状态。2016年1月20日患者病情稳定,情况良好,外周血中未见原始细胞,粒细胞逐渐回升,准予出院、定期化疗。
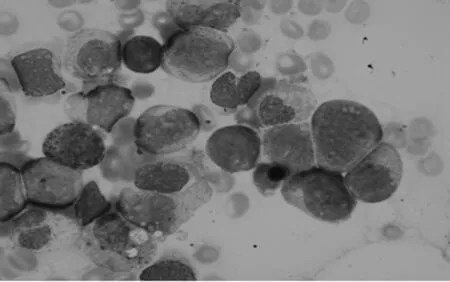
图1 骨髓涂片(瑞姬染色×100)

图2 骨髓活检(HGF染色×40)

图3 胃活检切片(HE染色×40)

图4 胃活检切片(MPO染色×40)
2 讨 论
GS误诊率高达47%,原发者甚至高达75%~86%。孤立部位的GS很难诊断,如有白血病外周血、或骨髓异常改变时有提示作用[3]。有些病例GS可能预示着疾病治疗后复发,而其他病例可能是发生急性白血病的最初迹象。该患者入院时三系计数正常,仅表现为“间断性上腹痛”。血常规显示三系细胞计数均正常,随后复查血常规显示白细胞计数逐渐升高以至最后无法分类。成人大约1/3 GS与骨髓疾病同时发生,1/3患者先前有GS病史。通过荧光原位杂交或细胞遗传学观察,约55%病例可检出染色体异常,该患者外送染色体回报:del(7)(q31),inv(16)(p13q22)idem,-2,add(17)(p13),+mar(6)。存在复杂染色体异常,多提示预后不良[4-5]。
GS定义为:髓系原始细胞浸润并破坏原有的组织结构。无论骨髓或外周血的状态如何,出现GS必须诊断AML[2]。原发疾病局限于GS的患者,精确分类可能有困难,因此本病例在初诊阶段一直误诊为淋巴瘤。GS的原始细胞常表现为成片的单个核细胞,在淋巴结则出现在滤泡间区。原始细胞核呈圆形或折叠,染色质纤细,点彩状染色质的特征通常比大B细胞淋巴瘤更明显。流式细胞免疫表型分析表明:GS不表达T系或B系淋巴细胞的特异性标记,表达粒系或粒-单核细胞的标记,如CD13、CD33、MPO、CD14或CD64。与其他部位的AML一样,异常表达淋巴系的抗原也很常见[2、6]。本病例骨髓流式结果回报:检测标本在CD45/SSC点图上射门分析,异常幼稚细胞群约占骨髓有核细胞总数49.5%,其免疫表型CD34++、CD33++、HLA-DR++、CD123++、CD9++、CD38+部分、CD117++、MPO++、CD13++、CD64+部分、CD19+少部分、CD11c+部分、CD15+少部分。单核细胞群约占25.4%,其比例明显升高,主要表达MPO、CD13、CD33、CD64、CD14、HLA-DR、CD11b、CD11c、CD123、CD38、CD9、CD15为分化成熟单核细胞;粒细胞约占13.1%,主要表达MPO、CD13、CD33、CD64、HLA-DR、CD11b、CD11c、CD9、CD15为部分分化粒细胞,其免疫表型未见明显异常。
GS的鉴别诊断主要针对淋巴瘤,尤其是分化较差的DLBL、LBL、母细胞样MCL。仅靠形态学鉴别有困难。纤细的核染色质和大量核分裂象有助于区分大B细胞淋巴瘤[2]。目前尚无一个针对GS诊断特异抗体,但是免疫表型对于诊断GS时仍是必不可少的。GS可表达的抗体谱系较广,这与细胞原始和分化阶段不同有关,关键在于抗体的搭配使用和结果的分析判断[7]。髓过氧化物酶是目前公认诊断GS最敏感和特异的标记物,可在粒细胞分化的各个阶段表达,但低分化母细胞型肿瘤细胞常不表达,髓系细胞肿瘤的阳性表达率高达93%[8]。
[1]Pileri SA,Orazi A,Falini B,et al.WHO Classification of Tumours of Hematopoietic and Lymphoid Tissuees[J].IARC,2008,17(2):140-141.
[2]陈刚,李小秋.血液病理学[M].北京:北京科学技术出版社,2013:795.
[3]范菲菲,尚可,贾永旭,等.原发性粒细胞肉瘤1例并文献复习[J].肿瘤基础与临床,2010,23(6):533-534.
[4]Li XP,Liu WF,Ji SR,et al.Isolated pancreatic granulocytic sarcoma:a case report and review of the literature[J].World J Gastroenterol,2011,17(4):540-542.
[5]李素毅,周健,宋永平,等.粒细胞肉瘤28例临床分析[J].肿瘤防治研究,2013,40(3):273-277.
[6]于慧,孙雪梅,陈薇,等.粒细胞肉瘤4例并文献复习[J].临床血液学杂志,2014,27(1):51-54.
[7]葛存锦,仝巧云,郑世华,等.小肠粒细胞肉瘤致消化道出血1例报告[J].中国实用外科杂志,2015,35(9):1028-1029.
[8]周志韶,朱岩,虞梅宁,等.粒细胞肉瘤18例临床病理分析[J].诊断病理学杂志,2011,18(5):329-332.
10.3969/j.issn.1673-4130.2016.24.064
C
1673-4130(2016)24-3524-03
2016-04-11
2016-06-29)
△通讯作者,E-mail:wenhuapiao@163.com。
