席夫碱稀土配合物与DNA的作用方式
2017-01-05李小芳冯小强朱元成
李小芳, 冯小强*, 杨 声, 朱元成
(1. 天水师范学院 化工学院, 甘肃 天水 741001; 2. 定西师专 化学系, 甘肃 定西 743000)
席夫碱稀土配合物与DNA的作用方式
李小芳1, 冯小强1*, 杨 声2, 朱元成1
(1. 天水师范学院 化工学院, 甘肃 天水 741001; 2. 定西师专 化学系, 甘肃 定西 743000)

席夫碱; 稀土; DNA; 循环伏安法; 光谱法
1 引 言
席夫碱具有碳氮双键的亚胺或甲亚胺基团,容易和金属离子配位得到结构各异的配合物,从而赋予了其丰富的功能活性,是潜在的一种新型抗癌、抗肿瘤和抗氧化药物[1-3]。近期国内研究者对席夫碱及配合物的合成和生物活性做了大量研究,如宁夏大学学者[4]发现合成的3,5-二碘水杨醛缩2,6-二氨基吡啶席夫碱金属配合物对藤黄微球菌有良好的抑制作用,并且是以插入方式与ct-DNA结合的;南华大学学者[5]合成的2-羟基-1-萘甲醛缩2,6-二氨基吡啶席夫碱以及钍配合物对枯草杆菌、大肠杆菌、乳酸菌有良好的抑制作用,且配合物的抑菌活性好于席夫碱本身;贵阳医学院学者[6]以三齿席夫碱配体H2L{1-苯基-3-[(2-羟基苯)亚胺]-1-丁酮}和单齿N-杂环[咪唑(Himdz),2-甲基咪唑(Mimdz)]分别与Ni2+配位得到的配合物,对金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌和奇异变形杆菌具有一定的抑菌活性;陕西科技大学学者[7]合成双乙酰基二茂铁双肼腙配体,分别与Cu2+、Ni2+、Zn2+、Pb2+、Cd2+合成的金属配合物比其配体有更高的抗菌活性。Ejiah等[8]通过体外抑菌法研究发现,水杨醛缩氨基苯甲酸席夫碱对细菌大肠杆菌、绿浓杆菌、金黄色葡萄球菌、粪肠球菌具有很好的抑菌活性。Raman[9]等合成的席夫碱金属(Cu2+、Ni2+、Co2+、Zn2+)配合物对伤寒沙门菌、大肠杆菌、金黄色葡萄球菌、枯草芽胞杆菌4种细菌和黑曲霉、黄曲霉、纹枯病菌3种真菌有很好的抑制作用,在氧化剂存在下仅有席夫碱铜配合物能够切割ct-DNA。
研究发现,大多数抗肿瘤药物的药理活性与DNA插入结合方式有关。因此,研究药物小分子与DNA间的作用机制,有助于揭示抗肿瘤药效机理,为寻求新型高效低毒抗肿瘤药物提供导向。稀土离子能有效地和核酸结合而优于过渡金属及其配合物。关于稀土配合物的合成及与生物大分子的相互作用研究较多[10-11]。以糠醛和对氨基苯磺酸制得的席夫碱为配体,与稀土离子(La3+,Nd3+,Eu3+)反应合成配合物,有可能筛选出比原来单一原料更低毒、高效和经济的抗菌、抗肿瘤药物。虽然席夫碱稀土配合物的合成和表征有过一些研究,但关于其与DNA相互作用的研究报道却很少。基于席夫碱独特的生理活性,本文合成了3种糠醛缩对氨基苯磺酸席夫碱的稀土配合物,通过紫外吸收光谱、荧光光谱和循环伏安法研究了席夫碱及稀土配合物分别与鲱鱼精DNA之间的作用模式。
2 实 验
2.1 材料与仪器
鲱鱼精DNA(Sigma公司)。RF-5301型荧光分光光度计(日本岛津公司);CHI660B电化学工作站(上海辰华仪器有限公司);UV-2450紫外-可见分光光度计(日本岛津公司)。
2.2 糠醛缩对氨基苯磺酸席夫碱及稀土配合物的制备
对氨基苯磺酸用40 mL 5%的NaOH溶液溶解,通入氮气,在60 ℃搅拌下加入等摩尔的糠醛,反应溶液即刻由淡黄色变为红棕色,最后变成褐色。继续恒温回流2 h。反应结束后,将反应液减压浓缩后加入大量无水乙醇,马上有黄色沉淀产生。抽滤、干燥得土黄色席夫碱,产率85%。
在席夫碱水溶液中缓慢加入等摩尔量的稀土氯化物,40 ℃恒温反应5 h,然后用5%NaOH调pH至弱碱性,即刻有沉淀产生。静置抽滤,干燥得稀土配合物。
2.3 席夫碱稀土配合物与鲱鱼精DNA的作用
DNA在金电极表面的自组装参看文献[12],电化学实验过程参看文献[13];紫外光谱和荧光光谱法研究稀土配合物与DNA相互作用的具体实验过程参看文献[14]。
3 结果与讨论
3.1 配合物表征
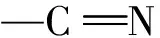
3.2 紫外光谱法研究配合物与DNA的作用
席夫碱配体及3种稀土配合物的紫外吸收光谱数据及图如表1和图1所示。席夫碱在246.5 nm和200.5 nm处产生2个很强的吸收峰。与稀土离子配位形成配合物后,吸收峰较席夫碱在246.5 nm和200.5 nm的吸收峰分别红移11~16 nm和蓝移5 nm。配合物除了出现配体的一些峰外,还在213~216 nm附近产生新的吸收峰。紫外光谱表明席夫碱与稀土离子配位成键形成了新的配合物。合成的3种稀土配合物的紫外光谱相似,说明它们的结构也相似。
席夫碱及3种稀土配合物在加入DNA前后的紫外光谱如图2所示。随着DNA不断加入到配合物溶液中,所引起的光谱扰动相对较大,吸收峰的形状虽然几乎没有变化,但吸光度逐渐下降,即出现了减色效应,在195 nm处的吸收峰峰位稍有红移趋势。吸光度降低,是由于配合物与DNA的磷酸基团发生了相互作用,使得DNA链的缠绕性增大,DNA的空间结构趋于缩拢,发色基团被部分内陷包裹,吸收跃迁偶极矩减小,导致发生减色效应。小分子吸收光谱出现减色效应和红移现象是该小分子与DNA发生嵌插作用的依据。从图2紫外吸收光谱的变化可判断3种稀土配合物及席夫碱均以嵌入方式与鲱鱼精DNA发生相互作用,从而形成了新的化合物[15]。此外,减色效应的大小与插入程度正相关,吸光度下降程度的大小也反映了小分子与DNA之间结合能力的强弱,一般而言,小分子的吸收峰强度下降越大,则与DNA的作用能力越强。在浓度相同的这3种配合物及席夫碱中,席夫碱-Eu和席夫碱-La分别与DNA作用后的减色程度更为明显,而席夫碱-Nd较小,席夫碱最小。这说明席夫碱-Eu和席夫碱-La插入程度较大,而席夫碱-Nd插入程度较小,席夫碱与DNA的插入程度最小,即与DNA间的作用能力顺序为:Eu (Ⅲ)>La(Ⅲ)>Nd(Ⅲ)>席夫碱。这可能是席夫碱配体与DNA发生作用的同时,稀土离子也参与了与带负电荷的DNA作用,最终导致DNA主链线电荷密度减小,缠绕增大,进而增强了与DNA的结合作用。
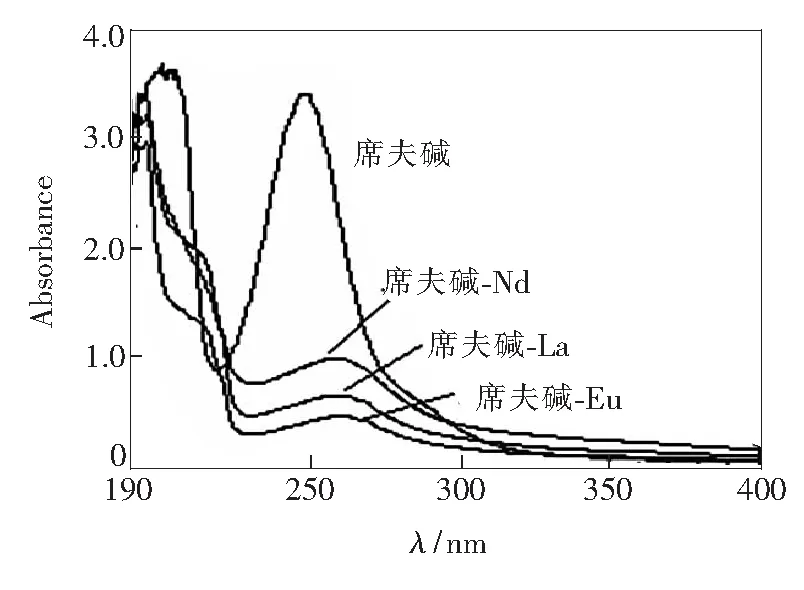
图1 席夫碱及3种稀土配合物的紫外吸收光谱
Fig.1 UV spectra of Schiff base and three kinds of complexes

表1 席夫碱及3种稀土配合物的紫外光谱数据
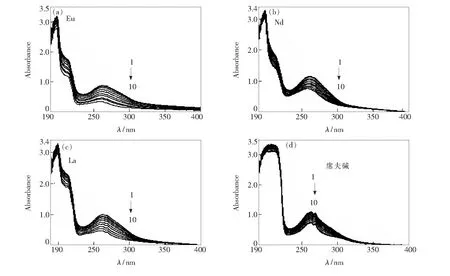
c(complex)=0.5 mg·mL-1, c(DNA)=0.1 mg·mL-1 (20 μL per scan, 1~10: 0~180 μL)
图2 DNA加入前后席夫碱及稀土配合物的紫外吸收光谱。(a) Eu配合物;(b) Nd配合物;(c) La配合物; (d) 席夫碱。
Fig.2 UV absorption spectra of Schiff base and complexes before and after DNA addding. (a) Eu complex. (b) Nd complex. (c) La complex.(d) Schiff.
3.3 荧光光谱法研究配合物与DNA的作用
游离态的中性红(NR)自身的荧光很弱,但当NR分子以嵌插方式与DNA结合后,体系的荧光强度会大幅度增大。但是,当有一个能取代键合的NR或能破坏DNA二级结构的分子加入时,NR-DNA体系的荧光会发生猝灭或部分猝灭[16]。以550 nm为激发波长,测得DNA-NR体系在596 nm处有一强的荧光发射峰,如图3所示。逐渐滴加席夫碱或稀土配合物时,明显看到在596 nm处的荧光强度也随之逐渐降低,峰位并没有明显的移动。这说明席夫碱及稀土配合物能够猝灭DNA-NR体系的荧光,即席夫碱及稀土配合物与NR一样,和DNA存在相同的作用机理,导致席夫碱及稀土配合物与NR竞争与DNA的结合,使得NR在DNA的结合位点上逐渐被置换出来,溶液中游离态的NR分子数增多,荧光较DNA-NR减弱。但席夫碱及稀土配合物的浓度增大到一定程度时,荧光强度下降幅度很小,说明此时席夫碱及稀土配合物、NR和DNA三者之间的作用达到平衡,与DNA的结合已经达到饱和。因此,可以推断出席夫碱及稀土配合物都能够与DNA以插入方式发生键合。此外,荧光强度的下降程度能够说明小分子与DNA作用强度,从图3的变化程度来看,滴加配合物后的DNA-NR体系的荧光强度下降程度远远大于席夫碱,说明席夫碱形成配合物后与DNA的作用强度强于席夫碱本身,这主要是稀土离子在起作用。
3.4 循环伏安法研究配合物与DNA的相互作用
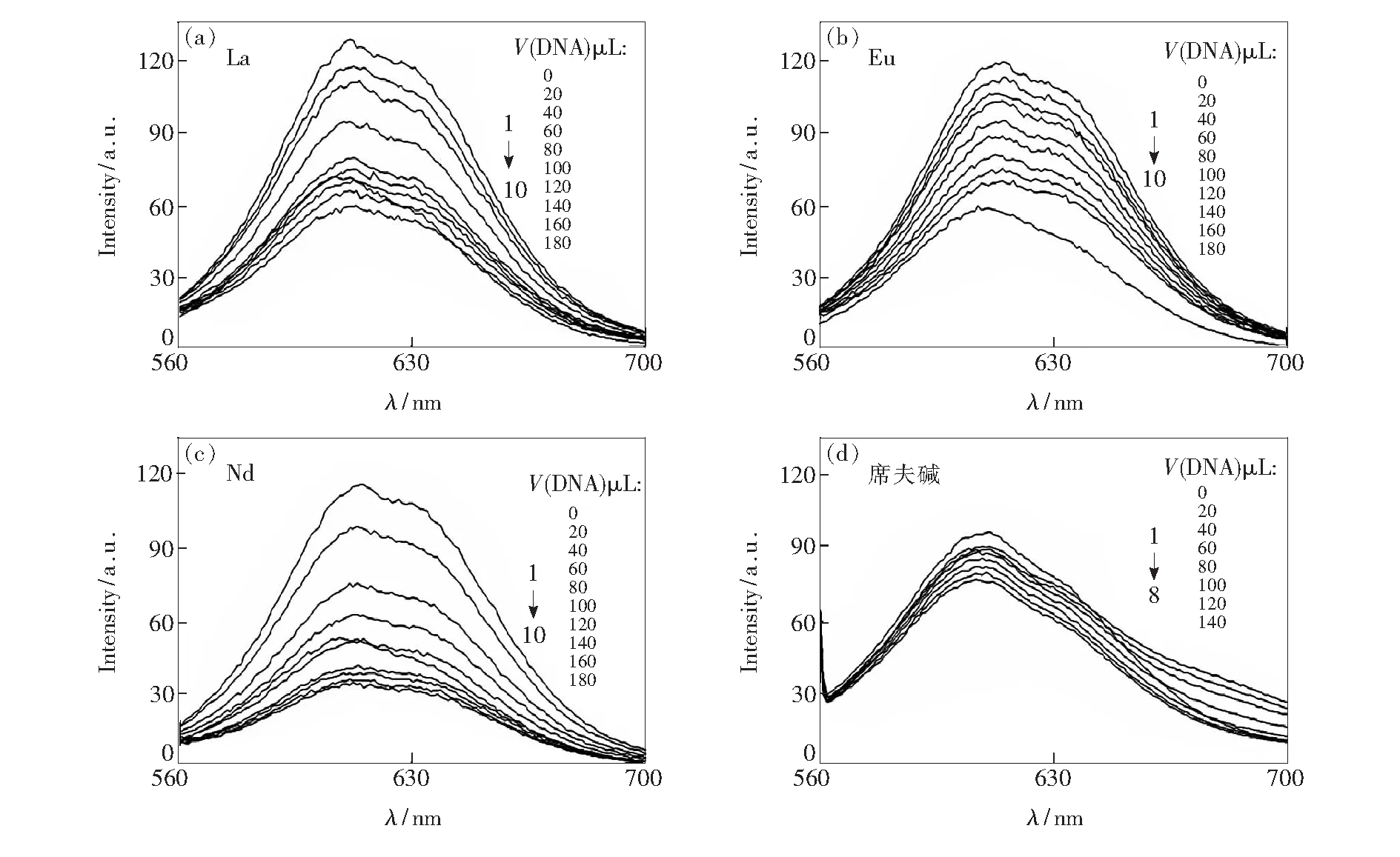
图3 席夫碱及稀土配合物对DNA-NR体系荧光光谱的影响。(a) La配合物;(b) Eu配合物;(c) Nd配合物;(d) 席夫碱。
Fig.3 Effect of Schiff base and complex on the fluorescence spectra of DNA-NR. (a) La complex. (b) Eu complex. (c) Nd complex. (d) Schiff.


图4 席夫碱配合物存在下,K4Fe(CN)6在Au/DNA电极上的循环伏安曲线。(a)Nd配合物;(b)La配合物;(c)Eu配合物。
Fig.4 CV curves of K4Fe(CN)6in Schiff base complex solution. (a) Nd complex. (b) La complex. (c) Eu complex.
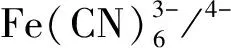

图5 席夫碱配合物存在下,扫速对K4Fe(CN)6在Au/ DNA电极上循环伏安曲线的影响。(a) Eu配合物;(b) La配合物;(c) Nd配合物。
Fig.5 Effect of scan rate on CV curves of K4Fe(CN)6in Schiff base complex solution. (a) Eu complex. (b) La complex. (c) Nd complex.
4 结 论

[1] 宋玉民,马俊怀,张玉梅. 姜黄素苯胺希夫碱稀土配合物的抑菌性研究 [J]. 化学试剂, 2013, 35(12):1069-1072. SONG Y M, MA J H, ZHANG Y M. Antibacterial properties of complexes of curcumin aniline Schiff base with rare earth [J].Chem.Reag., 2013, 35(12):1069-1072. (in Chinese)
[2] XU D F, MA S Z, DU G Y,etal.. Synthesis, characterization, and anticancer properties of rare earth complexes with Schiff base and o-phenanthroline [J].J.RareEarths, 2008, 26(5):643-647.
[3] 林明丽,刘醒民,崔秀兰,等. 稀土与苯并咪唑甲基酮缩二乙三胺Schiff碱配合物的合成、表征及生物活性 [J]. 稀土, 2004, 25(6):38-40. LIN M L, LIU X M, CUI X L,etal.. Synthesis, characterizition and biological activity of rare earth complexes with benzimidazole-semidiethylenetriamine Schiff base [J].Chin.RareEarths, 2004, 25(6):38-40. (in Chinese)
[4] 高敏,杨天林,李慧,等. 3, 5-二碘水杨醛缩2, 6-二氨基吡啶席夫碱及其金属配合物的制备及与ct-DNA的作用研究 [J]. 化学通报, 2011, 74(6):562-568. GAO M, YANG T L, LI H,etal.. Synthesis of 3, 5-diiodo-salicylalidehyde and 2, 6-diaminopyridine Schiff base andct-DNA cleavage by its metal complexes [J].Chemistry, 2011, 74(6):562-568. (in Chinese)
[5] 汤金辉,王宏青,王榆元,等. 2-羟基-1-萘甲醛缩2, 6-二氨基吡啶钍的席夫碱配合物的合成及其抑菌活性的研究[J]. 应用化工, 2014, 43(1):31-34. TANG J H, WANG H Q, WANG Y Y,etal.. Synthesis of 2-hydroxynaphthaldehyde and 2, 6-diaminopyridine Schiff base complex of thorium and bacteriostatic activity studies [J].Appl.Chem.Ind., 2014, 43(1):31-34. (in Chinese)
[6] 张奇龙,冯广卫,王丽,等. 基于Schiff 碱及咪唑类配体的镍(Ⅱ)配合物的合成、结构及其抑菌活性研究 [J]. 无机化学学报, 2014, 30(5):1025-1030. ZHANG Q L, FENG G W, WANG L,etal.. Synthesis, crystal structure and antibacterial activity of Schiff base Ni(Ⅱ) complexes containing Schiff base and imidazole [J].Chin.J.Inorg.Chem., 2014, 30(5):1025-1030. (in Chinese)
[7] 刘玉婷,殷艳佼,李鑫,等. 含二茂铁基Schiff 碱及其金属配合物的合成、表征及抑菌活性 [J]. 精细化工, 2014, 31(4):467-470. LIU Y T, YIN Y J, LI X,etal.. Synthesis and antibacterial activity of Schiff base bearing ferrocenyl and its metal complexes [J].FineChem., 2014, 31(4):467-470. (in Chinese)
[8] EJIAH F N, FASINA T M, FAMILONI O B,etal.. Substituent effect on spectral and antimicrobial activity of Schiff bases derived from aminobenzoic acids [J].Adv.Biol.Chem., 2013, 3(5):475-479.
[9] RAMAN N, FATHIMA S S A, RAJA J D. Designing, synthesis and spectral characterization of Schiff base transition metal complexes: DNA cleavage and antimicrobial activity studies [J].J.Serb.Chem.Soc., 2008, 73(11):1063-1071.
[10] 孙慧娟,王忠侠,吕杨超,等. 桂皮酸-邻菲啰啉稀土配合物的合成及其与DNA作用研究 [J]. 稀土, 2014, 35(6):27-32. SUN H J, WANG Z X, LV Y C,etal.. Studies on synthesis of REphen (cin)3and interaction with CT-DNA [J].Chin.RareEarths, 2014, 35(6):27-32. (in Chinese)
[11] 霍丽娜,刘伟,杨天林,等. 新型铈苦味酸配合物的合成、表征及其与白蛋白相互作用 [J]. 稀土, 2014, 35(2):37-43. HUO L N, LIU W, YANG T L,etal.. Synthesis, characterization and interaction of a novel Ce(Ⅲ) picorate complex with HSA, BSA and VOA [J].Chin.RareEarths, 2014, 35(2):37-43. (in Chinese)
[12] 胡全,张克军,金辉乐,等. 电化学法研究苯磺酰类5-氟尿嘧啶衍生物与双链和G-四链DNA的相互作用 [J]. 中国科学: 化学, 2012, 42(6):792-798. HU Q, ZHANG K J, JIN H L,etal.. Electrochemical investigation on the interaction of benzene sulfonyl 5-fluorouracil derivatives with double-stranded DNA and G-quadruplex DNA [J].Sci.Sin.Chim., 2012, 42(6):792-798. (in Chinese)
[13] 李小芳,冯小强,杨声,等. 丁二酰化壳寡糖稀土配合物与鲱鱼精DNA相互作用的电化学及光谱学研究 [J]. 发光学报, 2013, 34(12):1662-1666. LI X F, FENG X Q, YANG S,etal.. Interaction of succinic-oligochitosan rare earth complexes with herring sperm DNA by electrochemical and spectral methods [J].Chin.J.Lumin., 2013, 34(12):1662-1666. (in Chinese)
[14] 李小芳,冯小强,张宏伟,等. 甲基丙烯酸-8-羟基喹啉-镧配合物的合成及与鲱鱼精DNA相互作用的光谱学研究 [J]. 化学研究与应用, 2014, 26(9):1406-1410. LI X F, FENG X Q, ZHANG H W,etal.. Synthesis and DNA-binding of La(Ⅲ)complex with methacrylic acid and 8-hydroxyquinoline [J].Chem.Res.Appl., 2014, 26(9):1406-1410. (in Chinese)
[15] 王丽娟,杨天林,杨欢春. [RE(pic)L](pic)2·6H2O的合成、荧光性质及与DNA作用方式初探 [J]. 稀土, 2010, 31(6):6-11. WANG L J, YANG T L, YANG H C. Synthesis, fluorescence property and preliminary DNA-binding studies of [RE(pic)L] (pic)2·6H2O [J].Chin.RareEarths, 2010, 31(6):6-11. (in Chinese)
[16] 曹瑛,李一峻,何锡文. 中性红作为DNA作用方式光谱探针的研究 [J]. 高等学校化学学报, 1999, 20(5):709-712. CAO Y, LI Y J, HE X W. Studies on neutral red as interacting mode spectroscopic probe of DNA [J].Chem.J.Chin.Univ., 1999, 20(5):709-712. (in Chinese)
[17] RODRIGUEZ M, BARD A J. Electrochemical studies of the interaction of metal chelates with DNA. 4. Voltammetric and electrogenerated chemiluminescent studies of the interaction of tris (2, 2′-bipyridine) osmium(Ⅱ) with DNA [J].Anal.Chem., 1990, 62(24):2658-2662.
[18] PATIENTE N, SIERRA S, AIRAKSINEN A. Action of mutagenic agents and antiviral inhibitors on foot-and-mouth disease virus [J].VirusRes., 2005, 107(2):183-193.
[19] CARTER M T, RODRIGUEZ M, BARD A J. Voltammetric studies of the interaction of metal chelates with DNA. 2. Tris-chelated complexes of cobalt(Ⅲ) and iron(Ⅱ) with 1, 10-phenanthroline and 2, 2b′-bipyridine [J].J.Am.Chem.Soc., 1989, 111(24):8901-8911.
[20] ERKKILA K E, ODOM D T, BARTON J K. Recognition and reaction of metallointercalators with DNA [J].Chem.Rev., 1999, 99(9):2777-2796.

李小芳(1983-),女,甘肃甘谷人,硕士,实验师,2009年于兰州大学获得硕士学位,主要从事功能高分子及有机稀土配位的研究。
E-mail: tslxffxq@163.com

冯小强(1979-),男,甘肃华亭人,硕士,副教授,2007年于兰州大学获得硕士学位,主要从事功能高分子方面的研究。
E-mail: fengxiaoqiang1979@163.com
Interaction of Schiff Base Rare Earth Complexes with Herring Sperm DNA
LI Xiao-fang1, FENG Xiao-qiang1*, YANG Sheng2, ZHU Yuan-cheng1
(1.CollegeofChemicalEngineeringandTechnology,TianshuiNormalUniversity,Tianshui741001China;2.ChemistryDepartment,DingXiTeachers’College,Dingxi743000,China)
Schiff base; rare earth complex; DNA; cyclic voltammetry; spectra method
2016-03-08;
2016-04-05
国家自然科学基金(51063006); 天水师范学院“青蓝”人才工程和中青年教师科研项目(TSA1508)资助
1000-7032(2016)07-0873-08
O657.3
A
10.3788/fgxb20163707.0873
*CorrespondingAuthor,E-mail:fengxiaoqiang1979@163.com
