不同相对分子质量PEG-CHMC修饰乳剂对二次注射PE2000诱导产生ABC现象的研究
2017-01-05郭立刚黄振君邓意辉
焦 姣,孙 晶,范 迪,郭立刚,黄振君,邓意辉*
(沈阳药科大学 药学院,辽宁 沈阳 110016)
不同相对分子质量PEG-CHMC修饰乳剂对二次注射PE2000诱导产生ABC现象的研究
焦 姣,孙 晶,范 迪,郭立刚,黄振君,邓意辉*
(沈阳药科大学 药学院,辽宁 沈阳 110016)
目的研究比较不同相对分子质量PEG-CHMC修饰乳剂(PEG-CHMC coating emulsion,CHMCE)在大鼠体内的药动学行为及其对二次注射PEG2000-DSPE修饰乳剂(PEG2000-DSPE coating emulsion,PE2000)诱导的ABC现象,探究PEG相对分子质量对乳剂药动学行为及ABC现象的影响。方法以摩尔分数10% PEG修饰密度制备载药乳剂CHMCE和PE,以磷脂剂量5 μmol·kg-1进行大鼠尾静脉注射,分别于不同时间点进行静脉取血,处死大鼠后分离肝、脾组织,血浆和组织样品经处理后通过 HPLC分析药物含量。结果通过比较药动学参数AUC(0-240 min)、tMRT(0-240 min)可知,高相对分子质量CHMCE(1 000、2 000、5 000)的循环时间较低相对分子质量 CHMCE(400、600、800)有所延长,但延长程度不高;CHMCE诱导PE2000产生ABC现象的结果显示,低相对分子质量CHMCE无ABC现象,而高相对分子质量CHMCE诱导了一定强度的ABC现象(CHMCE1000、CHMCE2000和CHMCE5000的ABC index(0-60 min)分别为0.64、0.59和0.53)。结论PEG相对分子质量在CHMCE的药动学行为及ABC现象的产生中具有重要影响,研究结果对PEG相对分子质量在ABC现象中的影响规律进行了补充,为PEG化制剂相对分子质量的选择提供了一定借鉴。
药剂学;PEG相对分子质量;加速血液清除现象;聚乙二醇-胆固醇碳酸酯;循环时间;ABC index
近些年,使用聚乙二醇(polyethylene glycol,PEG)对纳米载药体系进行修饰,即 PEG化(pegylation)技术,极大地解决了载体易与血浆中调理素结合而被单核巨噬细胞系统(mononuclear phagocytic system,MPS)摄取这一应用障碍,延长载体在血液中的循环时间、提高载体的靶向性和降低载体的免疫原性,从而推进了纳米载药体系的应用与发展[1]。但是,Dams等[2]研究指出,PEG化脂质体间隔几天重复注射于同一动物体内时,二次注射制剂的血药浓度迅速降至较低水平 ,即产生了加速血液清除(accelerated blood clearance,ABC)现象。这一现象不仅削弱了PEG化制剂的长循环优势,也对临床应用造成了极大限制,引起了研究者们的广泛关注。
一般而言,PEG-二硬脂酰磷脂酰乙醇胺(N-(carbonyl-methoxy polyethyleneglycol)-1,2-distearoyl-sn-glycero-3-phos-phoethanolamine,PEG-DSPE)是制备PEG化载体的常用材料,其PEG与脂质间的连接键为酰胺键,此化学键在体内具有较高的稳定性、不易降解,使它作为TI-2型抗原持久地刺激脾脏边缘区B细胞,进而产生大量的抗-PEG IgM,加快了MPS对二次注射PEG化制剂的识别摄取[3-5],即诱导了ABC现象。针对此问题,Xu等[6]分别以羧酸酯键和碳酸酯键将脂质部分与 PEG连接起来,形成可断裂 PEG-脂质衍生物 PEG-CHEMS(methoxy poly(ethylene glycol) 2000-cholesteryl methylcarbonate,PEG-CHEMS)和聚乙二醇-胆固醇碳酸酯(methoxypoly(ethylene glycol)-cholesteryl methyl carbonate,PEG-CHMC),在体内酯酶的作用下,酯键逐渐断裂致使PEG脱落,降低了 PEG化制剂对脾脏的刺激作用从而减弱 ABC现象。遗憾的是,此研究并未考察PEG-CHMCES和PEG-CHMC对免疫系统的影响,也未进行其他PEG相对分子质量衍生物引发ABC现象的相关研究。早期有文章报道指出,PEG5000-DSPE 修饰脂质体诱导小鼠产生 ABC现象的程度远低于PEG2000-DSPE修饰脂质体所诱导ABC现象的程度[4],但未研究PEG相对分子质量小于1 000时对 ABC现象的影响。因此,本文作者制备了不同相对分子质量 PEG-CHMC修饰乳剂(PEG-CHMC coating emulsion,CHMCE),并对此乳剂在大鼠体内药动学行为及其诱导二次注射PEG2000-DSPE修饰乳剂(PEG2000-DSPE coating emulsion,PE2000)产生的ABC现象进行研究,以期探究不同相对分子质量(PEG)对CHMCE体内行为的影响,同时为解决ABC现象提供一个新思路。
1 仪器与材料
BS124s电子分析天平(德国Sartorius公司),JY92-2D超声波细胞粉碎机(宁波新芝科器研究所),DF-101S集热式恒温加热磁力搅拌器(巩义英峪予华仪器厂),Anke TDL80-2B离心机(上海安亭科学仪器厂),Type 37600 mixer(美国Thermolyne公司),P230高压恒流泵和HW-2000色谱数据处理工作站(大连依利特分析仪器有限公司),AT-130柱温箱(天津金洲科学仪器有限公司),高精度全自动交流稳压器(中川电气科技有限公司),Nicomp-380 激光粒度测定仪(美国PSS公司),EDTA-K2 抗凝真空采血管(湖南浏阳医用仪具厂),SHB-3循环水多用真空泵(郑州杜甫仪器厂),KQ5200B声波清洗器(昆山超声仪器有限公司)。
维生素E烟酸酯(tocopheryl nicotinate,TN,东北制药集团股份有限公司),蛋黄卵磷脂 E80 (E80,美国 LIPOID GmbH公司,注射级),聚乙二醇-胆固醇碳酸酯(methoxypoly(ethylene glycol)-cholesteryl methyl carbonate,PEG-CHMC,自行合成),聚乙二醇2000-二硬脂酰磷脂酰乙醇胺 ( N-(carbonyl-methoxy polyethyleneglycol-2000)-1,2-distearoyl-sn-glycero-3-phos-phoethanolamine, PEG2000-DSPE,美国Genzyme公司),中链油(MCT,辽宁铁岭北亚药用油有限公司),葡萄糖注射液(昆明南疆制药有限公司),灭菌注射用水(石家庄四药有限公司)。
Wistar 大鼠,雄性,体质量180~210 g,沈阳药科大学实验动物中心提供,许可证号SCXK(辽)2014-0001。
2 方法与结果
2.1 PEG化乳剂的制备和质量评价
2.1.1 乳剂的处方及工艺
以摩尔分数10%PEG2000-DSPE和PEG-CHMC修饰密度的乳剂制备如下。按处方量称取MCT 1.50 g、E80 0.35 g及TN 0.30 g,再分别称取PEG2000-DSPE 0.14 g或PEG400-CHMC 40 mg、PEG600-CHMC 50 mg、PEG800-CHMC 66 mg、PEG1000-CHMC 70 mg、PEG2000-CHMC 120 mg及PEG5000-CHMC 270 mg,分别于55 ℃水浴中溶解作为油相,搅拌条件下注入加热至相同温度的灭菌注射用水至100 mL,使最终总磷脂浓度为5 mmol·L-1。继续于55 ℃水浴中搅拌孵育10 min后即得初乳。初乳经200 W超声处理2 min后,400 W超声分散6 min(工作1 s,间歇1 s),0.22 μm的微孔滤膜过滤后即得载药乳剂。
2.1.2 乳剂的粒径、变异系数及zeta电位的测定
平均粒径(mean diameter,d)和变异系数(Coeff. of Var’n, C.V.)是乳剂的重要评价指标,它们的大小决定了微粒分散体系的物理稳定性。具体方法如下:将乳剂用蒸馏水稀释至适宜浓度后,用激光散射粒径测定仪测定该乳剂的、C.V.值及zeta电位,检测波长为632.8 nm,测定角为90°。不同相对分子质量CHMCE和PE的粒径和zeta电位见表1。

Table 1 The characterization of CHMCEn and PE2000表 1 CHMCEn和PE2000的表征
2.2 药动学实验样品的处理及分析
2.2.1 HPLC分析
色谱柱:Hypersil BDS C18柱(200 mm×4.6 mm,5 µm);流动相:甲醇-异丙醇(体积比80∶20);柱温:35 ℃;流速:1.0 mL·min-1;检测波长:264 nm;进样量:20 μL;内标:维生素E醋酸酯。
2.2.2 血浆样品处理方法
精密移取血浆样品100 µL置于1.5 mL离心管中,加入100 mg·L-1维生素E醋酸酯(内标)的甲醇溶液100 µL、甲醇100 µL及正己烷600 µL。涡旋混合提取5 min后,于1×104r·min-1离心10 min。移取正己烷层500 µL,氮气挥干。挥干的物质以流动相100 µL复溶,涡旋1 min混匀,于1×104r·min-1离心10 min,精密量取上清液20 µL进样分析。
2.2.3 组织样品处理方法
取组织0.5 g,于10 mL玻璃管中,加入生理盐水1 mL,于1.4×104r·min-1高速分散匀浆,精密移取组织匀浆液200 µL,置于5 mL离心管中,加入内标(维生素E醋酸酯)甲醇溶液100 µL、甲醇300 µL及正己烷1 200 µL,涡旋混合5 min后于1×104r·min-1离心10 min。移取正己烷层1 mL,40 ℃条件氮气挥干。挥干后物质以流动相100 µL复溶,涡旋1 min混匀,于1×104r·min-1离心10 min,取上清液20 µL进行HPLC分析。
2.3 不同相对分子质量CHMCE大鼠体内的药动学行为及ABC现象研究
2.3.1 实验方案及实验方法
取雄性Wistar大鼠,体质量180~210 g,随机分成14组,按表2方案进行尾静脉注射给药。对照组首次注射质量分数5%葡萄糖溶液,实验组首次按磷脂剂量5 µmol·kg-1注射PEG化乳剂。首次注射7 d后,对照组按磷脂计量5 µmol·kg-1静脉注射不同相对分子质量CHMCE,试验组注射PE2000,并分别于二次给药后的5、15、30、60、120、240 min经眼眶静脉丛取血,4 000 r·min-1离心10 min分离血浆。240 min时间点血样采集完毕后将大鼠脱颈处死,取出肝、脾,用生理盐水洗去残留血液后以滤纸吸干水分。按处理血浆及组织样品方法处理后,HPLC法检测药物浓度。
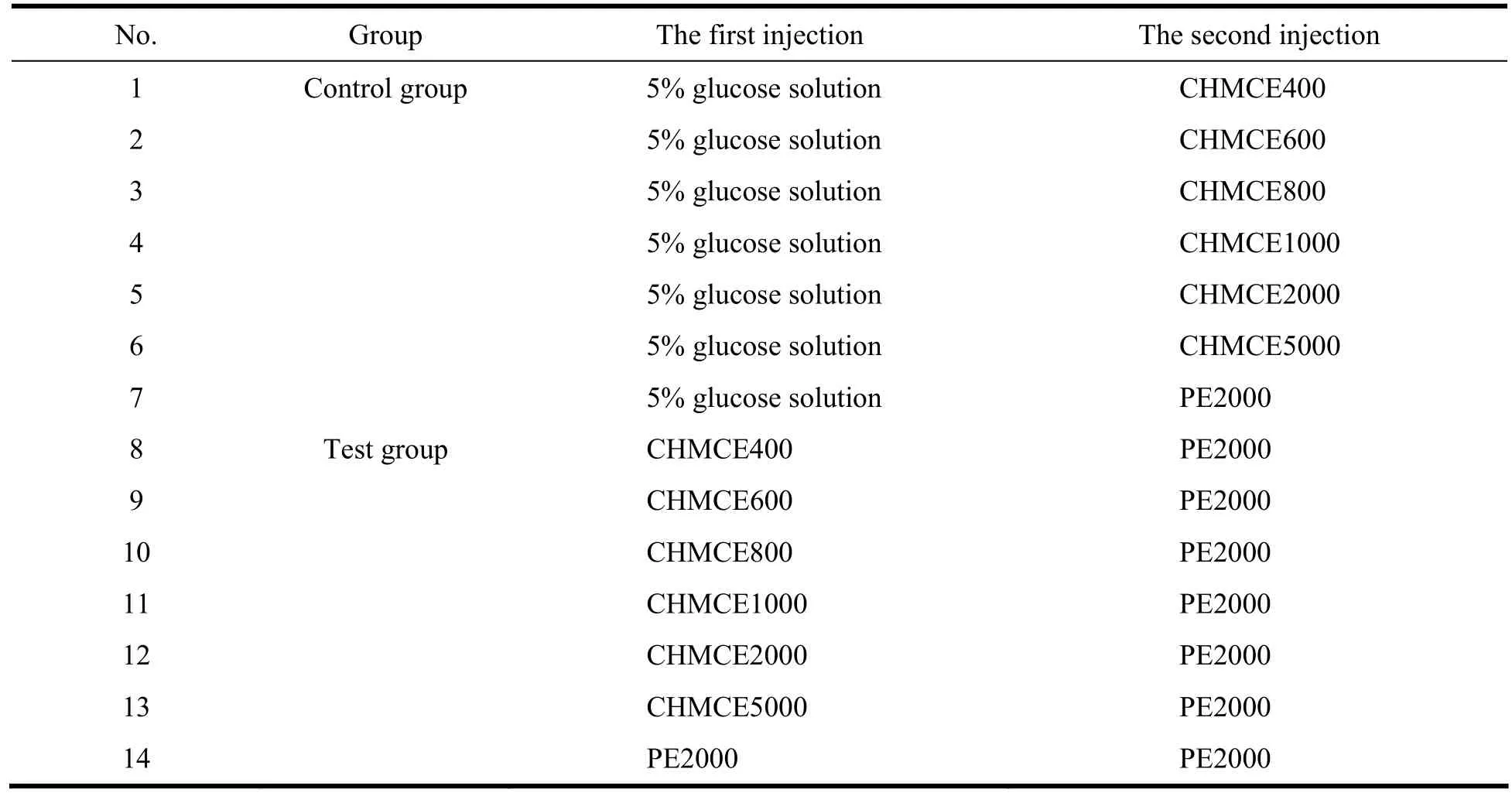
Table 2 The injection protocols for 10% PEG-CHMC emulsions in rats表 2 10%PEG-CHMCE修饰乳剂在大鼠体内的注射方案
2.3.2 不同相对分子质量PEG对CHMCE大鼠体内药动学行为的影响
2.3.2.1 首次注射不同相对分子质量CHMCE的药动学行为和组织分布
以上述制备的PE2000和CHMCEn对大鼠进行尾静脉注射给药,研究乳剂在大鼠体内的药动学行为和组织分布,结果见图1。

Fig. 1 The blood clearance profile of emulsions modified with PEG-CHMC of different PEG molecular weights in Wistar rats (±s, n=3)图 1 不同相对分子质量的PEG-CHMCE修饰乳剂在大鼠体内的清除现象(± s, n=3)
图1显示,不同相对分子质量CHMCE的循环时间基本一致,且明显低于PE2000。通过DAS 2.1.1软件对所有PEG化乳剂的药动学参数进行统计,结果见表3。CHMCE从低相对分子质量到高相对分子质量的药时曲线下面积(AUC)分别为(242.20±10.25)、(211.25±12.32)、(156.75±30.32)、(655.83±8.54)、(662.35±10.82)和(737.48±5.20) mg·min·L-1,平均滞留时间(tMRT)分别为(0.21±0.02)、(0.26±0.04)、(0.18±2.45)、(0.84±0.08)、(1.01±0.04)和(1.10±0.04)h。PE2000的AUC和tMRT分别为(3673.0±7.82)mg·min·L-1和(4.65±1.71)h,明显高于CHMCE,同时高相对分子质量CHMCE(1 000、2000、5 000)的AUC是低相对分子质量(400、600、800)的3、4倍。随PEG相对分子质量的增加,肝脏中的聚集量呈下降趋势,而脾脏的聚集量先增高后降低。总体来看,循环时间相对长的CHMCE1000、2000、5000的肝脾聚集量较低。
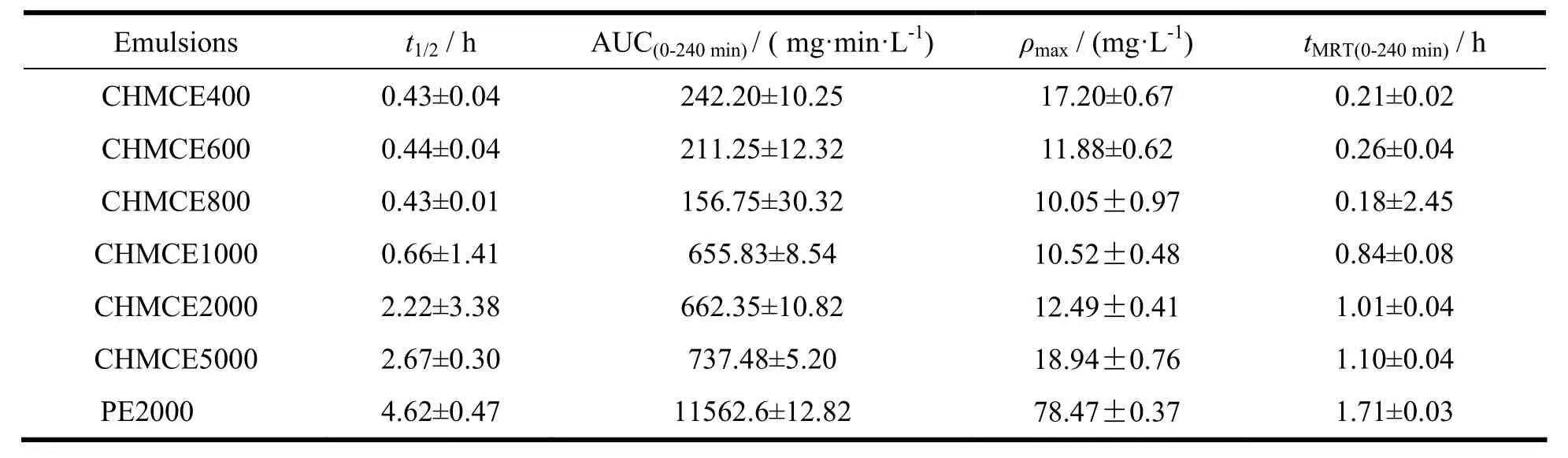
Table 3 Pharmacokinetic parameters of CHMCE and PE2000 estimated in rats(n=3)表 3 CHMCE和PE2000在大鼠体内的药动学参数
2.3.2.2 不同相对分子质量CHMCE对诱导二次注射PE2000产生ABC现象的影响
首次注射不同乳剂时,会对大鼠机体产生不同程度的刺激,从而对二次注射的乳剂造成加速血液清除现象。因此,为了比较不同相对分子质量CHMCE对加速血液清除现象的影响,作者将二次注射的乳剂设定为PE2000,而研究比较首次注射不同乳剂对加速血液清除现象的影响,结果见图2。
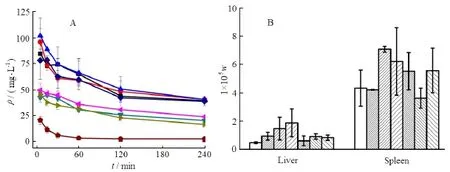
Fig. 2 Influence of PEG molecular weights on the subsequent injected PE2000 after initial administration of CHMCE(± s, n=3)图 2 不同相对分子质量PEG对二次注射PE2000的影响(±s, n=3)
由图2可知,首次注射CHMCE1000、2000、5000均引起二次注射PE2000药动学行为的改变,但ABC现象较PE2000明显减弱。而CHMCE400、600、800却未诱导二次注射PE2000的快速清除,二次注射的PE2000与单次注射无显著性差异,说明无ABC现象的产生。肝脾聚集量通过统计学分析显示各组无显著性差异。
2.4 ABC index的选择
为了量化的比较ABC现象发生的强烈程度,作者引用二次注射与首次注射制剂AUC比值作为衡量这种程度的标准,记为ABC index,其计算公式为ABC index = 二次注射的AUC(0-t)/首次注射的AUC(0-t)[5]。ABC index值越大,表明重复给药引起二次注射乳剂药动学行为的改变越小,即发生的ABC现象越弱。连续注射不同PEG化乳剂时,首次与二次注射0~240 min后不同时间段内的AUC比值见图3。结果显示AUC比值在注射后0~60 min内波动性较大,60 min后开始趋于平衡,因此,60 min之后的时间段均可选择,但考虑到ABC现象为一免疫反应,短时间内的变化情况更具代表性,所以选择0~60 min内的AUC比值作为衡量ABC现象强弱的指标。
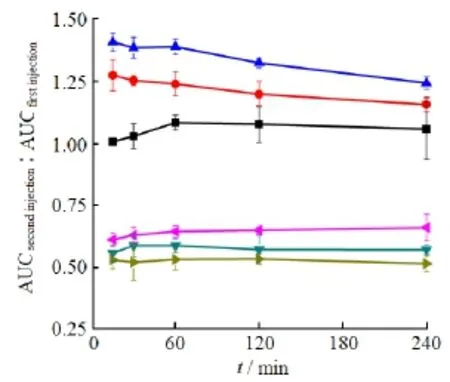
Fig. 3 The ratio of AUC(0-t)for the second injection to that of the first dose of PEGylated emulsions.图 3 二次注射PEG化乳剂与首次注射PEG化乳剂AUC(0-t)的比
2.5 ABC index(0-60 min)的比较
首次注射不同相对分子质量的CHMCE,二次注射PE2000时,首次与二次注射0~60 min内的AUC比值见表4。
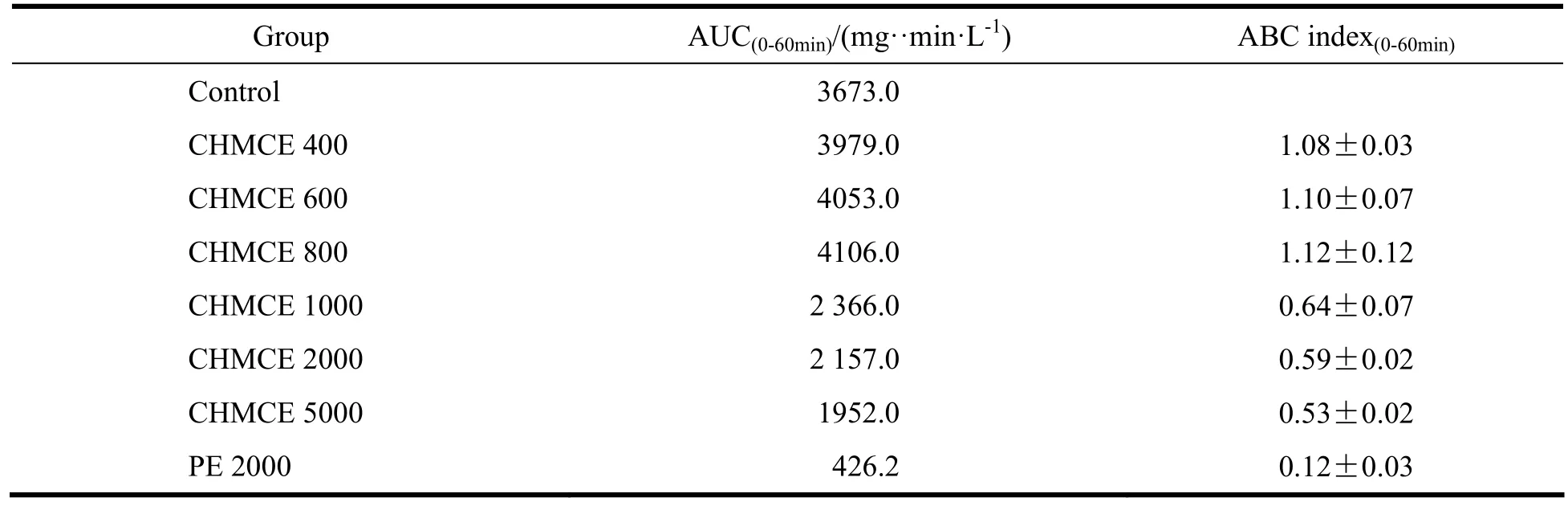
Table 4 The ABC index of the phenomenon induced by CHMCE with different PEG molecular weights表 4 不同相对分子质量的CHMCE引起的加速血液清除现象的ABC index。
将二次注射PE2000的AUC与首次注射PE2000的AUC比值作为ABC index(0-60 min)进行比较,结果见表4。CHMCE相对于PE2000来说,ABC现象的强度均有所降低(ABC index(0-60 min)大于 0.5)。不同相对分子质量 CHMCE诱导二次注射 PE2000的 AUC比值由小到大依次为CHMCE5000≈CHMCE2000≈CHMCE1000<CHMCE400≈CHMCE600≈CHMC800,即诱导的ABC现象逐渐减弱。
3 讨论
a. 从表2数据可以发现,CHMCE组不同相对分子质量乳剂的平均粒径均大于PE2000。这其中的原因是2种PEG-脂质衍生物的结构差异而使乳化作用不同,PEG-DSPE具有较长的亲酯双链,而本实验室合成的PEG-CHMC的亲脂链仅为较短的单链,所以前者的亲脂链在乳剂的油相中插入的更多;PEG-DSPE亲脂端与乳剂的油相MCT均具有烷基链,融合性较好,而PEG-CHMC亲脂端则为胆固醇结构,与 MCT的融合作用不如 PEG-DSPE。上述原因使 PEG-DSPE的乳化作用强于PEG-CHMC,结果制得PE的粒径相对较小。有文献指出,首次注射PEG化脂质体的粒径对诱导产生ABC现象的作用不大[2,7],因此不考虑粒径在本试验ABC现象中的影响。
b. PEG相对分子质量对CHMCE的循环时间存在一定影响。PEG是一个中性的聚合物,在水和有机溶剂中易溶,化学通式为HOCH2(CH2OCH2)nCH2OH。PEG的水溶性大多被认为是由于其亲水性的结构,水分子与PEG链醚键中的氧形成氢键,水分子定向与PEG结合,形成水化层包裹在PEG链表面,提高其表面亲水性和空间位阻,减小MPS识别概率以延长体内循环时间。Mori等[3]认为载体表面PEG所产生的水化层厚度随PEG相对分子质量的增大而增加,致密的水化层则是载体避免MPS识别摄取从而延长体内循环时间的主要原因。本试验将不同相对分子质量?PEG-CHMC修饰于乳剂表面,未观察到CHMCE循环时间随PEG相对分子质量的增加而显著延长,仅在高相对分子质量(1 000、2 000、5 000)和低相对分子质量(400、600、800)CHMCE间产生了一定差异,其原因是可断裂PEG-脂质衍生物亲水性部分与亲脂性部分间的连接键为可断裂的碳酸酯键,易被哺乳动物体内广泛存在的酯酶所水解[8],致使CHMCE进入大鼠体内后表面PEG分子逐渐断裂,乳剂失去了PEG水化层的保护而被快速清除,主要聚集在肝组织。PEG-CHMC在同等断裂条件下,长链的PEG分子从最初的“毛刷状”转变成“蘑菇状”对乳剂表面的覆盖程度更大[9],保护作用更强,因此我们能够观察到CHMCE1000、2000、5000在循环时间上具有一定优势。
c. Laverman等[10]研究指出,二次注射制剂的性质会影响ABC现象的强度,因此,本试验以具有明显长循环特性的PE2000作为二次注射制剂,更能有效表征首次注射制剂对ABC现象的影响。研究认为TI-2型抗原因具有较大的相对分子质量、整齐的表面排列以及较长的循环时间,这些特点能够保证其以相对长的时间与B细胞表面受体相互作用,产生持续的B细胞信号刺激,从而在不需要辅助T细胞的条件下刺激机体产生抗体[11]。表5的结果显示PE2000重复注射诱导了极为强烈的ABC现象(ABC index(0-60 min)为0.12),其主要原因之一是PEG2000-DSPE能够稳定存在于乳剂表面,保证了乳剂较长的循环时间从而增强了PE2000对脾脏B细胞的持久刺激作用。相较之,CHMCE则因可断裂PEG-CHMC的特性诱导了较弱的ABC现象。从本试验结果来看,CHMCE1000、2000、5000的循环时间比PE2000大大缩短,却依旧诱导了ABC现象的产生(ABC index(0-60 min)分别为0.64、0.59、0.53)。这一结果提示,高相对分子质量CHMCE诱导的ABC现象可能存在其他的影响因素。Kaminskas等[12]研究指出,首次以5 mg·kg-1尾静脉给予大鼠不同比例的PE-PC胶束(7 μmol·kg-1phospholipids),间隔7 d后再次注射相同磷脂剂量的PEG化脂质体,结果显示首次注射的胶束均诱导二次注射PEG化脂质体产生了强烈的ABC现象。本实验室所合成PEG-CHMC疏水端的胆固醇链长较短,而亲水端PEG链长相对较长,且随PEG相对分子质量的增加PEG-CHMC的亲水性逐渐增强。通过非离子表面活性剂亲水亲油能力(hydrophile-lipophile balance,HLB)值计算公式得到PEG-CHMC的HLB值随PEG相对分子质量由低到高依次为10.32、12.20、13.47、14.38、16.70和18.52[13],高相对分子质量PEG-CHMC亲水性强,更易于从乳剂表面脱落进而形成胶束。另外,Wang等[14]研究指出,PEG分子的-(CH2CH2O)n-重复片段可能是脾脏边缘区B细胞识别并产生相应抗体的关键,因此,重复片段较少、不能有效激活免疫细胞可能是小相对分子质量 CHMCE未诱导二次PE2000产生ABC现象的原因。所以,高相对分子质量CHMCE所诱导的ABC现象可能受多种因素影响,尚需进一步试验予以证实。
综上,本实验中CHMCE的药动学行为可因高相对分子质量PEG-CHMC(1 000、2 000、5 000)的修饰得到一定延长;对PE2000诱导产生ABC现象的结果显示,首次注射低相对分子质量CHMCE不诱导ABC现象产生,而当PEG相对分子质量达到1 000以上时,CHMCE因PEG-CHMC自身特性增加了对免疫细胞的刺激作用从而诱导了ABC现象,此试验条件下得到PEG相对分子质量对ABC现象的不同影响为解决ABC现象提供了一定参考。
[1] HARRIS J M, CHESS R B. Effect of pegylation on pharmaceuticals[J]. Nature Reviews Drug Discovery, 2003, 2(3): 214-221.
[2] DAMS E T, LAVERMAN P, OYEN W J, et al. Accelerated blood clearance and altered biodistribution of repeated injections of sterically stabilized liposomes[J]. Journal of Pharmacology and Experimental Therapeutics, 2000, 292(3):1071-1079.
[3] MORI A, KLIBANOV A L, TORCHILIN V P, et al. Influence of the steric barrier activity of amphipathic poly (ethyleneglycol) and ganglioside GM〈 sub〉 1〈/sub〉 on the circulation time of liposomes and on the target binding of immunoliposomes in vivo[J]. FEBS letters, 1991, 284(2): 263-266.
[4] ISHIDA T, ICHIKAWA T, ICHIHARA M, et al. Effect of the physicochemical properties of initially injected liposomes on the clearance of subsequently injected PEGylated liposomes in mice[J]. Journal of Controlled Release, 2004, 95(3): 403-412.
[5] ZHAO Y, WANG C, WANG L, et al. A frustrating problem: Accelerated blood clearance of PEGylated solid lipid nanoparticles following subcutaneous injection in rats[J]. European Journal of Pharmaceutics and Biopharmaceutics, 2012, 81(3): 506-513.
[6] XU H, WANG K Q, DENG Y H, et al. Effects of cleavable PEG-cholesterol derivatives on the accelerated blood clearance of PEGylated liposomes[J]. Biomaterials, 2010, 31(17): 4757-4763.
[7] KOIDE H, ASAI T, HATANAKA K, et al. Particle size-dependent triggering of accelerated blood clearance phenomenon[J]. International Journal of Pharmaceutics, 2008, 362(1): 197-200.
[8] SLEPUSHKIN V A, SIM ES S, DAZIN P, et al. Sterically Stabilized pH-sensitive liposomes intracellular delivery of aqueous contents and prolonged circulation in vivo[J]. Journal of Biological Chemistry, 1997, 272(4): 2382-2388.
[9] DE GENNES P. Conformations of polymers attached to an interface[J]. Macromolecules, 1980, 13(5): 1069-1075.
[10] LAVERMAN P, CARSTENS M G, BOERMAN O C, et al. Factors affecting the accelerated blood clearance of polyethylene glycol-liposomes upon repeated injection[J]. Journal of Pharmacology and Experimental Therapeutics, 2001, 298(2): 607-612.
[11] MOND J J, LEES A, SNAPPER C M. T cell-independent antigens type 2[J]. Annual Aeview of Immunology, 1995, 13(1): 655-692.
[12] KAMINSKAS L M, MCLEOD V M, PORTER H, et al. Differences in colloidal structure of PEGylated nanomaterials dictate the likelihood of accelerated blood clearance[J]. Journal of Pharmaceutical Sciences, 2011, 100(11): 5069-5077.
[13] 丁佩章. 表面活性剂及其HLB值[J]. 滨州师专学报, 1994(2): 3.
[14] WANG X, ISHIDA T, KIWADA H. Anti-PEG IgM elicited by injection of liposomes is involved in the enhanced blood clearance of a subsequent dose of PEGylated liposomes[J]. Journal of Controlled Release, 2007, 119(2): 236-244.
The exploration about ABC phenomenon induced by emulsions modified with PEG-CHMC of different molecular weight
JIAO Jiao, SUN Jing, FAN Di, GUO Ligang, HUANG Zhenjun, DENG Yihui*
(School of Pharmacy, Shenyang Pharmaceutical University, Shenyang 110016, China)
ObjectiveTo prepare PEG-CHMC emulsions(PEG-CHMC coating emulsion,CHMCE) withdifferent molecular weights and study theirs pharmacokinetic behavior and ABC phenomenon of PEG2000-DSPE emulsions (PEG2000-DSPE coating emulsion,PE2000). That is to explore the contribution of PEG weight in pharmacokinetic behavior and ABC phenomenon. Method With 10 % PEG modification density to prepare drug-loaded emulsions. The rats were administered PEG-modified emulsions by the intravenous (via the tail vein) injection of 5 μmol·kg-1phospholipids. At 5, 15, 30, 60, 240 min after the injection, the blood samples were collected. After withdrawing the last blood sample at 240 min, the rats were sacrificed and livers, spleens were excised. Then the drug concentration was determined through HPLC.Results The circulation time of high molecular weight CHMCE1000, 2000, 5000 was longer than low molecular weight CHMCE400, 600, 800 through comparing AUC(0-240 min)and MRT(0-240 min). The results of CHMCE induced ABC phenomenon to PE2000 illustrated that low molecular weight CHMCE didn’t induce ABC phenomenon. But high molecular weights CHMCE could induce ABC phenomenon, the ABC index(0-60 min)of CHMCE1000, CHMCE2000, CHMCE5000 were 0.64, 0.59, 0.53, respectively.ConclusionThe molecular weight of PEG that modified on the surface of CHMCE has an important influence on pharmacokinetic behavior and ABC phenomenon. These outcomes would supplement the affection law of PEG molecular weights to ABC phenomenon and provide a certain reference to select PEG molecular weights of PEGylated formulation.
Pharmaceutics; PEG molecular weight; accelerated blood clearance phenomenon; PEG-CHMC; circulation time; ABC index
R94
: A
(2016)06–0213–11
10.14146/j.cnki.cjp.2016.06.004
(本篇责任编辑:赵桂芝)
2015–05–08
国家自然科学基金资助项目(81072602)
焦姣(1989-), 女(汉族),山西运城人, 硕士研究生,E-mailjiaojiao_723@126.com;*通讯作者:邓意辉(1964-), 男(汉族), 湖南花垣人, 教授, 博士, 博士生导师, 主要从事药物靶向新剂型的研究,Tel.024-23986316,E-maildds-666@163.com。
