角鲨烯化吉西他滨理化性质的研究
2017-01-05张元元史方园
张元元,史方园,唐 星
(沈阳药科大学 药学院, 辽宁 沈阳 110016)
角鲨烯化吉西他滨理化性质的研究
张元元,史方园,唐 星*
(沈阳药科大学 药学院, 辽宁 沈阳 110016)
目的对角鲨烯化吉西他滨的理化性质进行研究,为制剂研究提供参考。方法合成角鲨烯化吉西他滨并用质谱、氢谱进行结构确证;利用紫外分光光度法、差示扫描量热法和粉末X-射线衍射对吉西他滨及其前药进行表征,并用HPLC法测定角鲨烯化吉西他滨的溶解度和表观油水分配系数。结果合成方法可行。合成的角鲨烯化吉西他滨与吉西他滨具有完全不同的晶型、溶解性能和油水分配系数。结论合成的前药较吉西他滨有较好的脂溶性,且其具有两亲性,在水中可自发形成自组装体。
药剂学;前药;理化性质;吉西他滨;角鲨烯化吉西他滨;胶束
吉西他滨( gemcitabine, Gem) 为2',2'-二氟-2'-脱氧胞苷类似物(化学结构式见图1),用于肺、胰腺、卵巢、乳腺、膀胱和胆囊癌等的治疗。该药物为周期特异性抗肿瘤药[1],在细胞内,通过脱氧胞苷激酶的作用,由5'位的磷酸化激活,使其转变成为三磷酸酯衍生物,该衍生物以复制方式嵌入DNA链终止链的生长,从而阻断癌细胞的增殖。目前,由礼来公司开发的产品—健择,已在90多个国家获得批准使用,为治疗非小细胞肺癌的一线药物。然而,市售的吉西他滨肿瘤选择性低、生物半衰期短、毒性高、易产生耐药性,从而限制了其抗肿瘤作用的充分发挥。
近几年,国内外有大量关于吉西他滨结构改造方面的研究[2]。例如Maria等通过将吉西他滨4位氨基与链状烃共价偶合,形成高度脂溶性吉西他滨衍生物;连艳菊等制备了十八酰基吉西他滨自组装体。
角鲨烯(squalene, Sq)是生物合成固醇类的中间物(化学结构式见图1),可为机体供氧,能抑制致癌物质的活性,辅助治疗癌症。同时,可以抑制癌细胞增殖,增加对癌症的抗性。因其生物兼容性及安全性,将药物角鲨烯化[3]成为药脂生物共轭体,已成为目前研究的热点。
作者利用角鲨烯对吉西他滨4位氨基进行结构改造,制备吉西他滨的衍生物—4-(n)-角鲨烯酰基吉西他滨(Sq-gem)(化学结构式见图1),旨在延长药物作用时间、提高药效、降低毒性。利用核磁共振(MR)对吉西他滨衍生物进行结构确证,并且采用差示扫描量热(DSC)、粉末X-射线衍射(XPRD)、红外光谱(IR)及高效液相色谱(HPLC)等技术对吉西他滨及其衍生物性质进行对比研究。制备了角鲨烯化吉西他滨自组装体,并对其体外性质及稳定性进行初步研究。
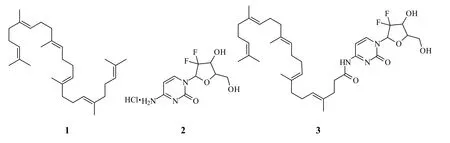
Fig.1 The chemical structure of squalene(1), gemcitabine(2) and squalene-gemcitabine (3)图 1 角鲨烯(1)、吉西他滨(2)和4-(n)-角鲨烯酰基吉西他滨(3)的化学结构式
1 仪器与材料
纳米粒度分析仪(英国马尔文仪器有限公司),FA–1104电子天平(上海民桥精密科学仪器有限公司),全扫描紫外分光光度计(Unico,美国),恒温水浴培养摇床(上海智城分析仪器制造有限公司),DSC-60差示扫描量热分析仪(日本岛津公司),D/Max-2400 X-射线荧光光谱仪(日本理学株式会社),Bruker 6-55 红外光谱仪(德国Bruker光谱仪器公司),DF-101S集热式恒温磁力搅拌器(巩义英峪予华仪器厂),HITACHI L-2000 高效液相色谱仪、HITACHI 紫外分光光度计(日本Hitachi公司),ARX400核磁共振仪(美国Bruker公司),Thermo C18色谱柱(250 mm × 4.6 mm,5 μm,美国Thermo公司)。
原料角鲨烯(TCI化成工业发展有限公司),原料盐酸吉西他滨(宁波天衡制药有限公司),其他药品或试剂(分析纯或药用辅料,市售)。
2 方法与结果
2.1 角鲨烯化吉西他滨的合成
角鲨烯化吉西他滨的合成路线参照文献[4]设计,具体路线见图2。简单地说,是将角鲨烯制备成角鲨烯酸后,由吉西他滨4位的氨基与角鲨烯酸通过酰胺反应共价结合得来的白色或类白色固体,通过硅胶柱分离纯化得到精品角鲨烯化吉西他滨,收率50%左右。

Fig. 2 Synthesis routes of the sq-gem图 2 角鲨烯化吉西他滨的合成路线
2.2 角鲨烯化吉西他滨的结构确证
所得衍生物通过质谱与氢谱确定结构,数据如下:1H-NMR (400 MHz, DMSO) (图3):δ 10.99 (1H,s,NHCO)、8.24 (1H,d,J = 7.6 Hz,CH=CH)、7.27 (1H,d,J = 7.6 Hz,CH=CH)、6.31 (1H,d,J = 6.5 Hz,—CH—O—)、6.17 (1H,t, J = 7.4 Hz,CH—OH)、5.28 (1H,t, J = 5.4 Hz,O—CH—CH2OH)、 5.09 (5H,m,C—CH═)、4.19 (1H,m,CH2OH), 3.90 (1H,m,CH2CO)、3.88 (1H,m,CH2CO)、3.67 (1H,m,CH2OH)、2.22 (2H,m,CH2CH2CO)、2.03~1.92 (16H,m,CH2)、1.64~1.54 (18H,m,CH3)。ESI-MS(m/z)(图4):646.40 [M+H]+和668.38[M+Na]+。由上述数据确定所合成的化合物为角鲨烯化吉西他滨。
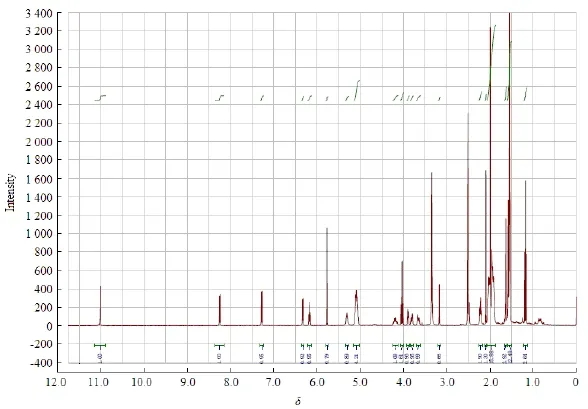
Fig. 3 The1H-NMR of squalene-gemcitabine图 3 角鲨烯化吉西他滨的1H-NMR谱图
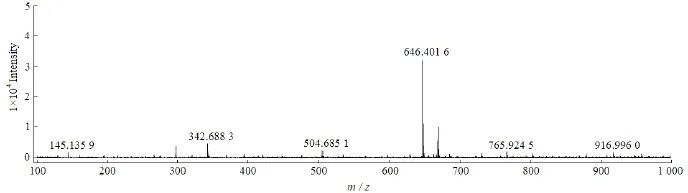
Fig. 4 The mass spectra of squalene-gemcitabine图 4 角鲨烯化吉西他滨的质谱图
2.3 角鲨烯化吉西他滨理化性质的测定
2.3.1 紫外光谱特性
取角鲨烯化吉西他滨适量,分别制成角鲨烯化吉西他滨乙醇溶液,以乙醇作为空白对照,按《中华人民共和国药典》2010 版二部附录IV A中紫外分光光度法,在波长200~400 nm内进行紫外扫描。吉西他滨前药紫外光谱分析(UV)结果见图5。由图5可见,角鲨烯化吉西他滨在242 nm 和250 nm 处吸收值最大,同时流动相在此处无吸收,而据报道,吉西他滨检测波长为268 nm。
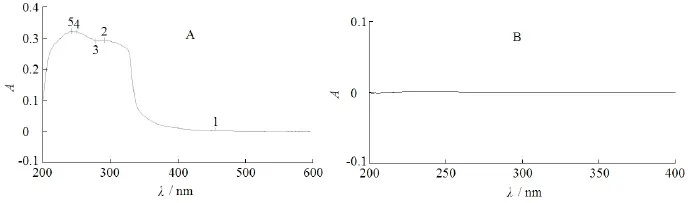
Fig. 5 The UV spectra of the Sq-gem in alcohol (A) and the alcohol (B)图 5 角鲨烯化吉西他滨乙醇溶液(A)和无水乙醇(B)的紫外扫描图谱
2.3.2 差示扫描量热 (DSC)法
取吉西他滨或角鲨烯化吉西他滨适量,置于分析仪的铝盘中,以氧化铝为参比物,置氮气流中,从-5 ℃到200 ℃,以10 ℃·min-1的速率升温扫描。吉西他滨以及角鲨烯化吉西他滨差示扫描量热分析测试(DSC)结果见图6。由图6可知,吉西他滨在168.6 ℃有1个明显的吸热峰,为药物结晶峰,而角鲨烯吉西他滨不存在结晶峰。

Fig. 6 The DSC maps of Gem and Sq-gem图 6 吉西他滨和角鲨烯化吉西他滨的DSC图谱
2.3.3 X-射线粉末衍射(XPRD)法
工作条件:CuKa 靶石墨单色器衍射束单色比,高压 56 kV,单流 182 mA,扫描 2θ 角度为 5°~60°,扫描速度为 0.2°·min-1。
吉西他滨以及角鲨烯化吉西他滨的 XPRD 测定结果见图 7。图7说明,吉西他滨为典型的晶体化合物,在8°~36° 内存在明显的晶体衍射峰,而在角鲨烯化吉西他滨中,药物的衍射峰消失。
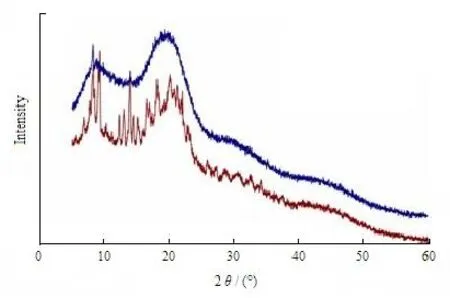
Fig. 7 The x-ray diffraction patterns of Gem and Sq-gem图 7 吉西他滨和角鲨烯化吉西他滨的XPRD图谱
2.3.4 液相分析法
角鲨烯化吉西他滨的色谱条件如下[4]:色谱柱为Thermo C18柱(250 mm × 4.6 mm, 5 μm),流动相为乙腈-水 (体积比85∶15),柱温为室温,流速为0.8 mL·min-1,波长为254 nm,进样量20 μL。
2.3.5 油中溶解度的测定
取大豆油、中链油、大豆油与中链油质量比1∶1的混合油各1 g,分别置于5 mL西林瓶中,再分别加入过量的角鲨烯化吉西他滨,用N2密封后置于恒温水浴培养摇床中,以25 ℃、100 r·min-1振摇约72 h以上,至溶解平衡。所得混合物放至室温后,离心,取上清液用无水乙醇稀释,过0.22 μm滤膜,取续滤液进高效液相色谱仪,分别记录峰面积,利用外标一点法计算前药在不同油中的溶解度。吉西他滨前药在不同油中溶解度结果如表1所示。结果显示,角鲨烯化吉西他滨在油中溶解度大小排序为:中链油>混合油>大豆油。
Table 1 The solubility of Sq-gem in different oils at room temperature (± s, n=3)表1 室温下角鲨烯化吉西他滨在不同油中的溶解度 (± s, n=3)

Table 1 The solubility of Sq-gem in different oils at room temperature (± s, n=3)表1 室温下角鲨烯化吉西他滨在不同油中的溶解度 (± s, n=3)
Species w(solubility) / % Soybean oil 0.747±6×10-3Medium chain triglycerides 1.226±5×10-3Mixed oil 1.006±8×10-3
2.3.6 油水分配系数的测定
取pH值为4.8、6.8、7.0、7.8的磷酸盐缓冲液(详见《中华人民共和国药典》2010版附录)各10 mL置于锥形瓶中,分别加入正辛醇10 mL,置恒温空气浴振荡器中,以100 r·min-1的速度振摇至分配平衡 (约72 h),静置至分层后,分离出两相均为饱和溶液。精密称取吉西他滨前药置于EP 管内,加入不同pH值的正辛醇饱和水相各1 mL,置恒温空气浴振荡器中振摇2 h,再分别加入水饱和的正辛醇溶液1 mL,再用恒温空气浴振荡约72 h至平衡。将溶液静置后,分离出水相与正辛醇相,取续滤液按“2.3.4“条色谱条件分别测定两相中的药物浓度,计算吉西他滨前药在25 ℃不同pH值条件下的表观油水分配系数[5],结果见表2。结果表明,吉西他滨前药在不同pH值介质下的表观油水分配系数均较高,而且其值大小相差不大。

Table 2 The partition coefficient of Sq-gem in different pH media at room temperature表 2 室温下,角鲨烯化吉西他滨在不同pH值介质中的表观油水分配系数
2.4 角鲨烯化吉西他滨自组装体的制备
角鲨烯化吉西他滨自组装体通过纳米沉淀法制备。过程如下,将角鲨烯化吉西他滨溶于无水乙醇制成2 g·L-1的乙醇溶液。取所得溶液1 mL,在1 000 r·min-1的机械搅拌下逐滴加至1 mL双蒸水中,形成自组装体。用旋转蒸发仪将所得自组装体中的乙醇于37 ℃挥去,即得自组装体样品。在5 ℃冷藏保存,备用。
2.5 自组装体的表征
2.5.1 自组装体粒度的测定
将上述样品用注射用水稀释,立即放入样品池内,将光强度 (intensity) 调节至300 kHz 左右,光源为HeNe激光 (λ0=633 nm),将操作参数中温度设为测定时的室温,开始测定,保持测定至Time history曲线趋于直线时停止,保存数据。胶束粒径为120 nm左右, 其分布较均匀, 跨度窄。
2.5.2 扫描电镜(TEM)法
取吉西他滨前药自组装体稀释后样品滴在铜网表面,使液滴尽量铺满整个铜网,1 min后用滤纸轻轻吸去边缘多余液体,再滴一滴质量分数2%磷钨酸溶液(pH值约为6.5)使液滴尽量铺满整个铜网,1 min后过0.45 µm滤膜并用滤纸轻轻吸去边缘多余液体,自然干燥后,上镜观察,并进行拍照。结果如图8所示,为球形,粒径约80 nm。

Fig. 8 The TEM images of the micelle dilution 100 times (A) and the dilution2 000 times (B)图 8 胶束稀释100倍(A)和稀释2 000倍(B)透射电镜图
3 讨论
a. 经结构确证,确定合成产物为角鲨烯化吉西他滨。紫外分光光度法发现,合成前药的最大吸收峰位置发生了蓝移,可能是角鲨烯与吉西他滨发生反应后,由于角鲨烯的空间位阻太大,从而导致吉西他滨的共轭度受到了影响。同时,对最大吸收波长进行确定,考虑末端吸收,选择248~252 nm作液相测定方法的检测波长。差示热扫描法研究发现,在角鲨烯化吉西他滨中,结晶峰消失,说明其以无定型状态存在。而X射线衍射结果中,吉西他滨角鲨烯化形成的前药中无结晶峰存在,同样证明其以无定形状态存在。对角鲨烯化吉西他滨不同油中的溶解度进行测定,结果显示其在不同油中均有较好的溶解度。而据报道吉西他滨为水溶性药物[6],在油中几乎不溶。由此可知,角鲨烯的引入大大改变了药物在油中的溶解性能,分析其原因主要是角鲨烯链为亲油基团,大大提高了药物的疏水性,并且其存在同时改变了药物的晶型使其变为无定型,在溶解过程中,无需破坏晶格。角鲨烯化吉西他滨的油水分配系数测定结果显示,log P为4.96±0.14,而吉西他滨的油水分配系数是0.05。结果表明,吉西他滨前药在不同 pH值介质下表观油水分配系数均较高,说明其亲脂性高,而且其值大小相差不大,说明其表观油水分配系数无pH值依赖性。
b. 因角鲨烯化吉西他滨具有两亲性,可用纳米沉淀法制成自组装体。动态散射法测得的角鲨烯化吉西他滨自组装体粒径为120 nm左右, 其分布较均匀, 跨度窄。与文献报道结果基本一致。使用TEM观察自组装体形态,与文献报道的形态一致[7],为球型。观察其粒径大约为80 nm,较粒度测定结果与文献报道结果均要小,可能由于制样时有干燥的过程,且测定过程中的高真空条件使得自组装体壳层吸附的水分子完全丧失,因而观察到的粒径较水化径大幅减小。
4 结论
本研究成功合成了前景良好的吉西他滨前药角鲨烯化吉西他滨。采用紫外分光光度法、差示扫描量热法和X-射线粉末衍射,鉴别前药为无定型,以完全不同于吉西他滨的状态存在。油中溶解度试验结果表明,前药在大豆油中溶解度小于中链油。油水分配系数测定结果表明,角鲨烯化吉西他滨具有较好的亲脂性。此外,其具有两亲性,在水中可自发形成自组装体。说明合成的前药较吉西他滨有不同的理化性质,具有广阔的应用前景。
[1] 罗扬. 吉西他滨治疗晚期非小细胞肺癌的现状[J]. 中国癌症杂志, 2001, 11(1): 74-77.
[2] CELIA C, COSCO D, PAOLINO D, et al. Gemcitabine-loaded innovative nanocarriers vs GEMZAR: Biodistribution, pharmacokinetic features and in vivo antitumor activity[J]. Expert Opinion on Drug Delivery, 2011, 8(12): 1609-1629.
[3] DESMAËLE D, GREF R, COUVREUR P. Squalenoylation: a generic platform for nanoparticular drug delivery[J]. Journal of Controlled Release, 2012, 161(2): 609-618.
[4] COUVREUR P, STELLA B, REDDY L H, et al. Squalenoyl nanomedicines as potential therapeutics[J]. Nano Letters, 2006, 6(11): 2544-2548.
[5] 徐文, 孙进, 张婷婷, 等. HPLC法测定冬凌草甲素的平衡溶解度和表观油水分配系数[J]. 沈阳药科大学学报, 2007, 24(4): 220-222.
[6] 王浩, 陈学思, 邓英杰. 吉西他滨聚 L-乳酸中空微球的制备及其酶解释放行为研究[J]. 中国药剂学杂志: 网络版, 2011, 9(2): 21-29.
[7] MAKSIMENKO A, MOUGIN J, MURA, S et al. Polyisoprenoyl gemcitabine conjugates self assemble as nanoparticles, useful for cancer therapy [J]. Cancer Letters, 2013, 334(2): 346-353.
Study on the physicoch emical characterizations of squalenegemcitabine
ZHANG Yuanyuan, SHI Fangyuan, TANG Xing*
(School of Pharmacy, Shenyang Pharmaceutical University, Shenyang 110016, China)
ObjectiveTo characterize squalene-gemcitabine in order to be a good reference in studying pharmaceutics.MethodsSqualene-gemcitabine was synthetized, and then the structure was confirmed; UV, DSC, and PXRD were applied to characterize the gemcitabine prodrug. Moreover, the solubility and the apparent octanol/water partition coefficients were determined by HPLC, respectively.Results It was feasible to synthetize the targeted compound, which was totally different with the plain drug-gemcitabine in the crystal form, solubility and the apparent octanol/water partition coefficients.Conclusions The synthetized prodrug is more lipophilic, compared with gemcitabine. And it is amphiphilic, which make it form spherical micelles spontaneously in water.
pharmaceutics; prodrug; properties; gemcitabine; squalene-gemcitabine; micelle
R943
A
(2016)06–0204–09
10.14146/j.cnki.cjp.2016.06.003
(本篇责任编辑:赵桂芝)
2015–05–11
张元元(1991–), 女(汉族), 浙江金华人, 硕士研究生,E-mailjuranmo1991@163.com; *
:唐星(1964–), 男(汉族), 陕西商县人, 教授, 博士, 博士生导师, 主要从事药剂学及中药现代化研究,Tel.024-23986343,E–mailtangpharm@sina.com.cn。
