硅胶吸附甘油磷脂酰胆碱的动力学和焓变的研究
2016-12-27张康逸张丽霞王兴国屈凌波刘元法
张康逸 张丽霞 王兴国 屈凌波 刘元法
(河南省农科院农副产品加工研究所1,郑州 450002)
(郑州大学化学系2,郑州 450001)
(江南大学食品学院3,无锡 214122)
硅胶吸附甘油磷脂酰胆碱的动力学和焓变的研究
张康逸1,2张丽霞1王兴国3屈凌波2刘元法3
(河南省农科院农副产品加工研究所1,郑州 450002)
(郑州大学化学系2,郑州 450001)
(江南大学食品学院3,无锡 214122)
主要研究硅胶吸附L-α-GPC的动力学和热力学特性对吸附过程的控制,发现界面扩散控制速率模型1-3(1-X)2/3+2(1-X)能很好的拟合硅胶的吸附过程。通过Freundlich方程和Langmuir方程对吸附平衡模拟,得到了Langmiur方程拟合硅胶吸附L-α-GPC的吸附等温线,计算出不同温度条件下的回归方程,相关系数均在0.99以上,并证实了硅胶的吸附为放热反应。同时,利用Clausius-Clapeyron方程计算出3个吸附量的硅胶吸附热力学参数分别为80、160和240 mg/g,焓变(ΔHAm)分别为24.85、23.82、22.72 kJ/mol。研究结果为进一步探讨工业化硅胶柱色谱制备高纯L-α-GPC提供了基础数据和理论参考。
甘油磷脂酰胆碱 硅胶柱色谱 动力学 热力学参数
甘油磷脂酰胆碱(L-alpha glycerylphosphorylcholine,L-α-GPC)由胆碱、甘油和磷酸盐组成,是乙酰胆碱和磷脂酰胆碱合成的胆碱源[1-2]。在治疗人体大脑的精神混乱和神经混乱方面具有重要的医药应用价值,如治疗阿尔茨海默氏症、小脑性共济失调、精神分裂症和双相情感障碍等,但是就作为药用原料及相关研究而言需要较高纯度的L-α-GPC[3-5]。硅胶柱层析纯化制备高纯L-α-GPC,具有产品纯度高、回收率高、操作简单、可重复性使用,以及和甘油磷脂酰乙醇胺(L-alpha glycerylphosphorylethanolamine,L-α-GPE)同步分离等优势[6-7]。因此,研究硅胶吸附L-α-GPC的动力学和热力学特性对吸附过程的控制具有重要的指导价值。
本研究采用非均相未反应核收缩模型[8]对硅胶的吸附过程进行模拟,并对硅胶吸附动力学中的速度控制模型进行探讨。分别用Freundlich方程[9]、Langmuir方程[10]对吸附平衡模拟,结合Clausius-Clapeyron[11]方程研究硅胶吸附L-α-GPC的热力学特性。通过对柱色谱中硅胶填料的吸附动力学和热力学研究,为L-α-GPC纯化的中试试验,以及工业化硅胶柱色谱制备提供重要的技术支持。
1 材料与方法
1.1 材料
1.1.1 原料与试剂
L-α-GPC(纯度,99.8%):自制;L-α-GPC(99%)标准品:Sigma公司(St. Louis, MO, USA);硅胶(柱色谱级;粒径75~150 μm;孔径20~30 nm;pH 6~7;含水量3%,比表面积600~800 m2/g):青岛海洋化工;甲醇:国药集团化学试剂有限公司。
1.1.2 仪器
DSHZ-300多用途水浴恒温振动器:江苏太仓市实验仪器厂;Waters1525高效液相色谱仪,美国Waters公司;GT16-3高速台式离心机:北京时代北利离心机有限公司;MixPlus漩涡震荡器:合肥艾本森科学仪器有限公司。
1.2 试验方法
1.2.1 原料预处理
L-α-GPC溶液配置:称取一定量制备的L-α-GPC样品,甲醇溶解,稀释成不同浓度的溶液。
硅胶的活化:称取150 g硅胶,放入托盘中,在120 ℃的烘箱中,干燥30 min进行活化。
1.2.2 硅胶吸附率和吸附量测定
准确称取活化的硅胶2 g放入100 mL具塞三角瓶中,加入50 mL浓度16.6 mg/mL的L-α-GPC溶液;在25 ℃,在95 r/min的恒温水浴震荡器上摇,均匀吸附;20 min取样,HPLC-ELSD分析L-α-GPC浓度。
硅胶吸附率和吸附量计算公式:

(1)

(2)
式中:X和Qe,分别为吸附率和吸附量/mg/g,活化硅胶重量计;C0为吸附原液中L-α-GPC的质量浓度/mg/mL;C为吸附后溶液中L-α-GPC的质量浓度/mg/mL;Ce为溶液平衡浓度/mg/mL;V为溶液的体积/mL;W为硅胶的干重/g。
1.2.3 静态吸附平衡
精确称取2 g活化硅胶(按1.2.2方法处理)置于100 mL的锥形瓶中,分别加入50 mL质量浓度16.6 mg/mL的L-α-GPC溶液;在25 ℃,在95 r/min的恒温水浴震荡器上摇,均匀吸附;HPLC-ELSD分析L-α-GPC浓度,确定吸附达到平衡所需的时间。
1.2.4 静态吸附等温线测定
称取2 g活化硅胶(按1.2.2方法处理)置于100 mL的锥形瓶中,加入L-α-GPC溶液50 mL;放在298、308、318 K的恒温水浴震荡器中,在95 r/min的转速下震荡吸附,吸附平衡后,取上清液,用HPLC-ELSD测定平衡时浓度(Ce),计算平衡吸附量(Qe),以平衡吸附量(Qe)对平衡浓度(Ce)作静态吸附等温线。
1.3 HPLC-ELSD
色谱条件:硅胶柱,ZORBAXRX-SIL(4.6×250 nm,5 μm),柱温35 ℃,漂移管温度30 ℃;采用二元梯度洗脱,流动相A(甲醇∶水=8∶1,V∶V),流动相B(甲醇),流速1.0 mL/min;A相的梯度,开始10 min,以40%梯度增加到60%,保持5 min,之后3 min,以60%梯度降低到40%;进样量20 μL。样品的定性通过标样保留时间比对,定量采用标样外标法。L-α-GPC标准曲线:Y=9.273 9X-8.379 9(R2=0.991),L-α-GPC质量浓度(1 mg/mL≤CGPC≤4 mg/mL)。
1.4 未反应核收缩模型模拟硅胶吸附过程
L-α-GPC在硅胶内进行吸附时,由于硅胶本身参与了吸附,它的内部条件会随时间变化,因此硅胶的吸附过程具有稳态特征。当L-α-GPC在硅胶内吸附时,假设它首先在硅胶表面进行吸附,当硅胶表面吸附点吸附完全后,L-α-GPC会随溶剂继续向硅胶内部扩散,逐渐形成吸附层。未吸附的硅胶层与已吸附的硅胶层在性质方面发生了巨大变化,这种变化使硅胶变成了一个非均相体系。吸附层形成后,L-α-GPC通过该吸附层继续向未吸附的硅胶层扩散,并将已吸附层向未吸附层推进,未吸附层逐步缩小,使整个吸附过程具有了非均相未反应核收缩模型的特征, 硅胶吸附L-α-GPC的未反应核模型见图1。
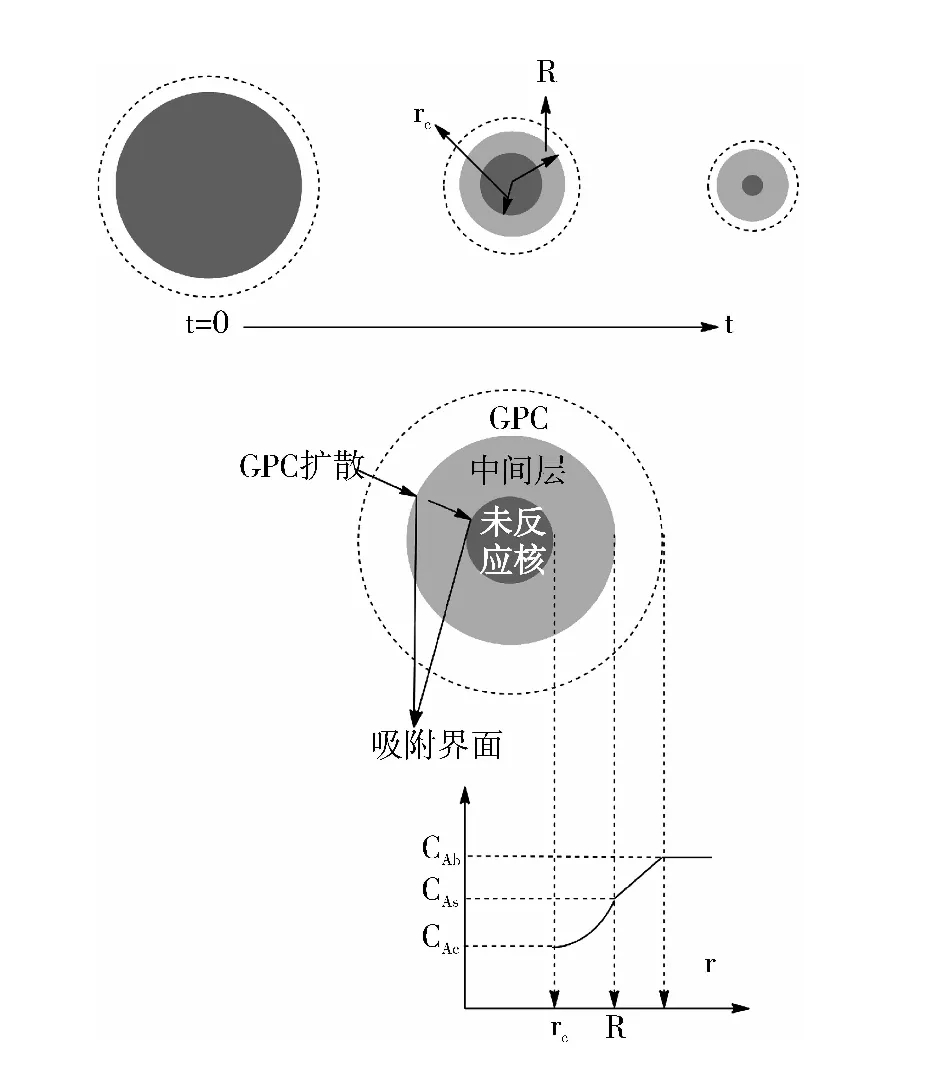
图1 硅胶吸附的未反应核收缩模型
根据这一假设,硅胶的吸附过程可能有3个速度控制步骤:(1)L-α-GPC通过硅胶与溶液的界面到达硅胶表面扩散速度控制步骤;(2)L-α-GPC与硅胶吸附点的吸附速度控制步骤; (3)L-α-GPC进入硅胶内部的速度控制步骤。一般情况,硅胶表面吸附点吸附L-α-GPC的速度比通过硅胶与溶液界面到达硅胶表面的扩散速度快,也比进入硅胶内部的速度快。因此,硅胶吸附L-α-GPC的速度控制模型仅能是界面扩散控制或者进入硅胶内部的速度控制。
假设:(1)忽略吸附过程温度波动;(2)L-α-GPC的吸附速度远远大于通过未饱和吸附层的扩散速度;(3)硅胶颗粒是具有中心对称的球形体;(4)硅胶吸附L-α-GPC的吸附量和孔隙率呈线性关系;(5) 吸附过程在拟稳态条件下进行;(6)L-α-GPC通过饱和吸附层和未饱和吸附层的扩散系数相同。
依据上述假设,未吸附的硅胶固体颗粒表面上L-α-GPC的浓度c1等于零。假设在一段时间内通过吸附层的扩散是拟稳态过程,即通过吸附层的扩散时间远远小于吸附层的厚度明显改变的时间。L-α-GPC吸附速率相对于时间t通过吸附层的扩散密度J1有如下关系:

(3)
且:

(4)


(5)

(6)
即:

(7)
吸附量的变化可通过未吸附硅胶颗粒的球形半径的变化来表征。因为:
(8)
式中:ρs、rp分别为L-α-GPC的摩尔密度和未吸附硅胶颗粒半径。为了确定吸附量与吸附时间的依赖关系,考虑化学计量后,对式(8)两边求导,可表示为:

(9)
将式(9)代入式(7)可得:

(10)
两边整理:

(11)
将此式在rp0与rp之间以及t=0和t之间积分得到:

(12)
硅胶的活性点完全吸附所需总时间t*,即rp=0时,所需的时间t*为:

(13)
吸附率X用未吸附硅胶颗粒的球形半径的变化来表征:

(14)
将吸附时间用吸附率X表达,最终得到t/t*与X的关系:

(15)
通过t对1-3(1-X)2/3+2(1-X)作图可以判定速度控制模型是否是界面扩散控制。
如果速度控制模型是L-α-GPC进入硅胶内部的速度控制,通过上述相类似的方法建立如下关系式:

(16)
通过研究可以发现,对于吸附过程,不同的速率控制模型,吸附量与吸附时间之间的关系不同,通过测定不同时间的吸附量,再根据上述3个关系式,即可以计算出硅胶吸附L-α-GPC的速率控制模型。
2 结果与讨论
2.1 硅胶吸附动力学
硅胶吸附L-α-GPC的吸附量随时间变化曲线见图2。从图中可以看出,硅胶在初始阶段快速吸附,然后逐渐趋缓,总的硅胶吸附量一直在增加,在4 min达到吸附平衡。
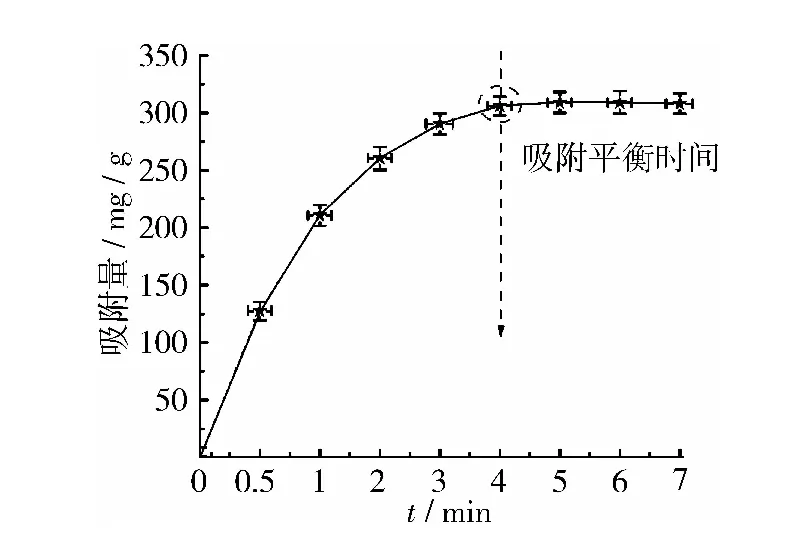
图2 吸附量与时间的关系
2.2 吸附速率控制模型
界面扩散控制速率模型:选择非均相未反应核收缩模型对图2的数据进行处理,根据前面推导的界面扩散控制速率模型的动力学方程(15),以1-3(1-X)2/3+2(1-X)对t作图,结果如图3。图中显示,1-3(1-X)2/3+2(1-X)与t有很好的线性关系,回归方程为Y=-0.006 92+0.218 97X,线性相关系数R2为0.996 21,这都说明了界面扩散控制速率模型为硅胶吸附L-α-GPC的扩散速度控制模式。

图3 1-3(1-X)2/3+2(1-X)与吸附时间t的关系
硅胶吸附速率控制模型:根据前面推导的速度控制模型动力学方程(16),以吸附率X对吸附时间t作图,结果如图4。图中显示吸附率X与t不成线性关系,这也说明了L-α-GPC进入硅胶内部的速度控制模式不是真实的硅胶吸附速率控制模型。

图4 吸附率X与吸附时间t的关系
通过对2种硅胶吸附L-α-GPC过程的速率控制模型进行分析,确定了硅胶吸附速率控制模型为界面扩散控制速率模式。
2.3 静态吸附平衡
静态平衡曲线可以判断硅胶吸附L-α-GPC的吸附平衡时间,从图5中可以看出,甲醇溶液中L-α-GPC的浓度随着时间的延长逐渐降低,在4 min内,浓度从16.6 mg/mL降低到4.3 mg/mL,然后趋于平衡。这说明在4 min硅胶吸附L-α-GPC达到吸附平衡。

图5 溶液中L-α-GPC浓度随吸附时间的变化
2.4 硅胶吸附热力学模型
硅胶吸附平衡模型确定:在设定的298、308和318 K 3个温度下,Ce吸附平衡浓度用HPLC-ELSD测定,Qe用公式计算,对Ce和Qe做图,硅胶吸附L-α-GPC的吸附等温线如图6。

图6 硅胶的吸附等温线
Freundlich方程进行吸附平衡模拟:
(17)
两边取对数得:

(18)
Langmiur方程进行吸附平衡模拟:

(19)
取倒数得:

(20)
分别用Freundlich方程中的(lgQe)~(lgCe),Langmiur方程中的(1/Qe)~(1/Ce)数据作图进行吸附平衡模拟,通过线性回归方程参数和相关系数R2来判定模拟的准确性,结果见表1。
由表1可以看出298、308和318K 3个温度下Freundlich方程和Langmiur方程对硅胶吸附等温线的模拟,Freundlich模拟出来的回归方程相关系数比较低,证明了这种模拟方法不适合硅胶吸附,Langmiur方程模拟的结果比较令人满意,不同温度条件下,回归方程的相关系数均在0.99以上。因此,在目前的试验条件下,用 Langmiur方程能更好的对硅胶吸附L-α-GPC的吸附等温线进行拟合。

表1 吸附方程的参数
在本研究用Langmiur方程对298、308和318K 3个温度条件的硅胶吸附等温线进行了拟合。根据图6可以得到不同温度下的回归方程:



从图6可以看出,上样浓度相同时,随着温度的升高,硅胶的吸附能力下降,这说明温度升高降低硅胶对L-α-GPC的吸附,这说明硅胶的吸附为放热反应。
硅胶吸附热力学分析:
Clausius-Clapeyron方程:
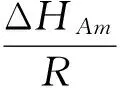
(21)
固定上样量(固定上样浓度和上样体积进行控制),由lnCe对1/T作图。

图7 硅胶吸附等容线
图7为硅胶吸附等容线,在80、160和240 mg/g 3个上样量条件下,lnCe对1/T作图,进行线性回归,根据公式(21)计算不同上样量的硅胶吸附热力学参数焓变(ΔHAm),结果见表2。

表2 不同上样量的硅胶吸附热
3 结论
通过研究自制样品L-α-GPC的硅胶吸附动力学和热力学,发现界面扩散控制速率模型1-3(1-X)2/3+2(1-X)能很好的拟合硅胶的吸附过程。同时,用Langmiur方程对硅胶吸附L-α-GPC的吸附等温线进行了拟合,计算出不同温度条件下的回归方程,相关系数均在0.99以上,并且证实了硅胶的吸附为放热反应。最后,利用Clausius-Clapeyron方程计算出80、160和240 mg/g 3个吸附量的硅胶吸附热力学参数,焓变(ΔHAm)分别为24.85、23.82、22.72 kJ/mol。
[1]Sigala S, Imperato A, Rizzonelli P, et al.L-alpha glycerylphosphorylcholine antagonizes scopolamine induced amnesia and enhances hippocampal cholinergic transmission in the rat [J]. Europen Journal of Pharmacology, 1992, 211(3):351-358
[2]Brownawell A M, Carmines E L, Montesano F, et al. Safety assessment of AGPC as a food ingredient [J]. Food and Chemical Toxicology, 2011, 49(6): 1303-1315
[3]Gozzoli M, Scolastico C. A process for the preparation ofL-alpha glycerylphosphorylcholine [P]. UK Patent, UK 2 058 792. 1981
[4]Ziegenfuss T, Landis J, Hofheins J. Acute supplementation with L-alpha glycerylphosphorylcholine augments growth hormone response to, and peak force production during, resistance exercise [J]. International Journal of Sport Nutrition and Exercise Metabolism, 2008(5):15
[5]De J M M M. Cognitive improvement in mild to moderate alzheimer's dementia after treatment with the acetylcholine precursor choline alfoscerate: a multicenter, double blind, randomized, placebo controlled trial [J]. Clinical Therapeutics, 2003, 25: 178-193
[6]Gunawan S, Kasim N S, Ju Y H. Separation and purification of squalene from soybean oil deodorize distillate[J].Separation Purification Technology, 2008, 2(60): 128-135
[7]Shin S J, Park C E, Baek N I, et al. Betulinic and oleanolic acids isolated from forsythia suspensa vahl inhibit urease activity of helicobacter pylori [J]. Biotechnology and Bioprocess Engineering, 2009, 14(2): 140-145
[8]Levenspiel O. Chemical reaction engineering [A]. 2rd Ed, Wiley, New York,1972
[9]Safarik I, Rego L F T, Borovska M, et al. New magnetically responsive yeast-based biosorbent for the efficient removal of water-soluble dyes [J]. Enzyme and Microbial Technology, 2007, 40(6): 1551-1556
[10]Kargi F, Cikla S. Biosorption of zinc(II) ions onto powdered waste sludge (PWS): kinetics and isotherms [J]. Enzyme Microbial Technology, 2006, 38(5): 705-710
[11]Çengel YA, Boles MA. Thermodynamics an engineering approach. mcgraw-hill series in mechanical engineering (3rd ed.) [D]. Boston, 2009.
Kinetics ofL-alpha Glycerylphosphorylcholine Adsorption by Silica Gel and Enthalpy Change
Zhang Kangyi1,2Zhang Lixia1Wang Xingguo3Qu Lingbo2Liu Yuanfa3
(Henan Academy of Agricultural Sciences Institute of Agricultural Products Processing1, Zhengzhou 450002)(Zhengzhou University Department of Chemistry2, Zhengzhou 450001)(Jiangnan University,School of Food Science and Technology3, Wuxi 214122)
The control of adsorption process of silica gel on the kinetics and thermodynamic of adsorption of L-alpha glycerylphosphorylcholine (L-α-GPC) was studied. The results showed that the adsorption process of silica gel can be well governed by interface diffusion control rate model 1-3(1-X)2/3+2(1-X). The adsorption isotherm ofL-α-GPC by silica gel could be described with the equation of Langmiur through the stimulation of adsorption balance by Freundlich and Langmuir equations, and then regression equation under different temperature conditions was calculated (related coefficient was above 0.99), and silica gel adsorption was identified as exothermic reaction. The silica gel adsorption thermodynamic parameters of three absorption measurements were 80, 160 and 240 mg/g respectively by Clausius-Clapeyron equation, and the adsorption enthalpy change (ΔHAm) was 24.85, 23.82, 22.72, respectively. The results provided the basic data and theoretical support for further exploration on the industrialized preparation of high purityL-α-GPC by silica gel column chromatography.
L-alpha glycerylphosphorylcholine, silica gel column chromatography, kinetics, thermodynamic parament
TS229
A
1003-0174(2016)03-0047-06
国家自然科学基金(31301502),河南省农业科学院优秀青年科技基金(2013YQ25)
2014-07-09
张康逸,男,1981年出生,博士,脂质科学
刘元法,男,1974年出生,教授,油脂加工
