足光散质量标准提高研究
2016-12-26阳文武朱泽兵杨潇潇李柏群
肖 琦,阳文武,朱泽兵,杨潇潇,李柏群
(1.重庆市万州食品药品检验所,重庆 404000; 2.重庆市三峡中心医院,重庆 404000)
足光散质量标准提高研究
肖 琦1,阳文武1,朱泽兵1,杨潇潇1,李柏群2
(1.重庆市万州食品药品检验所,重庆 404000; 2.重庆市三峡中心医院,重庆 404000)
目的 提高足光散的质量标准。方法 采用高效液相色谱法测定足光散中苯甲酸、水杨酸的含量。色谱柱为迪马C18柱(250 mm× 4.6mm,5 m),以甲醇-0.1%磷酸(45∶55)为流动相,流速为1.0mL/min,测定波长为226 nm。结果 供试品溶液与对照品溶液主峰保留时间一致,阴性对照品溶液无相应色谱峰出现。苯甲酸、水杨酸质量浓度分别在60.30~1 206.04 g/m L(r=0.999 8)和40.54~810.81 g/m L(r=0.999 7)范围内与峰面积线性关系良好;苯甲酸平均回收率为99.47%,RSD=0.76%(n=6),水杨酸平均回收率为95.93%,RSD=1.15%(n=6)。结论 该方法准确、重复性好,可用于足光散的质量控制。
足光散;苯甲酸;水杨酸;高效液相色谱法;质量标准
足光散由水杨酸(18%)、苯甲酸(12%)、硼酸(40%)、苦参(20%)和滑石粉(10%)组方,具有清热燥湿、杀虫敛汗的功效,主要用于手足癣、汗臭症的治疗[1]。其质量标准中苯甲酸和水杨酸的含量测定为滴定法,无单独的含量测定方法,已有文献报道用高效液相色谱(HPLC)法测定[2-3],但样品处理较复杂,流动相采用磷酸盐,色谱柱容易损坏。本研究中对其色谱条件和样品处理方法做了进一步优化,现报道如下。
1 仪器与试药
Agilent1100型高效液相色谱仪。苯甲酸、水杨酸对照品(成都市科龙化工厂,含量均大于99.5%);甲醇为色谱纯,磷酸为分析纯,水为超纯水;足光散(成都九芝堂金鼎药业有限公司,批号为150107;广东一禾药业有限公司,批号为1409106;武汉中联集团四药药业有限公司,批号为141120)。
2 方法与结果
2.1 色谱条件[2-7]
色谱柱:迪马 C18柱(250 mm×4.6 mm,5μm);流动相:甲醇-0.1%磷酸(45∶55);流速:1.0mL/min;波长:226 nm;进样量:10μL。
2.2 溶液制备
称取苯甲酸对照品0.121 21 g,精密称定,置20m L容量瓶中,称取水杨酸对照品0.203 72 g,精密称定,置25m L容量瓶中,分别加甲醇溶解定容,制成每1mL分别含苯甲酸、水杨酸6 030.20μg和8 108.06μg的对照品贮备液。分别吸取苯甲酸、水杨酸对照品贮备液5.0 m L和2.5 m L,置10 m L容量瓶中,制得含苯甲酸3 015.10μg/mL、含水杨酸2 027.02μg/mL的混合对照品溶液。取本品,研磨,混匀,称取4 g,精密称定,置具塞锥形瓶中,精密加入乙醇25m L,称定质量,超声处理30min,放冷,加乙醇补足减失的质量,摇匀,滤过,再精密吸取1mL,置100mL容量瓶中,加甲醇定容,摇匀,即得供试品溶液。按足光散处方及生产工艺制成缺苯甲酸、水杨酸的阴性样品,取阴性样品适量,按供试品溶液制备方法制成阴性对照品溶液。
2.3 方法学考察
专属性试验:分别精密吸取对照品溶液、供试品溶液和阴性对照品溶液各10μL,依法进样测定。结果阴性对照品溶液对测定无干扰,见图1。
线性关系考察:精密吸取质量浓度为3015.10μg/mL(苯甲酸)、2 027.02μg/mL(水杨酸)的混合对照品溶液0.20,0.40,1.00,2.00,4.00m L,置10m L容量瓶中,加甲醇定容,摇匀,按拟订色谱条件进样测定峰面积,以峰面积(A)对质量浓度(C)进行线性回归,得回归方程 A=0.124 3C-9.135 2,r=0.999 8(苯甲酸);A=0.263 0C-5.151 6,r=0.999 7(水杨酸)。结果表明,苯甲酸、水杨酸质量浓度分别在60.30~1 206.04μg/mL(n=5)和40.54~810.81μg/mL(n=5)范围内与峰面积线性关系良好。
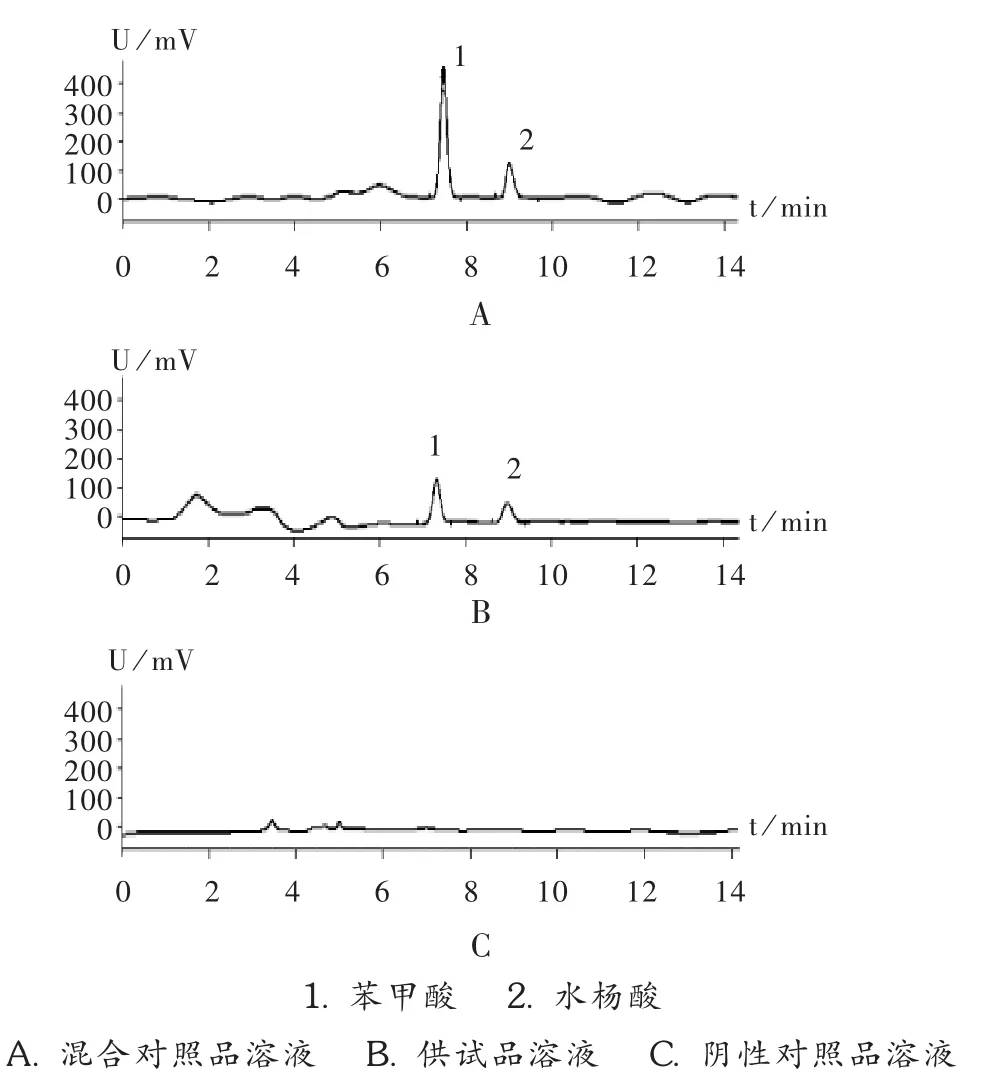
图1 高效液相色谱图
精密度试验:精密吸取苯甲酸、水杨酸混合对照品溶液10μL,连续进样6次,依法测定。结果峰面积的RSD分别为0.69%和1.12%(n=6),表明仪器精密度良好。
稳定性试验:取同一供试品溶液,每2 h进样1次,持续进样6次。结果苯甲酸、水杨酸峰面积的 RSD分别为0.90%和1.10%(n=6),表明供试品溶液在12 h内稳定。
重复性试验:取同一批样品6份,依法制备供试品溶液,进样测定。结果苯甲酸、水杨酸峰面积的 RSD分别为0.80%和1.20%(n=6),表明方法的重复性良好。
加样回收试验:精密量取已知含量的样品(批号为150107)6份,分别加入苯甲酸、水杨酸不同质量浓度混合对照品溶液适量,按拟订色谱条件进样测定,计算回收率。结果见表1。
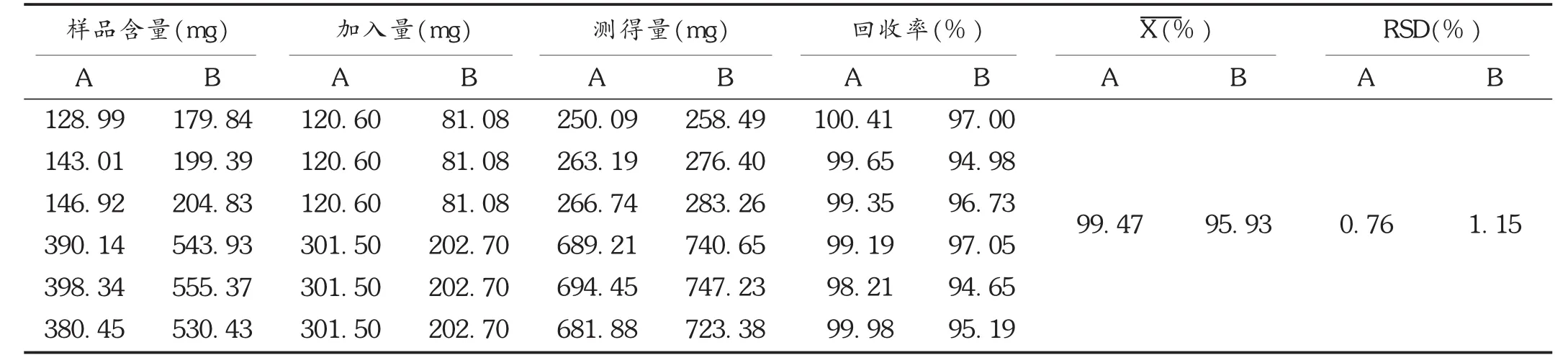
表1 加样回收试验结果(n=6)
2.4 样品含量测定
取本品3批(成都九芝堂金鼎药业有限公司,批号为150107;广东一禾药业有限公司,批号为1409106;武汉中联集团四药药业有限公司,批号为141120),依法制备供试品溶液,进样测定。结果见表2。

表2 样品含量测定结果(n=3)
3 讨论
本研究中利用HPLC法对足光散中苯甲酸、水杨酸的含量进行测定,采用乙醇超声提取,以甲醇磷酸水为流动相,优化了样品的处理方法和色谱条件,有利于保护色谱柱,同时方法的准确性、重复性好,可为足光散质量控制标准的提高提供参考。
[1]WS-10344(ZD-0344)2002-2012Z,国家食品药品监督管理局国家药品标准[S].
[2]李艳莉,吴晓华,马耀荣,等.反相高效液相色谱测定足光粉中苯甲酸、水杨酸的含量[J].佛山科学技术学院学报:自然科学版,2006,24(4):68-71.
[3]余小平.高效液相色谱法同时测定足光散中水杨酸、苯甲酸的含量[J].药物分析杂志,2005,25(8):955-957.
[4]张荣桂,马鸿雁.高效液相色谱法同时测定复方水杨酸酊中两种组分含量[J].中国药业,2006,15(6):17.
[5]黄 洁,李锋武,刘鹏鸣,等.反相高效液相色谱法测定复方水杨酸酊中水杨酸和苯甲酸含量[J].中国药业,2012,21(20):39-40.
[6]年四辉,李 萍,刘丽敏,等.HPLC测定板蓝根及其制剂中水杨酸、苯甲酸的含量[J].中国实验方剂学杂志,2012,18(21):92-95.
[7]李 莹,戴 博,宋 妍.三酸散的质量标准提高[J].中国药事,2014,28(9):1 005-1 008.
Im p rovem ent of Quality Standard of Zuguang Pow der
Xiao Qi1,Yang Wenwu1,Zhu Zebing1,Yang Xiaoxiao1,Li Boqun2
(1.Wanzhou Institute for Food and Drug Control,Chongqing,China 404000; 2.Chongqing Three Gorges Centre Hospital,Chongqing,China 404000)
Ob jective To improve the quality standard of Zuguang Powder.M ethods Salicylic acid and benzoic acid were identified by HPLC.The Diamonsil C18column(250 mm×4.6 mm,5μm)was used with the mobile phase of methanol-0.1%phosphoric acid(45∶55)at a flow rate of 1.0 mL/min,the detection wavelength was set at 226 nm.Results The peak retention time of the test solution corresponds to the reference solution with the negative control without the corresponding peaks.Benzoic acid was linear within 60.30-1 206.04μg/m L(r=0.999 8),salicylic acid was linear within 40.54-810.81μg/mL(r=0.999 7);the average recovery rate of benzoic acid was 99.47%,RSD=0.76%(n=6),the average recovery rate of salicylic acid was 95.93%,RSD=1.15%(n=6).Conclusion The method is accurate and repeatable,which can be used for the quality control of Zuguang Powder.
Zuguang Powder;benzoic acid;salicylic acid;HPLC;quality standard
R284.1;R286.0
A
1006-4931(2016)04-0073-03
肖琦(1978-),男,硕士研究生,主管药师,主要从事食品、药品、保健食品和化妆品的检验工作,(电话)023-58152309(电子信箱)1600818606@qq.com;李柏群(1971-),女,大学本科,副主任中药师,研究方向为中药临床及中药制剂的研发,本文通讯作者,(电话)023-58103218(电子信箱)bqlicn@163.com。
2015-04-09;
2015-08-21)
