荧光素钠/吲哚菁绿同步眼底血管造影不良反应文献分析
2016-12-24郭义明白凤芝
郭义明,于 倩,郭 鑫,白凤芝
(吉林大学中日联谊医院,吉林 长春 130033)
荧光素钠/吲哚菁绿同步眼底血管造影不良反应文献分析
郭义明,于 倩,郭 鑫,白凤芝
(吉林大学中日联谊医院,吉林 长春 130033)
目的 探讨荧光素钠/吲哚菁绿同步眼底血管造影(FFA/ICGA)不良反应的一般规律和特点,寻找相关风险因素,为临床安全合理用药提供参考。方法 以“荧光素钠”“吲哚菁绿”“不良反应”为主要检索词,检索中国期刊全文数据库,按纳入与排除标准共纳入7篇文献,得到符合标准的不良反应病例247例,进行资料的提取与统计分析。结果 FFA/ICGA不良反应发生率为7.50%,其中男84例(56.00%),女66例(44.00%);60岁以上老年患者发生率低;97.17%的不良反应发生在用药后5 min内;累及的系统/器官主要为消化系统损害(45.08%)、呼吸系统损害(32.06%)、皮肤及其附件损害(11.75%),临床表现以恶心(79例次)、呕吐(63例次)及鼻咽部不适(74例次)最常见;轻度不良反应占93.93%,中度及重度不良反应分别占4.05%和2.02%;过敏试验无法预测是否会发生不良反应。结论 FFA/ICGA是较安全的临床造影技术。FFA/ICGA不良反应发生速度快,必须重视造影开始后1 h内的监测,制订不良反应应对预案,确保临床用药安全。
荧光素钠;吲哚菁绿;眼底血管造影;药品不良反应;文献分析
眼底血管造影是诊断视网膜和脉络膜疾病的一种常用方法,荧光素钠眼底血管造影(FFA)可客观地记录视网膜循环的动态图像,用于检查视网膜循环疾病[1]。吲哚菁绿血管造影(ICGA)能很好地显示脉络膜血管结构或发现脉络膜新生血管,可用于检查脉络膜循环疾病[2]。荧光素钠/吲哚菁绿同步眼底血管造影(FFA/ICGA)可发挥2种检查技术各自的优势,一次性完成视网膜和脉络膜病变的临床诊断和追踪检查,减少对患者的损伤,目前临床应用日渐增多。现对近年来国内文献报道的FFA/ICGA不良反应进行了回顾性分析,探讨其规律和特点,以期为临床安全用药提供参考。
1 资料与方法
1.1 文献资料
检索中国期刊全文数据库(CNKI),以“荧光素钠”“吲哚菁绿”(包含“吲哚氰绿”“吲哚青绿”“靛青绿”)与“不良反应”为检索词,检索2014年12月31日以前的文献资料。
纳入标准:FFA/ICGA的文献,包括对照研究、病例研究、个案分析、临床观察。
排除标准:明确无不良反应发生、非病例报道、重复报道、二次文献研究、实验研究、综述摘要类文献、资料不全的文献。
检索结果:检索出文献18篇,排查后符合纳入标准的有7篇,涉及FFA/ICGA相关病例3 289例,发生不良反应的247例。
1.2 统计方法
将247例FFA/ICGA不良反应病例患者的年龄、性别、过敏试验、药品用法用量,以及不良反应的发生时间、累及系统/器官与临床表现、发生程度、处理与转归进行统计和分析。
2 结果
2.1 患者性别与年龄
247例不良反应中,明确患者性别的150例,其中男84例(56.00%),女66例(44.00%);性别不详97例;年龄12~84岁,明确年龄区间的123例(49.80%);年龄未归类的124例(50.20%)。见表1。

表1 247例患者年龄分布
2.2 过敏试验
247例不良反应中,用药前将荧光素钠与吲哚菁绿混合或分别进行过敏试验,采用肘静脉注射法或前臂划痕皮试法,观察15~20min,若未见过敏反应,按医嘱进行FFA/ICGA。
2.3 药品用法用量
过敏试验阴性的患者按荧光素钠与吲哚菁绿说明书规定,采用肘或手背静脉注射,5~10 s内快速推注荧光素钠注射液及注射用水溶解的吲哚菁绿,造影结束后患者留观30~60min,观察无异常后离开。20%荧光素钠用量为3m L,吲哚菁绿常规剂量为25mg,或按体重0.5~1.0mg/kg计算。见表2。
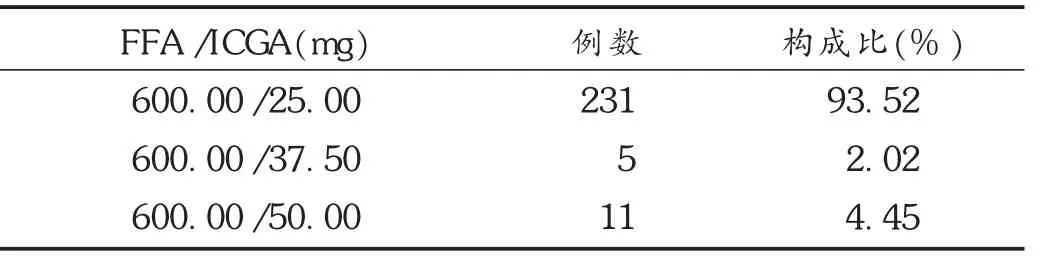
表2 FFA/ICGA用药剂量(n=247)
2.4 不良反应发生时间
247例不良反应主要发生在用药后2~5min,用药后1min发生28例。见表3。

表3 不良反应的发生时间(n=247)
2.5 不良反应累及系统/器官分布
247例不良反应累及7个系统/器官,分别为消化系统损害、呼吸系统损害、皮肤及其附件损害、全身性损害、神经系统损害、心血管系统损害及泌尿系统损害。其中消化系统损害所占比例最高,以恶心、呕吐为主要临床表现;呼吸系统损害以鼻咽部不适为主。见表4。

表4 不良反应累及系统/器官及临床表现
2.6 不良反应发生程度及处理与转归
Yannuzzi等[3]把眼底血管造影不良反应分为4类,轻度反应:恶心、呕吐、外渗、喷嚏及瘙痒等;中度反应:一过性心慌、荨麻疹、皮疹、晕厥、血栓性静脉炎、发热、局部组织坏死等;重度反应:气管或喉肌痉挛及过敏、休克、心肌梗死、癫痫样发作等;死亡。按Yannuzzi等的分类方法,247例不良反应以轻度为主,中度及重度不良反应很少,未出现死亡报告,见表5。轻度不良反应仅为一过性的体征表现,未经处理即完全恢复,中度不良反应患者可采取吸氧、口服葡萄糖酸钙和苯海拉明等措施,重度不良反应注射肾上腺素和地塞米松后恢复。247例不良反应有1例症状缓解时间为2 h,其余均在10~30min内转归。

表5 不良反应发生程度统计(n=247)
3 讨论
3.1 患者年龄与性别
247例FFA/ICGA所致的不良反应发生在各个年龄段。在123例明确年龄范围的病例中,21岁及以上年龄段的病例随着年龄的增长不良反应呈下降趋势,60岁以上患者发生率较低,表明随年龄的增长患者的反应性逐渐下降,对不良反应相对不灵敏,但老年人生理功能状态低下,常伴有心血管疾病,应谨慎用药。在150例已知性别的病例中,不良反应发生率男性(56.00%)高于女性(44.00%),表明不良反应与性别有一定相关性。3.2 不良反应与过敏试验、发生时间的关系
FFA/ICGA检查前的过敏试验是预防过敏反应发生的一项重要安全措施,247例病例在FFA/ICGA前均按规定进行了造影剂过敏试验,结果为阴性时才能进行造影,说明目前的过敏试验方法并不能很好地预测造影检查时是否会发生过敏反应,也无法判断与其他不良反应的相关性。用药后5 min内发生不良反应的比例占97.17%,可能是由于药液注射速度快,机体产生应激性反应,导致一过性组胺物质释放过多过快,引起小血管扩张而出现症状,所以造影开始时就要密切监测患者的生命体征,并持续监护患者1 h。
3.3 不良反应与药物因素
吲哚菁绿含有微量的碘,对碘过敏的患者用药后刺激机体产生相关的不良反应。荧光素钠在静脉内60%与血浆蛋白结合,吲哚菁绿静脉注射后95%与血浆蛋白结合,FFA/ICGA检查时,大分子物质瞬间进入体内与血浆蛋白结合成为半抗原,从而导至Ⅰ型过敏反应,严重时发生过敏性休克。FFA的不良反应,李艳艳等[4]报道为6.6%,陆莹等[5]报道为8.98%,丘红红[6]报道为5.2%。ICGA的不良反应国内报道较少,日本学者统计了2 820例吲哚菁绿脉络膜血管造影病例,不良反应占0.34%[7];陈有信等[8]报道为0.65%。本研究中统计的3 289例FFA/ICGA病例中发生不良反应的247例,发生率为7.51%,表明FFA/ICGA的不良反应与荧光素钠和吲哚菁绿直接相关,同步造影并不导致不良反应叠加,不良反应发生率无增加趋势。
3.4 不良反应累及系统/器官及临床表现
FFA/ICGA的不良反应以消化系统损害和呼吸系统损害为主,临床表现为恶心、呕吐和鼻咽部不适。其次为皮肤及其附件损害,表现为皮疹、瘙痒、皮肤潮红等。魏广川等[9]将FFA不良反应分为造影剂因素所致的过敏性反应和心因性因素所致的类过敏反应,前者涉及造影剂的浓度及注射速度等因素,采取过敏试验及口服抗过敏止吐药物等措施也无法预知有无不良反应发生,而后者涉及到医务人员的沟通和操作技巧,以及患者的年龄、性别、就医经验、应激能力、造影环境等,表现为恶心、呕吐、鼻咽部不适或者脸色苍白、大汗等症状,休息或深呼吸后症状可缓解。吲哚菁绿中微量碘引发的不良反应表现为恶心、口腔分泌物增加、荨麻疹、瘙痒及低血压等症状。由表4可见,FFA/ICGA不良反应兼具荧光素钠与吲哚菁绿的特点。
3.5 不良反应发生程度及转归
FFA的不良反应轻中度较多,严重不良反应极少,但有死亡病例报道[10]。一般认为,ICGA比FFA更安全且易于被患者耐受,以轻度不良反应为主,也有发生过敏性休克等严重不良反应的报道[2]。由表5可见,247例FFA/ICGA所致的不良反应主要为轻度反应,占93.93%,中、重度不良反应占比很小,无死亡病例,且绝大多数病例无需治疗即可自行恢复,少数中、重度不良反应及时治疗可获得良好的转归,表明FFA/ICGA是一项比较安全的技术。
3.6 FFA/ICGA风险控制因素
FFA/ICGA所致的不良反应发生速度快,对全身各脏器都有一定影响,临床应用中应严格掌握好适应证和禁忌证,造影前应监测肝肾功能等相关临床指标,采取恰当的沟通技巧,详询既往史、现病史、药物过敏史,尤其注意有无碘过敏史,并向患者介绍造影环境、方法及注意事项,以减少紧张情绪和恐惧心理等心因性因素导致的不良反应。对过敏体质者、哮喘患者、严重心血管疾病患者尽量不做眼底血管造影。造影过程中要密切观察患者的反应和生命体征,造影结束后留院观察1 h左右。造影室内要配备急救药品和抢救器材,制订周全的不良反应应对预案,对不同程度的不良反应采取相应的措施。
[1]魏文斌,杨丽红.荧光素眼底血管造影的临床应用[J].眼科研究,2006,24(1):1-4.
[2]文 峰.吲哚青绿血管造影术及其临床应用[J].眼科研究,2006,24(2):113-118.
[3]Yannuzzi LA,Rohrer KT,Tindel LJ,etal.Fluorescein angiography complication survey[J].Ophthalmology,1986,93(7):611-617.
[4]李艳艳,毕莉莉.眼底荧光素钠血管造影620例不良反应分析[J].中国误诊学杂志,2012,12(6):1 392.
[5]陆 莹,赵菊莲.进口与国产荧光素钠在眼底血管造影中不良反应的对比研究[J].眼科新进展,2012,3(23):233-236.
[6]丘红红.荧光素钠应用于荧光素造影检查眼底血管的安全性及不良反应特点[J].临床眼科杂志,2015,23(1):78-80.
[7]Akria O,Tokuhiko M,Kazuhiko H,etal.Survey of Complication of Indocyanine Green Angiography in Japan[J].Am JOphthalmol,1994,118(6):749-753.
[8]陈有信,韩宝玲,张承芬.靛青绿血管造影毒副作用的临床观察[J].中国实用眼科杂志,1998,16(3):158-159.
[9]魏广川,孙 伟.眼底荧光血管造影的不良反应及应对措施[J].中国实用眼科杂志,2006,24(6):636-637.
[10]向 方,张 雷.荧光素钠静脉注射致过敏性休克死亡1例[J].中华眼底病杂志,2002,18(3):220.
Literature Review of Adverse Drug Reaction Induced by Sim ultaneous Fundus Angiogrouphy w ith Sodium Fluorescein and Indocyanine G reen
Guo Yiming,Yu Qian,Guo Xin,Bai Fengzhi
(China-Japan Union Hospital of Jinlin University,Changchun,Jilin,China 130033)
Objective To investigate the characteristics and mechanism of adverse drug reactions(ADR)induced by simultaneous fundus angiogrouphy with sodium fluorescein and indocyanine green(FFA/ICGA)to find out its risk factors,and provide technical support for safe and rational use of drugs in clinic.M ethods ″Sodium fluorescein″″indocyanine green″and″adverse reaction″were used as key words to retrieve the CNKI database.7 articles which met the inclusion and exclusion criteria were extracted,247 ADR cases were enrolled and analyzed.Results FFA/ICGA incidence of ADR was 7.50%,56.00% were male,44.00% were female,patients aged over 60 patients appear to have lower ADR occurrence rate;ADR within 5 min after medication was 97.17%;systems and organs mainly involved in ADR were digestive system damage(45.08% ),respiratory system damage(32.06% ),skin and its accessories damage(11.75%);nausea(79 cases),vomiting(63 cases)and nose pharynx ministry unwell(74 cases)were the most common reported ADR;mild ADR accounted for 93.93%,moderate and severe ADR accounted for 4.05% and 2.02% respectively;the allergy test cannot predict whether adverse reactions occur.Conclusion FFA/ICGA is safe clinical imaging technology,but the ADR happen faster,it is important to pay attention to the ADR caused by FFA/ICGA,especially to strengthen patient surveillance within 1 hour after medication,plans for reasonable ADR,in order to prevent adverse drug reactions and ensure the safe drug use in clinic.
sodium fluorescein;indocyanine green;fundus angiogrouphy;adverse drug reaction;literature review
R969.3;R981+.2
A
1006-4931(2016)06-0064-03
郭义明(1964-),男,主任药师,研究方向为纳米药物制备及医院药学,(电子信箱)guoyiming6@163.com;白凤芝(1966-),女,副主任护师,研究方向为临床护理学,本文通讯作者,(电子信箱)572340556@qq.com。
2015-07-13)
