探究浓度对铜与硝酸反应的影响
2016-12-23
探究浓度对铜与硝酸反应的影响
刘赞许夏勇
铜和硝酸的反应实验是硝酸氧化性体现的一个重要的演示实验,也是掌握硝酸氧化性的很有必要的一个实验。因此它是高中化学经常考的一类计算题。
一、实验目的
对比观察浓、稀硝酸与铜反应的实验现象。
二、实验器材
实验仪器:铁架台、具支试管、烧杯、玻璃导管、橡皮管、止水夹、10mL注射器、塑料瓶、橡皮塞。
实验药品:铜丝、浓硝酸(体积比2∶1)、稀硝酸(体积比3∶5)、碳棒、40%氢氧化钠溶液、澄清石灰水、大理石、氧气。
三、实验原理及装置说明
实验原理如下,装置如图所示。
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
3NO2+H2O=2HNO3+NO
2NO+O2=2NO2

四、不同浓度硝酸与铜反应的影响
1.不同浓度硝酸与铜反应的产物
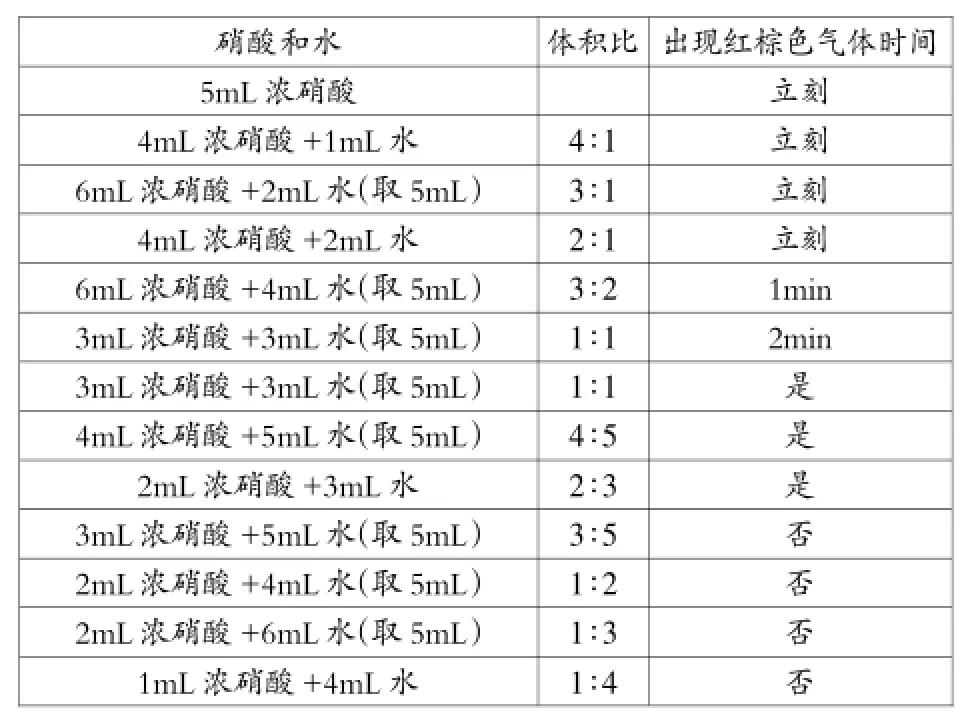
硝酸和水体积比出现红棕色气体时间5mL浓硝酸立刻4mL浓硝酸+1mL水4∶1立刻6mL浓硝酸+2mL水(取5mL)3∶1立刻4mL浓硝酸+2mL水2∶1立刻6mL浓硝酸+4mL水(取5mL)3∶2 1min 3mL浓硝酸+3mL水(取5mL)1∶1 2min 3mL浓硝酸+3mL水(取5mL)1∶1是4mL浓硝酸+5mL水(取5mL)4∶5是2mL浓硝酸+3mL水2∶3是3mL浓硝酸+5mL水(取5mL)3∶5否2mL浓硝酸+4mL水(取5mL)1∶2否2mL浓硝酸+6mL水(取5mL)1∶3否1mL浓硝酸+4mL水1∶4否
2.稀硝酸与铜反应

原电池原理(收集20mL气体)3mL稀硝酸+5mL水(取5mL)3∶5 5min 3min 2mL稀硝酸+4mL水(取5mL)1∶2 8min 5min 2mL稀硝酸+6mL水(取5mL)1∶3>10min>5min 1mL稀硝酸+4mL水1∶4>10min>5min硝酸和水体积比时间(收集20mL气体)
说明:选用浓硝酸的质量分数为65%~68%,量取液体选用10mL的注射器,铜丝缠绕在一根碳棒上(5号干电池的电极),铜与硝酸反应均在无氧的环境下进行。
通过实验可知,如需加快反应速率,铜与稀硝酸的反应可采用原电池原理,稀硝酸(体积比为3∶5)与铜反应能避免NO2生成,且反应速率较快。浓硝酸(体积比为2∶1)与铜反应实验速率适中,现象明显,便于观察。
五、实验步骤
1.组装实验仪器,检查装置的气密性。
2.向右边试管中先加入约0.6g大理石,打开开止水夹1、3、4,关闭开止水夹2,用注射器吸入6mL稀硝酸,将稀硝酸注入试管中,排尽装置内空气。
3.试管中不再产生气体时,关闭开止水夹3、4,打开开止水夹2,将可抽动的铜丝插入稀硝酸溶液中,铜丝表面有气泡产生,溶液变蓝色,氢氧化钠溶液中有稳定气泡产生。3mim后,关闭开止水夹1、2,将铜丝抽离液面,用注射器抽取试管内气体,再吸入空气,观察注射器内气体颜色由无色变为红棕色,实验完毕后,打开开止水夹1、2。
4.向左边具支试管中加入5mL浓硝酸,注射器中吸入10mL蒸馏水,打开开止水夹2、3,关闭开止水夹1、4,将可抽动的铜丝插入浓硝酸溶液中,铜丝表面有气泡产生,溶液变绿色,红棕色气体充满试管上部。将铜丝抽离液面,关闭开止水夹3,用注射器注入蒸馏水,观察试管中气体颜色的变化。然后用注射器抽取试管内3mL气体,再吸入少量空气,观察注射器内气体颜色的变化。实验完毕后,打开开止水夹1。
六、实验结论
1.装置将铜与浓、稀硝酸,NO2与H2O、NO与O2等反应实验整合于一体,有极佳的对比效果,可以很明显地观察到铜与浓、稀硝酸反应后溶液颜色的不同和产生气体的不同。
2.通过对浓、稀硝酸的初步界定,可推断出稀硝酸(体积比3∶5)、浓硝酸(体积比2∶1)与铜反应,现象最为明显。
3.实验在封闭体系中进行,真正地观察到了NO和NO2的颜色,实验现象明显,实验过程无NO2和NO气体排放,对环境无污染。
(作者单位:华容县第一中学)
