室温条件下Salen配合物催化氧化安息香
2016-12-21周步杰毛国亮陈中杭于文艳沈海民
周步杰, 毛国亮, 陈中杭, 方 慧, 于文艳, 沈海民
(浙江工业大学 化学工程学院,浙江 杭州 310014)
室温条件下Salen配合物催化氧化安息香
周步杰, 毛国亮, 陈中杭, 方 慧, 于文艳, 沈海民
(浙江工业大学 化学工程学院,浙江 杭州 310014)

以Salen配合物为催化剂,探究催化氧化安息香的清洁工艺条件。在室温条件下,由水杨醛、乙二胺反应制得席夫碱并与金属醋酸盐合成[M(Salen)](M=Mn, Co, Ni, Cu, Zn),同时使用红外光谱、核磁共振、XRD和XPS进行表征。以所得5种金属配合物为催化剂,探究对安息香氧化反应的催化性能。以空气为氧化剂,Co(Salen)为催化剂,优化了反应工艺。在优化条件下,探究了其他金属Salen配合物的催化性能,并用活性炭和分子筛固载Co(Salen),进行催化剂回收套用实验。实验表明,Mn(Salen)的催化性能最好,在催化剂含量为原料物质的量的6%,以DMF为溶剂,室温下反应60 min,苯偶酰的收率可达到80%以上。催化剂经分子筛吸附后可回收套用3次。该方法在室温下反应,节省能源,降低成本,符合绿色化学要求,为苯偶酰的清洁生产提供理论依据。
席夫碱配合物; 安息香; 催化氧化; 空气; 室温
0 引 言
安息香的氧化产物主要是苯偶酰即二苯基乙二酮,是一种重要的有机化工原料,也是合成药物苯妥英钠的中间体,在医药、日用化学品和香料生产中有着广泛的应用[1]。苯偶酰的合成方法很多,较为成熟的是安息香氧化,该路线收率高,是最常用的合成路线[2]。催化氧化安息香制备苯偶酰的氧化剂有很多种,常见有:铬酸盐[3]、硝酸[4]、高锰酸盐[5]、氯化铁[6]、硫酸铜[7]等。但上述氧化剂或多或少存在着环境污染严重、后处理困难等问题,并且这些氧化剂不可循环使用,成本较高。
近20年来,人们为寻找更好的氧化剂进行了广泛研究[8-9]。氧气和双氧水作为清洁、环保的氧化剂,逐渐进入大家的视野。但是上述两种氧化剂存在氧化反应活性不高、催化氧化反应速率较慢等不足,使得无法在氧化安息香中得到广泛应用。为提高氧气及双氧水氧化安息香的活性,一系列安息香催化氧化技术被研究并开发[10-13],其中希夫碱配合物催化氧化安息香就是一种比较重要的催化工艺[14-17]。本研究从绿色化学角度出发,以[M(Salen)](M=Mn, Co, Ni,Cu, Zn)为催化剂,空气为氧化剂,探究并优化了催化氧化安息香合成苯偶酰的反应条件,并对催化剂的回收利用作了研究。研究表明,Mn(Salen)的催化性能最好,以DMF为溶剂,催化剂与原料摩尔比0.06∶1.00,KOH与原料摩尔比0.7∶1.0,室温下反应60 min,苯偶酰的收率可达到80%以上。这些研究显著提高了苯偶酰的收率、室温反应降低了生产成本、扩大其应用范围,使低能耗、绿色化合成苯偶酰成为可能。
1 实验部分
1.1 实验原理
希夫碱合成方程式:

Salen配合物制备方程式:

安息香催化氧化方程式:
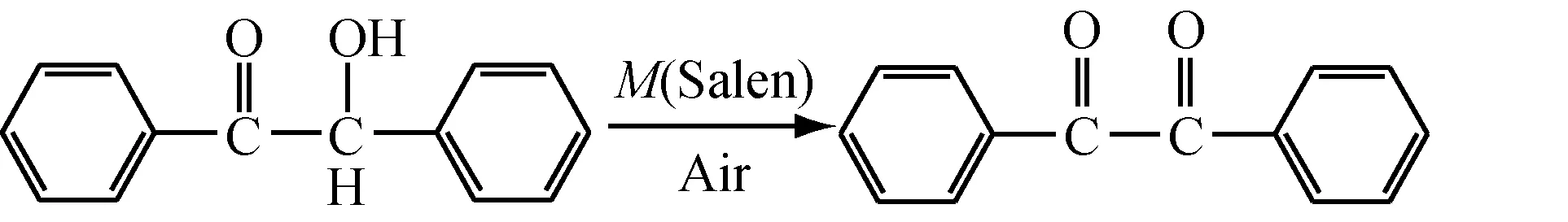
其中:M(Salen)分别为:Co(Salen)、Mn(Salen)、Ni(Salen)、Cu(Salen)和Zn(Salen)。
1.2 仪器与主要试剂
(1) 仪器。熔点测定仪(瑞士BUCHI公司B-545型),红外光谱(美国Thermo公司Nicolet 6700型),核磁共振波谱仪(瑞士Bruker公司ANANCEIII 500M型),质谱(美国VARIAN公司VARIAN1200型),旋转蒸发仪(瑞士BUCHI公司R-205型),真空干燥箱(上海精宏公司DZF-6201型)以及常规有机合成和提纯仪器。
(2) 试剂。安息香(上海安耐吉化学,99%),水杨醛(上海安耐吉化学,98%),乙二胺(上海阿拉丁化学,>99%),四水合乙酸钴(上海安耐吉化学,99%),一水合乙酸铜(II)(上海安耐吉化学,99%),二水合乙酸锌(上海安耐吉化学,99%),四水合乙酸镍(上海安耐吉化学,99%),四水合乙酸锰(上海安耐吉化学,99%),DMF(无锡海项有限公司,分析纯),无水乙醇(安徽安特有限公司,分析纯),氢氧化钾(杭州萧山化学试剂厂,分析纯),无水碳酸钾(杭州萧山化学试剂厂,分析纯),氢氧化钠(杭州萧山化学试剂厂,分析纯),无水碳酸钠(杭州萧山化学试剂厂,分析纯),活性炭(雨蓝科技有限公司),分子筛(上海埃彼)等。
1.3 希夫碱的合成
在50 mL单口圆底烧瓶中,将6.104 8 g(0.05 mol)水杨醛溶于10 mL无水乙醇中,室温水浴搅拌,待混合均匀后开始滴加1.501 9 g(0.025 mol)乙二胺与10 mL乙醇的混合溶液,滴加速度为1滴/5 s,片刻即有亮黄色固体析出。薄层色谱法(TLC)跟踪记录反应进程(展开剂为V环乙烷∶V乙酸乙酯=4∶1)。反应2 h左右,TLC检测水杨醛已完全反应。将产品在冰箱中冷却6 h,抽滤,无水乙醇重结晶,得黄色晶体,50 °C真空干燥6 h,得黄色晶体5.66 g,收率84.5%。M.p.: 127.1~127.4 ℃(文献值127~128 ℃[18]),IR(KBr,νmax, cm-1): 2 899.4(ν=C-H),1 634(ν-C=N),1 450(νPh-H);1H NMR(CDCl3,×10-6),δ: 13.20(s, 2H),8.36(s, 2H),6.8~7.4(m, 8H),3.96(t, 4H);MS(m/z)%: 291.1([M+Na]+), 269.1([M+H]+);13C NMR(CDCl3, ×10-6),δ: 166.45, 160.97, 132.34, 131.44, 118.63, 118.60, 116.90, 59.67。
1.4M(Salen)的合成
以Co(Salen)为例,在500 mL三口瓶中,氮气氛围下将12.074 0 g (0.045 mol)席夫碱配体和11.208 6 g(0.045 mol)四水合乙酸钴溶于320 mL无水乙醇。加热回流8 h,溶液呈深棕色。待粗产品冷却至室温后,置于冰箱中冷却6 h,抽滤,得暗红色固体,采用无水乙醇(100 mL)加热回流,浸渍法洗涤,50 °C下真空干燥6 h,得暗红色晶体18.90 g,收率72.6%。IR(KBr,νmax, cm-1): 2 929.6(ν=C-H),1 605.7(ν-C=N),1 449.0(νPh-H),1 328.7(νPh-O)。
采用相同的方法,分别选取四水合乙酸锰、二水合醋酸锌、一水合乙酸铜(II)、四水合乙酸镍(II) 与希夫碱配合,得到棕色的Mn(Salen)、墨绿色的Cu(Salen)、奶黄色的Zn(Salen)和砖红色的Ni(Salen)。
1.5 安息香催化氧化

1.6 催化剂回收
催化剂回收采用文献中报道的物理吸附方法[20],即在乙醇溶液中分别用活性炭和分子筛做载体进行催化剂M(Salen)吸附。在250 mL三口圆底烧瓶中,将上述0.35 g Co(Salen)催化剂溶于100 mL无水乙醇中,投入4 g活性炭或4 g NaY型分子筛,45 ℃搅拌12.0 h,使其负载在无机载体上,风干,采用同1.5中的方法进行实验,考查其催化活性以及循环利用次数。
2 结果与讨论
2.1 溶剂量对希夫碱合成的影响
分别选用20、30、40、50 mL无水乙醇为溶剂,研究溶剂量对希夫碱合成的影响,结果见表1。

表1 溶剂量对希夫碱合成的影响
上述实验条件:水杨醛6.11 g (0.05 mol),乙二胺1.50 g (0.025 mol),室温下搅拌反应2 h。
从上述实验数据可以看出,收率均在80%以上,收率相差不大。当溶剂量为20 mL时,反应进行一段时间后有大量固体析出,搅拌器无法正常搅拌,影响反应进程。从绿色环保角度考虑,溶剂量选择30 mL。
2.2 催化剂的XRD与XPS表征
Salen配体与金属离子是否成功配合是安息香催化氧化的关键,除红外光谱外,氢谱、碳谱以及质谱较难表征难溶性配合物,所以对所制备配合物进行了XRD与XPS表征,结果如图1~10所示。

图1 Co(Salen) XRD图

图4 Zn(Salen) XPS图

图7 Mn(Salen) XRD图

图10 Ni(Salen) XPS图
从上述表征结果看,所制备5种配合物XRD图对应的峰值与标准图谱一致,同时从XPS图可看出,所合成5种配合物金属离子化学状态均为+2价,结合红外光谱中羟基峰明显消失,可以判定配合物已成功合成。
2.3 催化剂用量对安息香催化氧化反应的影响
在安息香用量为2.10 g(10 mmol)、60 ℃ 搅拌90 min、KOH 0.61 g (11 mmol),DMF为10 mL的条件下反应,探究催化剂用量对安息香催化氧化反应的影响,其结果见表2。
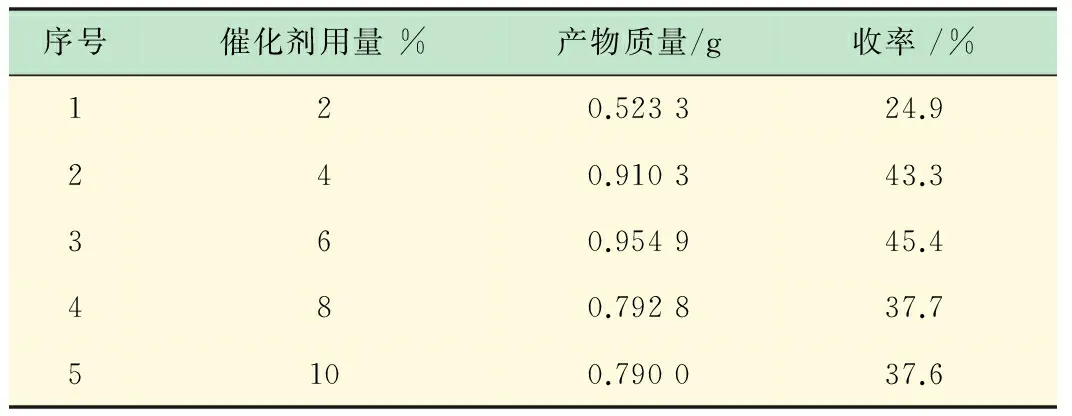
表2 催化剂用量对反应的影响
从上述实验数据可知,催化剂物质的量为原料物质的量6%时收率较高。因此,选取此催化剂用量6%作为安息香催化氧化反应的较佳反应条件。
2.4 反应时间对安息香催化氧化反应的影响
在较佳催化剂用量情况下,分别考察反应时间为30、45、60、75、90 min下的收率,探究反应时间对氧化反应的影响,其结果见表3。
从反应结果来看,反应进行60 min后,产物收率较高,增加反应时间,收率变化不大。为了节省能源,选取反应时间60 min作为安息香催化氧化反应的较佳反应时间。

表3 反应时间对反应的影响
实验条件:安息香2.10 g (10 mmol),KOH 0.61 g (11 mmol),Co(Salen) 0.19 g (0.6 mmol),DMF 10 mL,60 ℃下搅拌
2.5 反应温度对安息香催化氧化反应的影响
在调整后条件下,温度分别选取室温、40、60、80、100 ℃,探究温度对氧化反应的影响,其结果见表4。
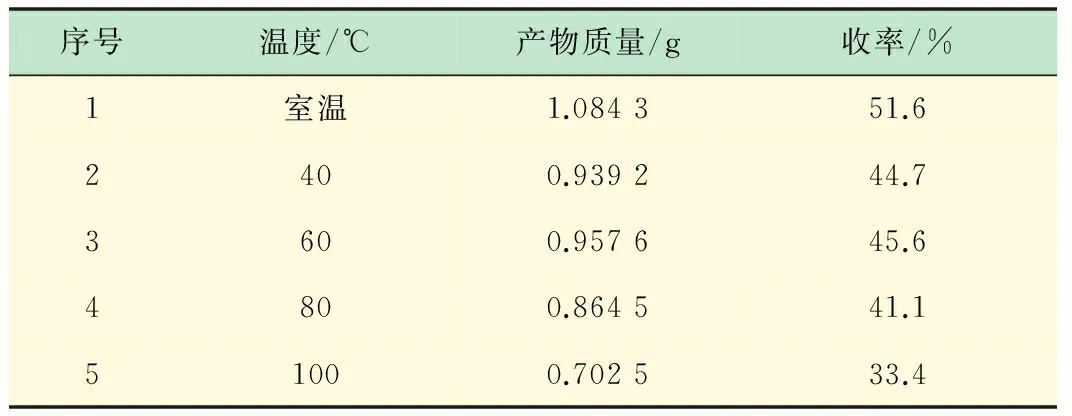
表4 反应温度对反应的影响
实验条件:安息香2.10 g (10 mmol),KOH 0.61 g (11 mmol),Co(Salen) 0.19 g (0.6 mmol),DMF 10 mL,实验温度下搅拌60 min
从上述实验数据可得,室温下即可达到相对较高的收率,而且室温下进行反应使反应条件变得更为简单。因此,选取室温作为安息香催化氧化反应的较佳反应温度。
2.6 碱用量对安息香催化氧化反应的影响
在调整后的条件下,原料与KOH摩尔比分别选取1∶0.3、1∶0.7、1∶1.1、1∶1.5、1∶1.9,探究碱用量对氧化反应的影响,其结果见表5。
上述实验数据可得,当KOH与原料摩尔比为0.3∶1时,产物收率相对较低,增加KOH用量到KOH与原料摩尔比为0.7∶1.0时,收率77.0%,继续增加KOH用量,产品收率开始下降。当碱用量达到1.90 mol时,基本得不到产品,过量KOH会促进副反应(如二醇乙醇酸重排)发生,产品收率下降。因此,选KOH 7 mmol为安息香催化氧化反应的较佳碱用量。

表5 碱用量对反应的影响
实验条件:安息香2.10 g (10 mmol),Co(Salen) 0.19 g (0.6 mmol),DMF 10 mL,室温下搅拌60 min
2.7 溶剂量对安息香催化氧化反应的影响
在调整后的条件下,DMF量分别选取10、15、20、25、30 mL,探究溶剂量对氧化反应的影响,其结果见表6。
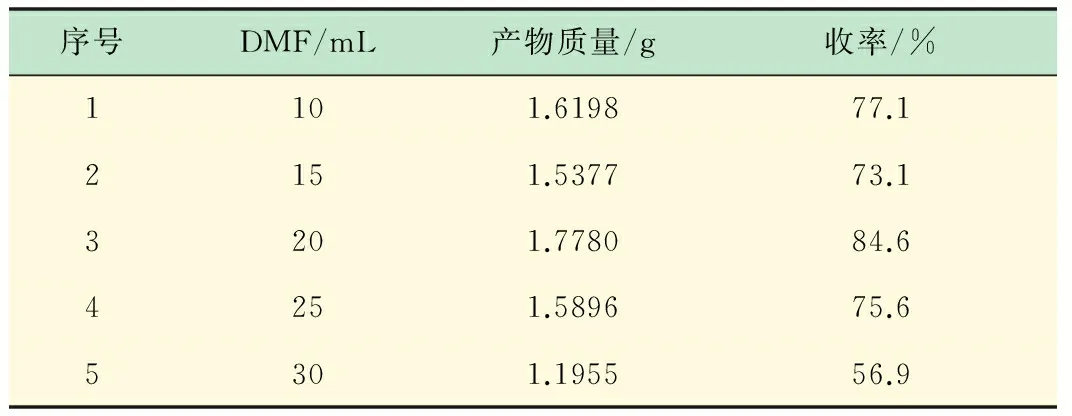
表6 溶剂量对反应的影响
从上述实验数据可得,在DMF为20 mL时,反应收率较高。收率变化的趋势是随着溶剂量的增加先增加后减小,在溶剂较少的时候浓度较大,副反应较多,而当浓度过低时反应未完全进行导致收率较低。因此,选取DMF 20 mL为安息香催化氧化反应的较佳溶剂量。
2.8 碱种类对安息香催化氧化反应的影响
在优化后的条件下,分别选取KOH、NaOH、Na2CO3、K2CO3为碱,探究碱种类对氧化反应的影响,其结果见表7。
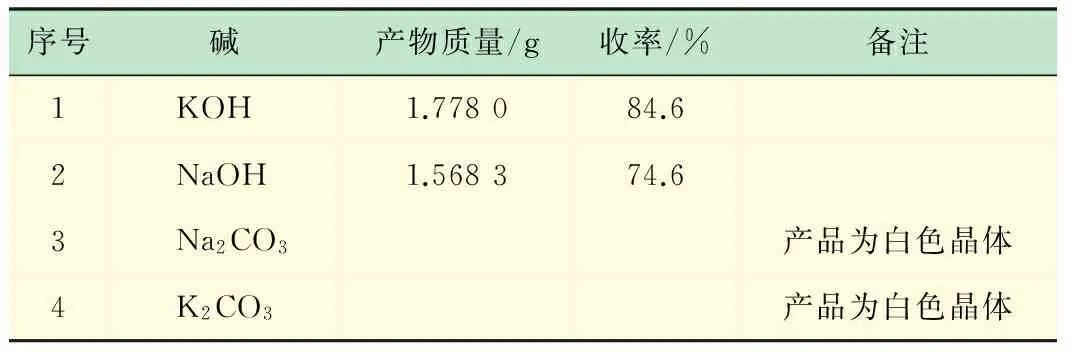
表7 碱种类对反应的影响
实验条件:安息香2.10 g (10 mmol),Co(Salen) 0.19 g (0.6 mmol),DMF 20 mL,室温下搅拌60 min
上述实验数据可得,碱为KOH时收率较高,NaOH的收率低于KOH。根据高效液相色谱谱图分析得到以Na2CO3与K2CO3为碱所得到的白色晶体大部分为原料安息香,即在较佳反应条件下,Na2CO3与K2CO3作为碱,安息香催化氧化效果很差。
2.9 不同Salen配合物对安息香催化氧化反应影响
在优化后的条件下,分别以Co(Salen)、Cu(Salen)等5种配合物为催化剂,探究金属配合物种类对反应的影响,其结果见表8。

表8 不同金属配合物对氧化反应的影响
实验条件:安息香2.10 g (10 mmol),KOH 0.40 g (7 mmol),DMF 20 mL,室温下搅拌60 min
从上述实验数据可以明显看出,Cu(Salen)、Zn(Salen)催化性能较差,而Mn(Salen)与Co(Salen)两者相差不多。除此之外,根据TLC跟踪的结果显示,Ni(Salen)、Cu(Salen)、Zn(Salen)催化氧化反应1 h后安息香未完全反应,而Mn(Salen)催化氧化反应在约45 min时就反应完全。由此可见,对于安息香催化氧化性能而言,Mn(Salen)>Co(Salen)>Ni(Salen)>Cu(Salen)>Zn(Salen)。不难发现,作为同一周期的这5种金属元素,其二价正离子与希夫碱配体形成的Salen配合物的催化性能随着原子序数的增大而减小。
2.10 重复实验结果
根据所得反应较优条件对Co(Salen)催化氧化反应重复3次实验,平均收率83%,其结果见表9。

表9 较优条件下反应的平均收率
实验条件:安息香2.10 g (10 mmol),Co(Salen) 0.19 g (0.6 mmol),KOH 0.40 g (7 mmol),DMF 20 mL,室温下搅拌60 min
由实验结果可看出,在较优条件下,反应平均收率为83%,重复性较好。
2.11 催化剂的回收及重复使用
以吸附有Co(Salen)的活性炭和分子筛作为催化剂,其他条件为较优条件,考察所制备固载化催化剂的重复使用性能,其结果见表10、表11。实验条件:安息香2.10 g (10 mmol),KOH 0.40 g (7 mmol),Co(Salen) 0.19 g (0.6 mmol),DMF 10 mL,室温下搅拌60 min。
从上述实验数据可得,固载在活性炭和分子筛上的催化剂均可以回收重复使用3次,并且保持较高的催化性能,说明用物理吸附法对催化剂回收再利用是切实可行的。
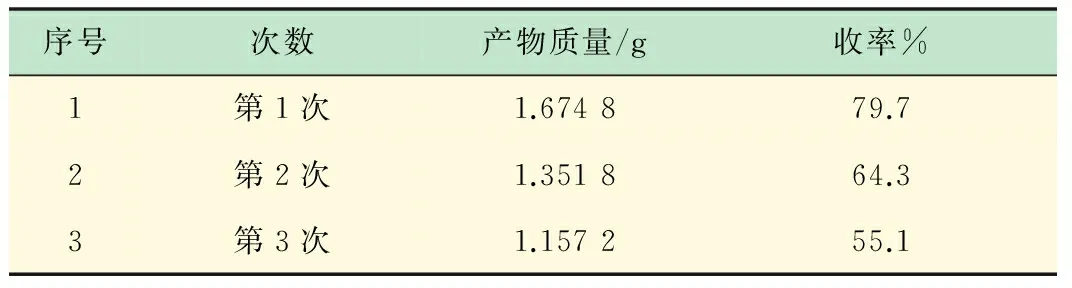
表10 活性炭吸附Co(Salen)的重复使用性能

表11 分子筛吸附Co(Salen)的重复使用性能
3 结 语
本文以水杨醛和乙二胺为原料合成了Salen配体,分别与Co(OAc)2·4H2O,Cu(OAc)2·H2O,Zn(OAc)2·2H2O,Ni(OAc)2·4H2O和Mn(OAc)2·4H2O进行反应得到相应的配合物,并对合成的配合物结构进行了红外光谱、XRD以及XPS表征,表征得金属离子被成功络合,并且金属离子化学价态均为+2价。将所得的Salen配合物催化剂用于安息香催化氧化反应,当2.1 g (10 mmol) 安息香被空气氧化时,以10 mL DMF为溶剂,加入0.19 g (0.6 mmol) Co(Salen) 和0.4 g (7mmol) KOH时,室温下反应60 min,产品的收率最高可达87%,平均收率83%。该方法室温反应,无需加热,节省能源,反应后处理简单,贯彻了绿色化学理念,开辟了合成苯偶酰的新工艺。
[1] 杨 征,白 佳,王小燕,等. 苯偶酰类化合物的合成及应用研究进展[J]. 化学试剂,2011,33(1):33-38.
[2] 田 勇,于伟民,李 猛,等. 苯偶酰的合成[J]. 化学与粘合,2000(4):184-186.
[3] 蔡东亚,牛永生,张贵生,等. 氯铬酸甲铵/硅胶对苯偶姻的氧化研究[J]. 化学试剂,2000,22(4):228-229.
[4] 高 妍,张志强,周袭非,等. 间二氨基苯偶酰的合成[J]. 化学试剂,2005,27(10):627-628.
[5] 黄 玲,陶 清,王冬明,等. 高锰酸钾氧化安息香的实验研究[J]. 应用化工,2013,42(7):1281-1283.
[6] Shaikh M, Sahu M, Gavel P K,etal. Ferrites catalyzed aerobic oxidation of benzoin and its extension to enantioselective version[J]. Catalysis Communications, 2015, 64(5):18-21.
[7] 刘长辉,蒋 颂. 苯偶酰类化合物的合成[J]. 化工时刊,2009,23(5):25-27.
[8] 赵 梅,黄汝琪,李恩霞,等. 安息香氧化反应的研究进展[J]. 山东科学,2013,26(5):29-32.
[9] 刘耀华. 微波辐射下苯偶姻合成苯偶酰的反应[J]. 光谱实验室,2010,27(6):2370-2372.
[10] LI B, WANG J, FU J,etal. Selective liquid phase oxidation of benzoin to benzil over transition metals doped MCM-41 with air[J]. Catalysis Communications, 2008, 9(10): 2000-2002.
[11] Safari J, MansouriKafroudi Z, Zarnegar Z. Co3O4-decorated carbon nanotubes as a novel efficient catalyst in the selective oxidation of benzoins[J]. Comptes Rendus Chimie, 2014, 17(9):958-963.
[12] 李伟宏,周 佳. 活性炭负载CuO催化氧化苯偶姻反应研究[J]. 化学世界,2014,55(10):612-623.
[13] 蔡哲斌,石振贵. Fe2O3/Al2O3催化氧化苯偶姻制备苯偶酰[J]. 有机化学,2002,22(6):446-449.
[14] Venkatachalam G, Raja N, Pandiarajan D,etal. Binuclear ruthenium(Ⅲ) Schiff base complexes bearing N(4)O(4) donors and their catalytic oxidation of alcohols[J]. Spectrochim Acta A Mol Biomol Spectrosc, 2008, 71(3), 884-891.
[15] Afshari M, Gorjizadeh M, Nazari S,etal. Cobalt salophen complex supported on magnetic nanoparticles as an efficient reusable catalyst for oxidation of benzylic alcohols[J]. Oriental Journal of Chemistry, 2013, 29(4): 1523-1530.
[16] 陶 琼,包旭辉,范慧阳,等. Ni(Salen)配合物的合成及其催化性能研究[J]. 广东化工,2015, 42(20): 63-69.
[17] 黄 玲,王冬明,徐金光,等. 苯偶酰的简便合成[J]. 广州化工,2012,40(8):115-116.
[18] 丁 成,倪金平,唐 荣,等. 安息香的绿色催化氧化研究[J]. 浙江工业大学学报,2009,37(5):542-544.
[19] 章思规.精细有机化学品技术手册[M]. 北京: 科学出版社,1991:265.
[20] 彭鸿杰,康战锋,张玉霞,等. 分子氧氧化环己烯负载型催化剂的制备与选择[J]. 河南化工,2007,24(5):13-15.
The Catalytic Oxidation of Benzoin by Salen Complexes at Room Temperature
ZHOUBu-jie,MAOGuo-liang,CHENZhong-hang,FANGHui,YUWen-yan,SHENHai-min
(College of Chemical Engineering, Zhejiang University of Technology, Hangzhou 310014, China)
To overcome the shortcomings in the catalytic oxidation of benzoin to benzils, such as environmental pollution, a cleaning process for catalytic oxidation of benzoin was explored using Salen complexes as catalysts. Five Schiff bases were synthesized from salicylaldehyde and ethylene diamine at room temperature, then [M(Salen)](M=Mn, Co, Ni, Cu, Zn) was synthesized at the presence of metal acetate. The structure of ligands and catalysts were characterized by infrared spectrum (IR), nuclear magnetic resonance (NMR), X-ray diffraction (XRD) and X-ray photoelectron spectroscopy (XPS). The obtained five metal complexes were applied to the oxidation of benzoin to investigated their catalytic properties. The optimum process conditions for the reaction were explored with air as the oxidant and Co(Salen) as a catalyst, and the catalytic performance of other metal Salen complexes and Co(Salen) which was loaded on active carbon or molecular sieve were also explored. It was shown that Mn(Salen) possessed the best catalytic properties. When the catalyst content was 6% of the substance, more than 80% benzil yielded can be reached at room temperature for 60 min with DMF as solvent. When Co(Salen) was adsorbed onto molecular sieve, the catalyst can be recycled for three times. This synthetic strategy possesses advantages such as room temperature reaction, energy-saving, and low costs, which can properly realize the concept of green chemistry, and provide theoretical basis for the clean production of benzils.
Schiff base complexes; benzoin; catalytic oxidation; air; room temperature
2015-11-11
国家自然科学基金项目(21306176);浙江省自然科学基金(LQ14B020002);浙江工业大学科研启动基金(G2817101103);浙江工业大学校自然科学基金(2014XY003)资助项目
周步杰(1995-),男,浙江温州人,本科生,从事化学工程研究。Tel.:15990070837;E-mail:zbujie@163.com
沈海民(1983-),男,河北蔚县人,讲师,主要从事水相仿生催化研究及水相环境污染物快速吸附研究。
Tel.:15988460002;E-mail:haimshen@zjut.edu.cn
O 625.4
A
1006-7167(2016)08-0021-06
