精蛋白生物合成人胰岛素注射液(预混30R)强化治疗初发2型糖尿病的临床研究Δ
2016-12-19周慧敏窦婵婵陈志花郭艺璇吕晓静河北医科大学第一医院石家庄050031
王 郡,周慧敏,董 斌,窦婵婵,陈志花,郭艺璇,吕晓静(河北医科大学第一医院,石家庄 050031)
·药物与临床·
精蛋白生物合成人胰岛素注射液(预混30R)强化治疗初发2型糖尿病的临床研究Δ
王郡*,周慧敏#a,董斌,窦婵婵,陈志花,郭艺璇,吕晓静#b(河北医科大学第一医院,石家庄050031)
目的:探讨精蛋白生物合成人胰岛素注射液(预混30R)(以下简称“诺和灵30R”)强化治疗对初发2型糖尿病患者血糖、糖化血红蛋白(HbA1c)及胰岛B细胞功能等的影响。方法:将68例2型糖尿病初发患者根据随机数字表法分为观察组和对照组,各34例。对照组患者口服阿卡波糖+格列美脲;观察组患者皮下注射诺和灵30R,根据血糖水平调整胰岛素注射剂量及次数。两组患者的血糖控制目标均为空腹血糖(FBG)3.9~7.2 mmol/L、餐后2 h血糖(2 hPG)7.8~10.0 mmol/L。比较两组患者的FBG、2 hPG、HbA1c、血糖达标时间、体质量指数(BMI)和胰岛B细胞功能。结果:治疗前,两组患者的FBG、2 hPG、HbA1c及BMI比较,差异均无统计学意义(P>0.05);治疗后,两组患者的FBG、2 hPG和HbA1c均较治疗前明显降低,且观察组明显低于对照组,血糖达标时间亦明显短于对照组,差异均有统计学意义(P<0.05);两组患者的BMI在治疗前后比较差异无统计学意义(P>0.05)。治疗前,两组患者的胰岛素抵抗指数(HOMA-IR)、胰岛素分泌指数(HOMA-B)、糖负荷后30 min胰岛素净增值与葡萄糖净增值的比值(I30/G30)比较,差异均无统计学意义(P>0.05);治疗后,两组患者的HOMA-IR较治疗前明显降低,HOMA-B和I30/G30较治疗前明显升高,且观察组患者的上述指标明显优于对照组,差异均有统计学意义(P<0.05)。两组患者均未见明显不良反应发生。结论:诺和灵30R强化治疗能够更为有效地降低初发2型糖尿病患者血糖和HbA1c水平,缩短血糖达标时间,改善胰岛B细胞功能,且安全性较好。
精蛋白生物合成人胰岛素注射液(预混30R);初发2型糖尿病;强化治疗;血糖;糖化血红蛋白;胰岛B细胞
2型糖尿病是我国常见的内分泌系统慢性疾病,发病率逐年升高,随之发生的心血管系统、神经系统、肾脏并发症也越来越多见,对患者的生活质量和生命安全均造成严重影响[1]。2型糖尿病最突出的病理生理特征是胰岛素分泌相对不足、外周组织和器官出现胰岛素抵抗,进而造成血糖水平升高[2]。采用胰岛素强化治疗不仅能够控制血糖水平,还能够解除高糖环境的毒性作用,对胰岛B细胞的功能发挥保护和改善作用,有助于长期预防糖尿病慢性并发症的发生[3]。本研究主要探讨了精蛋白生物合成人胰岛素注射液(预混30R)(以下用其商品名“诺和灵30R”作为简称)对初发2型糖尿病患者血糖、糖化血红蛋白及胰岛B细胞功能等的影响。
1 资料与方法
1.1纳入与排除标准
纳入标准:(1)初诊为2型糖尿病,经口服葡萄糖耐量(OGTT)试验确诊为2型糖尿病的患者;(2)空腹血糖(FBG)≥7.8 mmol/L,糖化血红蛋白(HbA1c)≥7.5%;(3)病程≤1年;(4)患者均知情同意并签署知情同意书。
排除标准:(1)糖尿病急性并发症患者;(2)严重心血管疾病与充血性心力衰竭患者;(3)严重肝、肾、心脏疾病的患者;(4)Ⅰ型糖尿病和继发性糖尿病患者;(5)妊娠及哺乳期妇女。
1.2研究对象
本研究方案经医院医学伦理委员会审核批准后,选择2012年5月-2014年9月在我院诊治的初发2型糖尿病患者68例作为研究对象,其中男性44例、女性24例,年龄40~78岁。采用随机数字表法分为观察组和对照组,各34例,两组患者的性别、年龄、病程、体质量指数(BMI)、FBG、餐后2 h血糖(2 hPG)、HbA1c等一般资料比较,差异均无统计学意义(P>0.05),具有可比性,详见表1。
1.3治疗方法
对照组患者给予阿卡波糖和格列美脲口服治疗。阿卡波糖片(商品名:拜唐苹,德国Bayer Vital GmbH,注册证号:H20130906,规格:50 mg)在进第一口餐时口服,开始剂量为50 mg,qd,随后增至50 mg,tid;格列美脲片(商品名:万苏平,江苏万邦生化医药股份有限公司,批准文号:国药准字H20031079,规格:1 mg)餐前口服,开始剂量为1 mg,qd,后期根据血糖监测结果可调整为最高剂量5 mg,qd。观察组患者给予诺和灵30R(丹麦Novo Nordisk A/S,注册证号:国药准字J20120027,规格:400IU/10ml/支)皮下注射,根据血糖水平调整注射剂量及次数,使每日剂量控制在0.3~1.0 IU/kg。两组患者的血糖控制目标均为:FBG 3.9~7.2 mmol/L、2 hPG 7.8~10.0 mmol/L,同时给予必要的饮食指导和运动指导。
1.4观察指标
(1)治疗前后分别采用美国强生稳豪血糖仪检测两组患者的FBG和2 hPG,采用高效液相色谱仪检测HbA1c,并比较两组患者的血糖达标时间和BMI。(2)治疗前后分别采用胰岛素释放试验检测两组患者的空腹胰岛素(FINS),计算胰岛素抵抗指数(HOMA-IR)、胰岛素分泌指数(HOMA-B)和糖负荷后30 min胰岛素净增值与葡萄糖净增值的比值(I30/G30)。HOMA-IR=(FBG×FINS)/22.5;HOMA-B=20×FINS/(FBG-3.5)。(3)观察两组患者的不良反应发生情况。
1.5统计学方法
采用SPSS 21.0软件对数据进行统计分析。计量资料以±s表示,采用t检验;计数资料以例表示,采用χ2检验。P<0.05表示差异有统计学意义。
2 结果
表1 两组患者一般资料比较(±s ,n=34)Tab 1 Comparison of general data between 2 groups(±s,n=34)

表1 两组患者一般资料比较(±s ,n=34)Tab 1 Comparison of general data between 2 groups(±s,n=34)
组别观察组对照组t/χ2P性别,例男21 23>0.258>0.05女BMI,kg/m213 11年龄,岁48.85±5.58 49.10±5.37>0.188>0.05病程,年6.21±0.45 6.18±0.42>0.284>0.05 25.36±3.42 25.11±3.12>0.315>0.05 FBG,mmol/L 10.32±1.41 10.25±1.36>0.208>0.05 2 hPG,mmol/L 16.68±2.21 16.65±2.12>0.057>0.05 HbA1c,% 11.25±1.12 11.22±1.14>0.105>0.05
2.1两组患者血糖达标时间及治疗前后的血糖、HbA1c及BMI比较
治疗后,观察组患者的血糖达标时间为(5.51±0.66)d,对照组患者的血糖达标时间为(9.28±0.97)d,观察组明显短于对照组,差异有统计学意义(P<0.05)。
治疗前,两组患者的FBG、2 hPG、HbA1c及BMI比较,差异均无统计学意义(P>0.05);治疗后,两组患者的FBG、2 hPG和HbA1c均较治疗前明显降低,且观察组患者的FBG、2 hPG和HbA1c均明显低于对照组,差异均有统计学意义(P<0.05);两组患者的BMI在治疗前后比较差异无统计学意义(P>0.05),详见表2。
表2 两组患者治疗前后血糖、HbA1c及BMI比较(±s, n=34)Tab 2 Comparison of blood glucose,HbA1c and BMI between 2 groups before and after treatment(±s ,n=34)

表2 两组患者治疗前后血糖、HbA1c及BMI比较(±s, n=34)Tab 2 Comparison of blood glucose,HbA1c and BMI between 2 groups before and after treatment(±s ,n=34)
注:与治疗前比较,t=9.390~22.088,*P<0.05;与对照组比较,t=4.348~9.121,#P<0.05Note:vs.before treatment,t=9.390-22.088,*P<0.05;vs.control group,t=4.348-9.121,#P<0.05
BMI,kg/m225.11±3.12 25.34±3.25 25.36±3.42 25.01±2.45组别对照组观察组时期治疗前治疗后治疗前治疗后FBG,mmol/L 10.25±1.36 7.65±0.87*10.32±1.41 6.04±0.55*#2 hPG,mmol/L 16.65±2.12 8.86±0.75*16.68±2.21 8.12±0.65*#HbA1c,% 11.22±1.12 8.32±1.02*11.25±1.12 6.54±0.54*#
2.2两组患者治疗前后胰岛B细胞功能比较
治疗前,两组患者的HOMA-IR、HOMA-B和I30/G30比较,差异均无统计学意义(P>0.05);治疗后,两组患者的HOMA-IR较治疗前明显降低,HOMA-B和I30/G30较治疗前明显升高,且观察组患者的HOMA-IR明显低于对照组,HOMA-B和I30/G30明显高于对照组,差异均有统计学意义(P<0.05),详见表3。
表3 两组患者治疗前后胰岛B细胞功能比较(±s ,n=34)Tab 3 Comparison of islet B-cell function between 2 groupsbefore and after treatmen(t±s ,n=34)
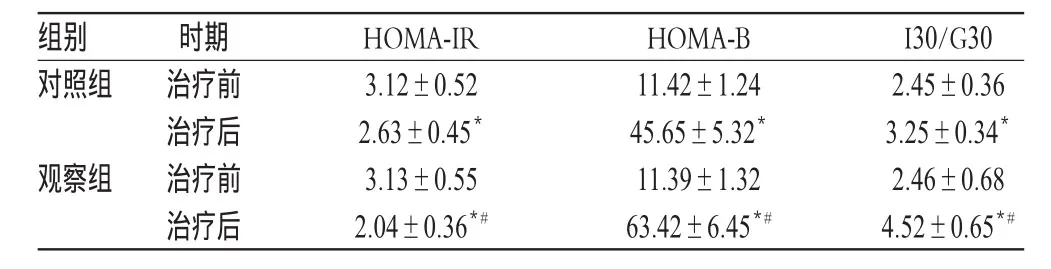
表3 两组患者治疗前后胰岛B细胞功能比较(±s ,n=34)Tab 3 Comparison of islet B-cell function between 2 groupsbefore and after treatmen(t±s ,n=34)
I30/G30 2.45±0.36 3.25±0.34*2.46±0.68 4.52±0.65*#组别对照组观察组时期治疗前治疗后治疗前治疗后HOMA-IR 3.12±0.52 2.63±0.45*3.13±0.55 2.04±0.36*#HOMA-B 11.42±1.24 45.65±5.32*11.39±1.32 63.42±6.45*#
注:与治疗前比较,t=4.155~469.081,*P<0.05;与对照组比较,t=5.970~12.393,#P<0.05
Note:vs.before treatment,t=4.155-469.081,*P<0.05;vs.control group,t=5.970-12.393,#P<0.05
2.3不良反应
两组患者均未见明显不良反应发生。
3 讨论
近年来关于2型糖尿病的研究认为,对于初发的2型糖尿病患者而言,若能尽早给予胰岛素强化治疗,不仅有助于降低血糖水平、解除高糖环境的毒性作用,还能够保护胰岛功能并使其得到部分恢复[4]。国外学者报道,部分初发的2型糖尿病患者在接受胰岛素强化治疗后,仅通过运动干预和饮食控制即可使血糖水平控制在理想范围[5]。在2型糖尿病的初发阶段,胰岛B细胞功能的损伤是可逆的,此时进行胰岛素强化治疗能够减轻胰岛B细胞的负担,使胰岛功能在一定程度上得到改善和恢复,进而在停用胰岛素后的较长时间内继续发挥生理功能,使患者的病情得到长期有效的控制[6]。
胰岛素强化治疗是相对于常规胰岛素治疗而言的。基础胰岛素注射是最常规的糖尿病治疗方案,能够补充胰岛素的基础需要量,但对餐后血糖高峰的控制并不理想[7];联合使用口服降糖药物来控制血糖会进一步加重胰岛负担,内源性胰岛素不断分泌会造成胰岛功能过早衰竭,不利于长期血糖水平的控制[8]。诺和灵30R是胰岛素强化治疗的常用药物,包含30%的中长效胰岛素和70%的短效胰岛素,每日2次或3次给予餐前皮下注射能够有效模拟生理性胰岛素的分泌,不仅能够控制餐后血糖高峰,还能够保持24 h内胰岛素的基础需要量,有助于稳定血糖、减少低血糖事件的发生风险[9]。本研究针对初发2型糖尿病患者制订了诺和灵30R的治疗方案,结果表明,治疗后观察组患者的FBG、2 hPG和HbA1c均明显低于对照组,血糖达标时间明显短于对照组,说明胰岛素强化治疗的降糖效率更高、时效性更强,能够根据患者血糖水平对药物剂量进行精确调整,使患者血糖在较短时间内降至理想水平。
胰岛B细胞功能异常与胰岛素抵抗是诱发2型糖尿病的最基本环节,2型糖尿病患者的胰岛素分泌不足,胰岛B细胞功能减退高达50%,而且随着病程的延长,胰岛B细胞功能将以每年6%~8%的速度下降[10-11]。胰岛素强化治疗最突出的价值在于解除高糖毒性对胰岛B细胞功能的损伤作用,通过外源性补充胰岛素的方式来使胰岛B细胞得到充分休息、内分泌功能尽快恢复,从而有利于血糖水平的长期控制[12]。本研究中,治疗后观察组患者的HOMA-IR明显低于对照组,HOMA-β和I/G30明显高于对照组,提示诺和灵30R有助于改善糖尿病患者的胰岛B细胞功能。
综上所述,诺和灵30R强化治疗能够更为有效地降低初发2型糖尿病患者血糖和HbA1c水平,缩短血糖达标时间,改善胰岛B细胞功能,且安全性较好。本研究的局限性在于样本量较小,且缺乏对患者血糖与HbA1c、胰岛B细胞功能的动态分析,可能会对结论造成偏倚,有待于扩大样本展开进一步研究。
[1]王平,赵蕾,徐锌,等.地特胰岛素联合利拉鲁肽治疗血糖控制不佳2型糖尿病患者的临床观察[J].中国糖尿病杂志,2015,23(6):524.
[2]Giugliano D,Tracz M,Shah S,et al.Initiation and gradual intensification of premixed insulin lispro therapy versus Basal{+/-}mealtime insulin in patients with type 2 diabetes eating light breakfasts[J].Diabetes Care,2014,37(2):372.
[3]陈进,刘秀珍,戴武,等.2种方案治疗口服降糖药无效2型糖尿病的数据包络分析[J].中国药房,2014,25(34):3 169.
[4]刘玉红,李吉生.预混胰岛素类似物强化治疗2型糖尿病临床观察[J].实用糖尿病杂志,2013,9(6):51.
[5]Moghissi E.Management of type 2 diabetes mellitus in older patients:current and emerging treatment options[J]. Diabetes Ther,2013,4(2):239.
[6]张伟,廖琳.2型糖尿病治疗中预混胰岛素类似物剂量调整的探讨[J].中华糖尿病杂志,2015,7(6):398.
[7]Farasiu E,Ivanyi T,Mozejko-Pastewka B,et al.Efficacy and safety of prandial premixed therapy using insulin lispro mix 50/50 3 times daily compared with progressive titration of insulin lispro mix 75/25 or biphasic insulin aspart 70/30 twice daily in patients with type 2 diabetes mellitus:a randomized,16-week,open-label study[J].Clin Ther,2011,33(11):1 682.
[8]王宜文,伍俊妍,姚慧玲,等.胰岛素及其类似物在我院门诊2型糖尿病患者中的使用情况分析[J].中国药房,2013,24(28):2 672.
[9]牛建生,张玲,郝尧,等.预混人胰岛素类似物等剂量3次餐时注射对糖尿病患者强化降血糖的疗效[J].中国老年学杂志,2014,34(15):4 344.
[10]吴胜利,谢爱霞.胰岛素强化治疗对新诊断2型糖尿病胰岛功能的影响[J].新疆医学,2014,44(11):14.
[11]罗惠金,陈容平,杨锐,等.对比沙格列汀、二甲双胍联合罗格列酮三联方案与胰岛素强化方案治疗2型糖尿病患者的有效性及对α、β细胞功能的影响[J].中华内分泌代谢杂志,2015,31(6):515.
[12]Arai K,Takai M,Hirao K,et al.Present status of insulin therapy for type 2 diabetes treated by general practitioners and diabetes specialists in Japan:Third report of a crosssectional survey of 15 652 patients[J].J Diabetes Investig,2012,3(4):396.
(编辑:胡晓霖)
Clinical Study of Isophane Protamine Biosynthetic Human Insulin Injection(Premix 30R)in the Intensive Treatment of Primary Type 2Diabetes
WANG Jun,ZHOU Huimin,DONG Bin,DOU Chanchan,CHEN Zhihua,GUO Yixuan,LYU Xiaojing(The First Hospital of Hebei Medical University,Shijiazhuang 050031,China)
OBJECTIVE:To investigate the effects of intensive treatment of Isophane protamine biosynthetic human insulin injection(premix 30R,called“Novolin 30R”for short)on blood glucose,HbA1c and islet B cell function of patients with primary type 2 diabetes.METHODS:68 patients with primary type 2 diabetes were divided into observation group and control group by random number table method,with 34 cases in each group.Control group1c,the time of blood glucose reaching the standard,BMI and islet B cell function were compared between 2 groups.RESULTS:FBG,2 hPG,HbA1c and BMI of 2 groups had no statistical significance before treatment(P>0.05);compared to before treatment,FBG,2 hPG and HbA1c of 2 groups were decreased significantly after treatment,and observation group were significantly lower than those of control group;the time of blood glucose reaching the standard was significantly shorter than control group,with statistical significance(P<0.05).There was no statistical significance in BMI between 2 groups before and after treatment(P>0.05).Before treatment,HOMA-IR,HOMA-B and I30/G30 of 2 groups had no statistical significance(P>0.05);compared to before treatment,HOMA-IR of 2 groups were decreased significantly,while HOMA-B and I30/ G30 were increased significantly after treatment;the indexes of observation group was significantly better than that of control group with statistical significance(P<0.05).No obvious ADR was found in 2 groups.CONCLUSIONS:Intensive treatment of Novolin 30R can effectively reduce blood glucose and HbA1c levels of patients with primary type 2 diabetes,shorten the time ofblood glucose reaching standard and improve islet B cell function with good safety.
acarbose+glimepiride orally;observation group
Novolin 30R subcutaneously,and the dose and times of injection were adjusted according to blood glucose level. The target fasting blood glucose(FBG)and 2 h postprandial blood glucose(2 hPG)were 3.9-7.2 mmol/L and 7.8-10.0 mmol/L. FBG,2 hPG,HbA
Isophane protamine biosynthetic human insulin injection(premix 30R);Primary type 2 diabetes;Intensive treatment;Blood glucose;Glycated hemoglobin;Islet B cell
R857.3
A
1001-0408(2016)32-4522-03
10.6039/j.issn.1001-0408.2016.32.18
河北省科学技术研究与发展计划项目(No.07276101D-1)
*主管护师。研究方向:内分泌科学。电话:0311-85917201。E-mail:467893122@qq.com
#a通信作者:主任医师,博士。研究方向:内分泌科学。电话:0311-85917203。E-mail:zhouhuimindoctor@163.com
#b通信作者:副主任护师。研究方向:内分泌科学。电话:0311-85917201。E-mail:lvxiaojing2009@sina.com
(2015-12-09
2016-05-25)
