胆固醇基键合相-反相高效液相色谱法测定正辛醇/水分配系数
2016-12-14乔俊琴韩艺源练鸿振
梁 超, 乔俊琴,2, 韩艺源, 练鸿振,2*
(1. 南京大学化学化工学院, 江苏 南京 210023; 2. 南京大学现代分析中心, 江苏 南京 210093)
胆固醇基键合相-反相高效液相色谱法测定正辛醇/水分配系数
梁 超1, 乔俊琴1,2, 韩艺源1, 练鸿振1,2*
(1. 南京大学化学化工学院, 江苏 南京 210023; 2. 南京大学现代分析中心, 江苏 南京 210093)
通过反相高效液相色谱法系统地考察了中性和弱酸性化合物在新型胆固醇基键合相色谱柱(Cholester柱)上的保留行为。以甲醇和乙腈为有机调节剂,建立了保留因子(k)与有机调节剂比例(φ)间的关系,并外推获取100%水相为流动相时的logkw;同时进一步建立并验证了不同流动相下正辛醇/水分配系数的对数(logKow)和logkφ(logkw)间的模型,并预测了部分化合物的logKow。结果表明,使用Cholester柱测定logKow时,甲醇比乙腈更适合作为有机调节剂;对中性化合物和中性状态的酸性化合物,可以用任意甲醇比例下获取的logkφ预测logKow;对存在离解的酸性化合物,依然用外推方式获取的logkw预测logKow。将采用Cholester柱与文献中采用C18柱、C8柱建立的logKow-logkφ模型进行对比,结果表明化合物与胆固醇基键合相存在特别的作用。
反相高效液相色谱;胆固醇基键合相色谱柱;正辛醇/水分配系数
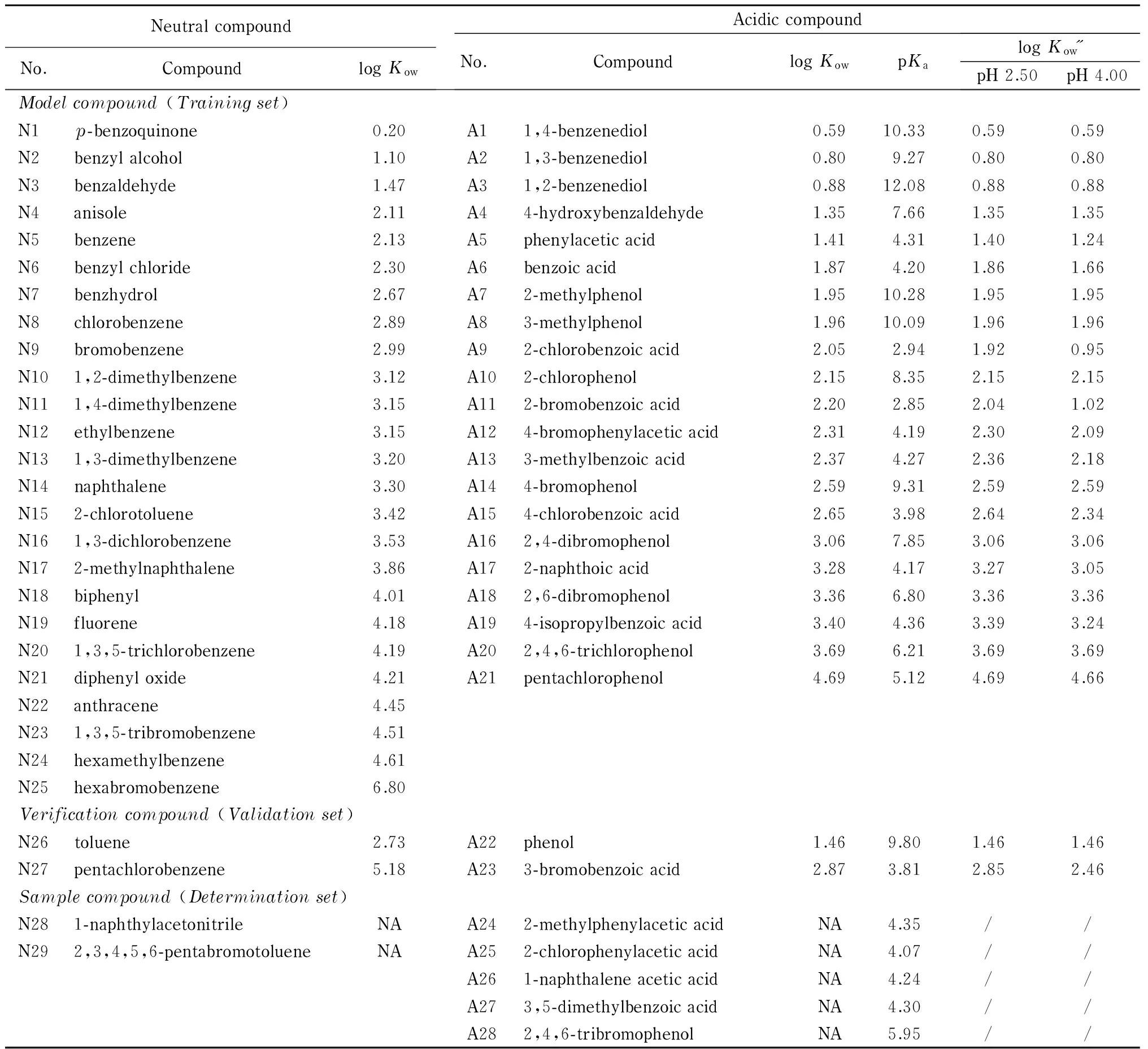
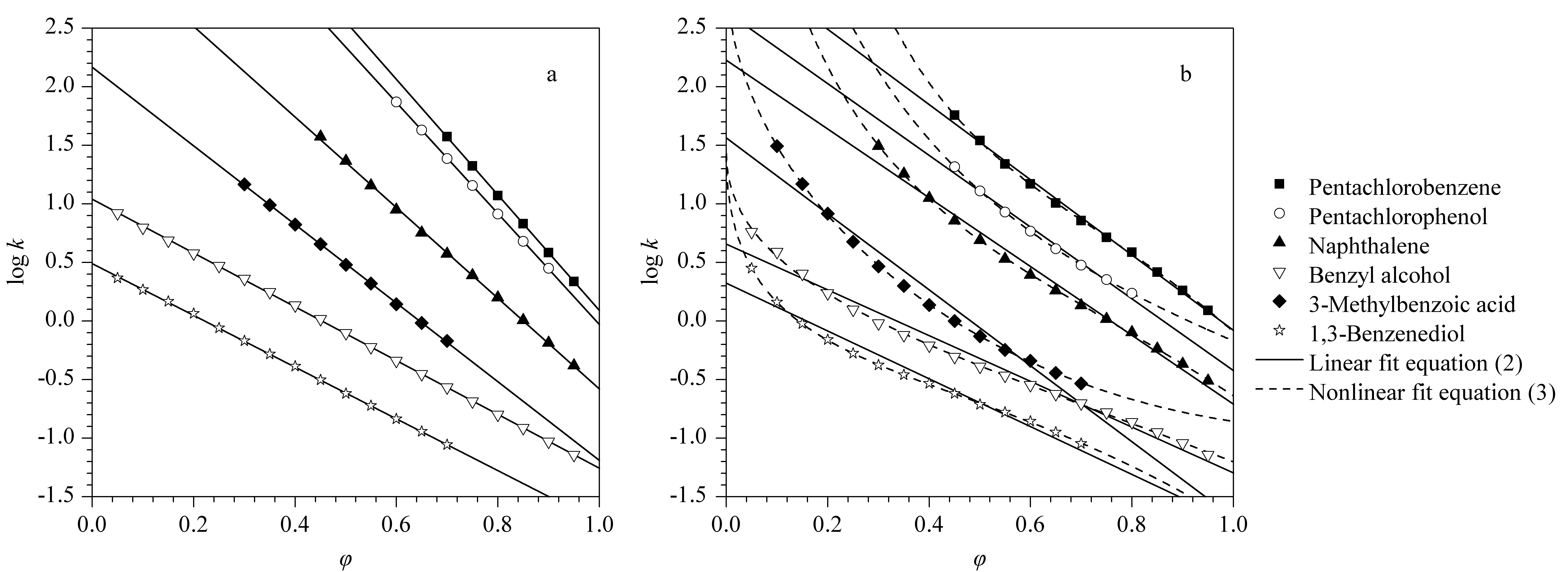
正辛醇/水分配系数(Kow)是表征物质疏水性的重要参数,logKow常用于研究药物在生物体内的吸收、分布、代谢、排泄和毒性(ADMET),在药物设计、环境污染物毒性和定量结构-活性关系(QSAR)的研究中具有重要作用[1,2]。现有logKow的获取途径主要有理论计算法[3]和实验测定法[4-6]。理论计算法更加方便,但准确度较低,随着化合物复杂性的增加,其可靠性逐渐降低,所以在条件允许的情况下应尽量采用实验测定法。经济合作与发展组织(OECD)推荐了3种经典的logKow实验测定方法:摇瓶法(SFM)[4]、慢搅法(SSM)[5]和反相高效液相色谱(RP-HPLC)法[6]。SFM和SSM属于直接测定法,这类方法耗时长,样品用量大且对样品纯度要求高,只适于测定-2 一些课题组开发了多种梯度洗脱测定logKow的方法[8-12],但这些方法的准确度较低,且与等度洗脱法间缺乏系统的比较。等度洗脱法的研究目前主要围绕实验中流动相的选择和新型固定相的应用。流动相方面:在测定离解化合物时,高氯酸、乙酸、氨水等简单酸/碱化合物可代替缓冲盐作为离子抑制剂,大部分基于简单酸/碱化合物的流动相与质谱检测仪兼容,使无紫外吸收化合物的logKow的测定成为可能[13-16];由于硅胶基质色谱柱上残留的硅羟基会影响离解化合物,尤其是碱性离解化合物的保留行为,因此将三乙胺、正癸胺、正辛醇等物质作为硅羟基“掩蔽剂”加入流动相中,“掩蔽剂”的加入对离解化合物的logKow的测定有一定改善[17]。固定相方面:一些不含硅羟基的新型聚合物色谱柱用来测定离解化合物的logKow[7];一些烷基上嵌有氨基(-NH2)和苯基(-Ph)的非单纯烷基键合相色谱柱也可用来预测logKow,这类色谱柱由于存在π-π、氢键等非疏水作用力,预测logKow时往往需要在保留模型中引入修正项以改善模型的相关性,而修正项的加入又会带来新的误差[18]。 图 1 胆固醇键合相的化学结构Fig. 1 Chemical structure of cholesteryl-bonded phase 将胆固醇基(cholesteryl)与硅胶进行化学结合(见图1),制备具有高性能的反相Cholester色谱固定相,其主要作用力及使用的流动相和C18柱相同,但因胆固醇基存在立体刚性结构而与C18柱的保留行为不同。Cholester柱已成功用于番茄红素[19]和类固醇激素[20]等具有立体结构的化合物的分离。但目前关于Cholester柱保留行为的研究很少,有文献[21]指出,用Cholester柱可以直接建立任意有机调节剂比例(φ)下logKow-logkφ的关系来预测logKow,从而节约实验时间,但未给出logKow-logkφ和logKow-logkw关系的比较。目前只有硅胶基质的商品化Cholester柱,其pH适用范围为2~8,不适于碱性化合物的分析。Janicka等[22]用Cholester柱测定logKow时选择乙腈为有机调节剂,建立logk-φ线性模型来获取logkw,但其仅测定了φ在0.40~0.60范围内的logk,并不能反映全乙腈比例范围下logk-φ的真实趋势。本实验分别以甲醇和乙腈为有机调节剂,磷酸缓冲盐为离子抑制剂,系统地研究了采用胆固醇基键合相-RP-HPLC法时,29种中性化合物和28种弱酸性化合物的保留行为,并比较了logKow-logkφ和logKow-logkw的线性关系。 RP-HPLC法利用色谱系统模拟正辛醇/水分配体系,求得化合物的logKow值[7]: log \%K\%ow=\%a\%log \%k\%+\%b\% (1) 其中,a和b为拟合系数。此方程称为Collander方程,是RP-HPLC法测定化合物Kow的基础。研究表明,通过线性溶剂强度模型[23]外推得到100%水相中k的对数值(logkw)与logKow有更好的相关性[7]: log \%k\%=log \%k\%w-\%S\%φ (2) logKowand pKavalues were literature values obtained from the database module of ACD/Labs software; logKow″ values were calculated with logKowand pKa; NA: no literature logKowvalue available; /: not applicable. 2.1 仪器、试剂与材料 Alliance 2695高效液相色谱仪,配有真空脱气机、数码四元泵和120位自动进样器、996紫外-可见二极管阵列(PDA)检测器(美国Waters公司); SevenMulti型pH/电导率/离子综合测试仪,配有Mettler Toledo Inlab®413 pH电极、参比溶液为pH 2.00和pH 7.01的缓冲溶液(瑞士Mettler-Toledo公司)。流动相pH值为加入有机调节剂前水相缓冲液的pH值。 甲醇和乙腈(HPLC级,美国Honeywell公司);磷酸(纯度≥85.0%,国药集团化学试剂有限公司);磷酸二氢钾(KH2PO4,纯度≥99.5%,南京化学试剂有限公司)。实验用水均为娃哈哈纯净水(杭州娃哈哈集团)。实验所用29种中性化合物(苯系物)和28种酸性化合物(苯甲酸、苯酚类)的具体信息见表1,其纯度均大于98%,分别购自美国AccuStandard公司、美国Acros公司、美国Sigma-Aldrich公司、日本TCI公司、国药集团化学试剂有限公司和北京百灵威公司,用甲醇分别配制质量浓度为1 g/L的标准工作溶液,于4 ℃冰箱中储存,待用。实验中,将目标分析物分为3组:模型化合物组(training set)、验证化合物组(validation set)及待测化合物组(determination set)。 2.2 色谱条件 色谱柱:Cosmosil Cholester柱(150 mm×2.0 mm, 5 μm,日本Nacalai Tesque公司);柱温:30 ℃;等度洗脱;流速:0.2 mL/min;进样体积:1 μL;进样浓度:50 mg/L。流动相:①甲醇-水;②甲醇-20 mmol/LKH2PO4缓冲液(以下简称缓冲液A, pH 2.5); ③甲醇-缓冲液A(pH 4.0); ④乙腈-水;⑤乙腈-缓冲液A(pH 2.5); ⑥乙腈-缓冲液A(pH 4.0)。水相为100%水时测定中性化合物;水相为缓冲液A时测定酸性化合物。检测波长为各物质的最大吸收波长,所有样品的tR均为至少3次独立进样的平均值。 图 2 化合物在(a)甲醇和(b)乙腈为有机调节剂时的log k-φ关系(pH 2.5)Fig. 2 Relationships between log k and φ of compounds with (a) methanol and (b) acetonitrile as organic modifiers (pH 2.5) 2.3 实验方法 在不同流动相条件下,根据样品的疏水性,每个样品至少在4个不同φ(0.95~0.05,每隔0.05取一个比例)下测定tR。tR使用双点校正法(DP-RTC)[25]进行校正。保留因子按公式k=(tR-t0)/t0计算,其中t0为死时间,用尿嘧啶测定。建立各物质的logk-φ关系,并外推至100%水相,得到logkw。 采用Origin 9.0 (美国Origin Lab公司)对拟合模型进行统计分析。 3.1 建立logk-φ模型外推logkw 建立logk-φ模型外推logkw是经典RP-HPLC法测定logKow的基础。目前鲜有文献报道采用Cholester柱时化合物logk-φ的关系,因此需大量实验获取数据点,以推断logk-φ关系。甲醇和乙腈为有机调节剂时,6种不同疏水性的中性和弱酸性化合物的logk-φ关系见图2,其中弱酸性化合物为pH 2.5条件下的数据。甲醇为有机调节剂时,logk-φ在较宽的φ范围(0.05~0.95)内线性关系良好;当乙腈为有机调节剂时,logk-φ在较宽φ范围内呈曲线关系。Shoenmakers提出一种描述logk-φ关系的非线性模型[26]: (4) 由图2可知,同一个化合物在甲醇和乙腈两种有机调节剂下外推获得的logkw存在较大差异。理论上,100%水相条件的logkw与有机调节剂无关,两种有机相体系外推logkw值的不同主要来自于拟合模型的不同。在100%水相条件下,样品的tR较长且不稳定,因此logkw无法通过实验获得。 图 4 中性化合物和酸性化合物在甲醇或乙腈体系中的log Kow (log Kow″)-log kφ关系Fig. 4 Relationships of log Kow (log Kow″)-log kφ for neutral compounds and acidic compounds with methanol or acetonitrile as organic modifierMeOH: methanol; ACN: acetonitrile. 甲醇为有机调节剂时,化合物的logk-φ存在良好的线性关系,根据方程(2)预测的logkw可能更接近实际值;乙腈为有机调节剂时,logk-φ若用方程(2)进行直线拟合,得到的logkw小于实际值,用方程(4)进行非线性拟合时,相关性得到较大提高,但获得的logkw却大于实际值。进一步考察了乙腈条件下的logk-φ非线性模型,以苯甲醇(N2)为例,分别用3种乙腈范围(0.05~0.95,0.40~0.95和0.05~0.40)的数据建立logk-φ非线性模型(见图3),得到的结果并不相同。用高比例(0.40~0.95)/低比例(0.05~0.40)条件下得到的非线性模型预测低/高比例的logk均与实验值有差距。因此,在使用Cholester柱时,不适合用非线性模型预测logkw。 图 3 苯甲醇在不同乙腈范围的log k-φ非线性模型Fig. 3 Nonlinear models of log k-φ from different acetonitrile ranges for benzyl alcohol a. 0.05-0.95; b. 0.40-0.95; c. 0.05-0.40; nonlinear models were fitted with black spots. 3.2 logKow(logKow″)-logkφ模型的建立 根据以下公式计算酸性化合物的logKow″: logKow″=logKow-log(1+10pH-p\%K\%a) (5) 部分logKow(logKow″)-logkφ的线性关系见图4。不同流动相下中性和酸性化合物的logKow(logKow″)-logkφ关系见表2。 表 2 不同流动相条件下中性和酸性化合物log Kow (log Kow″)-log kφ的线性关系 * logkwobtained from equation (2); # logkwobtained from equation (4);N: the number of compounds investigated; S.E.: the standard error; adj.R2: the adjusted squared correlation coefficient; SD: standard deviation;F: the Fisher’s test value. 当甲醇为有机调节剂时,中性化合物和酸性化合物外推所得的logkw与logKow(logKow″)建立的logKow(logKow″)-logkw线性关系良好(R2约为0.98),而在任意甲醇比例下建立的logKow(logKow″)-logkφ线性关系均不如logKow(logKow″)-logkw。在pH4.0时,部分酸性化合物建立的logKow(logKow″)-logkφ中的R2为0.91~0.93。对中性化合物及pH 2.5条件下离解已基本被抑制的弱酸性化合物,logKow(logKow″)-logkφ线性关系尚可(R2>0.94)。疏水性不同的物质适用φ的范围不 同,所以只有疏水性差异不大的化合物可以建立某一甲醇比例下的logKow(logKow″)-logkφ模型。本课题组曾证明结构类似的中性和酸/碱化合物可以一起作为模型化合物建立logKow″-logkw模型[28,29]。甲醇条件下中性和酸性混合化合物组的logKow″-logkw线性关系中斜率接近1、截距为常数,与使用C18柱时的结果一致[28,29]。 当乙腈为有机调节剂时,无论通过线性模型还是非线性模型获取的logkw,其误差均比甲醇体系大,因而logKow(logKow″)-logkw线性关系比甲醇体系差。而在任意乙腈比例下建立的logKow(logKow″)-logkφ线性关系总体上优于logKow(logKow″)-logkw,因此如果选择乙腈为有机调节剂,则不需外推获取logkw。 表 3 log Kow (log Kow″)-log kφ模型的验证 * logKowvalues were literature values obtained from the database module of ACD/Labs software; Error=logKowcalculated in this work-logKow*. 3.3 logKow(logKow″)-logkφ模型的验证 为测试3.2节所建立模型的可靠性,分别选择了2种中性化合物(甲苯(N26)、五氯苯(N27))和2种酸性化合物(苯酚(A22)、间溴苯甲酸(A23))进行验证。采用甲醇-水、乙腈-水体系建立的中性化合物logKow-logkφ模型计算N26和N27的logKow;采用甲醇/乙腈-缓冲液A(pH 2.5和4.0)为流动相下建立的弱酸性化合物logKow″-logkφ模型计算A22和A23的logKow″,根据方程(5)反推得到logKow。通过本实验模型得到的logKow与文献报道进行比较,结果见表3。对中性化合物,无论甲醇还是乙腈做有机调节剂,任意比例下建立的logKow-logkφ模型均可得到较为准确的logKow,无需外推logkw;对酸性化合物,利用在甲醇体系中的logKow″-logkφ模型计算得到logKow比乙腈体系更准确。3.4logKow的测定 用甲醇-水流动相体系建立的logKow-logkφ模型测定1-萘乙腈和五溴甲苯的logKow,用甲醇-缓冲液A(pH 2.5和4.0)流动相体系建立的logKow″-logkφ模型测定邻甲基苯乙酸、邻氯苯乙酸、1-萘乙酸、3,5-二甲基苯甲酸和2,4,6-三溴酚的logKow(见表4)。本实验得到的logKow与计算值接近,但化合物越复杂,计算值的误差越大,如五溴甲苯和2,4,6-三溴酚。 表 4 样品化合物log Kow的测定 * logKowwas calculated by Advanced Chemistry Development (ACD/Labs) Software V11.02 (1994-2012 ACD/Labs). 表 5 不同色谱柱上中性和酸性化合物log Kow (log Kow″)-log kφ线性关系比较 PCBs: polychlorinated biphenyls; PBDEs: polybrominated diphenyl ethers; PCDDs: polychlorinated dibenzodioxins;N, S.E., adj.R2, SD andFare the same as in Table 2. 3.5 Cholester柱、C18柱、C8柱logKow(logKow″)-logkφ模型的对比 OECD标准方法规定,将甲醇作为测定logKow的有机调节剂,因此比较本实验甲醇体系中使用Cholester柱和前期工作中使用C18柱和C8柱时获取的logKow(logKow″)-logkφ模型[17,29,30](见表5)。由表5可知,在3种色谱柱上,无论是中性化合物还是酸性化合物外推至100%水相的logkw总是比任意φ下的logkφ与logKow(logKow″)的相关性好。使用logkw预测logKow时,Cholester柱和C18柱、C8柱基本没有区别(R2>0.97)。而使用logkφ预测logKow时,Cholester柱与C18柱、C8柱的结果不同,对中性化合物,Cholester柱获得的logkφ与logKow的相关性明显优于C18柱和C8柱;对酸性化合物,Cholester柱与C18柱获得的logkφ与logKow″的相关性差距不大,但当酸性化合物存在部分离解时,C18柱的logKow″-logkφ相关性优于Cholester柱。说明化合物与胆固醇基和C18、C8的作用存在差异,值得后续进一步研究。 本文系统地考察了新型Cholester柱用于RP-HPLC法测定logKow的可行性。用Cholester柱测定logKow时,甲醇比乙腈更适合作为有机调节剂。对中性化合物和中性状态的酸性化合物,可以直接用任意甲醇比例下获取的logkφ预测logKow;而对存在离解的酸性化合物,为获得更加可靠的logKow数据,依然推荐用外推方式获取的logkw预测logKow。作为一种新型键合相柱,化合物在Cholester柱上展现出与C18柱不同的保留行为,仍值得后续进一步研究。 [1] Mazak K, Noszal B. Eur J Pharm Sci, 2014, 62: 96 [2] Pham-The H, Gonzalez-Alvarez I, Bermejo M, et al. Mol Inf, 2013, 32(5/6): 459 [3] Pallicer J M, Rosés M, Ràfols C, et al. ADMET & DMPK, 2014, 2(2): 107 [4] OECD Guideline for Testing of Chemicals, No. 107 Partition Coefficient (n-Octanol/Water): Shake Flask Method, 1995 [5] OECD Guideline for Testing of Chemicals, No. 123 Partition Coefficient (n-Octanol/Water): Slow-Stirring Method, 2006 [6] OECD Guideline for Testing of Chemicals, No. 117 Partition Coefficient (n-Octanol/Water), High Performance Liquid Chromatography (HPLC) Method, 2004 [7] Liang C, Lian H Z. TrAC-Trends Anal Chem, 2015, 68: 28 [8] Valko K, Bevan C, Reynolds D. Anal Chem, 1997, 69(11): 2022 [9] Krass J D, Jastorff B, Genieser H G. Anal Chem, 1997, 69(13): 2575 [10] Donovan S F, Pescatore M C. J Chromatogr A, 2002, 952(1/2): 47 [11] Kubik L, Struck-Lewicka W, Kaliszan R, et al. J Chromatogr A, 2015, 1416: 31 [12] Wiczling P, Struck-Lewicka W, Kubik L, et al. J Pharm Biomed Anal, 2014, 94: 180 [13] Ming X, Han S Y, Qi Z C, et al. Talanta, 2009, 79(3): 752 [14] Han S Y, Ming X, Qi Z C, et al. Anal Bioanal Chem, 2010, 398(6): 2731 [15] Han S Y, Liang C, Zou K, et al. Talanta, 2012, 101: 64 [16] Qi Z C, Han S Y, Wu Z Y, et al. Cur Anal Chem, 2014, 10: 172 [17] Han S Y, Liang C, Yu H M, et al. RSC Adv, 2015, 5: 28840 [18] Yamagami C, Kawase K, Fujita T. Quant Struct-Act Relat, 1999, 18(1): 26 [19] Zhang L F, Zhang H W. Journal of Food Science and Biotechnology, 2010, 29(5): 698 张连富, 张环伟. 食品与生物技术学报, 2010, 29(5): 698 [20] Soukup J, Bocian S, Jandera P, et al. J Sep Sci, 2014, 37(4): 345 [21] Janicka M, Pachuta-Stec A. J Sep Sci, 2014, 37(12): 1419 [22] Janicka M, Sztanke M, Sztanke K. J Chromatogr A, 2013, 1318: 92 [23] Snyder L R, Dolan J W, Gant J R. J Chromatogr A, 1979, 165(1): 3 [24] Zou H F, Zhang Y K, Hong M F, et al. J Chromatogr A, 1992, 625(2): 169 [25] Han S Y, Qiao J Q, Zhang Y Y, et al. Chemosphere, 2011, 83(2): 131 [26] Schoenmakers P J, Billiet H A H, de Galan L. J Chromatogr A, 1983, 282: 107 [27] Hsieh M M, Dorsey J G. J Chromatogr A, 1993, 631(1/2): 63 [28] Han S Y, Qiao J Q, Zhang Y Y, et al. Talanta, 2012, 97: 355 [29] Liang C, Han S Y, Qiao J Q, et al. J Sep Sci, 2014, 37(22): 3226 [30] Liang C, Qiao J Q, Ge X, et al. Chinese Journal of Chromatography, 2014, 32(6): 426 梁超, 乔俊琴, 葛欣, 等. 色谱, 2014, 32(6): 426 Determination of n-octanol/water partition coefficient by reversed-phase high performance liquid chromatography with cholesteryl-bonded phase LIANGChao1,QIAOJunqin1,2,HANYiyuan1,LIANHongzhen1,2* (1. School of Chemistry & Chemical Engineering, Nanjing University, Nanjing 210023, China;2. Center of Modern Analysis, Nanjing University, Nanjing 210093, China) Retention behaviors of neutral and weak acidic compounds were studied systematically on a novel cholesteryl-bonded phase column. The relationships between retention factor (k) with volume fraction of organic modifier (φ) were established for each compound with methanol and acetonitrile as organic modifiers. The values of logkwcorresponding to 100% water as mobile phase were obtained by extrapolating procedure. Models of the logarithm ofn-octanol/water partition coefficient (logKow) versus logkφ(logkw)withdifferentmobilephaseswereestablished.Thevaluesoflogkwofsomecompoundswerepredictedwithvalidatedmodels.TheresultsindicatedthatmethanolasorganicmodifierwasmoresuitablefordeterminationoflogKowwithcholestercolumnsthanacetonitrile.Forneutraloracidiccompoundsinneutralforms,thevaluesoflogkwcouldbepredictedwithlogkφfrom mobile phases with any volume fraction of methanol; for acidic compounds ionized in the mobile phases, the values of logkwwere predicted with the extrapolated logkwvalues. Comparison of logKow-logkφmodelsestablishedoncholestercolumnsinthisworkwiththoseestablishedonC18andC8columnsfromthe indicatedthatitexistsspecialinteractionsbetweencompoundsandthecholesteryl-bondedphase,whichdeservesfurtherstudy. reversed-phasehighperformanceliquidchromatography(RP-HPLC);cholesteryl-bondedchromatographiccolumns; n-octanol/waterpartitioncoefficient(Kow) 10.3724/SP.J.1123.2016.09002 2016-08-31 国家自然科学基金(21275069,21577057). Foundation item:National Natural Science Foundation of China (Nos. 21275069, 21577057). O A 邹汉法研究员纪念专辑(上)·研究论文 * 通讯联系人.Tel:(025)83685941,E-mail:hzlian@nju.edu.cn.
1 理论部分
2 实验部分
3 结果与讨论







4 结论
