蛹虫草发酵大米的成分分析及体外抗氧化活性研究
2016-12-09朱振元贾长英孙会轻
朱振元,贾长英,孙会轻
(天津科技大学食品工程与生物技术学院,天津 300457)
蛹虫草发酵大米的成分分析及体外抗氧化活性研究
朱振元,贾长英,孙会轻
(天津科技大学食品工程与生物技术学院,天津 300457)

虫草米,水溶性非淀粉多糖,体外抗氧化,清除自由基
蛹虫草(Cordycepsmilitaris)又名北冬虫夏草,是我国传统的中药材之一。属子囊菌门、子囊菌纲、肉座菌目、麦角菌科、虫草属[1]。蛹虫草有虫草素[2]、虫草酸[3]、虫草多糖、超氧化物歧化酶(SOD)[4]等多种活性物质,具有延缓衰老[5]、抗肿瘤[6]、提高免疫力[7]、改善肾脏功能等作用。从2009年开始,蛹虫草被批准成为新资源食品进而被广泛应用于功能食品的研发[8],如蛹虫草保健黄酒[9]、蛹虫草保健茶饮料[10]、蛹虫草功能性酱油[11]等。朴美子等[12]研究发酵虫草米,即利用固态发酵技术,将虫草菌丝体加入大米,经发酵得到含有虫草功能性成分的虫草米,并证明其具有一定免疫活性。但已有研究中对于虫草米是否具有其它活性未有报道。
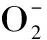
1 材料与方法
1.1 材料与仪器
大米 市售;蛹虫草菌株 实验室保存;甘露醇、虫草素、DPPH、三羟甲基氨基甲烷(Tris)均为分析纯,购于sigma公司;高碘酸钠、乙酸胺、冰醋酸、乙酰丙酮、L-鼠李糖、铁氰化钾、三氯乙酸、氯化铁、硫酸亚铁、水杨酸、双氧水、邻苯三酚、无水乙醇等试剂 均为分析纯,购于天津北方天医化学试剂厂。
GHX-9160B-1型隔水式恒温培养箱 上海福玛实验设备有限公司;LS-B50L型立式压力蒸汽灭菌器 上海华线医用核子仪器有限公司;超净工作台 苏净集团安泰公司;ESJ2054型电子分析天平 沈阳龙腾电子称量仪器有限公司;KQ-400KDB超声波清洗仪 昆山市超声仪器有限公司;TDL-5-A离心机 上海安亭科学仪器公司;Agilent 1260型高效液相色谱仪 美国安捷伦公司;SP-2102紫外分光光度计 上海光谱仪器有限公司。
1.2 蛹虫草液体培养基的制备
液体培养基:葡萄糖4%,蛋白胨1%,KH2PO40.1%,MgSO40.1%,121 ℃灭菌25 min,备用;在无菌操作台上,用接种针取1 mm2大小的蛹虫草菌置于液体培养基,培养温度25 ℃,摇床转速150 r/min培养3 d。
1.3 大米发酵培养
取30 g大米装入三角瓶,以料液比1∶1.2加水,121 ℃,灭菌25 min得大米培养基,以20 mL/100 g接种量加种子液,搅拌均匀,于22 ℃黑暗发酵9 d,再经过光照转色,每天光照12 h,一周后干燥处理。
1.4 营养和功能性成分测定
1.4.1 虫草米中虫草素含量测定 取虫草米粉0.50 g,溶于30 mL蒸馏水中,超声提取30 min,4000 r/min离心10 min,取上清液于50 ℃条件下旋转蒸发1 h得待测样。采用高效液相色谱法测定虫草素含量[13]。
1.4.2 虫草米中虫草酸含量测定 取虫草米粉0.50 g,置于50 mL三角烧瓶中,加25 mL蒸馏水,80 ℃水浴1 h,离心,将上清液转移至50 mL容量瓶中,残渣重复提取一次,定容,备用。采用比色法测定虫草酸含量[14]。
1.4.3 水溶性非淀粉多糖(SNSP)含量测定 虫草米粉碎,按料液比1∶20加蒸馏水,80 ℃水浴2 h,4000 r/min离心10 min,收集上清液,重复三次,合并提取液,浓缩,得虫草米提取液;以同种方法得普通大米提取液。
分别在虫草米、大米提取液中加入50 IU/gα-淀粉酶,于95 ℃酶解15 min后冷却至60 ℃,再按100 IU/g的添加量添加糖化酶,于60 ℃保温1 h后冷却、定容并离心。上清液加入5倍体积的无水乙醇,于4 ℃静置过夜后离心,得到的沉淀用80%乙醇洗涤,重复3次。待挥干试剂后,沉淀用蒸馏水(50±1) ℃溶解,定容,得多糖溶液。采用苯酚-硫酸法测定多糖含量,以葡萄糖为标准(用0.9的系数校正)[15]。
1.4.4 淀粉含量测定 参照GB/T 5009.9-2008食品中淀粉的测定酶水解法。
1.5 抗氧化活性测定
1.5.1 样品处理 虫草米粉碎,按料液比1∶20加蒸馏水,60 ℃超声2 h,提取三次,合并提取液,浓缩,得到浓度分别为1、2、3、4、5 mg/mL虫草米提取液;以同种方法得普通大米提取液。
1.5.2 还原能力的测定 本实验参考Oyaizu方法[16]并稍改动。将1 mL样品加入到pH为6.6的2.5 mL磷酸缓冲液(0.2 mol·L-1)中,加质量分数为1%的铁氰化钾溶液2.5 mL,混合物于50 ℃水浴20 min。然后加入质量分数为10%的三氯乙酸2.5 mL,混合物4000 r·min-1离心10 min,吸取2.5 mL上清液,加入2.5 mL蒸馏水,再加入0.5 mL质量分数为0.1%的氯化铁溶液,混匀静置10 min,以VC为阳性对照,在700 nm波长下测吸光度,以吸光度表示还原能力。
式中:A0为空白对照液的吸光值;Ax为样品液吸光值。
1.5.4 羟自由基(·OH)清除率测定 由Fenton法产生·OH[18]。在试管中依次加入9 mmol·L-1FeSO42 mL,9 mmol·L-1水杨酸-乙醇溶液2 mL,待测液2 mL,8.8 mmol·L-1H2O22 mL,其中H2O2启动整个反应。37 ℃反应30 min后,以蒸馏水为空白调零,在510 nm处测样品吸光度,以维生素C做阳性对照,同时设空白对照。
式中:Ax为样品液清除自由基吸光值;A0为空白对照的吸光值;Ax0为不加水杨酸时提取液自身的吸光度。
1.5.5 DPPH·清除率测定 采用Chen等的方法[19]并稍改动。取样品液2 mL,加入2 mL 0.2 mmol·L-1的DPPH-乙醇溶液,室温避光反应30 min,在517 nm下测吸光度。同时测定2 mL DPPH溶液与2 mL溶剂混合后测定的吸光值Ac及2 mL样品与2 mL无水乙醇混合后的吸光值Ab。
1.6 数据处理
每个实验3次重复,数据以平均值±标准差表示。采用SPSS17.0软件对数据进行方差分析,差异显著水平为p<0.05。
2 结果与分析
2.1 虫草固态发酵米形态
由图1可知,接种蛹虫草菌的大米培养基,在黑暗条件下培养7~8 d,白色菌丝布满大米培养基,光照后,大米从白色逐渐转成橘红色。干燥处理后,得到色泽均匀,颗粒从外到内皆呈橘红色的虫草米。干燥后称重,每100 g大米经虫草菌发酵可得70.57 g虫草米。

图1 虫草米干燥前后图Fig.1 Appearance of Cordyceps militaris rice before and after drying
2.2 虫草菌发酵前后大米成分变化
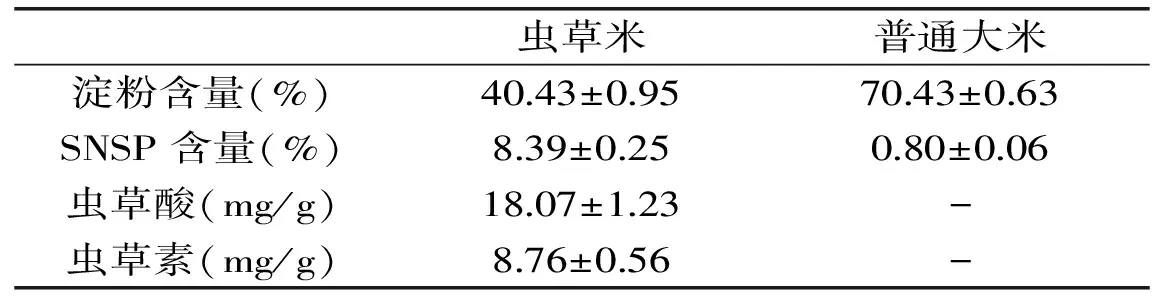
表1 虫草米、普通大米营养成分比较(干基)
注:-代表未检出。
由表1可以看出,经蛹虫草菌发酵大米后得到的虫草米含有虫草特有的功能性成分虫草酸、虫草素,且含量分别为18.07、8.76 mg/g。未经虫草菌发酵的普通大米淀粉含量高达70.43%,水溶性非淀粉多糖(SNSP)含量只有0.80%,而发酵后的虫草米中淀粉含量降低到40.43%,SNSP含量明显提高,达到8.39%。说明虫草菌在固态发酵条件下可有效的利用并降解大米中的淀粉,以致虫草米中淀粉含量大大降低,SNSP含量显著升高,提高了大米淀粉的消化吸收率和营养价值[20]。
2.3 虫草米的还原能力
还原力的强弱是测定物质抗氧化性的重要指标。由图2可知,虫草米与普通大米提取液随着浓度增加还原能力逐渐增强,虽然前者的还原能力始终高于后者,但和维生素C相比,还原能力仍有显著差异。浓度为3 mg/mL时,虫草米提取液、普通大米提取液的吸光度值分别为0.293、0.140,当浓度高于3 mg/mL时,虫草米提取液的还原能力显著(p<0.05)高于普通大米提取液的还原能力。虫草米中SNSP含量的增加可能与其还原能力的增强有关。
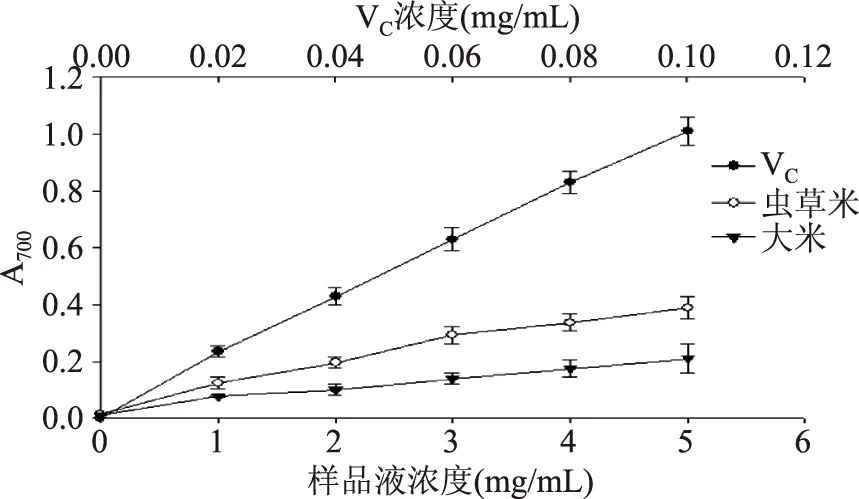
图2 VC、虫草米、普通大米还原能力Fig.2 Reducing power of VC,Cordyceps militaris rice and ordinary rice
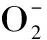

图3 VC、虫草米、普通大米对·的清除效果Fig.3 Scavenging activities of VC,Cordyceps militaris riceand ordinary rice against superoxide anion free radicals
2.5 虫草米对·OH的清除能力
羟自由基是目前所知活性氧中对生物体毒性最强,危害最大的一种自由基[22]。对羟基自由基的清除能力也是物质抗氧化的重要指标之一。如图4所示,普通大米提取液对·OH的清除能力随着浓度的增加几乎没有变化,但是虫草米提取液对·OH的清除能力随浓度的增加缓慢上升,且与提取液浓度呈正相关。提取液浓度为5 mg/mL时,虫草米提取液、普通大米提取液对·OH的清除率分别为38%、14.5%,虫草米提取液对·OH的清除能力显著(p<0.05)高于普通大米。

图4 VC、虫草米、普通大米对·OH的清除效果Fig.4 Scavenging activities of VC,Cordyceps militaris rice and ordinary rice against hydroxyl free radicals
2.6 虫草米对DPPH自由基的清除能力
DPPH·在有机溶剂中是一种很稳定的自由基,广泛用于抗氧化剂评价体系中[23]。如图5所示,与VC标准液对DPPH·的清除能力不同,虫草米提取液和普通大米提取液对DPPH·的清除率与浓度之间存在明显量效关系。随着虫草米及大米提取液浓度的增加,清除率增加很明显,且前者对DPPH·的清除能力始终显著(p<0.05)高于后者。提取液浓度为5 mg/mL时,虫草米提取液、普通大米提取液对DPPH·的清除率分别为79.1%、30.10%,说明虫草米提取液对DPPH·有较好的清除能力。

图5 VC、虫草米、普通大米对DPPH自由基的清除效果Fig.5 Scavenging activities of VC,Cordyceps militaris riceand ordinary rice against DPPH free radicals
3 结论
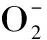
[1]Alexopoulos C J,Blackwell M,Mims C W.菌物学概论[M]. 北京:中国农业出版社,2002:293.
[2]Cunning Gham K G,Manson W,Spring F S,et al. Cordycepin,a metabolic product isolated from cultures ofCordycepsmilitaris-(Linn). Link[J]. Nature,1950,166:949-951.
[3]林威真. 甘露醇分析检测技术研究进展[J]. 河南化工,2010,27(2):5-6.
[4]WANG ZS,GU YX,YUAN QS. Effect of nutrition factors on the synthesis of superoxide dismutase,catalase,and membrane lipid peroxide levels inCordycepsmilitarisMycelium[J]. Current Microbiology,2006,52(1):74-79.
[5]王立强,黄竹清,于淼,等. 北虫草提取物抗衰老作用的初步研究[J]. 解放军预防医学杂志,2014,32(6):487-489.
[6]Lee HH,Kim SO,Kim GY,et al. Involvement of autophagy in cordycepin-induced apoptosis in human prostate carcinoma LNCaP cells[J]. Environ Toxicol Pharmacol,2014,38(1):239-250.
[7]Liu JY,Feng CP,Li X,et al. Immunomodulatory and antioxidative activity ofCordycepsmilitarispolysaccharides in mice[J]. Original Research Article International Journal of Biological Macromolecules,2016,86:594-598.
[8]王雅玲,代玲玲,赵铁男. 蛹虫草功能食品的最新研究进展[J]. 食品工业科技,2008,29(11):285-287.
[9]岳春,葛中巧,何际芳,等. 蛹虫草菌保健黄酒的研究[J]. 酿酒科技,2006,148(10):70-72.
[10]岳春. 蛹虫草保健茶饮料的研制[J]. 中国酿造,2008,195(18):86-89.
[11]车振明. 利用人工蛹虫草培养基酿制功能型酱油的研究[J]. 食品科学,2003,24(3):67-69.
[12]朴美子,巴媛媛,王永显,等. 北冬虫夏草米固态发酵最佳工艺[J].食品与生物技术学报,2011,30(2):302-305.
[13]NY/T2116-2012 中华人民共和国农业行业标准虫草制品中虫草素和腺苷的测定(高效液相色谱法)[S].北京:中国农业出版社,2012.
[14]胡淑琴,陈智毅,邹宇晓,等. 比色法测定15种食用菌中甘露醇的含量[J]. 现代食品科技,2010,26(8):901-902.
[15]代小梅. 紫甘薯非淀粉多糖提取工艺研究[J]. 江苏调味副食品,2014(4):20-24.
[16]Oyaizu M. Studies on products of browning reactions:antioxidant activities of products of browning reaction prepared from glucose amine[J]. J PJ Nutr,1986,44:307-315.
[17]Cheung Y C,Siu K C,Liu Y S,et al. Molecular properties and antioxidant activities of polysaccharide-protein complexes from selected mushrooms by ultrasound-assisted extraction[J]. Process Biochemistry,2012,47(5):892-895.
[18]Zeng YW,Zhao JL,Peng YH. A comparative study on the free radical scavenging activities of some fresh flowers in Southern China[J]. LWT-Food Science and Technology,2008,41(10):1586-1591.
[19]Chen X L,Wu G H,Huang Z L. Structural analysis and antioxidant activities of polysaccharides from culturedCordycepsmilitaris[J]. International Journal of Biological Macromolecules,2013,58(1):18-22.
[20]韩建荣,赵文倩,高宇英. 灵芝固态发酵降解玉米淀粉的初步研究[J]. 食品与发酵工业,2004,14(7):59-61.
[21]李正鹏,祝嫦巍,吴萍,等. 富锗树舌胞外多糖的体外抗氧化活性研究[J]. 现代食品科技,2013,29(8):1791-1795.
[22]Murcia M A,Jimenez A M,Mart nez-Tome M. Evaluation of the antioxidant properties of Mediterranean and Tropical fruits compared with common food additives[J]. Journal of Food Protection,2001,64(12):2037-2046.
[23]Awika J M,Rooney L W,Wu X L,et al. Screening methods to measure antioxidant activity of sorghum(Sorghum bicolor)and sorghum products[J]. Journal of Agricultural and Food Chemistry,2003,51(23):6657-6662.
Study on compositions and antioxidant activities of fermented rice byCordycepsmilitaris
ZHU Zhen-yuan,JIA Chang-ying,SUN Hui-qing
(College of Food Engineering and Biotechnology,Tianjin University of Science and Technology,Tianjin 300457,China)
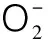
Cordycepsmilitarisrice;SNSP;antioxidationinvitro;scavenging free radical
2016-04-11
朱振元(1969-),男,博士,教授,研究方向:生物资源与功能食品,E-mail:zhyuanzhu@tust.edu.cn。
国家星火计划重点项目(2015GA610001);天津市东丽区科技型中小企业发展专项基金产学研合作项目。
TS218
A
1002-0306(2016)20-0000-00
10.13386/j.issn1002-0306.2016.20.000
