基于可再生原料的表面活性剂复配体系的优异润湿性:吸附和胶束化过程中的协同效应
2016-12-08PatrycjaSzumaAlicjaMowinska
PatrycjaSzumała•AlicjaMo´win´ska
(波兰格但斯克技术大学,化学学院,油脂和洗涤剂技术系)
王勇译
(中国日用化学工业研究院,山西太原,30001)
基于可再生原料的表面活性剂复配体系的优异润湿性:吸附和胶束化过程中的协同效应
PatrycjaSzumała•AlicjaMo´win´ska
(波兰格但斯克技术大学,化学学院,油脂和洗涤剂技术系)
王勇译
(中国日用化学工业研究院,山西太原,30001)

本文研究了由可再生原料制备的三种表面活性剂(APG、AE、脂肪酸钠)复配后的表面性能,主要目的是优化一元、二元、三元复配溶液和不同pH条件下产生最佳润湿性的复配表面活性剂比例。结果表明:几种复配表面活性剂溶液在界面张力、临界胶束浓度和混合胶束化过程中存在协同效应。AE-APG复配后展现了最佳润湿性能。AE-APG-脂肪酸钠三元复配体系在聚四氟乙烯表面和玻璃表面的接触角随着浓度增大而略微减小。此外,所有复配溶液在酸性、碱性及中性介质中都展现了良好的表面性能。与其他pH条件下相比,当pH=7时,AE∶脂肪酸钠(1∶2)、AE:APG(2∶1)和AE∶APG∶脂肪酸钠(1∶1∶1)提高了铝表面和玻璃表面的润湿力。以上研究表明:使用很少的表面活性剂可以达到清洗、润湿和增溶的效果,同时还可降低成本、保护环境。
表面活性剂;表面活性;润湿性;三元复配;协同效应
1 引言
工业洗涤剂、润湿剂和调理剂通常都是多种类型表面活性剂的混合物。这些混合体系展现了良好的协同效应,即混合后的某一性能比单一组分的性能有所提高[1]。低浓度就可以达到理想的性能,可有效降低成本和环境污染。
APG和AE应用广泛,因为其不仅易生物降解和高效清洗油脂,而且来源于可再生原料[2]。APG具有极好的生态毒性[3]和界面性能(低界面张力和良好的水溶性)[4]。由于它有良好的发泡性能和低的皮肤刺激性,所以,它被广泛地应用在洗涤剂中[5]。AE是最常见的一类非离子表面活性剂,主要应用于粉末和液体清洗、洗涤产品和化妆品中。它易生物降解。脂肪酸钠是一种最常见的表面活性剂,来源于可再生资源[6]。研究此类表面活性剂复配体系的表面活性有助于确定其在商业产品中的应用以及开发适用于不同工业过程中的表面活性剂配方。
润湿性是一项很重要的表面性质。Jurado等人[2,7]分析了APG和AE溶液的润湿性能和去污性能,认为复配后的去污和润湿性能最好。其他研究也表明[8],APG与其他表面活性剂复配后润湿力增强。材料表面和润湿浓度随pH变化而改变,表面性能与表面活性剂分子间的相互作用有关。
本文研究了APG、AE和脂肪酸钠的润湿性以及三者复配体系在吸附和胶束化过程中的协同作用。具体而言,研究了复配表面活性剂的浓度、摩尔比和pH对表面张力、接触角和分子间相互作用力的影响。
2 实验部分
2.1 原料
APG(C8~C10,聚合度1.6,平均分子式C8.6G1.6
[9]),购自Brenntag;脂肪酸钠(C12~C18,平均分子式C13.4Na),购自Coda;AE(7EO,C12~C14,平均分子式C13E7),购自PCC Exsol。制备溶液的水为去离子水,其20℃时表面张力为73.1±0.5mN/m。用Britton-Robinson缓冲溶液调节pH[10],所需的化学试剂如磷酸、醋酸、硼酸和氢氧化钠等均购自Sigma Aldrich。表面活性剂水溶液的pH用pH计测定。
2.2 方法
表面张力用悬滴法测定。通过测定和分析液滴的形状计算表面张力。液滴达到平衡后测定三次,每个样品重复三次,实验最终结果为九次测定值的算术平均值。
接触角用DSA测定。铺展动力学通过三种不同表面进行研究:铝表面、玻璃表面和聚四氟乙烯表面。固体表面先用丙酮清洗,待丙酮蒸发干后测定标准溶液(如去离子水)的表面张力以确定表面纯度。测定30、40和50s后的接触角大小。每个样品重复测五次。实验最终的结果为十五次测定值的算术平均值。液滴形状分析依赖于液滴大小、接触角、对称性和液滴形貌。本文选用Young-Laplace(固定液滴形貌,适合于对称液滴)和circle fi tting 进行分析(测定高-宽)。
为了确定单一和复配表面活性剂的表面活性,计算了一系列的参数:
① 表面压(Πcmc),溶剂表面张力和溶液表面张力的差值[11]
Πcmc= g0- gCMC
饱和吸附量(Γmax),由表面张力-浓度曲线得到的吸附参数[12,13]
Γmax= -a/(RTn)
其中:a为表面张力-浓度曲线的斜率(cmc之前);R为气体常数(8.314 J/mol K);T为温度(K);n为界面上表面活性剂的分子数量
③ 单个分子所占最小面积(Amin)[13]
Amin=1018/(NavΓmax)
④ 表面张力降低效率(pC20)[14]
pC20= -log(C20)
C20为表面张力降低20mN/m所需的表面活性剂的浓度。
3 结果与讨论
3.1 单一表面活性剂溶液的表面活性
为了确定单一表面活性剂(AE,APG和脂肪酸钠)的表面活性,测定了单一表面活性剂表面张力-浓度曲线,如图1所示。从曲线中可以得到cmc和 gcmc。胶束化和吸附的各项参数列于表1和表2。

图1 APG、脂肪酸钠和AE的表面张力-浓度曲线
AE的cmc最低。相关的文献数据表明C12EO7的cmc更低[15],这可能是由于不同的碳链长度和EO分布造成的。APG和脂肪酸钠的表面性能与文献中一致[15,16]。AE降低表面张力的效率也很高。pC20表明表面活性剂的浓度接近于产生界面最大吸附量的最低浓度[17]。
脂肪酸钠的cmc/C20比值最大。该参数用来表示表面活性剂在界面吸附的趋势大小,通常与胶束形成趋势大小有关[18]。此外,脂肪酸钠也具有较高的吸附效率(pC20)。脂肪酸钠的Πmax值最大(表1),该参数表示降低表面张力的能力[17]。
APG的Γmax最大,Amin最小(表2)。这表明APG分子在界面上的堆积最紧密。通常具有直链和大的头基(相对于疏水链的横截面积)的表面活性剂在界面上形成更加紧密、有效的堆积[17]。另外,APG吸附和胶束化参数与文献中一致[18]。
上述三种表面活性剂都具有较好的表面性能。鉴于大多数工业品是表面活性剂的混合物,因此,以下将考察这三种表面活性剂复配体系在不同摩尔比时的表面活性。

表1 单一表面活性剂溶液胶束化参数

表2 单一表面活性剂溶液吸附参数
3.2 二元复配和三元复配体系的表面活性和相互作用
为了研究表面性剂复配体系降低表面张力和cmc的效率,制备了以下复配体系:(a)AE∶脂肪酸钠,摩尔比1∶1,1∶2,2∶1;(b)AE∶APG,摩尔比1∶1,1∶2,2∶1;(c)AE∶APG∶脂肪酸钠,摩尔比1∶1∶1。 图2为表面张力-浓度曲线。AE∶脂肪酸钠=1∶2时,gcmc最低(26mN/m)。这是该复配体系降低表面张力的最大能力。与其他二元复配体系相比较,降低AE∶脂肪酸钠的摩尔比(2∶1,1∶1,1∶2),cmc和Amin均减小(表3)。另一方面,AE∶脂肪酸钠=2∶1时,该复配体系具有最高的降低表面张力的效率(C20=2.8×10-5mol/dm3)。AE∶APG具有最低的CMC(摩尔比2∶1,cmc= 1.18×10-4mol/dm3)。该复配体系具有最高的Γmax和最低的Amin(表4)。三元复配体系具有相对较高的cmc,也能够显著降低水的表面张力(gcmc= 26.76 mN/m)。
另外一个重要的发现是所有的表面活性剂体系(除了AE∶APG=1∶2)的cmc都比单一组分的cmc低,这表明三种表面活性剂之间存在协同效应。
复配体系中表面活性剂分子间相互作用会增强或减弱其性能。为了确定他们之间的相互作用,用以下参数进行表征:

上式中,X1为混合吸附单分子层中表面活性剂1的摩尔分数;C,C分别为某个给定表面张力值所需的表面活性剂1和表面活性剂2的水相摩尔浓度;C1,C2分别为某个给定表面张力所需表面活性剂1和表面活性剂2在混合表面活性剂中的水相摩尔浓度;
为在气/液界面形成混合吸附单分子层中的分子间相互作用参数。
II. 混合表面活性剂在水相形成混合胶束的分子间相互作用参数,

图1 APG、脂肪酸钠和AE的表面张力-浓度曲线

表3 复配表面活性剂溶液胶束化参数

表4 复配表面活性剂溶液吸附参数
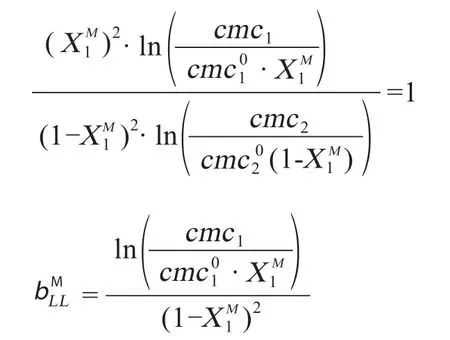
bLL,为负值,表明分子间相互吸引;为正值,则表示相互排斥。
复配体系的相互作用,可以通过以下条件进行判定:
i降低表面张力效率产生协同效应的条件是[19,20]:



ii在形成混合胶束产生协同效应的条件是[20]:
iii在表面张力降低效能方面产生协同效应的条件是[20]:

其中,a为表面张力曲线的斜率。
3.3 表面活性剂复配体系的润湿性能
对于吸附和胶束化最好的复配体系(AE∶脂肪酸钠=1∶2;AE∶APG=2∶1),测定其在三种固体表面(聚四氟乙烯、铝、玻璃)的接触角。此外,对三元复配体系(AE∶APG∶脂肪酸钠=1∶1∶1)的润湿性能也进行了研究。图3(a-c)为接触角-浓度曲线。
从图3可以发现:表面润湿性最好的是玻璃表面。所有玻璃表面的最大接触角对应的表面活性剂浓度均低于该复配体系的cmc,且接近界面饱和吸附时体相中的表面活性剂浓度。其他文献报道中也发现单独的非离子表面活性剂也具有相似的现象[21]。当浓度达到cmc后,复配体系溶液在三种固体表面的接触角均迅速下降;随着浓度的增加,润湿性逐渐增强。聚四氟乙烯、铝和玻璃表面的最小接触角值分别为44.2o、27.8o和11.9o。这表明三元复配体系(AE∶APG∶脂肪酸钠=1∶1∶1)增强了疏水表面(聚四氟乙烯)和亲水表面(玻璃)的润湿性,但是所需的表面活性剂浓度较高。

表5 分子间相互作用参数

图3 不同摩尔比复配体系的接触角-浓度曲线

图4 pH=5,7,9时,复配溶液表面张力-浓度曲线
在表面测试过程中发现,聚四氟乙烯表面润湿性最差[22]。用硅表面活性剂处理的表面润湿过程常被称为“超级铺展”。然而,相关数据表明:有机硅表面活性剂溶液在涂了硅膜的聚四氟乙烯表面的接触角约为50~60o。本研究表明:碳氢表面活性剂的二元与三元复配体系也能够有效润湿聚四氟乙烯表面。
3.4 pH对表面活性剂复配体系表面活性和润湿性的影响
在本实验中,考察了不同pH下二元复配体系(AE∶脂肪酸钠=1∶2;AE∶APG=2∶1)和三元复配体系(AE∶APG∶脂肪酸钠=1∶1∶1)的表面性能。图4为在pH=5,7,9下的表面张力-浓度曲线。所有的体系在很宽的浓度范围内均可将表面张力降低至30mN/m以下。这表明:复配体系在酸性、中性和碱性条件下均有很好的表面活性。
在AE/APG和三元复配体系中,pH=7时的cmc最低。pH=5时的gcmc最低。pH=5,9时,AE/APG复配体系的cmc值均大于在去离子水中得到的cmc。AE/脂肪酸钠复配体系则显示了相反的关系:pH=5时cmc最低,pH=7时表面张力gcmc最低。AE/脂肪酸钠复配体系的cmc随pH的增加而增大。

表6 不同pH条件下表面活性和分子间相互作用参数
所有复配体系在pH=5,7,9条件下,在降低表面张力和形成混合胶束时都产生了协同效应(表6)。
此外,还考察了不同pH对复配体系润湿性的影响。pH=7时,复配体系在三种固体表面的润湿力最大。图3(d-f)为pH=7时三种表面的接触角-浓度曲线。可以看出,AE/脂肪酸钠复配体系在聚四氟乙烯和铝表面的接触角随着浓度的增加而增加,直到浓度接近0.0008和0.0006mol/dm3。在玻璃表面,浓度超过0.0002 mol/dm3后,接触角逐渐降低。AE/脂肪酸钠复配体系在聚四氟乙烯、铝和玻璃表面的最小接触角分别为:48.6o、6.3o和4.4o。AE/APG复配体系在聚四氟乙烯、铝和玻璃表面的最小接触角分别为(44.1o,3.5o和4.4o)。pH=5,9时,在聚四氟乙烯和金属/玻璃表面的接触角不超过50o和12o。因此,pH=7时,润湿力得到了很大的提升。当接触角q 接近0时,认为润湿液体的润湿性最好。
通过研究了三元复配体系的接触角,可以得出以下结论:该体系在铝和玻璃表面的润湿性相似(如图3f);最小接触角值分别为5.5°和8.0°。这些值比二元复配体系的θ值高,三元复配体系在铝表面和玻璃表面仍展现了良好的润湿性。
[1]RosenMJ,ZhuZH,GaoT(1993)Synergisminbinarymixtureofsurfactantsmixturecontainingmono-anddisulfonatedalkyl-anddialkyldiphenylethers.JColloidInterfSci157:254–259.
[2]JuradoE,BravoV,Luzo´nG,Fernandez-SerranoM,Garcia-RomanM,Altmajer-VazD,VicariaJM(2007)Hard-surfacecleaningusinglipases:enzyme–surfactant.interactionsandwashingtests.JSurfactDeterg10:61–70.
[3]AndreeH,MiddelhauveB(1991)Possibleapplicationsofalkylpolyglucosidesindetergentsanddishwashingagents.TensideSurfDeterg28:413–418.
[4]NickelD,NitschC,KurzendorferP,VonRybinskiW(1992)Interfacialpropertiesofsurfactantmixtureswithalkylpolyglycosides.ProgColloidPolymSci89:249–252.
[5]BalzerD,HuelsAG(1991)Alkylpolyglucosides,theirphysicochemicalpropertiesandtheiruses.TensideSurfDeterg28:419–427.
[6]SzymanskiA,WyrwasB,SwitZ,JaroszynskiT,LukaszewskiZ(2000)Biodegradationoffattyalcoholethoxylatesinthecontinuousflowactivatedsludgetest.WaterRes34:4101–4109.
[7]JuradoE,VicariaJM,Fernandez-ArteagaA,ChachalisP,Garcıa-MartınJF(2010)Wettingpowerinaqueousmixturesofalkylpolyglucosidesandethoxylatedfattyalcohols.JSurfDeterg13:497–501.
[8]AleksejczykRA,UrferAD(1995)Alkylglycosidecompositionswithimprovedwettingproperties.USAPatent5,385,750.
[9]BravoV,JuradoE,ReyesA,GarciaAI,Bailon-MorenoR,CuevasArandaM(2005)Determinationofaveragemolecularweightofcommercialsurfactants:alkylpolyglucosidesandfattyalcoholethoxylates.JSurfactDeterg8:341–346.
[10]MongayC,Cerda´MA(1974)Britton–Robinsonbufferofknownionicstrength.AnalChim64:409–412.
[11]DaviesT,RidealEK(1963)Interfacialphenomena.AcademicPress,London.
[12]ChattorajDK,BirdiKS(1984)AdsorptionandtheGibbssurfaceexcess.PlenumPress,NewYork.
[13]DaviesJT(1951)Thedistributionofionsunderachargedmonolayer,andasurfaceequationofstateforchargedfilms.ProcRSocLond208:224–247.
[14]RosenMJ,MurphyDS(1991)Effectofthenonaqueousphaseoninterfacialpropertiesofsurfactants.2.Individualandmixednonionicsurfactantsinhydrocarbon/watersystems.Langmuir7:2630–2635.
[15]Lo´pez-CervantesaJL,Gracia-FadriqueaJ,CalvobE,AmigobA(2013)Surfacetensions,densities,andspeedsofsoundforaqueoussolutionsoflauryletherethoxylates.FluidPhaseEquilib356:193–200.
[16]DongR,HaoJ(2010)Complexfluidsofpoly(oxyethylene)mon oalkylethernonionicsurfactants.ChemRev110:4978–5022.
[17]EastoeJ(2009)Adsorptionofsurfactantsatinterfaces.In:Colloidscience:principles,methodsandapplications.Wiley-Interscience,NewYork.
[18]RosenMJ,SulthanaSB(2001)Theinteractionofalkylglycosideswithothersurfactants.JColloidandInterfSci239:528–534.
[19]GuB,RosenMJ(1989)Surfaceconcentrationsandmoleculeinteractionsincationic–anionicmixedmonolayersatvarioussurfaces.JColloidInterfSci129:537–553.
[20]TanfordC(1980)Thehydrophobiceffect:formationofmicellesandbiologicalmembranes.Wiley-Interscience,NewYork.
[21]SzymczykK,ZdziennickaA,Jan´czukB(2015)Adsorptionandwettingpropertiesofcationic,anionicandnonionicsurfactantsintheglass-aqueoussolutionofsurfactant-airsystem.MaterChemPhys162:166–176.
[22]RadulovicJ,SefianeK,ShanahanMER(2009)Spreadingandwettingbehaviouroftrisiloxanes.JBionicEng6:341–349.
Perfectly Wetting Mixtures of Surfactants from Renewable Resources: The Interaction and Synergistic Effects on Adsorption and Micellization
Patrycja Szumała • Alicja Mo´win´ska
(Department of Fats and Detergents Technology, Faculty of Chemistry, Gdansk University of Technology)
Translated by Wang Yong
(China Research Institute of Daily Chemical Industry, Taiyuan 30001, Shanxi, China)
This paper presents a study of the surface properties of mixtures of surfactants originating from renewable sources, i.e., alkylpolyglucoside (APG), ethoxylated fatty alcohol (AE), and sodium soap (Na soap). The main objective was to optimize the surfactant ratio which produces the highest wetting properties during the analysis of the solution of the individual surfactants, toward three-component mixtures, and at different pH values. The results showed the existence of a synergistic effect in lowering the interfacial tension, critical micelle concentration and the formation of mixed micelles in selected solutions. We found that best wetting properties were measured for the binary AE:APG mixtures. It has been demonstrated that slightly lower contact angles values were observed on Teflon and glass surfaces for the AE: APG:- soap mixtures but the results were obtained for higher concentration of the components. In addition, all studied solutions have very good surface properties in acidic, basic and neural media. However, the AE:soap (molar ratio of 1:2), AE:APG (2:1) and AE:APG:soap (1:1:1) compositions improved their wetting power at pH 7 on the aluminium and glass surfaces, as compared to solutions at other pH values tested (selected H values close to zero—perfectly wetting liquids). All described effects detected would allow less surfactant to be used to achieve the maximum capacity of washing, wetting or solubilizing while minimizing costs and demonstrating environmental care.
surfactant;surface activity;wettability;ternary combination;synergistic effect
TQ423
A
1672-2701(2016)11-42-08
