高纯三甲基锑的制备
2016-12-08徐耀中
徐耀中
(苏州大学材料与化学化工学部,江苏 苏州 215123)
高纯三甲基锑的制备
徐耀中
(苏州大学材料与化学化工学部,江苏 苏州 215123)
摘要:本文详细地介绍了高纯三甲基锑制备的全部过程,包括格氏试剂的合成、三甲基锑粗品的制备和浓缩,重点介绍了三甲基锑的纯化和检测,产品经检测有机纯度≧99.9%,无机杂质含量≤1ppm,达到6N标准。
三甲基锑;高纯;格氏试剂
三甲基锑是一种MO源(金属有机化合物),它的化学性质比较活泼,在空气中会发生自燃。三甲基锑常用作发光二极管制造中GaAs、GaP、GaAsP等沉积层的N型掺杂剂。在半导体工业中,通过MOCVD制备二元化合物薄膜,如GaSb和InSb;三元化合物薄膜,如InAsSb、GaAsSb、GaPSb和InPSb,另外还有四元化合物薄膜,如GaInAsSb和InAsSbBi。这些薄膜的性质跟三甲基锑的纯度关系非常大,极少量的杂质都会给半导体沉积层的性能带来极大的影响,因此需要高纯的三甲基锑(杂质含量≤1ppm)。
从20世纪40年代开始,国外已对三甲基锑的合成和纯化做过研究,在C.H.Bamford等人和Donald.C.Mente等人的报道中,使用了如下的方法:
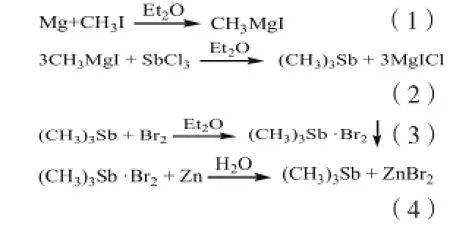
在该反应中,首先用格氏法制备粗品,接着采用液溴和三甲基锑络合成固体[(CH3)3Sb·Br2]沉淀。然后过滤洗涤,除去乙醚和反应生成的杂质。接着用锌粉将三甲基锑还原出来,最后将粗品提纯,得到高纯度的三甲基锑。
此方法的优点在于:[(CH3)3Sb· Br2]为不溶于乙醚的固体,可以通过过滤和洗涤除去乙醚和相关杂质;然而缺点在于:操作步骤多;分离方法繁琐;产品容易氧化;原料种类多;废弃物多且难处理;产品中锌杂质含量高;并且由于有过滤和清洗步骤,导致产品收率低,一般在50%左右。另一方面,由于三甲基锑和水不发生反应,通过1H NMR反映出在产品中出现含微量水的频率较高,微量的水会导致薄膜材料的良率下降很多,这在半导体产业中是不允许的。
本工作目标是优化TMSb的制备方法,提高产品的产率和纯度;简化操作步骤,减少有毒有害物质的使用,实现“绿色化学”和环境的可持续发展。我们计划通过控制原料纯度,对不同的分离方法进行试验,最终选用特殊精馏装置,直接分离出目标产物,简单高效地得到了高纯三甲基锑,并且上述高纯TMSb的质量指标符合国际一流水平,它的产业化将会填补国内空白。
1.实验部分
1.1 原料
三氯化锑:分析纯99%,阿拉丁试剂公司;碘甲烷:分析纯,精制。
乙醚:分析纯,精制。
1.2 三甲基锑粗品的制备
格氏试剂法合成三甲基锑:在四口烧瓶中,氮气保护下,按照Mg和CH3I分别为3mol和2.9mol的比例投料,在7mol的乙醚溶液中合成格氏试剂。在合成好的格氏试剂中,滴加含有0.9mol的三氯化锑乙醚溶液,合成三甲基锑。反应完毕,釜内为三甲基锑、乙醚、卤化镁和未反应完的少量原料的黑色混合物溶液。在常压下蒸出乙醚,当釜温升至60℃,维持出料半小时,回收的乙醚中平均含有10%质量分数的三甲基锑,可以用于下次格氏反应。
通过减压蒸馏装置,将三甲基锑和乙醚的混合物蒸出待用,釜中剩下白色卤化镁固体。将蒸出的混合物取样,以氘代苯做溶剂,得到核磁结果,通过核磁计算出乙醚质量含量为5.1%。详情如图1和表1所示。
1.3 纯化
由于乙醚和三甲基锑互溶性好,加上乙醚挥发性好,蒸汽压高,导致三甲基锑粗品提纯的难点在于乙醚不易完全除去,所以先前都是通过三甲基锑和液溴形成不溶于乙醚的固体以便除去乙醚。
通过分析元素核外电子排布,我们发现,锑是VA族元素,和ⅢA族元素的铝、镓、铟元素形成的烷基化合物含有空轨道能和乙醚形成络合物不同,理论上通过直接分离的方式是可以将混合物中的乙醚完全除去的,关键在于分离的装置和条件,我们选择了几种分离方式作为对比。
1.3.1 实验一:常压简单蒸馏
(1)在惰性气体手套箱中,将400mL上述混合物(通过1H NMR检测,大约含有560g三甲基锑有效成分)加入到500mL带有温度计套管的烧瓶中,通过简单蒸馏,首先蒸出乙醚。
(2)当顶温上升到78℃~81℃并保持稳定,换瓶接收中间馏分。
(3)蒸馏结束,称重,得到465g馏分。取核磁分析1H NMR。
实验结果与结论:
经核磁检测,以质量比计算,上述中间馏分中含有2.4%质量分数的乙醚,分离效果差。
1.3.2 实验二:常压精馏
(1)投料量与实验一相同。精馏柱选用特制并填充有θ型316L不锈钢填料的玻璃精馏柱。冷凝管选用直型冷凝管。
(2)加热后顶温由常温上升至34.8℃,开始出馏分。
(3)釜温持续上升并最终稳定在82.1℃~83.5℃之间。当顶温上升至60.1℃并稳定,换瓶接收中间馏分。由于出料速度慢,以及精馏柱的保温不是绝对保温,所以顶温和理论沸点温度不同。
(4)精馏结束,称重,得到452g馏分,收率约为80.7%,取核磁分析1H NMR。
实验结果与结论:
经核磁检测,以质量比计算,上述中间馏分中含有274ppm的乙醚。利用精馏柱分离比简单蒸馏的效果好,但是不能完全除去乙醚。
1.3.3 实验三:减压精馏
通过上述两种实验,确定三甲基锑和乙醚无络合,可以加热分离。本实验在实验二的基础上,希望通过减压精馏的方式,将馏出的乙醚及时抽去或收集到杜瓦瓶中。
(1)投料情况、精馏柱和填料使用与实验二相同,釜更换为1000mL带有温度计套管的单口烧瓶。惰性气体手套箱外,设置带有杜瓦瓶保护的真空系统,杜瓦瓶用液氮冷却,真空系统与惰性气体手套内三甲基锑精馏系统的尾气端连接。
(2)根据三甲基锑常压沸点80.6℃,调节系统真空度(绝压)为36kPa,将三甲基锑的沸点拉低至50℃左右,与此同时,乙醚的沸点降为7.8℃左右。
(3)控制冷凝管的温度在-10℃~-5℃,调节真空阀门开启度,直至有少量馏分出来。
(4)由于乙醚的蒸出,釜温渐渐下降,全部接入真空后,对釜进行加热。
(5)当釜温升至52℃,顶温先持续下降并在短时间内升高至41.4℃,标志着乙醚已被除尽,这时馏出的馏分基本为三甲基锑,保持出料30分钟。换瓶接收中间馏分。
(6)精馏结束,中馏分接收393g,收率70%,取核磁分析1H NMR。
实验结果与结论:
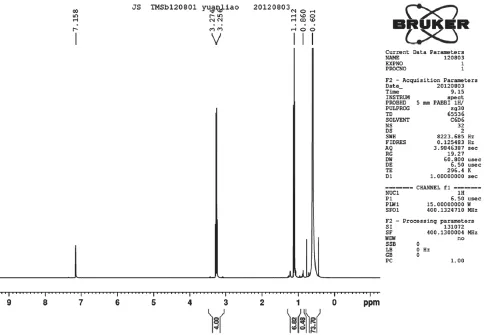
图1 TMSb和乙醚混合物的核磁氢谱

表1 TMSb和乙醚混合物核磁氢谱位移说明
经核磁检测,上述中间馏分中无乙醚,达到完全分离效果,乙醚被蒸出的同时及时被抽走,由于三甲基锑沸点不高,导致部分三甲基锑也被抽到杜瓦瓶中,使收率变低。
1.34实验四:先减压精馏,再常压精馏
本实验在实验三的基础上,分析出通过减压精馏的方式可以完全分离乙醚,且乙醚是在精馏前段被除去,为了避免三甲基锑损耗过大,本实验在除完乙醚后再做常压精馏以提纯三甲基锑。
(1)前段操作,和实验三的1~4步相同。
(2)通过顶温变化判断乙醚通过减压精馏被除尽,保持出料30分钟。
(3)将减压精馏装置转换为常压精馏,换瓶接收中间馏分。
(4)精馏结束,得到中间馏分接收463g,收率82.6%,取核磁分析1H NMR。
实验结果与结论:
经核磁检测(如图2所示),上述中间馏分无乙醚,达到完全分离效果。另外,我们分别对低沸馏分和釜残做了1H NMR检测,图谱显示:低沸馏分中含有大量乙醚,高沸点釜残中含有大量有机杂质。由中间馏分的ICP-OES检测报告(表3)可以看出,所有的无机杂质的含量都在仪器检出限以下,整体无机杂质含量小于1ppm,说明该馏分的纯度达到了6N。
1.4 重复实验
为了验证实验的重复性并优化实验条件,我们选择了不同的投料量和真空度做为对比,结果发现:当混合物原料中乙醚含量≤3%时,分离的成功率比较大;减压精馏真空度(绝压)为35kPa时,分离的效果比较好,收率都能稳定在80%以上。

表2 分析报告
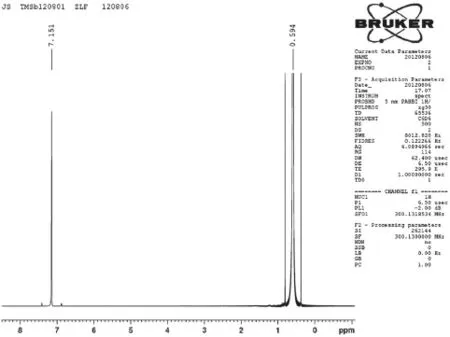
图2 TMSb中间馏分1H NMR谱图
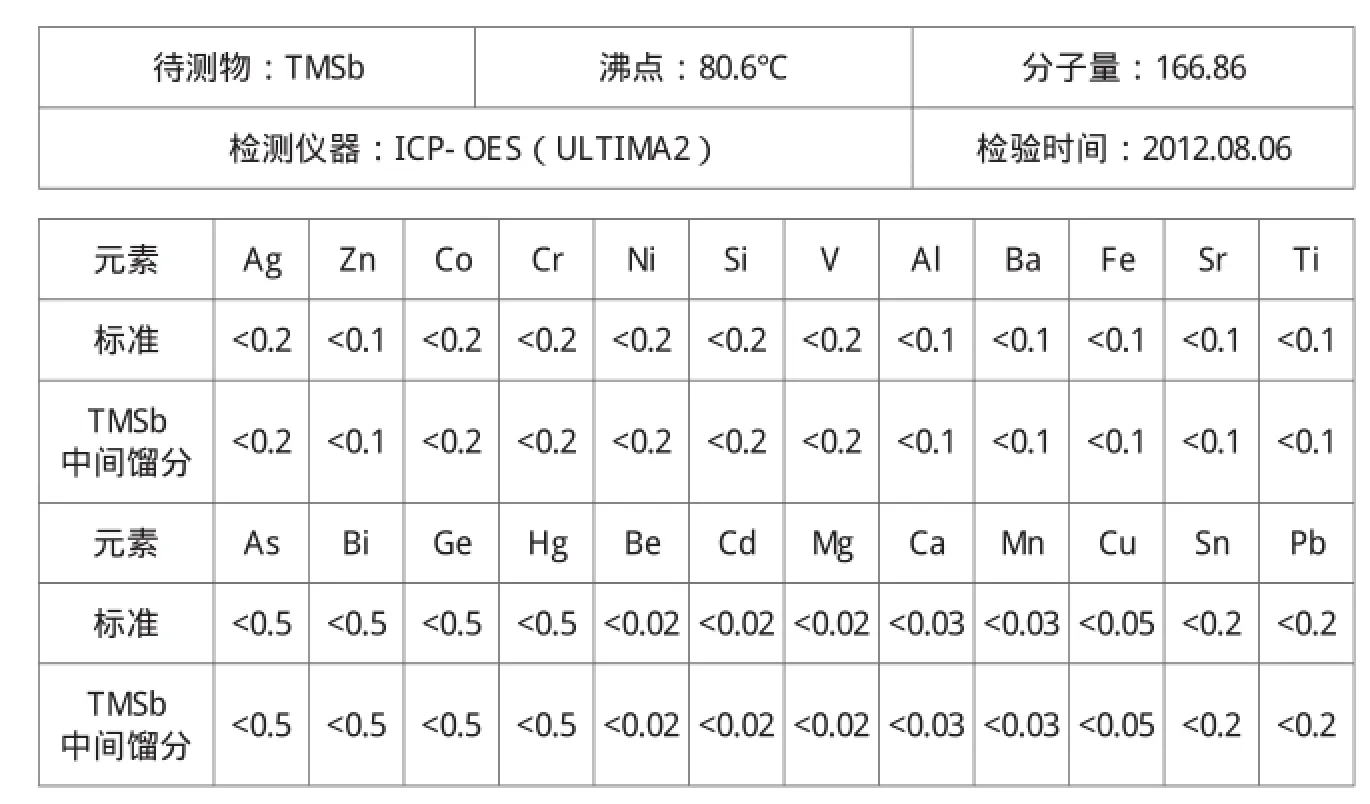
表3 TMSb中间馏分ICP-OES检测结果
结论
(1)经上述实验,证明通过简单蒸馏和常压精馏,都可以使三甲基锑粗品中乙醚含量降低,但是很难将乙醚完全除净;通过全程减压精馏,尽管可以得到高纯三甲基锑,但收率偏低。
(2)通过特殊精馏装置,采用先减压精馏再常压精馏,可以得到理想的效果。产品通过1H NMR分析,有机纯度达到99.9%;通过ICP-OES检测,无机杂质小于1ppm,纯度达到6N。
(3)本方法步骤少,操作简便,减少了原料种类,避免了锌元素的引入;收率稳定,重复性好。按投入的SbCl3计算,该方法收率能稳定在80%以上,适合大量生产。
(4)合成过程中使用的溶剂可以回收并循环使用,减少了废弃物的排放,符合“绿色化学”的要求。
(5)本方法合成的三甲基锑是高纯MO源,指标达到国际一流水平,可以直接在国内外LED和半导体企业的生产线上使用。它的国产化将会大大加快国内LED产业的发展和产业链升级;给国内半导体企业的跨越式发展提供强有力的支撑。
[1] C. A. Larsen, S. H. Li, and G. B. Stringfellow⋆, Chem. Mater. 1991, 3, 39-44.
[2]阎圣刚,张琳,阎晓彬.直接气相色谱法分析三甲基锑中的有机杂质[J].稀有金属,1994(5):396-397.
[3] C. H. Bamford, D. L. Levi, and D. M. Newitt, J. Chem. Soc. 1946, 468.
[4] DONALD. C. MENTE, JERRY L. MILLS, and ROYE. MITCHE, L, Inorg. Chem. 1975, 14, 123-126.
TG146
A
