高效液相色谱法和生物效价测定法在缩宫素注射剂质量控制中的对照研究
2016-12-07徐容
徐容
(南通卫生高等职业技术学校药学医技系,江苏 南通 226000)
高效液相色谱法和生物效价测定法在缩宫素注射剂质量控制中的对照研究
徐容
(南通卫生高等职业技术学校药学医技系,江苏 南通 226000)
目的 采用高效液相色谱法(HPLC)对缩宫素注射剂进行质量控制,同时与传统的生物效价测定法进行比照,观察两种方法的优劣。方法 选取8个企业生产的100个批次的缩宫素注射剂,分别采用HPLC法和生物效价法对样本进行测定,并将结果进行比较,并进一步观察样品的长期稳定性。结果 两种方法检测的缩宫素含量除两家药企外(P=0.027、P=0.011),其他企业生产的缩宫素含量差异无统计学意义(P=0.556、0.637、0.614、0.559、0.315、0.429);8家药企的缩宫素注射剂含量在55.9%~126.1%之间,平均98.5%,其中有三个企业生产的缩宫素注射剂含量相对偏低;缩宫素注射剂储存2年后其效价显著降低,差异有统计学意义(P=0.025)。结论 采用HPLC法对缩宫素注射剂测定,操作相对简便,灵敏度和准确度高,有效避免了生物效价测定法因动物个体差异造成的误差,同时也能将人为测定的误差控制在较小的范围内。另缩宫素注射剂最佳存贮期为2年,时间过长会导致药剂中部分有效成分降解。
缩宫素;HPLC法;质量控制;稳定性
缩宫素(oxytocin)注射剂是临床产科常用药物,主要用于催产、引产及产后因宫缩无力导致的子宫出血等症状[1]。它主要通过结合妊娠子宫平滑肌上相应的受体,刺激子宫节律性收缩,在产妇宫缩无力难产时,增加子宫收缩强度和频率,使胎儿顺利娩出,此外,它还可刺激乳腺平滑肌,促进乳汁分泌[2]。目前,国产缩宫素注射剂生产厂家繁多,质量控制是不可或缺的重要环节,国家药典中对于缩宫素质量控制的主要方法还是生物效价测定法[3],但该法由于用到动物实验,可能会因动物个体差异产生一定的误差,另外对研究人员的操作要求较高,后期在结果处理时人为因素干扰较大[4]。为建立一种更加客观、简便、准确的质控方法,笔者通过不断改进,建立以HPLC法测定宫缩素质量的检测方法,并与生物效价测定结果进行对照,现将结果报告如下。
1 仪器和试剂
主要实验仪器包括美国Thermo公司TSQ Quantum Ultra三重四级杆液相色谱质谱联用仪,美国Agilent公司HP1100高效液相色谱仪,傅里叶变换红外光谱仪,紫外分光光度计,紫外灯,奥尔科特立体器官测定系统,乙腈等。标准品缩宫素由中国食品药品检定研究院提供(批号150529-200902),去氨加压素的标准品由GL Biochem公司生产(批号P100518-ZG061714)规格为每瓶5.7 mg,纯度98.87%。本研究中用来分析的8个企业生产共100个批次的缩宫素注射剂规格均为10 IU·mL-1,另外取江苏省食品药品监督检验研究院2013年国家评价性抽验缩宫素注射液留样,在10~20 ℃,相对湿度30%~50%下储存,作为药物稳定性的研究标本。
2 试验方法
2.1 生物效价测定法测定缩宫素效价 本研究中的生物效价测定法采用的是大鼠离体子宫法,实验前48 h于大鼠子宫两侧皮下注射乙烯雌酚,实验当天取处死小鼠子宫置于离体器官恒温水浴装置中,用生物记录仪张力传感器连接,供试品和标准品分别用生理盐水进行稀释,分为高低不等的4个剂量,按照2010年版《中国药典》[5]中缩宫素生物测定法标准执行,借助药典中量反应平行线法对得到的实验结果进行可靠性检验,排除不可靠的实验结果后,按照剩余结果计算效价。
2.2 高效液相色谱法(HPLC)测定缩宫素效价 缩宫素HPLC法测定中,填充剂为十八烷基硅烷键合硅胶,取940 mL磷酸二氢钠(0.1 mol·L-1)溶液,同时加入60 mL(0.1 mol·L-1)磷酸氢二钠溶液混匀,通过磷酸溶液将pH值调至6.0,取上述缓冲液作为流动相A,将乙腈和水按照1∶1比例混匀,作为流动相B,按照以下标准进行梯度洗脱,洗脱时间0、5、35、35.1、45 min,对应流动相A百分率75%、75%、35%、75%、75%,对应流动相B百分率25%、25%、65%、25%、25%。取适量去氨加压素和缩宫素标准品,配制系统适用性试验溶液,其中每毫升溶液中含5 μg去氨加压素和5 IU缩宫素,将试验溶液分离度控制在5.0以上。取缩宫素标准品通过流动相A稀释至10 IU·mL-1作为对照溶液,另取适量待检的缩宫素注射液,通过流动相A进行稀释,稀释浓度为10 IU·mL-1,作为供试品溶液,取供试品溶液100 μL进样,通过外标法计算峰面积从而最终得出待检注射剂中缩宫素含量。
3 方法学考察
3.1 专属性考察 首先,按照“2.2”项中的方法配制只含有辅料的空白样品溶液进样,色谱图见图1,通过图1可以明确辅料对于样品测定中的主峰无干扰。本研究中,我们通过多种破坏性试验,使待检样本中产生出各种杂质,作为缩宫素杂质对照品,通过观察主峰和杂质的分离情况,为缩宫素注射剂质量控制提供数据支持。其中,破坏性试验取试验样品三份,加入1 mL浓度为1 mol·L-1盐酸,1 mL浓度为1 mol·L-1氢氧化钠溶液,沸水中加热三种方法进行破坏,将破坏后的溶液pH调至7,按照“2.2”项中方法进样,分析色谱图(见图2),可以发现经过破坏性试验产生的杂质对照品中各杂质与主峰分离度好,不干扰样品测定。

图1 空白辅料色谱图
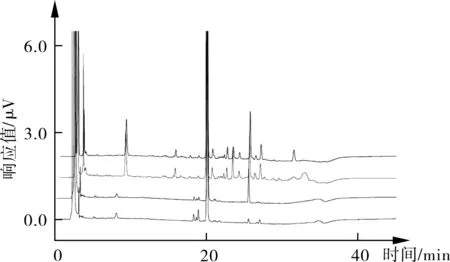
图2 样品与杂质对照品主峰分离度色谱图
3.2 建立标准曲线 以流动相A将适量缩宫素标准品依次稀释成23.04、11.52、5.76、2.88、1.44、0.72、0.36 IU·mL-1的六种溶液,各取6种溶液100 μL,依次通过HPLC色谱仪进行分析,将得到的色谱图中缩宫素标准品的峰面积(A)和分别对应的浓度(C)进行线性回归,从而建立标准曲线方程:Y=6.847×10-6X+0.432,r=0.998,同时也说明在此浓度范围内,缩宫素的浓度与峰面存在良好的线性关系。
3.3 稳定性试验 将“2.2”项下方法制备的供试品溶液分别于0、12、18、24、35 h时间点进行进样分析,计算上述时间点下测得的缩宫素峰值面积,未发现显著性下降,证明供试品溶液的稳定性较好。
3.4 检验限度和定量限度 通过流动相A稀释缩宫素标准品,浓度0.01~1 IU·mL-1,按照“2.2”项下方法进样,通过色谱图观察得出检验限度为0.15 IU,定量限度为0.51 IU。
3.5 重复性实验 分别量取100 μL缩宫素注射剂样品6份,按照“2.2”项方法进样,观察色谱图,通过外标法计算得出各样品含量平均值为98.4%,RSD<1.0%,证明该法具有良好的重复性。
3.6 回收率实验 取缩宫素标准品溶液3份,将浓度调至2、10、30 IU·mL-1,分别取上不同浓度的缩宫素标准品溶液1 mL,同9份已知含量的缩宫素注射剂样品混匀,通过液相色谱-二级质谱连用(LC-MS/MS)法测得从低到高三种浓度混合溶液的回收率分别为99.25%(RSD=0.72%),99.41%(RSD=0.51%),98.92%(RSD=0.78%),平均回收率为99.27%。
3.7 统计学方法 数据统计采用SPSS17.0进行分析,组内比较采用配对t检验,多组间比较采用方差分析,率比较采用χ2检验,进一步的组间比较采用LSD检验,相关性分析采用Pearson相关性分析,P<0.05表示差异有统计学意义。
4 结果
4.1 缩宫素注射剂含量测定 以“2.2”项方法对8家企业生产的100个批次缩宫素注射剂样品含量进行测定的色谱图见图3,通过计算各样品含量在55.9%~126.1%之间,平均98.5%,其中有3个企业生产的缩宫素注射剂含量偏低。对各企业的缩宫素注射剂含量测定结果进行方差分析发现,其差异有统计学意义(F=3.724,P=0.031,P<0.05),表明这些企业在生产缩宫素注射剂过程中投料量差异较大,造成这些差异主要属于人为原因造成,不在系统误差之列,另外个别企业不同批次的缩宫素注射剂含量之间也存在差异,离散度较大,说明该企业产品质量波动较大,应适当改进,见图4。

图3 各企业缩宫素注射剂色谱图
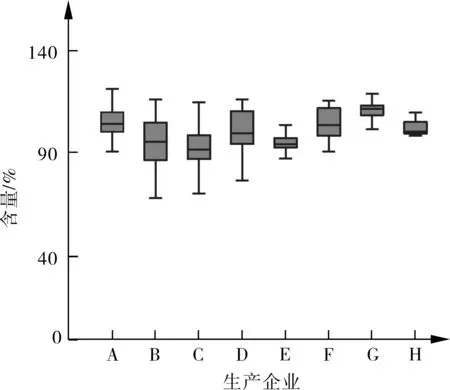
图4 各生产企业缩宫素注射剂含量
4.2 HPLC法和生物效价测定法测定缩宫素标准品的精密度比较 根据“2.1”项和“2.2”项方法对缩宫素标准品效价进行测定发现,生物效价测定法9次测量结果分别为9.73、9.91、9.56、9.95、10.02、9.68、9.86、10.14、10.32 IU·mL-1,测定值变动范围9.56~10.32 IU·mL-1,相对标准偏差RSD=3.4%,平均效价9.91 IU·mL-1;HPLC法的9次测量结果分别为9.78、9.82、9.91、9.88、9.89、9.96、9.85、9.79、9.88 IU·mL-1,测定值变动范围9.78~9.96 IU·mL-1,相对标准偏差RSD=0.65%平均效价9.86 IU·mL-1。提示HPLC法精密度要高于生物效价测定法。
4.3 HPLC法和生物效价测定法测定企业缩宫素样品的效价比较 分别在“2.1”和“2.2”项方法下对本研究的8个企业100批次的试验样品进行测定后比较,结果显示,两种方法检测的缩宫素含量除两家药企外,其他企业生产的缩宫素差异无统计学意义(P>0.05),见表1,将两者进行Pearson检验显示,两者差异有统计学意义(r=0.624,P<0.05)。

表1 两种方法的含量测定结果比较
4.4 缩宫素注射剂长期稳定性分析 将2013年和2014年国家评价性抽验缩宫素注射液留样通过“2.2”项方法进行检测,同该企业最新生产的缩宫素注射剂含量水平进行比照发现,2013年生产的缩宫素注射剂有效成分含量明显降低(P=0.025),但2014年生产的制剂含量与2015年生产的制剂含量比较差异无统计学意义(P=0.419),表明该制剂存在长期贮存效价降低的风险。
5 讨论
《中国药典》中现行的缩宫素注射剂含量测定标准中,以大鼠离体子宫收缩为实验基础,操作较复杂,且试验周期长,人为因素造成的误差较大,对操作人员的要求高,且重复性欠佳[5]。这些问题如果得不到有效解决,会对企业在药物生产时出现投料偏差的问题,导致药物整体质量和效果达不到临床要求,造成患者治疗的延误[6-9]。随着HPLC技术以及检验设备的不断优化,越来越多的政府药检机构及药物生产企业开始使用该法来实现药物的质量控制,由于该法操作简单,灵敏度和专属性强,只要操作人员严格按照操作流程执行,其结果一般较为客观准确,并且可重复性好[10]。
本研究显示,HPLC法同药典中传统的生物效价测定法对本组宫缩素注射剂样品的检测结果差异不大,而结合该法的其他优越性,有必要将药典中的标准质量检测方法更换。其次,通过HPLC法检测8家药企共100个批次的缩宫素注射剂质量发现,有2家企业通过这两种方法测得的缩宫素质量差异较大,其余企业产品差异无统计学意义,这可能与用到的动物个体之间存在差异较大或者人为误差等导致。另外,本研究对缩宫素注射剂贮存稳定性进行检测后发现,该药物(10~20 ℃,相对湿度30%~50%)2年后其效价均不同程度较低,提醒临床使用该药物时,应注意生产日期,对于2年以上的该药物,应尽量避免给患者使用。
综上所述,应用HPLC法测定缩宫素注射剂,具有灵敏度高、专属性强、灵敏度高、准确性好、操作简单等优点,本研究为宫缩素质量控制水平的提高具有一定的价值。
[1] 王庆祥,吴丽美,赵俊林,等.预注小剂量间羟胺对缩宫素所致剖宫产产妇血流动力学变化的影响[J].临床麻醉学杂志,2015,31(4):326-328.
[2] 姜广利,王保莲,杨颖,等.缩宫素鼻喷雾剂对排乳的影响[J].现代临床医学,2011,37(3):177-178.
[3] 李海芳,钱德明.缩宫素生物效价测定实验的几点体会[J].中国药品标准,2008,9(4):247-249.
[4] 谷舒怡,黄坚,唐黎明.长效缩宫素的生物效价测定方法研究[J].药物分析杂志,2016,36(1):165-170.
[5] 国家药典委员会.中国药典 [S].北京:中国医药科技出版社,2015:1074.
[6] 李海芳,耿文宁,闫明俞.缩宫素注射液效价测定的不确定度评定[J].中国药房,2015,26(5):2575-2578.
[7] 黄青,张婷,陆益红,等.HPLC法测定缩宫素注射液中三氯叔丁醇的含量及其应用[J].中国药品标准,2014,15(6):413-416.
[8] 蔡婷婷,单荣芳,赵娜萍,等.药物临床试验质量控制中发现的问题及改进措施[J].实用药物与临床,2014,17(9):1210-1213.
[9] 曹雨,孔毅,张聪颖,等.HPLC测定缩宫素原料药的含量[J].华西药学杂志,2013,28(4):412-414.
[10] 李松涛,赵红玲,高杨,等.缩宫素的制备[J].中国医药工业杂志,2015,46(1):7-9.
A comparative study on the quality control of oxytocin injection by HPLC and BA
XU Rong
(DepartmentofPharmacyandMedicalTechniques,NantongHealthHigherOccupationTechnicalSchool,Nantong,Jiangsu226000,China)
Objective To compare the advantages and disadvantages of HPLC and BA which control the quality of oxytocin injection.Methods We selected 100 batches of oxytocin injection which were produced by 8 enterprises,chose HPLC and BA to measure the samples and compared the test results.Results Differences between the two methods for detecting the oxytocin levels in oxytocin injection produced by two companies were significant (P=0.027,P=0.011),while differences among other oxytocin injection manufacturers were not statistically significant (P=0.556,0.637,0.614,0.559,0.315,0.429).The oxytocin injection content of 8 pharmaceutical companies were within 55.9%~126.1%,averaged 98.5%.The contents of oxytocin injection produced by three enterpriseswere relatively low.After 2 years of storage,the titer of oxytocin injection was significantly decreased with statistically significant difference (P=0.025).Conclusions HPLC used to determine oxytocin injection is relatively simple,sensitive and accurate,which can not only effectively avoid the error due to individual differences of BA,but also control human error of determination within a small range.Besides,the best storage duration for oxytocin injection is 2 years.
Oxytocin;HPLC method;Quality control;Stability
10.3969/j.issn.1009-6469.2016.10.014
2016-06-15,
2016-07-19)
