顶空毛细管气相色谱法测定奥格列汀中有机溶剂残留量
2016-12-07郑飞华国栋项颖张彦丽张谦张超
郑飞,华国栋,项颖,张彦丽,张谦,张超
(北京中医药大学东方医院药学部,北京 100078)
顶空毛细管气相色谱法测定奥格列汀中有机溶剂残留量
郑飞,华国栋,项颖,张彦丽,张谦,张超
(北京中医药大学东方医院药学部,北京 100078)
目的 观察顶空毛细管气相色谱法(GC)测定奥格列汀原料药中乙醇、乙酸乙酯、甲苯3种残留溶剂的效果。方法 采用GC法进行残留溶剂测定。色谱柱采用DB-5弹性石英毛细管气相色谱柱,规格为50 m×0.32 mm×0.6 μm;进样口温度为150 ℃,分流比1∶10;柱温程序为首先在40 ℃下保持6 min,再以每分钟15 ℃的速率升温至180 ℃;仪器配有氢火焰离子化检测器(FID),检测器温度为240 ℃;载气为高纯氮气,流速为恒流1 mL·min-1;取0.2 mL顶部平衡气体进样。顶空条件为:N,N-二甲基甲酰胺(DMF)为溶剂,溶液浓度200 g·L-1,加热时间30 min,加热器温度100 ℃,传输线温度105 ℃。结果 在相应色谱条件下,各残留溶剂均可基线分离。测得乙醇、乙酸乙酯、甲苯分别在10.06 ~2 012 mg·L-1、10.10 ~2 020 mg·L-1、1.78 ~356 mg·L-1范围内线性关系良好。乙醇、乙酸乙酯和甲苯的平均回收率分别为97.91%(n=9)、96.48%(n=9)、95.58%(n=9)。乙醇、乙酸乙酯、甲苯三种溶剂日内精密度RSD分别为2.13%(n=6)、4.84%(n=6)、5.41%(n=6),日间精密度RSD分别为1.98%(n=12)、4.51%(n=12)、5.09%(n=12)。结论 GC法操作简便、重现性好、结果准确可靠,可以用于奥格列汀原料药中残留溶剂的测定。
奥格列汀原料药;有机溶剂残留;顶空气相色谱法
奥格列汀(Omarigliptin)是美国默沙东公司开发的糖尿病治疗药物。奥格列汀每周只需口服一次,可产生持续的二肽基肽酶-4(DPP-4)抑制作用,增加了患者的适应性。奥格列汀具有全新的降血糖机制,其作用机制是通过抑制体内DPP-4酶对胰高血糖素样肽-1(GLP-1)的降解作用,延长GLP-1的作用时间,从而提高血液中内源性GLP-1和葡萄糖依赖性促胰岛素释放肽(GIP)的浓度,并最终改善血糖控制。同时其具有不增加体质量、不会引起低血糖反应、不会引起水肿等优越性[1-5]。
在制备奥格列汀过程中使用了多种有机溶剂,包括乙醇、乙酸乙酯、甲苯。过量摄入有机溶剂对人体有害,因此中国药典规定了原料中有机溶剂的限量。本研究参考有关文献[6-7]建立了顶空毛细管气相色谱法(GC)对3批奥格列汀存在的乙醇、乙酸乙酯、甲苯残留溶剂进行测定,现报告如下。
1 仪器与试药
1.1 仪器 本研究采用GC-2014型气相色谱仪(日本岛津公司),色谱仪配有FID检测器和顶空进样器。色谱过程所用载气为高纯氮气,检测器所用的氢气和空气均为发生器自制。色谱过程中使用色谱柱为DB-5型弹性石英毛细管气相色谱柱(美国安捷伦公司),规格为50 m×0.32 mm×0.6 μm。称重所用天平为XS5型分析天平(瑞士梅特勒托利多公司)。
1.2 试药 奥格列汀为企业自制(原料药,纯度大于99.5%,批号20150921,20151015,20151225,由南京丰特药业有限公司提供);乙醇、乙酸乙酯、甲苯、N,N-二甲基甲酰胺(DMF)均为色谱纯,购自Merck公司。
2 方法结果
2.1 色谱条件 色谱柱:DB-5弹性石英毛细管气相色谱柱(50 m×0.32 mm×0.6 μm);进样口温度:200 ℃,分流比1∶10;柱温程序:起始温度40 ℃保持6 min,再以每分钟15 ℃的速率升温至180 ℃;检测器:FID检测器,检测器温度:250 ℃;载气:N2,恒流:1 mL·min-1;进样量:0.2 mL顶部平衡气体。顶空条件如下: DMF为溶剂,溶液浓度200 g·L-1,加热时间30 min,加热器温度100 ℃,传输线温度105 ℃。
2.2 溶液的配制 取乙醇500 mg,精密称定,置于50 mL洁净容量瓶中,迅速加DMF溶解并稀释至刻度,得乙醇对照品储备溶液。同法制得乙酸乙酯储备、甲苯对照储备溶液。乙醇储备液、乙酸乙酯储备液、甲苯储备液浓度分别为10.06、10.10、1.78 g·L-1。精密量取乙醇、乙酸乙酯、甲苯储备液各0.1 mL,置同一100 mL容量瓶中,用DMF稀释至刻度,摇匀,作为相当于限度浓度1%的对照品工作溶液。同法分别量取0.5、1、2.5、5、10、20 mL作为5%、10%、25%、50%、100%、200%的系列对照品工作溶液。取奥格列汀自制品(批号:20150921)2 000 mg,精密称定,置10 mL容量瓶中。加入适量DMF,微微振摇使溶解并用DMF稀释至刻度,摇匀,作为供试品溶液。
2.3 系统适用性试验 精密量取“2.2” 项下100%对照品溶液2 mL置于顶空瓶中,迅速密封瓶口,按“2.1”项下色谱条件进行测定,记录色谱图,色谱图见图1。其中乙醇、乙酸乙酯、甲苯的保留时间分别为3.991、5.059、9.432 min,各对照品之间分离度均大于1.5,计算理论塔板数均大于10 000。从空白样品中可以看出DMF对测定无干扰。表明该法专属性良好。
2.4 线性关系 分别精密移取“2.2”项下系列对照品溶液2 mL置于顶空瓶中,迅速密封瓶口,按“2.1”项下色谱条件进行测定。分别以各溶剂的峰面积为纵坐标(Y),浓度为横坐标(X),进行线性回归。线性回归结果为:乙醇在10.06 ~2 012 mg·L-1范围内线性方程为Y=1 827X+356(r=0.999 7);乙酸乙酯在10.10 ~2 020 mg·L-1范围内线性方程为Y=13 489X-5 341(r=0.999 4);甲

A.对照品
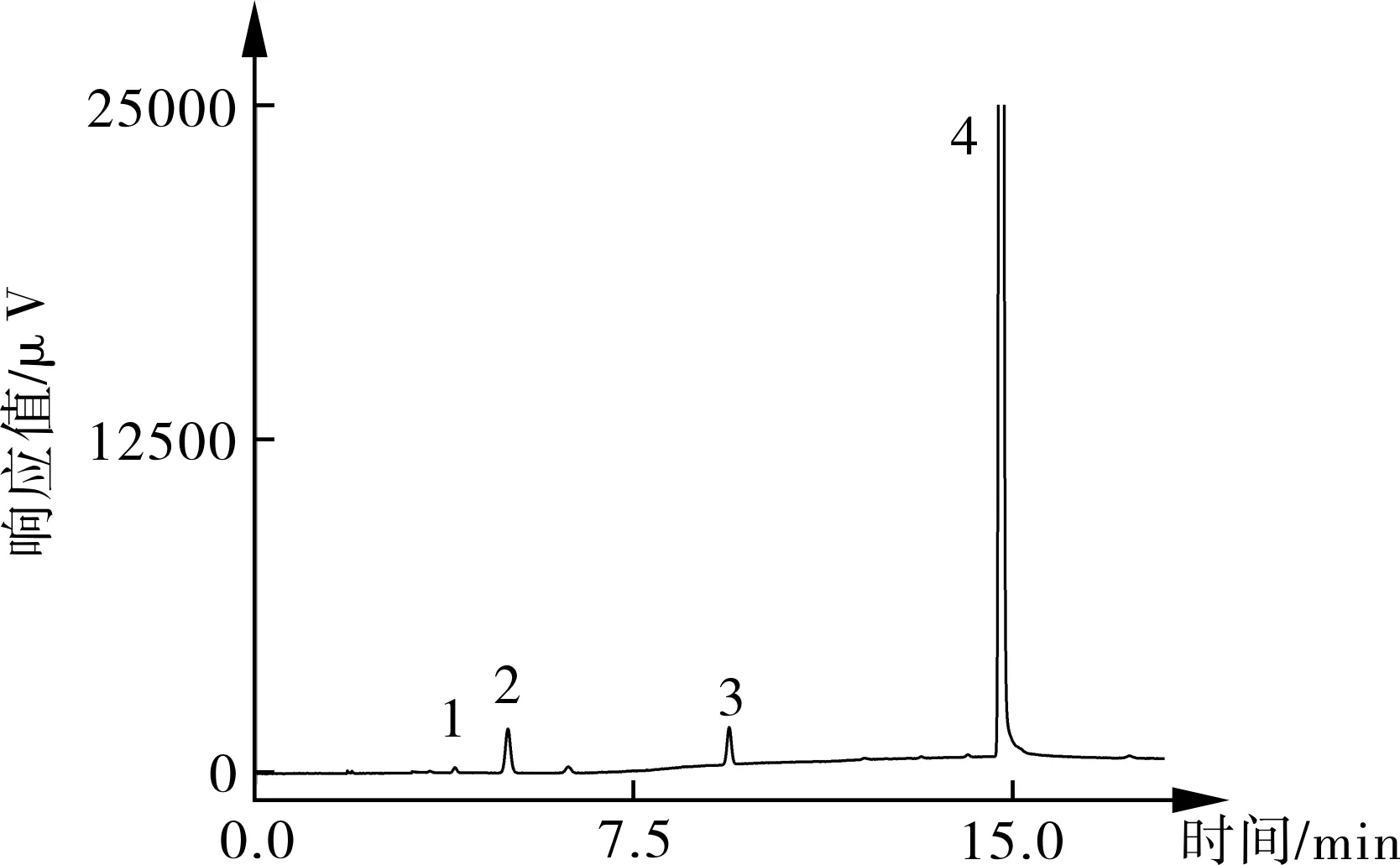
B.供试品
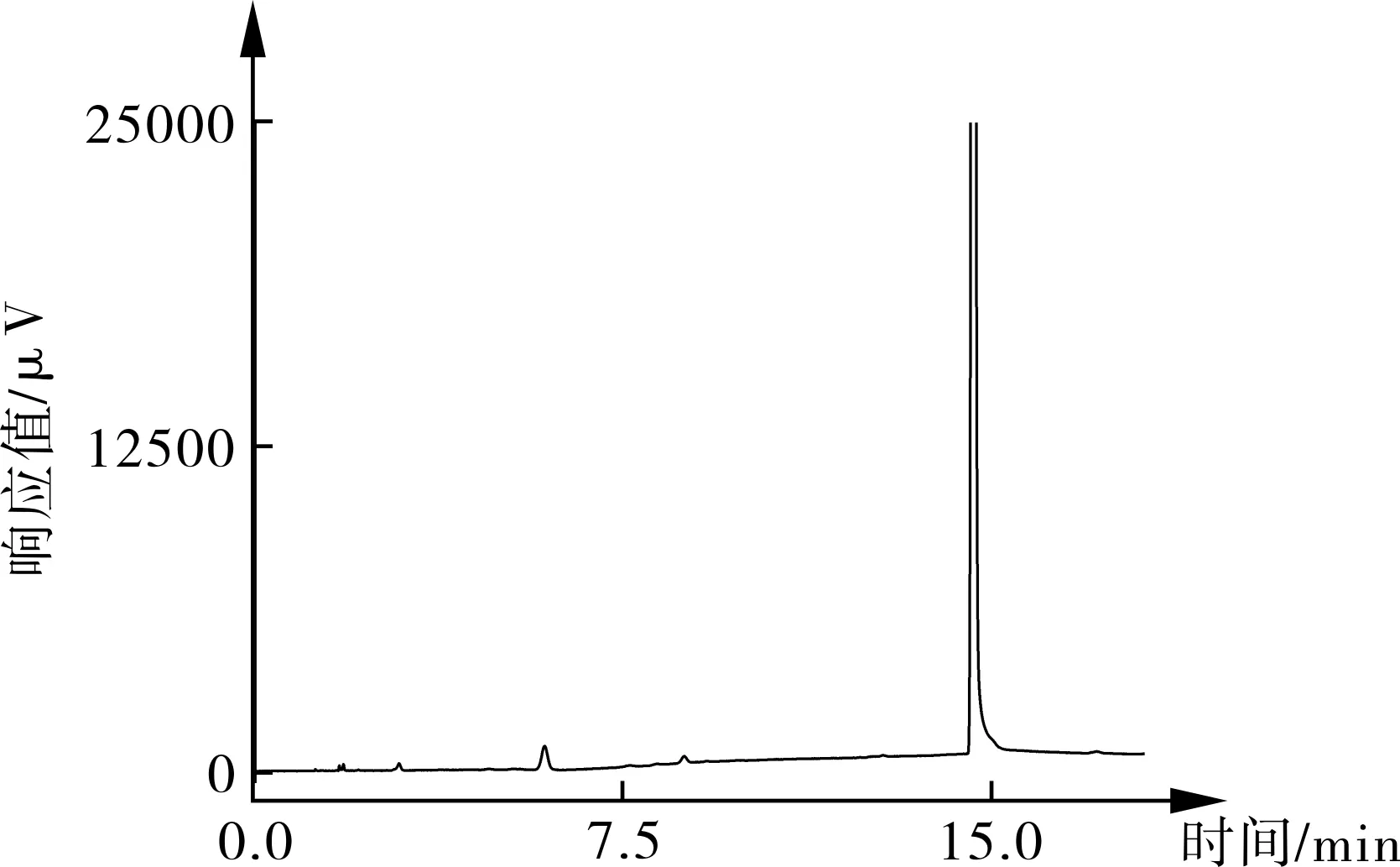
C.空白样品
注:1.乙醇;2.乙酸乙酯;3.甲苯;4.DMF。
图1 气相色谱图
苯在1.78~356 mg·L-1范围内线性方程为Y=65 829X-2 758(r=0.999 5)。结果表明,乙醇、乙酸乙酯、甲苯分别在10.06~2 012 mg·L-1、10.10 ~2 020 mg·L-1、1.78 ~356 mg·L-1范围内线性关系良好。
2.5 回收率 取奥格列汀自制品(批号:20150921)2 000 mg,精密称定,置于10 mL容量瓶中。再从“2.2”项下对照品储备液中分别精密量取0.8 mL放入奥格列汀自制品容量瓶中,用DMF稀释至刻度,摇匀,精密量取2 mL置于顶空瓶中,密封瓶口,作为80%回收率的溶液。同法称量2 000 mg自制品分别加入1.0、1.2 mL对照品储备液制备100%、120%的加样回收测定溶液。将各加样回收溶液按“2.1”项下色谱条件进行测定,使用外标法定量。计算得乙醇回收率为97.91%,RSD为1.54%(n=9);乙酸乙酯的回收率96.48%,RSD为2.60%(n=9);甲苯的回收率95.58%,RSD为3.74%(n=9)。具体数据见表1。
2.6 仪器精密度 精密量取“2.2”项下100%对照品溶液2 mL置于顶空瓶中,迅速密封瓶口,按“2.1”项下色谱条件将同一溶液重复测定6次,计算各溶剂色谱峰面积的RSD。结果表明乙醇、乙酸乙酯、甲苯的峰面积RSD分别为1.3%、0.8%、0.6%。结果表明仪器精密度良好。
2.7 日内精密度和日间精密度 取奥格列汀自制品(批号:20150921)2 000 mg,精密称定,按“2.2”项下方法进行处理,共处理12份,分别按“2.1”项下色谱条件进行测定,当日测定6份、隔日测定6份,外标法计算各残留溶剂含量。测得日内精密度结果为:乙醇的平均含量为0.021%,RSD为2.13%(n=6);乙酸乙酯的平均含量为0.052%;RSD为4.84%(n=6),甲苯的平均含量为0.0083%,RSD为5.41%(n=6)日间精密度结果为:乙醇的平均含量为0.020%,RSD为1.98%(n=12);乙酸乙酯的平均含量为0.052%;RSD为4.51%(n=12),甲苯的平均含量为0.0082%,RSD为5.09%(n=12)。

表1 回收率测定结果(n=9)
注:回收率(%)=(测得量-原料药中所含溶剂量)/加入量×100%。
2.8 检测限和定量限 精密移取“2.2”项下乙醇储备液80 μL、乙酸乙酯储备液10 μL、甲苯储备液10 μL,至同一10 mL容量瓶中,用DMF定容,摇匀,再逐级稀释制成测定溶液。分别取各测定溶液2 mL,置顶空瓶中,立即密封,按“2.1”项下色谱条件检测,并计算信噪比。当信噪比为10∶1时的样品浓度为定量限,此时乙醇浓度为5.04 mg·L-1,乙酸乙酯浓度为0.63 mg·L-1,甲苯浓度为0.11 mg·L-1。当信噪比为3∶1时的样品浓度为检测限,此时乙醇浓度为1.68 mg·L-1,乙酸乙酯浓度为0.21 mg·L-1,甲苯浓度为0.04 mg·L-1。
2.9 样品测定 取3批自制品各2 000 mg,精密称定,按“2.2”项下供试品溶液制备项下方法进行处理,按“2.1”项下色谱条件下进行测定,色谱图见图1,按照外标法计算各溶剂的含量,结果见表2。

表2 三批样品溶剂残留量/(%,n=3)
3 讨论
3.1 气相色谱条件的选择和优化 药典中提倡使用水作为溶解样品的溶剂,但是乙酸乙酯在水中溶解度较小,且奥格列汀水中溶解性较差,因此未选用水作为溶剂来溶解样品。经过尝试多种溶剂后发现,DMF可以充分溶解奥格列汀自制品和三种待测溶剂,同时DMF在相应溶剂位置无保留,因此选择DMF可以得到良好的专属性。
选定溶剂后,紧接着考察了顶空加热时间。分别考察加热时间为20、30、40、50 min时各个溶剂的挥发量。发现各溶剂在30 min时峰面积已经达到平台期,实验结果表明30 min后瓶中气体挥发已经达到了平衡,因此选择30 min作为顶空加热的时间。本试验中待测残留溶剂沸点相差大,故选择程序升温。经摸索,确定升温程序为起始柱温40 ℃保持6 min,再以每分钟15 ℃的升温速率升至180 ℃。使用该条件可以缩短检测时间,提升试验效率。
3.2 溶剂残留量 根据《中国药典》2015年版四部附录0861项残留溶剂测定法规定[8],原料药中乙醇、乙酸乙酯、甲苯的含量分别不得超过0.5%、0.5%、0.089%。经测定,三批奥格列汀自制品的溶剂残留均远小于药典规定限度。本方法中三种溶剂的检测浓度和定量浓度均远低于药典规定,方法学中精密度、线性等各项均符合药典相应规定,以上结果表明该方法用于测定奥格列汀中溶剂残留重现性好、结果准确可靠。
[1] Tesfaye B,Ranabir S R,Ping C,et al.Omarigliptin (MK-3102):a novel long-acting DPP-4 inhibitor for once-weekly treatment of type 2 diabetes[J].Journal of Medicinal Chemistry,2014,57(8):3205-3212.
[2] Sheu WH,Gantz I,Chen M,et al.Safety and efficacy of omarigliptin (MK-3102),a novel once-weekly DPP-4 inhibitor for the treatment of patients with type 2 diabetes[J].Diabetes Care,2015,38(11):2106-2114.
[3] Chen P,Feng D,Qian X,et al.Structure-activity-relationship of amide and sulfonamide analogs of omarigliptin[J].Bioorganic & Medicinal Chemistry Letters,2015,25(24):5767-5771.
[4] Burness CB.Omarigliptin:First global approval[J].Drugs,2015,75(16):1947-1952.
[5] Addy C,Tatosian D,Glasgow XS,et al.Pharmacokinetic and pharmacodynamic effects of multiple-dose administration of omarigliptin,a once-weekly dipeptidyl peptidase-4 inhibitor,in obese participants with and without type 2 diabetes mellitus[J].Clinical Therapeutics,2016,38(3):516-530.
[6] 谢嵩,徐济萍,杨磊.顶空气相色谱法测定苯甲酸阿格列汀原料药中3种有机溶剂残留量[J].中国药房,2015,26(9):1269-1271.
[7] 姜建国,宋更申,张西如,等.顶空气相色谱法测定洛伐他汀原料药中的有机溶剂残留量[J].中国药房,2011,22(17):1607-1608.
[8] 国家药典委员会.中国药典(四部)[S].北京:中国医药科技出版社,2015:附录0861项.
Determination of residual organic solvents in omarigliptin by headspace gas chromatography
ZHENG Fei,HUA Guodong,GONG Ying,et al
(DepartmentofPharmacy,DongfangHospitalofBeijingUniversityofTCM,Beijing100078,China)
Objective To establish a method to determine residual solvents in omarigliptin bulk drug.Methods The headspace GC was performed with DB-5 capillary column with standard of 50 m×0.32 mm×0.6 μm.The condition of GC was as follows:the inlettemperature was 150 ℃;the injection volume was 0.2 mL with separation ratio of 1∶10;the column temperature was programmed with an initial temperature below 40 ℃,maintained for 6 min,then raised to 180 ℃ with a rate of 15 ℃·min-1,and maintained for another 5 min.The detector was equipped with FID with a temperature of 240 ℃.The carrying gas was N2with the flow rate of 1 mL·min-1.DMF was used as solvent for omarigliptin with the concentration of 200 g·L-1.The solution was heated at 100 ℃ for 30 mins.The temperature of transferring line was 105 ℃.Results All solvents can be separated completely with good linear relationship in the range of 10.06 ~2 012 mg·L-1(ethanol), 10.10 ~2 020 mg·L-1(ethyl acetate) and 1.78 ~356 mg·L-1(toluene).The average recoveries of ethanol,ethyl acetate and toluene were 97.91% (n=9),96.48% (n=9),and 95.58% (n=9) respectively.Conclusions All the results demonstrate that this method is simple,reproducible and accurate enough for the determination of residual solvents in omarigliptin bulk drug.
Omarigliptin;Residual organic solvent;Headspace GC
华国栋,男,主任药师,研究方向:中药学,临床药学,药事管理,E-mail:zhaojhuagd@126.com
10.3969/j.issn.1009-6469.2016.10.012
2016-06-13,
2016-08-08)
