微电流作用下锌板电置换提镉新工艺
2016-12-07何静王夏阳叶龙刚张家玮杨建广戚春萍
何静,王夏阳,叶龙刚,张家玮,杨建广,戚春萍
(中南大学 冶金与环境学院,湖南 长沙,410083)
微电流作用下锌板电置换提镉新工艺
何静,王夏阳,叶龙刚,张家玮,杨建广,戚春萍
(中南大学 冶金与环境学院,湖南 长沙,410083)
为解决传统锌粉置换提镉流程复杂、锌粉消耗大和镉绵纯度低的难题,提出以锌板作阳极,钛网为阴极,在微电流作用下置换海绵镉的工艺,考察电流密度、温度、pH及极距等因素对电置换效率的影响。研究结果表明:在电流密度为0.5 mA/cm2,极距为3 cm,pH为1.0和温度为40 ℃的条件下,提镉率可达96%以上,镉绵纯度达97%以上,在此条件下获得的海绵镉为六方晶系,是层片状正六方形的树枝状晶体。随着电流密度增大、温度升高以及pH降低,提镉率都有不同程度地增大,而极距对提镉率的影响不明显。
微电流;锌板;电积;置换;海绵镉
镉作为一种重有色金属,因其柔软及富延展性,且表面易氧化,易切削加工,在镀镉、制造合金、颜料、塑料稳定剂、电池等方面得到广泛的应用[1−2]。镉在自然界没有独立的矿床,常伴生于铅锌矿中,是铅锌冶炼生产的副产品,约95%的镉从铅锌生产过程中被回收[3]。随着铅锌冶炼技术的迅速发展以及对环境影响的重视,镉的回收在铅锌冶炼中具有重要的意义。湿法炼锌厂每年都会产出大量的铜镉渣,一般含Cd质量分数为5%~10%,Cu质量分数为2%~5%,Zn质量分数为28%~50%[3],铜镉渣经酸浸后,除铜得到含镉料液,其处理方式有锌粉置换[4−7]、氨法提镉[8−11]、萃取分离锌镉[12−14]、电积等,其中锌粉置换的方法应用最为广泛。传统的锌粉置换存在很多问题,如:制得的海绵镉疏松,表面容易吸附锌粉且难于洗净夹带的杂质;搅拌使海绵镉聚集成团,易把锌粉包夹在海绵镉颗粒内,得到的海绵镉纯度较低。由于在锌粉置换过程中易产生包容现象,锌粉的反应并不完全,造成锌粉使用量大,海绵镉品位(即质量分数)低,不能满足一般电镉生产的质量要求。锌粉置换反应中搅拌速度对锌置换率的影响较大,搅拌器的搅拌速度越快锌的置换率越高,但搅拌速度过快对搅拌桨的要求也比较高[15],同时,由于两段置换流程复杂,难以避免操作中的金属损失,并会对周围的水域、土壤等造成一定程度的污染[16−18]。本工艺以锌板为阳极,以钛网为阴极,在微电流作用下电置换提取镉绵。本工艺采用低电流密度强化置换过程,简化流程,避免了工艺过程中镉的损失,降低其对环境的威胁并制得纯度达96%以上的镉绵产品。除此之外,用锌板置换代替以往的锌粉置换,锌电积得到的锌板表面活性大,可直接用于置换镉,从而降低了成本。本工艺适用于湿法炼锌中铜镉渣的处理,操作简单且成本较低,为工业化生产提供参考。
1 试验
1.1试验原料和方法
本试验采用的原料为镉绵堆浸氧化造液,原料来源为湖南水口山冶炼厂,其主要成分如表1所示。由表1可见:试液中主要含镉和锌,还有少量锰、铁、铋等杂质。
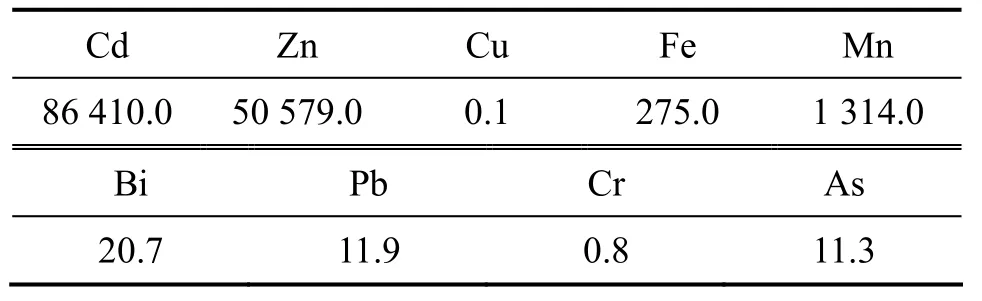
表1 镉绵堆浸造液的主要元素质量浓度Table 1 Mass concentrations of main elements in sponge cadmium heap leaching liquid mg/L
试验采用微电流作用下强化置换的方法,以提高锌的置换率和海绵镉纯度。本工艺的原则流程如图1所示。

图1 锌板微电流作用下电置换提镉原则流程图Fig. 1 Principle flow chart of cadmium electracting using zinc plate under micro current
具体试验步骤为:量取400 mL料液于500 mL烧杯中,置于恒温磁力搅拌器中加热到指定温度,以锌板为阳极,钛网为阴极,阴极板与阳极板长×宽均为75 mm×130 mm,其中阴极钛网网孔直径为5 mm。通电后,每隔一段时间刮下阴阳极板上的沉积物,测量此时电解液的体积后,取少量电解液分析其中的Zn和Cd的质量分数,电解结束后将电解液过滤,再分析电解后液的Zn和Cd的质量分数,同时分析渣中Cd的质量分数。
样品中化学成分用IRIS IntrepidⅡ电感耦合等离子体发射光谱仪(ICP)进行分析;用Rigaku D/Max 2500型X线衍射仪(XRD)分析镉绵中的物相;镉绵表面形貌用JSM−5600LV型扫描电镜(SEM)进行分析。
1.2试验原理
本文所提工艺为在微电流作用下在电解槽中进行的置换反应,主要过程在阳极完成,涉及置换和电溶解2个过程。置换过程的机理是用较活泼的金属插入到含活泼性相对较小的金属离子溶液中,即形成原电池。根据原电池理论,还原剂锌在负极上失电子发生氧化反应,形成锌离子进入溶液,而溶液中的镉离子得电子发生还原反应,生成金属镉。在锌板表面形成被置换金属覆盖的表面区,随着置换反应和电积反应的进行,阳极发生氧化反应,释放电子,正电荷自阳极进入溶液,主要发生以下反应:Cd2++Zn=Zn2++Cd。而电溶解则是锌板在流入电子时发生的氧化还原,Zn−2e=Zn2+,使锌板不断地溶解,从而露出新的锌表面,使反应不断进行。同时,在阴极由于电流的作用会发生电积反应,Cd,Zn,Fe,Cu,Bi,Sb,Pb和Cr等金属离子都可能析出。
表2所示为在298.15 K下水溶液中某些电极的标准电极电势[19],可初步估计电解过程中各种金属离子在阴极上放电析出的先后顺序。但由于电流强度较小,实际在阴极析出的金属是微量的。
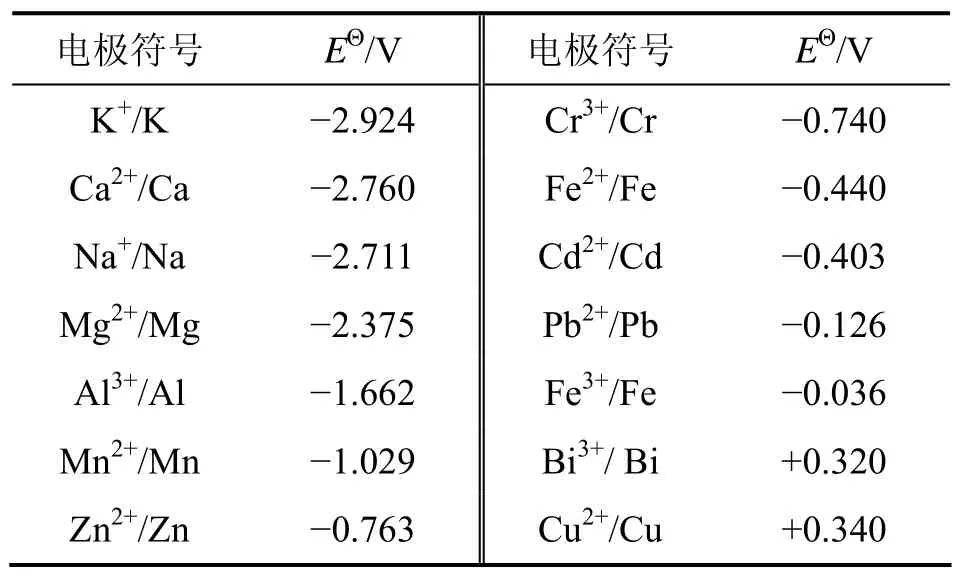
表2 298.15 K下水溶液中某些电极的标准电极电势EΘTable 2 Standard electrode potential of electrode in aqueous solution under 298.15 K
根据各金属/金属离子的标准电极电势及其在实际溶液中离子浓度,对电解液杂质离子的实际反应电极电势可用下式计算:

溶液中Cd2+的质量浓度为10~100 g/L,得Cd2+/Cd的电极电势与其电极电势相近的Fe2+在此条件下不会被置换,而比Cd2+电极电势高的离子如Pb2+,Fe3+和Cu2+则会被置换出来,但由于这几种元素在溶液中质量分数极低,其影响可忽略不计。
2 试验结果及讨论
2.1电流密度对提镉效率的影响
在体系温度为25 ℃,极板间距为3 cm,电解液体积为400 mL,总反应时间为480 min的条件下,考察电流密度分别为0.1,0.5,1.0和3.0 mA/cm2时电解过程中提镉率随时间的变化,结果如图2所示。
由图2可知:在反应时间相同的条件下,当电流密度大于0.5 mA/cm2时,提镉率随电流密度的增大幅度较小,但均较电流密度为0.1 mA/cm2条件下所得的提镉率增大明显;反应480 min后,提镉率均达到了95%,镉的置换率相差较小,且随试验时间的延长,提镉率慢慢趋于平稳。由于本试验要求在微电流的条件下反应,且电流密度越大,耗电量越大,溶液蒸发量越大,副反应的影响也越大,故决定采用电流密度为0.5 mA/cm2进行后续试验。

图2 不同电流密度下提镉率与时间的关系Fig. 2 Relationship between cadmium rate and time under different current densities
2.2极距对提镉效率的影响
在体系温度为25 ℃,电解液体积为400 mL,电流密度为0.5 mA/cm2,总反应时间为480 min的条件下,考察极距分别为3,5和7 cm时,电解过程中提镉率随时间变化,结果如图3所示。

图3 不同极距条件下提镉率与时间的关系Fig. 3 Relationship between cadmium rate and time under conditions of different pole pitches
由图3可知:在120~360 min内,当反应时间相同时,极板间距减小提镉率略有升高,但升高幅度较小;当反应480 min后,不同极距的电置换提镉率均达95%;因此,极距对镉的电置换影响较小,选择合适的极距主要考虑试验中与其他因素的相互协调,本试验选择极距为3 cm作为综合试验的条件。
2.3温度对提镉率的影响
在极板间距为3 cm,电解液体积为400 mL,电流密度为0.5 mA/cm2,总反应时间为240 min的条件下,考察温度分别为25,40和60 ℃时,电解过程中提镉率随时间的变化,结果如图4所示。
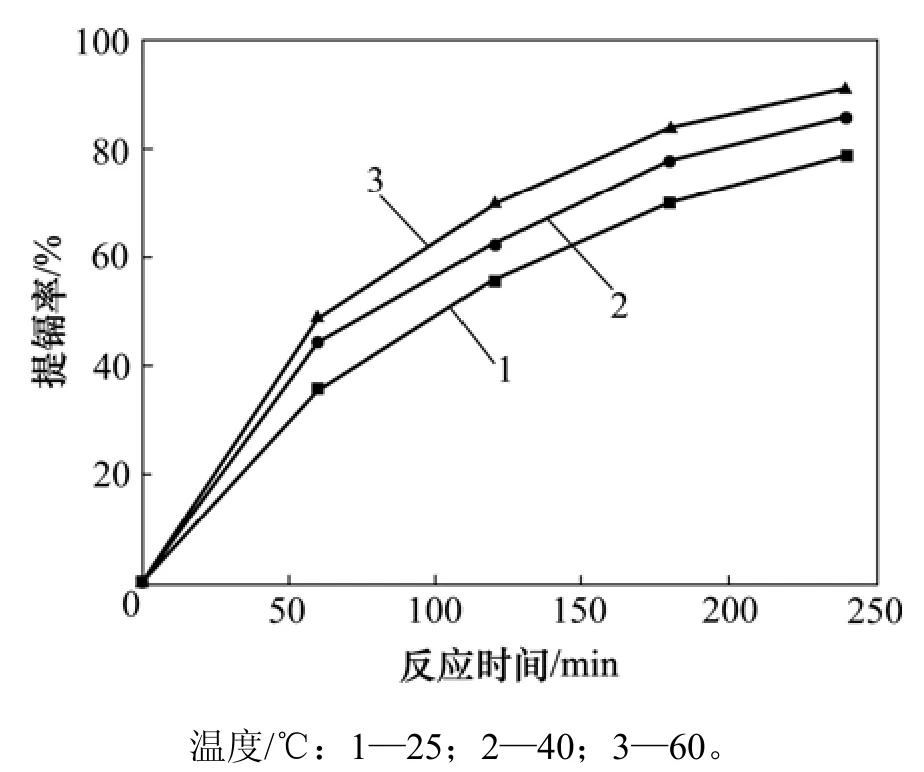
图4 不同温度下提镉率与时间的关系Fig. 4 Relationship between cadmium rate and time under different temperatures
由图4可知:温度对镉的置换有明显的影响,随温度的升高,镉置换率明显增大。这是由于温度升高,加快了电解液中镉离子的运动,同时加速了锌板表面的溶解,从而使溶液中镉浓度成分均匀,促进镉的置换。在反应时间相同,且当反应温度分别为25,40和60 ℃时,镉的置换率呈增长趋势。反应240 min后,镉的置换率均超过78%,当温度为40 ℃和60 ℃时,提镉率均达85%以上,且差距较小,但当温度为60 ℃时,反应消耗的能量多,溶液蒸发量大,消耗锌板多。因此,试验温度为40 ℃较适宜。
2.4pH对提镉率的影响
在极板间距为3 cm,电解液体积为400 mL,电流密度为0.5 mA/cm2,反应时间为480 min的条件下,考察反应溶液pH分别为4.5,3.0,2.0和1.0时电解过程中提镉率随时间变化,结果如图5所示。
由图5可知:随pH的降低,镉的置换率逐渐增大。当pH保持不变时,随着反应的进行,镉的置换率会随着时间的延长而增加,但当反应进行360 min后,镉的置换速率略有下降。与pH为4.5,3.0和2.0条件下相比,pH为1.0时所得的提镉率最大。这是因为此时的酸度大,加快了锌板表面锌的溶解,使更多新的锌表面露出,从而提高镉的置换率,但酸度太高对生产过程不利,因此,综合试验pH选为3.0。

图5 不同pH下提镉率与时间的关系Fig. 5 Relationship between cadmium rate and time under different pH
3 海绵镉的表征
根据单因素试验,得最优试验条件如下:极板间距为3 cm,电流密度为0.5 mA/cm2,温度为40 ℃,溶液pH为3.0,以锌板为阳极,钛网为阴极,反应时间为480 min。在此条件下进行了3次综合试验。将电置换得到的镉绵在抽滤洗涤后烘干24 h,磨料、过74 μm筛分后并进行ICP全分析、XRD检测以及SEM分析,并对电置换残液进行ICP全分析。
3.1综合试验结果
试验结果如表3所示。由表3可见:在最优条件下,料液中镉质量浓度由86.41 g/L分别降至2.89,3.07及2.22 g/L,锌由50.58 g/L提高到97.80 g/L以上,锌的质量浓度接近电锌溶液的锌质量浓度,因此,该溶液经净化后可直接进行电积提锌;同时,电置换获得的镉绵品位分别达到98.9%,99.1%和97.8%,而主要杂质锌的质量分数均低于0.1%。
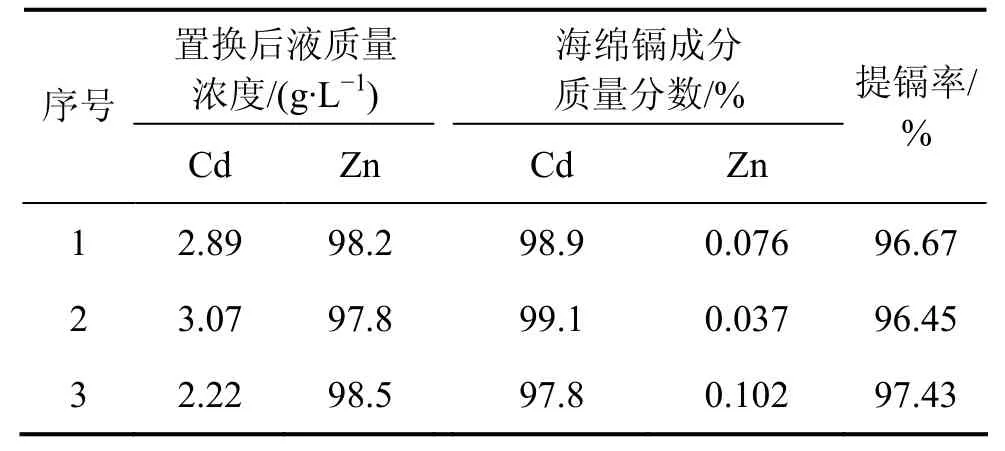
表3 综合试验结果Table 3 Results of comprehensive experimental
由表3可知:锌板在微电流作用下电置换提镉率达96.4%以上,较传统的锌粉置换提镉有更好的效果,同时得到更纯的产品。其中,1号试验的电置换残液成分如表4所示,海绵镉全分析结果如表5所示。

表4 1号电置换残液的化学成分(质量浓度)Table 4 Compositions of No.1 electric displacement residual liquid mg/L
由表1和表4可以看出:在微电流作用下,电置换反应后溶液中Zn质量浓度增加到98.2 g/L,而Fe,Bi,Pb,Cr和As等杂质元素的离子质量浓度均有不同程度的下降,Mn浓度则变化不大,这是由于反应以置换为主,在锌板电置换镉时,其他电极电势比锌正的元素也会析出,导致其相对质量浓度的下降。
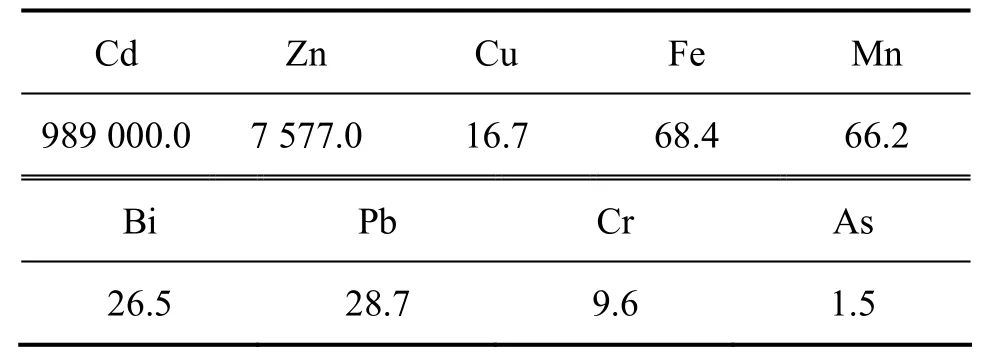
表5 1号海绵镉的化学成分(质量分数)Table 5 Compositions of No.1 sponge cadmium μg/g
由表5可以看出:电置换获得的海绵镉纯度比传统锌粉置换的海绵镉的高,达到了98.9%,杂质质量分数相对较小。
3.2XRD表征
对1号海绵镉进行XRD检测,如图6所示。由图6可见:产品中主要存在的成分为元素Cd,其余还有少量的Cd(OH)2,可能是由于Cd2+的水解产生。
3.3SEM表征
将锌板在微电流作用下电积提镉得到的产品海绵镉经过滤去除水分后,烘干、研磨、过筛后进行电镜扫描分析,结果如图7所示。
由图7可以看出:海绵镉为六方晶系,由层片状的正六方形构成树枝状晶体,由于海绵镉的生长方式为树枝状,避免了锌粉的被包裹以及夹带,从而提高其纯度。

图6 1号海绵镉XRD谱Fig. 6 XRD patterns of No.1 sponge cadmium

图7 海绵镉SEM图Fig. 7 SEM images of sponge cadmium
4 结论
1) 通过单因素试验得出锌板在微电流作用下电积提镉的最佳条件如下:极间距为3 cm,温度为40 ℃,电流密度为0.5 mA/m2,pH为3.0。在此条件下,提镉率可达96%以上,镉绵纯度达97%以上。
2) 电流密度增加、温度升高以及pH降低,均有利于提镉率升高,其中温度对提镉率的影响最显著,而极板间距则影响较小。
3) 镉绵主要组成为金属Cd,电置换得到的海绵镉为六方晶系,由层片状的正六方形构成树枝状晶体。
4) 采用锌板微电流作用电积提镉流程简单,操作简单,对锌材料的要求低,生产成本较低,易于实现工业化。
[1] KIM S H, YOON D S, YOU Y J, et al. In-situ observation of a dendrite growth in an aqueous condition and a uranium deposition into a liquid cadmium cathode in an electrowinning system[J]. Journal of Nuclear Materials, 2009, 385(1): 196−199.
[2] 刘文臣, 张翠丹, 王会轻, 等. 炼钢含锌灰渣提炼锌、镉的工艺研究[J]. 河北冶金, 2015(3): 77−78. LIU Wenchen, ZHANG Cuidan, WANG Huiqing, et al. Process research for extracting zinc and cadmium from zinc-bearing slag in steel making[J]. Hebei Metallurgy, 2015(3): 77−78.
[3] 邵琼, 杜霞, 汪玲, 等. 铜镉渣的回收利用现状[J]. 湿法冶金, 2003, 22(2): 66−68. SHAO Qiong, DU Xia, WANG Ling, et al. Present status of reutilization of copper-cadmium slag[J]. Hydrometallurgy of China, 2003, 22(2): 66−68.
[4] 蒋继穆. 我国锌冶炼现状及近年来的技术进展[J]. 中国有色冶金, 2006, 35(5): 19−23. JIANG Jimu. Current status and recent technical progress of zinc smelting in China[J]. China Nonferrous Metallurgy, 2006, 35(5): 19−23.
[5] ZHOU Ping, LI Dongmei, CHEN Zhuo. Mass transfer process in replacement-column purification device in zinc hydrometallurgy [J]. Transactions of Nonferrous Metals Society of China, 2014, 24(8): 2660−2664.
[6] 汤顺贤, 陈科彤, 万宁, 等. 从铜镉渣中提取海绵镉的试验研究[J]. 矿冶, 2014, 23(5): 65−68. TANG Shunxian, CHEN Ketong, WAN Ning, et al. Study on extraction of sponge cadmium from copper cadmium slag[J]. Mining and Metallurgy, 2014, 23(5): 65−68.
[7] 李剑利. 海绵镉置换过程中的生产控制[J]. 有色矿冶, 2013, 29(1): 39−41. LI Jianli. The production control in the process of the sponge cadmium displacement[J]. Non-ferrous Mining and Metallurgy, 2013, 29(1): 39−41.
[8] 赵效如, 何学斌, 冀晓宏. 铜镉渣浸出工艺改进的研究[J]. 有色冶金, 1998(5): 23−25. ZHAO Xiaoru, HE Xuebin, JI Xiaohong. Study on the modification of soak technics of sediment of copper and cadmium[J]. Nonferrous Metals, 1998(5): 23−25.
[9] 刘海洋, 颜文斌, 石爱华, 等. 从铜镉渣中析出铜锌镉的氧化氨浸工艺[J]. 吉首大学学报(自然科学版), 2010, 31(2): 97−100. LIU Haiyang, YAN Wenbin, SHI Aihua, et al. Research on leaching process of copper, zinc and cadmium from copper-cadmium slag[J]. Journal of Jishou University (Natural Science Edition), 2010, 31(2): 97−100.
[10] GABALLAH I, KANARI N. Recycling policy in the European Union[J]. JOM-Journal of the Minerals Metals and Materials Society, 2001, 53(11): 24−27.
[11] 唐谟堂, 张鹏, 何静, 等. Zn()Ⅱ-(NH4)2SO4·H2O体系浸出锌烟尘[J]. 中南大学学报(自然科学版), 2007, 38(5): 867−872. TANG Motang, ZHANG Peng, HE Jing, et al. Leaching of zinc ash in Zn()Ⅱ-(NH4)2SO4·H2O system[J]. Journal of Central South University (Science and Technology), 2007, 38(5): 867−872.
[12] SOLE K C, HISKEY J B. Solvent extraction characteristics of thiosubstituted organophosphinic acid extractants[J]. Hydrometallurgy, 1992, 30(1): 345−365.
[13] XIE Keng, WEN Jiankang, HUA Yixin. Selective separation of Cu(), Zn(ⅡⅡ) and Cd(Ⅱ) by solvent extraction[J]. Rare Metals, 2008, 27(3): 230−231.
[14] MELLAH A, BENACHOUR D. The solvent extraction of zinc and cadmium from phosphoric acid solution by di-2-ethylhexyl phosphoric acid in kerosene diluent[J]. Chemical Engineering and Processing, 2006, 45(8): 684−690.
[15] 曾懋华, 奚长生, 彭翠红, 等. 冶锌工业废渣中镉的回收利用[J]. 韶关学院学报, 2003, 24(12): 56−59. ZENG Maohua, XI Changsheng, PENG Cuihong, et al. Reclaim and utilization of cadmium from the annealled zinc industry sediment[J]. Journal of Shaoguan University, 2003, 24(12): 56−59.
[16] 袁贵有. 从铜镉渣中回收镉的试验研究[J]. 有色金属再生与利用, 2006 (12): 21−22. YUAN Guiyou. Experimental research of recovering cadmium from slag bearing copper and cadmium[J]. Non-ferrous Metals Recycling and Utilization, 2006 (12): 21−22.
[17] 李秉龙, 银涛, 帅丽芳, 等. 镉污染及其防治对策[J]. 中国保健营养, 2013(7): 790−791. LI Binglong, YIN Tao, SHUAI Lifang, et al. Pollution and countermeasures of cadmium[J]. China Health Care and Nutrition, 2013(7): 790−791.
[18] PANAYOTOVA M. Use of zeolite for cadmium removal from wastewater[J]. Journal of Environmental Science & Health Part A, 2000, 35(9): 1591−1601.
[19] 张平民, 关鲁雄, 唐瑞仁, 等. 工科大学化学[M]. 长沙:湖南教育出版社, 2002: 469. ZHANG Pingmin, GUAN Luxiong, TANG Ruiren, et al. Advanced chemistry for engineering[M]. Changsha: Hunan Education Press, 2002: 469.
(编辑 刘锦伟)
A new process of electrical replacement for cadmium extraction by zinc plate under micro current
HE Jing, WANG Xiayang, YE Longgang, ZHANG Jiawei, YANG Jianguang, QI Chunping
(School of Metallurgy and Environment, Central South University, Changsha 410083, China)
In order to solve the shortcomings in the process of the traditional cadmium extraction by zinc powder cementation, including complex process, great consumption of zinc powder, low-purity sponge cadmium, high production cost and much damage to environment, a new process of replacement for sponge cadmium extraction by zinc plate during the action of microcurrent was proposed. In this process, zinc plate was used as anode and titanium mesh as cathode. The effects of different factors on the replacing ratio were examined such as current density, temperature, pH value and the polar distance. The results show that the cadmium rate is higher than 96% and the purity of sponge cadmium is more than 97% under the optimum conditions (current density of 0.5 mA/cm2, polar distance of 3 cm, pH of 1 and temperature of 40 ℃). Sponge cadmium obtained under this condition is hexagonal, lamellar positive hexagonal dendrite. The cadmium cementation ratio has different degrees of growth when the current density increases, the temperature rises and the pH decreases, while the polar distance has little effect on it.
microcurrent; zinc plate; electrodeposit; cementation; sponge cadmium
TF819.2
A
1672−7207(2016)03−0711−06
10.11817/j.issn.1672-7207.2016.03.001
2015−05−23;
2015−06−29
湖南省科技重大专项(2012FJ1010);国家自然科学基金资助项目(51174240) (Project(2012FJ1010) supported by the Major Scientific and Technological Projects Supervision of Hunan Province; Project(51174240) supported by the National Natural Science Foundation of China)
何静,教授,从事稀散金属冶金和清洁冶金研究;E-mail: he6213@163.com
