他克莫司治疗重症肌无力患者的临床效果及安全性评价
2016-12-06姚广明赵真真
姚广明赵真真
他克莫司治疗重症肌无力患者的临床效果及安全性评价
姚广明1赵真真2
目的 探讨他克莫司治疗重症肌无力患者的临床效果及安全性。方法 选取2015年1—12月医院收治的150例重症肌无力患者作为研究对象,按入院时间先后将其分为观察组与对照组,各75例。对照组患者给予甲基强的松龙,观察组患者则给予他克莫司。测定两组患者持续治疗4个月后治疗效果,同时使用日常生活能力量表(ADL)、美国MG基金会(MGFA)疾病严重程度评价量表、徒手肌力评定(MMT)以及Osserman对患者治疗前后日常生活能力、病情相关指标变化情况进行评估,统计患者治疗前后体内乙酰胆碱受体抗体(AchR-Ab)浓度及治疗期间不良反应发生情况。结果 观察组患者治疗的总有效率明显高于与对照组,差异有统计学意义(P<0.05);治疗后,观察组患者的临床相对评分以及Osserman评分均明显低于对照组,ADL评分、MGFA疾病严重程度评价量表评分、MMT评分均明显高于对照组,差异均有统计学意义(均P<0.05);治疗后,观察组患者的AchR-Ab浓度明显低于对照组,差异有统计学意义(P<0.05)。结论 他克莫司治疗重症肌无力患者相较于传统甲基强的松龙治疗效果显著,可有效降低患者体内AchR-Ab水平,缓解肌无力等症状,提高生活能力,且安全性高。
他克莫司;重症肌无力;甲基强的松龙;不良反应
重症肌无力是一种临床较常见的自身免疫性疾病,是由于自身神经与肌肉接头处传递功能障碍而导致全身或局部骨骼、肌肉无力,极易发生疲劳现象,可对患者的正常生活造成严重影响[1]。免疫抑制剂、肾上腺糖皮质激素等均是治疗重症肌无力的常用药物,而他莫克斯作为肾上腺素糖皮质激素减量的辅助用药已广泛应用于重症肌无力患者的治疗中。本研究就他克莫司治疗重症肌无力患者的临床效果及安全性进行分析,现报道如下。
1 资料与方法
1.1 一般资料 选取2015年1—12月我院收治的150例重症肌无力患者作为研究对象,按入院时间先后将其分为观察组与对照组,各75例。观察组患者中,男35例,女40例,年龄20~65岁,平均(36± 9)岁,病程6个月至12年,平均(5.2±1.4)年;重症肌无力临床分级标准(Osserman评级)[2]:Ⅱb型20例,Ⅲ型28例,Ⅳ型22例,Ⅴ型5例。对照组患者中,男33例,女42例,年龄20~66岁,平均(36±9)岁,病程6个月至12年,平均(5.4± 1.4)年;Osserman评级:Ⅱb型18例,Ⅲ型29例,Ⅳ型23例,Ⅴ型5例。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性
1.2 纳入及排除标准 纳入标准:①均符合Osserman评级中针对该病的诊断与分级标准[3];②本研究治疗前3个月患者未接受过糖皮质激素、环孢素A等免疫抑制剂药物治疗;③均符合本院医学伦理委员会相关要求,均签署了知情同意书。排除标准[4]:①恶性肿瘤、严重感染性疾病等;②严重肝脏、肾脏、心脏等脏器功能障碍;③妊娠期及哺乳期女性。
1.3 治疗方法 对照组患者给予甲基强的松龙(Pfizer Manufacturing Belgium NV,比利时,批号:20130303,规格:40 mg/支),初始用药剂量为1.0 mg/(kg·d),早晚各1次,持续用药7 d后根据患者用药耐受性以及症状变化情况调整用药剂量,最终将药物剂量调整为10~15 mg/(kg·d)作为维持剂量,用药频率仍然为早晚各1次。观察组患者则给予他克莫司(Astellas Ireland Co Ltd,爱尔兰,批号:20150195,规格:1 mg×10粒×5板)治疗,用药剂量为0.1 mg/(kg·d),用药频率为早晚各1次。两组患者均持续治疗4个月,治疗期间严禁服用其他与本病治疗相关的药物,护理人员应密切注意患者生命体征指标及临床症状变化,针对患者治疗期间出现的异常症状及时给予相应护理、治疗措施,必要时可遵医嘱要求患者停止服用药物。
1.4 观察指标 ①测定两组患者治疗效果:首先使用许贤豪[5]的绝对临床评分法测定两组患者治疗前后临床症状积分,同时统计患者临床相对评分(%)=(患者治疗前绝对评分-治疗后绝对评分)/治疗前绝对评分×100%,依据患者临床相对评分变化情况作为患者治疗效果评定标准。痊愈:患者相对评分≥90%;显效:患者相对评分为50%~89%;有效:患者相对评分为25%~49%;无效:患者相对评分<25%。总有效率(%)=(痊愈例数+显效例数+有效例数)/总例数×100%。②使用日常生活能力量表(ADL)、美国MG基金会(MGFA)疾病严重程度评价量表、徒手肌力评定(MMT)以及Osserman对患者进行评估,统计两组患者治疗前后日常生活能力、病情相关指标变化情况[6]。③测定两组患者治疗前后体内乙酰胆碱受体抗体(AchR-Ab)浓度,同时统计其治疗期间不良反应发生情况。
1.5 统计学分析 采用SPSS 18.0统计软件进行数据分析,计量资料以±s表示,组间比较采用t检验,计数资料以百分率表示,组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 治疗效果比较 观察组患者治疗的总有效率明显高于与对照组,差异有统计学意义(P<0.05),见表1。
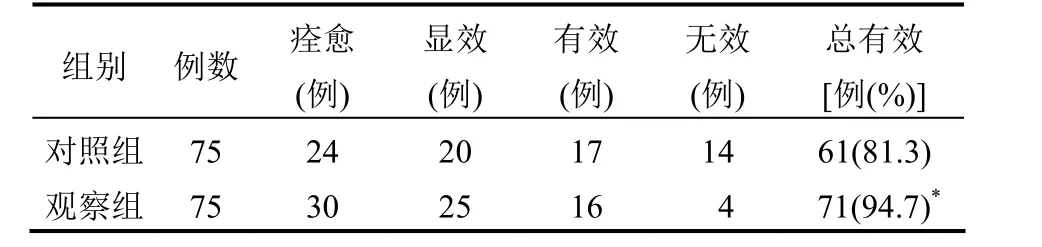
表1 两组患者治疗效果比较
2.2 各评分量表评分比较 治疗前,两组患者的临床相对评分、ADL评分、MGFA疾病严重程度评价量表评分、MMT评分以及Osserman评分差异均无统计学意义(均P>0.05);治疗后,观察组患者的临床相对评分以及Osserman评分均明显低于对照组,ADL评分、MGFA疾病严重程度评价量表评分、MMT评分均明显高于对照组,差异均有统计学意义(均P<0.05)。见表2。
2.3 AchR-Ab浓度比较 治疗前,两组患者的AchRAb浓度差异无统计学意义(P>0.05);治疗后,观察组患者的AchR-Ab浓度明显低于对照组,差异有统计学意义(P<0.05)。见表3。
2.4 不良反应发生情况比较 观察组患者中,血象改变2例,白细胞数量下降2例,血小板数量降低3例,谷氨酸转氨酶升高2例,血糖升高2例,不良反应发生率为14.7%(11/75);对照组患者中,血象改变3例,白细胞数量下降2例,血小板数量降低3例,谷氨酸转氨酶升高3例,血糖升高2例,不良反应发生率为17.3%(13/75)。两组患者治疗期间不良反
应发生率差异无统计学意义(χ2=0.20,P>0.05)。
表2 两组患者治疗前后各项量表评分比较(分,±s)
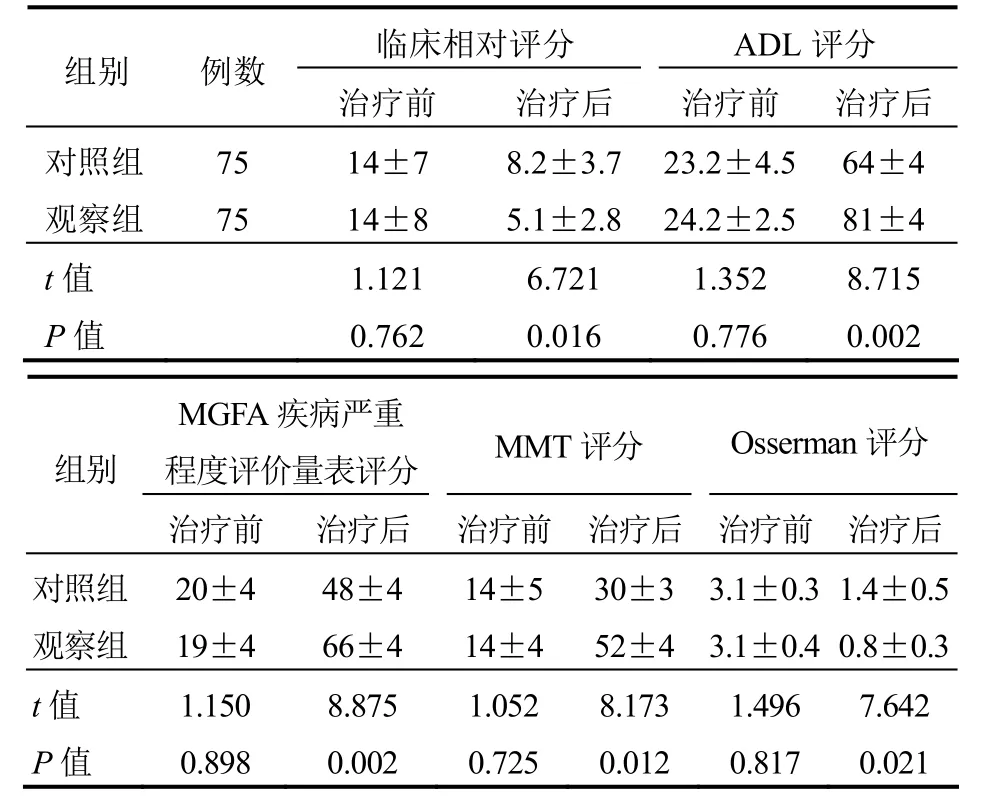
表2 两组患者治疗前后各项量表评分比较(分,±s)
组别 例数 治疗前 治疗后 治疗前治疗后临床相对评分 ADL评分对照组 75 14±7 8.2±3.7 23.2±4.564±4观察组 75 14±8 5.1±2.8 24.2±2.581±4 t值 1.121 6.721 1.352 8.715 P值 0.762 0.016 0.776 0.002组别MGFA疾病严重程度评价量表评分 MMT评分 Osserman评分治疗前 治疗后 治疗前 治疗后 治疗前治疗后对照组 20±4 48±4 14±5 30±3 3.1±0.3 1.4±0.5观察组 19±4 66±4 14±4 52±4 3.1±0.4 0.8±0.3 t值 1.150 8.875 1.052 8.173 1.4967.642 P值 0.898 0.002 0.725 0.012 0.8170.021
表3 两组患者治疗前后AchR-Ab浓度比较(nmol/L,±s)
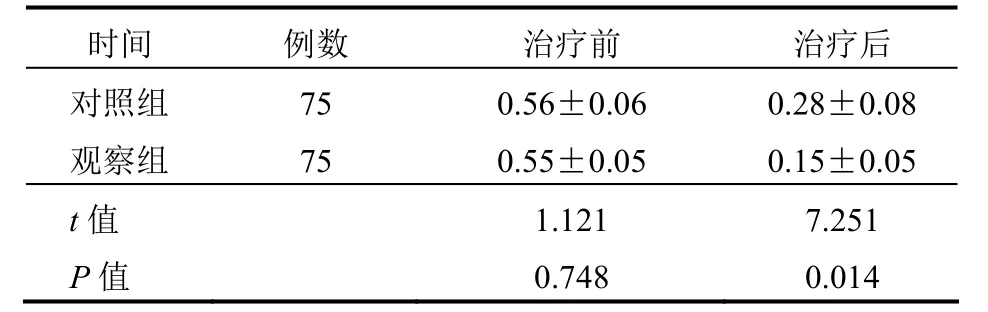
表3 两组患者治疗前后AchR-Ab浓度比较(nmol/L,±s)
时间 例数 治疗前 治疗后对照组 75 0.56±0.06 0.28±0.08观察组 75 0.55±0.05 0.15±0.05 t值 1.121 7.251 P值 0.748 0.014
3 讨论
重症肌无力发病与先天遗传以及自身免疫系统缺陷有关,同时,患者也极易受外界感染、药物、环境等多种因素的影响。临床研究显示,重症肌无力发病可能与与胸腺增生存在一定联系[7],65%~80%重症肌无力患者伴有胸腺增生症状,同时10%~20%重症肌无力患者存在胸腺瘤。相关研究认为,重症肌无力是一种由乙酰胆碱受体抗体介导的依赖体内T细胞并且补体直接参与导致的神经与肌肉接头处传递功能障碍[8]。目前,临床上针对重症肌无力患者仍然缺乏彻底治愈的方法,现有的治疗方案虽然能够充分缓解患者症状但仍然会对患者造成一定影响,甚至会出现严重并发症而危及患者生命安全。
目前,临床针对重症肌无力患者的治疗方案包括硫唑嘌呤等药物治疗以及激素冲击疗法、血浆置换法、丙种球蛋白应用法等。临床实践证实,激素治疗是当前治疗效果最佳的方法之一[9],80%的患者对激素治疗有良好的耐受性,并且疗效显著。他克莫司是一种从链霉菌属中分离出的大环内酯类抗生素,其作为一种新型免疫抑制剂,能够以高度的脂溶性作用于人体内各器官、血管等组织结构中,以高度选择性对辅助性T细胞发挥着极强的抑制作用。临床实践证实,他克莫司免疫抑制效果显著[10]。将他克莫司应用于治疗重症肌无力,其能够直接对患者T细胞发挥作用,然后可与蛋白质结合进行代谢,治疗效果明显,且不良反应发生率较低,可避免以往激素类药物应用过程中对患者生命安全造成的严重威胁。但需要注意的是,不同体质患者体内蛋白质浓度不同,所以临床在应用他克莫司治疗过程中,应该密切监测患者体内血药浓度,做好并发症预防护理与治疗工作。
本研究结果显示,观察组患者治疗的总有效率明显高于与对照组;治疗后,观察组患者的临床相对评分以及Osserman评分均明显低于对照组,ADL评分、MGFA疾病严重程度评价量表评分、MMT评分均明显高于对照组,AchR-Ab浓度明显低于对照组。提示他克莫司治疗重症肌无力患者相较于传统甲基强的松龙治疗效果显著,可有效降低患者体内AchR-Ab水平,缓解肌无力等症状,提高生活能力,且安全性高。
[1] 张文帅.他克莫司治疗难治性重症肌无力的疗效与安全性观察[J].临床医药文献杂志,2016,3(8)∶1569,1571.
[2] 彭明丽,赵冠人,温筱煦,等.重症肌无力患者他克莫司血药浓度监测[J].中南药学,2015,13(2)∶144-146.
[3] 孙睿.评价他克莫司治疗全身型重症肌无力(MG)的疗效及不良反应[J].中国继续医学教育,2015,7(8)∶238-239.
[4] 裴耀华,王磊,史延锋,等.他克莫司治疗慢代谢型重症肌无力的疗效[J].广东医学,2012,33(7)∶1004-1005.
[5] 许贤豪.获得性自身免疫性重症肌无力[J].中华内科杂志,1998, 19(3)∶210-211.
[6] 王志强.他克莫司治疗难治性重症肌无力疗效与安全性探讨[J].中国实用医药,2014,9(9)∶1601.
[7] 童卫杭,刘丽宏,李鹏飞,等.重症肌无力患者他克莫司血药质量浓度与CYP3A5基因多态性的相关性研究[J].北京师范大学学报(自然科学版),2010,46(4)∶503-505.
[8] 陈玉萍,李月敏,王卫,等.他克莫司治疗激素依赖性重症肌无力的疗效观察[J].解放军医学杂志,2015,40(1)∶46-49.
[9] 林婧,卜碧涛.他克莫司治疗重症肌无力1例报道[J].神经损伤与功能重建,2010,5(2)∶147-148.
[10] 徐亮.小剂量他克莫司在难治性重症肌无力中的应用[J].中国实用神经疾病杂志,2014,17(7)∶27-29.
R746.1
A 【DOI】10.12010/j.issn.1673-5846.2016.11.017
1沈阳市红十字会医院,辽宁沈阳 110013
2沈阳市第四人民医院,辽宁沈阳 110031
