紫背天葵的高效液相色谱法指纹图谱分析
2016-12-06邵考珍何淑莹
邵考珍 何淑莹
紫背天葵的高效液相色谱法指纹图谱分析
邵考珍 何淑莹
目的 探讨紫背天葵的高效液相色谱法(HPLC)指纹图谱。方法 采用色谱柱Shim-pack VP-ODS(250 mm× 4.6 mm,5 μm);以0.5%H3pO4(V/V)为流动相A,以50 %乙腈为流动相B(V/V),进行梯度洗脱;流速为0.8 ml/min;柱温30 ℃;检测波长为280 nm;进样量10 μl;运行时间为80 min。理论板数按矢车菊素-3-O-葡萄糖苷计算,不得低于3000。结果 建立了紫背天葵的HPLC指纹图谱。讨论 采用HPLC构建“紫背天葵”指纹图谱,探讨指纹图谱的技术要点及检测条件,以能反映该品种整体特征的HPLC指纹图谱作为质量评价方法,对现有质量控制方法作出积极而又必要的补充和提高,为建立统一的质量标准奠定基础,从而建立新的质量标准。
紫背天葵;高效液相色谱法;指纹图谱
紫背天葵是秋海棠科秋海棠属的多年生无茎草本植物,别名为红天葵、红叶、红水葵、散血子等,分布于中国的广东、福建、江西、海南、香港、湖南、广西、浙江等地,生长于海拔700m至1120m的地区,一般生长于悬崖石缝中、山地山顶疏林下石上、山顶林下潮湿岩石上及山坡林下。其可做清凉饮料,具有清热解毒、凉血活血及润肺止咳的功效,主治暑热高热、肺热咳嗽咯血、跌打扭伤、血瘀疼痛、疮毒疥癣、水火烫伤等[1-3]。近年来,随着研究的逐步开展,紫背天葵的新作用和用途不断被发现。现代研究表明,紫背天葵主要含有大量花色苷、黄酮苷、氨基酸、活性多糖化合物、生物碱和微量元素等有效活性成分,以矢车菊素-3-O-葡萄糖苷、矢车菊-3-O-芸香糖苷等花色苷为主要活性化学成分[4-8]。目前,相关研究报道除少量药理研究外,主要集中于不同成分的提取及稳定性研究上,而对质量控制和质量标准的研究极其罕见[9],对高效液相色谱法(HPLC)指纹图谱的研究则未见报道。由于市面上紫背天葵的质量良莠不齐,不同产地的紫背天葵疗效差距较大,本研究拟采用HPLC构建紫背天葵的指纹图谱,以便建立能反映该品种整体特征的质量评价方法,从而保证中药质量稳定、保证临床疗效和使用安全,同时更有利于开发新的临床应用,促进资源有效的规范化和规模化开发利用。
1 仪器与试剂
1.1 仪器 Agilent 1200高效液相色谱仪,包括四元
泵、脱气机、二极管阵列检测器、柱温箱;Chemstation工作站;HN-1006型超声波清洗机(广州市华南超声设备有限公司)。
1.2 药品与试剂 矢车菊素-3-O-葡萄糖苷对照品(Hyphytochem公司,批号:20160201,纯度:≥98%);甲醇、乙腈为色谱纯,其他试剂为分析纯,水为高纯水。广东、广西、湖南、福建等不同产地的紫背天葵经广州市皮肤病防治所副主任中药师龙惠鉴定,均为秋海棠科秋海棠属干燥全草。
2 方法与结果
2.1 供试品溶液的制备 取紫背天葵药材粉碎并过40目筛。精密称取粉末1 g,置于具塞锥形瓶中,精密加甲醇25 ml,称定质量,超声处理30 min。取出,冷却至室温,再称定质量,用甲醇补足减少重量。摇匀,滤纸滤过,再以0.45 μm滤膜滤至进样瓶,即为供试品溶液。
2.2 对照品溶液的制备 精密称取矢车菊素-3-O-葡萄糖苷对照品适量,加甲醇制成0.1 mg/ml溶液,避光保存,作为对照品溶液。
2.3 色谱条件 色谱柱:Shim-pack VP-ODS(250 mm ×4.6 mm,5 μm);以0.5% H3pO4(V/V)为流动相A,50%乙腈为流动相B(V/V),按表1程序进行梯度洗脱;流速:0.8 ml/min;柱温:30 ℃;检测波长:280 nm;进样量:10 μl;运行时间:80 min。理论板数按矢车菊素-3-O-葡萄糖苷计算,不低于3000。梯度洗脱程序见表1。

表1 梯度洗脱程序表
2.4 方法学考察
2.4.1 精密度试验 取同一批紫背天葵供试品溶液,连续进样6次,记录色谱图。以矢车菊素-3-O-葡萄糖苷为参照峰,计算主要色谱峰的相对保留时间和相对峰面积的相对标准偏差(RSD)。结果显示,各色谱峰的相对保留时间的RSD%≤0.1%,相对峰面积的RSD%<1%。另以第1次测定的色谱图为参照,使用相似度计算软件计算相似度,相似度平均值为0.999。试验结果表明,该方法的精密度良好(表2)。

表2 精密度试验结果(相对峰面积)
2.4.2 稳定性试验 取同一份紫背天葵供试品溶液,分别于0、2、4、8、12、18、24 h进样测定,记录色谱图。以矢车菊素-3-O-葡萄糖苷为参照峰,计算主要色谱峰的相对保留时间和相对峰面积的RSD。结果显示,各色谱峰的相对保留时间的RSD%<1%,相对峰面积的RSD%<3%。另以第1次测定的色谱图为参照,使用相似度计算软件计算相似度,相似度平均值为0.910。表明供试品溶液在24 h内稳定性良好(表3)。
2.4.3 重复性试验 取同一批供试品6份分别进样测定,记录色谱图。以矢车菊素-3-O-葡萄糖苷为参照峰,计算主要色谱峰的相对保留时间和相对峰面积的RSD。结果显示,各色谱峰的相对保留时间的RSD%<1%,相对峰面积的RSD%<3%。另以第1份测定的色谱图为参照,使用相似度计算软件计算相似度,相似度平均值为0.900。结果见表4。
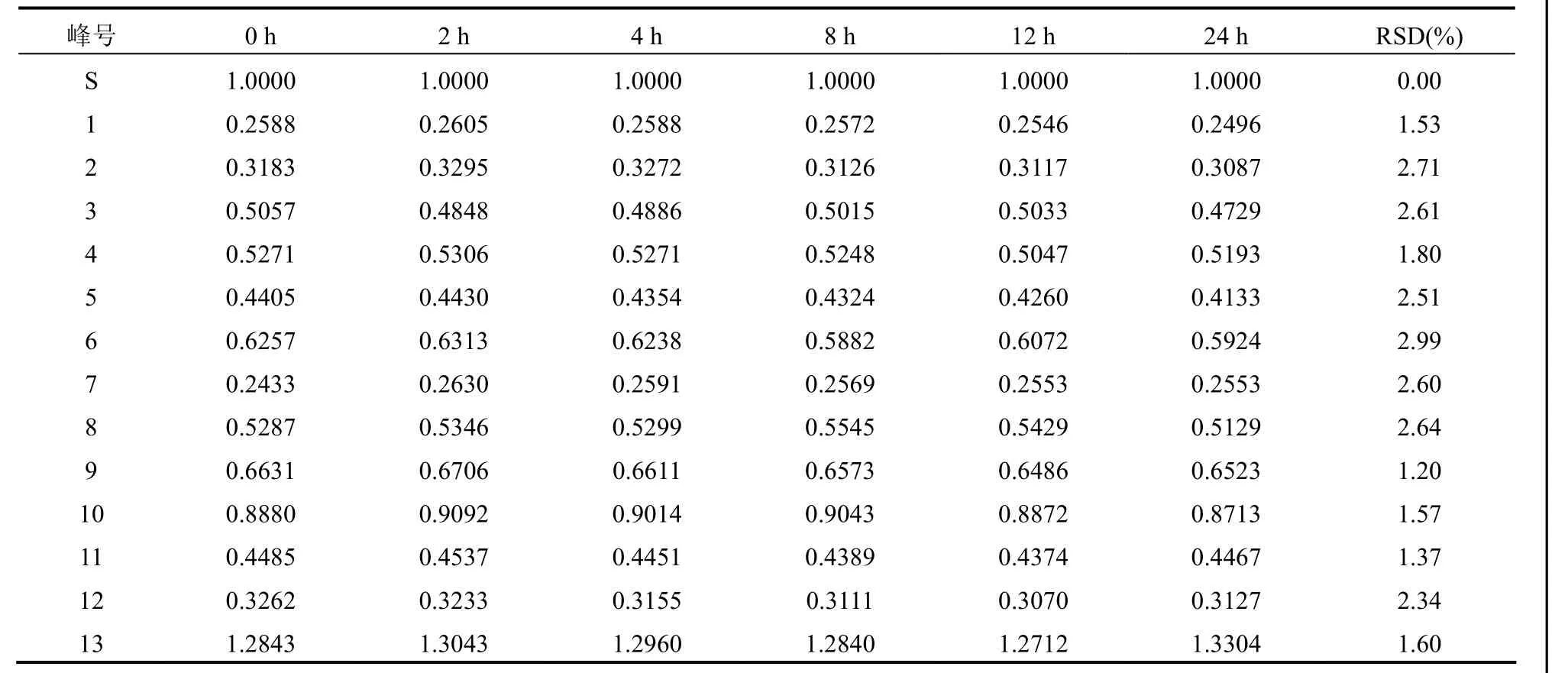
表3 稳定性试验结果(相对峰面积)

表4 重复性试验结果(相对峰面积)
2.5 指纹图谱及解析
2.5.1 共有峰标记 通过对10批紫背天葵进行了指纹图谱的分析,以矢车菊素-3-O-葡萄糖苷为参考峰,标定了25个共有峰。分别为1号(5.230 min)、2号(7.750 min)、3号(8.078 min)、4号(10.143 min)、5号(11.204 min)、6号(12.717 min)、7号(14.934 min)、8号(16.201 min)、9号(16.603 min)、10号(16.944 min)、11号(18.091 min)、12号(18.660 min)、13号(19.315 min)、14号(19.671 min)、15号(22.826 min)、16号(26.049 min)、17号(39.656 min)、18号(39.853 min)、19号(42.168 min)、20号(42.451 min)、21号(43.811 min)、22号(45.055 min)、23号(46.220 min)、24号(47.421 min)、25号(50.276 min)。见图2。
2.5.2 相似度计算 本研究采用中国药典委员会推荐的中药色谱指纹图谱相似度评价系统(2004年A版),对10批不同产地的紫背天葵样品HPLC图谱进行评价,通过与系统生成的对照图谱进行比较,得到各种来源的供试品相似度在0.309~0.968。结果见表5及图1~3。

表510 批不同产地的紫背天葵样品相似度
3 讨论
3.1 供试品制备方法的考察 根据文献资料,曾试验以体积分数分别为50%、60%、70%、80%、90%、
100%的甲醇为溶剂。从HPLC图谱看,50%甲醇HPLC图谱杂质最多、基线不平,其他浓度依次改善,100%甲醇最佳。采用超声30 min的方法进行提取,操作简单、图谱特征稳定。

图1 矢车菊素-3-O-葡萄糖苷对照品HPLC色谱图

图2 紫背天葵样品的HPLC指纹图谱
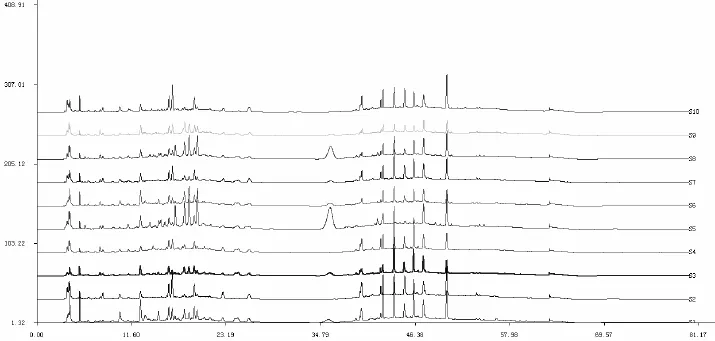
图310 批不同产地的紫背天葵HPLC色谱图
3.2 色谱条件的优化 曾试验过的流动相系统有以下两种:①乙腈-(0.1%~0.5%)磷酸溶液;②(0.1%~0.5%)磷酸溶液-50%乙腈,经过试验发现:0.5%磷酸溶液-50%乙腈按表1的程序进行梯度洗脱,所得色谱峰的数量、分离度、分布均匀程度最高。以每分钟0.8 ml的流速至80 min时色谱峰已完全洗脱。
3.3 小结 采用HPLC构建“紫背天葵”指纹图谱,以能反映该品种整体特征的HPLC指纹图谱作为质量评价方法,对现有质量控制方法作出积极而又必要的补充和提高,为建立统一的质量标准奠定基础,从
而可以建立新的质量标准,更进一步加强对紫背天葵的质量控制,保证临床用药的安全有效,开发新的临床应用,促进资源有效的规范化和规模化开发。
[1] 中华人民共和国国家药典委员会.中国药典[M].北京∶中国医药科技出版社,2010.
[2] 中华人民共和国国家医药管理局《中华本草》编委会.中华本草[M].上海∶上海科技出版社,2000∶493-495.
[3] 中国中药编辑委员会.中国本草[M].上海∶上海科学技术出版社, 2000∶495.
[4] 段志芳,章炜中,黄丽华.紫背天葵多糖提取与含量测定[J].中成药,2007,29(2)∶274-276.
[5] 许旋,卢忠,罗一帆.对不同等级紫背天葵微量元素含量的测定[J].广东微量元素科学,2000,7(4)∶55-57.
[6] 刘巍然,周法兴.紫背天葵水提液析出物化学成分研究[J].中国药学杂志,1991,26(8)∶467-468.
[7] 李红缨,杨海贵,植中强.紫背天葵红色素理化性质的研究[J].肇庆学院学报,2002,23(2)∶76-79.
[8] 崔蕊静,申淑琦,郭朔.复合酶协同微波处理提取紫背天葵叶片总黄酮工艺[J].中国食品学报,2014,14(2)∶72-77.
[9] 谭雄斯,王景.紫背天葵研究进展[J].中国民族民间医药,2012, 21(14)∶40-41.
Analysis of high performance liquid chromatography Semiaquilegia fingerprint
Shao Kaozhen He Shuying
Objective To study high performance liquid chromatography of Begonia fimbristipula (HPLC) fingerprint. Methods Uses the chromatographic column Shim-pack VP-ODS(250 mm×4.6 mm,5 μm);H3pO4at 0.5%(V/V)as mobile phase A,with 50% acetonitrile as mobile phase B(V/V),with gradient elution;The flow rate of 0.8 ml/min;column temperature 30 ℃;detection wavelength of 280 nm;ample quantity 10 μl;the running time of 80 min.Theoretical plate number according to the knapweed-3-O-glycosidase calculation,is not less than 3000.Result The HPLC fingerprint of Begonia fimbristipulata Hance is established.Conclusion The significance of establish the Begonia fimbristipulata Hance HPLC fingerprint:use the High performance liquid chromatography (HPLC)to construct "Begonia fimbristipulata Hance"fingerprint,discusses the technical key points of fingerprints and testing conditions,to reflect the overall characteristics of the HPLC fingerprint of breed as quality evaluation method,respond positively to the existing quality control method and the necessary supplement and improve,in order to establish the quality standard of unified foundation,so as to set a new standard of quality.
Begonia fimbristipulata Hance;HPLC;Fingerprint
R927.11
A 【DOI】10.12010/j.issn.1673-5846.2016.11.003
佛山市南海区第七人民医院,广东 528247
邵考珍(1975-),主管中药师。研究方向:中药HPLC指纹图谱
