氯吡脲人工抗原的合成与鉴定
2016-12-02肖石妹鄢爱平万益群
肖石妹,鄢爱平,肖 芳,万益群,,郭 岚,,*
(1.南昌大学化学学院,江西 南昌 330031;2.南昌大学分析测试中心,江西 南昌 330047)
氯吡脲人工抗原的合成与鉴定
肖石妹1,鄢爱平2,肖 芳1,万益群1,2,郭 岚1,2,*
(1.南昌大学化学学院,江西 南昌 330031;2.南昌大学分析测试中心,江西 南昌 330047)
为合成新的、有效的氯吡脲(forchlorfenuron,CPPU)人工抗原,在无水三氯化铝的催化作用下,采用傅克反应对CPPU小分子进行结构改造。采用碳二亚胺(carbodiimide,EDC)法将半抗原分别与牛血清白蛋白(bovine serum albumin,BSA)和卵清蛋白(ovalbumin,OVA)进行偶联,获得CPPU的免疫抗原(CPPU-BSA)和包被抗原(CPPU-OVA)。采用质谱、元素分析和核磁共振氢谱对CPPU半抗原(CPPU-COOH)的分子结构式进行鉴定;采用紫外光谱和高性能基质辅助激光解吸电离-飞行时间质谱对偶联物的结构和相对分子质量进行鉴定。结果显示成功合成出CPPU人工抗原,为其抗体的制备和免疫学方法的构建提供了参考。
氯吡脲;半抗原;人工抗原;合成;鉴定
氯吡脲(forchlorfenuron,CPPU)是一种高活性的植物生长调节剂[1],具有加速细胞有丝分裂、促进细胞的增大和分化、防止落花落果、促进果实膨大等作用,常用于脐橙、柑橘、猕猴桃、葡萄、西瓜、黄瓜等果蔬的农业生产中。残留于果蔬中的CPPU可能会对人类及其他生物造成潜在的威胁,美国环保署在《农药毒性确认和管理》中指出,长期接触CPPU会引起体内蛋白质代谢的紊乱,造成肺气肿和体型消瘦。各国对食品中CPPU的最大残留限量不同,范围为0.01~0.1 mg/kg,如澳大利亚规定猕猴桃中CPPU的最大残留限量为0.01 mg/kg,美国为0.04 mg/kg,欧盟为0.05 mg/kg,日本为0.1 mg/kg[2-3]。我国规定食品中CPPU最大残留限量为黄瓜、西瓜、甜瓜不大于0.1 mg/kg,猕猴桃、葡萄、橙、枇杷不大于0.05 mg/kg[4]。因此,开展食品中CPPU残留快速检测新技术研究对食品安全生产、现场监督都有着十分重要的现实意义。
CPPU残留检测目前主要采用固相萃取-高效液相色谱[5]、液相色谱[6]、气相色谱-质谱联用[7]、液相色谱-质谱联用[8]等技术,这些方法的准确度和精密度较高,但存在检测成本高、周期长及操作繁琐等缺陷,不适于大规模现场筛查。与色谱等分析技术相比,免疫分析法基于抗原与抗体特异性结合的测定原理,具有样品前处理简单、样品用量少、检测成本低、选择性高及分析速度快等特点。该法已广泛应用于食品中真菌毒素[9]、农药[10-11]、兽药[12]残留等危害物的检测,但目前鲜见其应用于食品中CPPU残留分析的报道。
小分子物质只有反应原性,而不具备免疫原性[13],要想获得其抗体,构建免疫学分析方法,必须首先与大分子蛋白载体偶联合成全抗原,这要求小分子化合物本身具有或者通过衍生得到活性基团(如氨基、羧基、重氮盐等)才能与载体进行交联反应[14-15]。CPPU本身无活性基团,因此,本研究采用傅克反应在CPPU的苯环上引入活性基团羧基链,然后与载体蛋白交联成功制备CPPU的人工抗原。本研究合成方法简单、有效,拓宽了可选用的抗原合成方法,为CPPU抗体的进一步制备提供了前期研究基础。
1 材料与方法
1.1 试剂
CPPU(纯度≥98%)、丁二酸酐 上海百灵威公司;N-羟基琥珀酰亚胺(N-hydroxysuccinimide,NHS)、1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(1-(3-dimethylaminopropyl)-3-ethylcarbodiimide hydrochloride,EDC)、N,N-二甲基甲酰胺(N,N-dimethyllformamide,DMF,分析纯)、无水三氯化铝、盐酸 上海生工生物工程股份有限公司;牛血清白蛋白(bovine serum albumin,BSA)、卵清蛋白(ovalbumin,OVA) 美国Sigma公司;1×PBS透析液(0.01 mol/L,pH 7.4):NaCl 8 g,KCl 0.2 g,KH2PO40.2 g,Na2HPO4·12H2O 2.9 g,蒸馏水定容至1 000 mL;甲醇、乙腈(色谱纯,99.9%) 美国Tedia公司;芥子酸(4-hydroxy-3,5-dimethoxycinnamic acid,TFA) 上海阿拉丁生化科技股份有限公司;其余试剂均为国产分析纯。
1.2 仪器与设备
AV 600核磁共振波谱仪 瑞士布鲁克公司;5800基质辅助激光解吸电离飞行时间质谱仪 美国AB Sciex公司;6430三重串联四极杆液质联用仪 美国Agilent公司;EL Ⅲ元素分析仪 德国Elementar公司;MX5微量天平 瑞士Mettler Toledo公司;2501PC紫外-可见分光光度计 日本岛津公司;摇床 上海智诚电子有限公司;DF-101S集热式恒温加热磁力搅拌器 巩义市予华仪器有限责任公司;SM2涡旋混合器 德国IKA公司;Milli-Q超纯水仪 美国Millipore公司。
1.3 方法
1.3.1 CPPU半抗原的制备
采用傅克反应[16-17]合成CPPU半抗原(CPPU-COOH)。采用无水DMF做溶剂,CPPU(2.48 g)、丁二酸酐(1 g)、无水三氯化铝(13.35 g)按1∶1∶10的物质的量比进行投料。将DMF(2.2 mL)逐滴加入到装有无水三氯化铝的烧瓶中,不断搅拌使其充分溶解,待瓶口不再有白雾冒出时放入油浴中。把CPPU和丁二酸酐的混合物加入到烧瓶中,反应2 h后,把反应液慢慢倒入90 mL冰水中,加6 mL浓度为12 mol/L的浓盐酸,冷却静置后过滤水洗,得到粗品,再用DMF/甲醇对粗品进行重结晶纯化,得到淡粉色固体物质。其合成路线见图1。
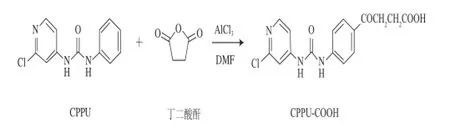
图1 CPPU半抗原合成路线Fig. 1 Synthetic route of CPPU-COOH
1.3.2 CPPU半抗原的结构鉴定
1.3.2.1 元素分析仪对半抗原的最简式鉴定
采用元素分析仪对纯化后的CPPU-COOH进行分析测定。C、H、N 3 种元素的测定用对氨基苯磺酸作为标准品校准仪器,然后再称取5 mg样品置于还原管和燃烧管中燃烧,同时通氦气(He)和氧气(O2),He流量为200 mL/min,O2流量为25 mL/min;O元素的测定用苯甲酸作为标准品校准仪器,然后再称取1.5 mg样品置于燃烧管中燃烧,只通O2,流量为200 mL/min。
1.3.2.2 液相色谱-质谱联用仪对半抗原的相对分子质量鉴定
采用三重串联四极杆液相色谱-质谱联用仪对纯化后的CPPU-COOH的分子式进行分析。色谱柱为Eclipse XDB-C18Column(4.6 mm×50 mm,1.8 μm);流动相为100%的色谱纯甲醇;流速为0.3 mL/min;进样量为5 μL;设定扫描范围为m/z 50~500;雾化气压力为40 psi;干燥气流速为11.0 L/ min;干燥气温度为300 ℃;毛细管电压为4.0 kV。在电喷雾离子源(electron spray ionization,ESI)离子源的正负离子模式下同时检测,再以分子离子为母离子做二级质谱正负离子扫描。
1.3.2.3 核磁共振对半抗原的分子结构式鉴定
结合核磁共振对CPPU原料和CPPU-COOH的氢原子进行氢谱鉴定。称取5 mg样品置于核磁管中,用氘代试剂二甲基亚砜(dimethyl sulfoxide,DMSO)充分溶解样品,再对充分溶解的样品进行扫描,样品测定前的等待时间为1 s,采集时间为3.1 s,每个样品的扫描次数为16 次。
1.3.3 EDC法制备人工抗原
1.3.3.1 EDC法制备免疫抗原
[18]的方法,准确称取CPPU-COOH 3.48 mg溶于200 μL DMF中,加入NHS 1.38 mg(另溶于200 μL DMF),再加入2.88 mg溶解好的EDC(另溶于300 μL DMF),室温条件下振荡反应12 h(溶液1);称取6.8 mg BSA(CPPU-COOH与BSA的物质的量比为100∶1)溶于2 mL 1×PBS中(溶液2)。再将溶液1逐滴加入溶液2中,边加边振荡,冰浴振荡反应12 h。反应混合物移入处理好的透析袋中,用超纯水透析3 d,每天换3 次透析液,即得到CPPU免疫抗原(CPPU-BSA),合成路线见图2。
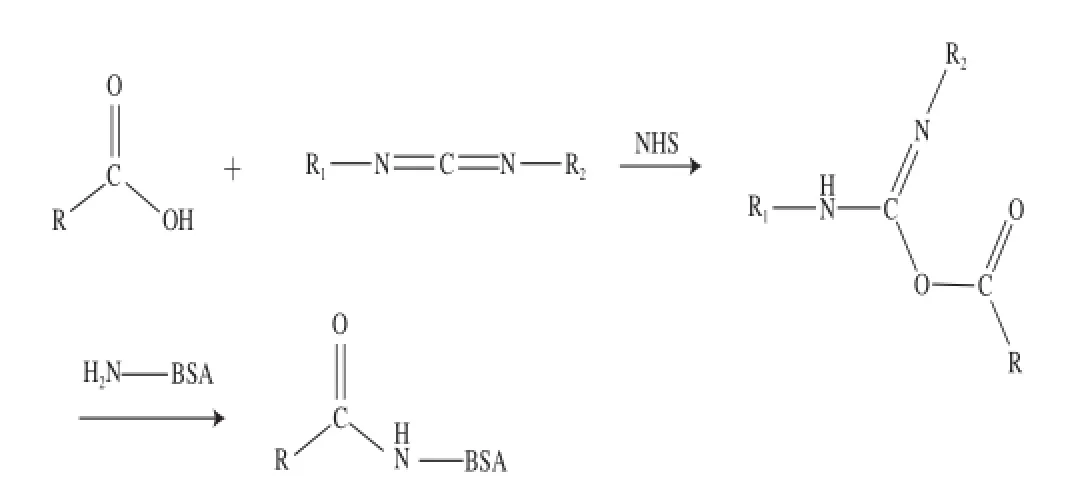
图2 CPPU免疫抗原的EDC法合成路线Fig. 2 Synthetic route of immunogen by EDC method
1.3.3.2 EDC法制备包被抗原
参考文献[19]的方法,称取CPPU-COOH 3.48 mg溶于200 μL DMF中,加入NHS 3.45 mg(溶于200 μL DMF),再直接加入2.88 mg EDC(另溶于300 μL DMF),室温振荡反应12 h(溶液3);称取4.5 mg OVA(CPPU-COOH与OVA的物质的量比为100∶1)溶于1.8 mL 1×PBS中(溶液4)。溶液3与溶液4混匀后,冰浴振荡反应12 h。同上透析即得到CPPU免疫抗原(CPPU-OVA),合成路线同图2。
1.3.4 CPPU人工抗原的鉴定
1.3.4.1 紫外光谱分析
将半抗原(CPPU-COOH)、全抗原(CPPU-OVA,CPPU-BSA)和载体蛋白(BSA、OVA)分别用超纯水稀释至质量浓度范围在0.01~0.1 mg/mL之间,使得物质的吸光度在0.2~0.8之间,用超纯水做参比溶液,测定物质的吸光度[20-21]。
1.3.4.2 高性能基质辅助激光解吸电离-飞行时间质谱(matrix-assisted laser desorption/ionization time of flight mass spectrometry,MALDI-TOF-MS)分析
基质辅助溶液的配制[22]:将34 μL 0.15% TFA与17 μL的乙腈混合,再加入适量的TFA使溶液达到过饱和状态,超声20 min,3 000 r/min 离心5 min,取上清液备用。
载体蛋白BSA、OVA以及偶联物CPPU-BSA、CPPU-OVA脱盐后分别与基质辅助溶液混合,点到样品靶上,放入质谱仪内进行激光扫描。通过相对分子质量数据的改变说明半抗原与蛋白偶联成功与否,并计算出蛋白与半抗原的偶联比[23],CPPU与载体蛋白的结合比按以下公式计算。
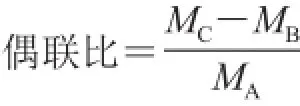
式中:MA、MB和MC分别表示半抗原、载体蛋白、全抗原的相对分子质量。
2 结果与分析
2.1 CPPU半抗原的分子结构式鉴定
2.1.1 元素分析仪对半抗原的测定结果
采用元素分析仪对半抗原合成产物的C、H、O、N 4种元素的含量进行测定,Cl的含量通过差减法求得。通过各个元素的百分含量推测物质的最简式(表1)。由表中数据可知合成产物与目标化合物(C16H14ClN3O4)具有相同的最简式。
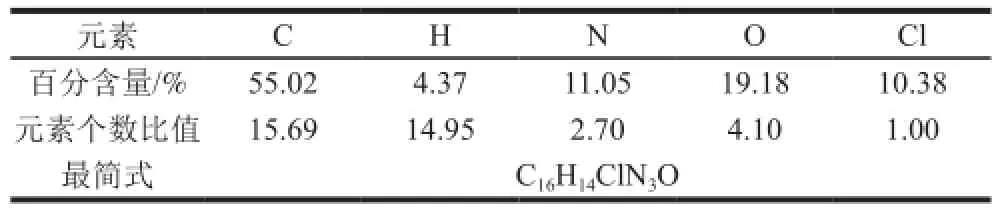
表1 元素分析数据Table 1 Elemental analysis of the hapten
2.1.2 CPPU-COOH的质谱鉴定
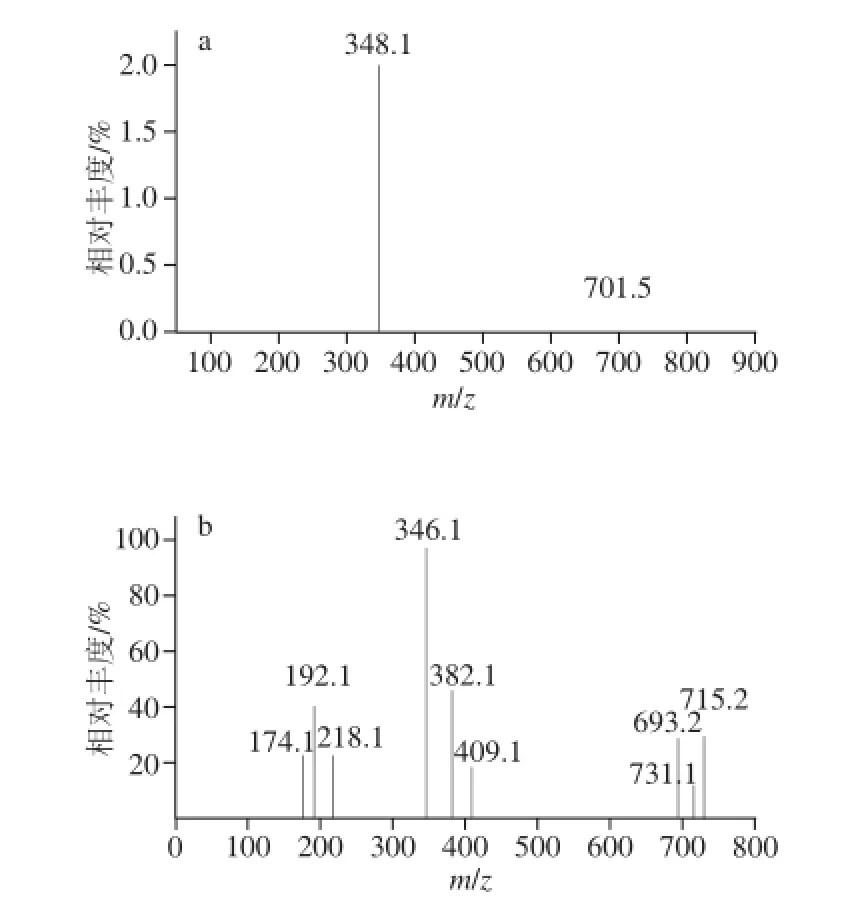
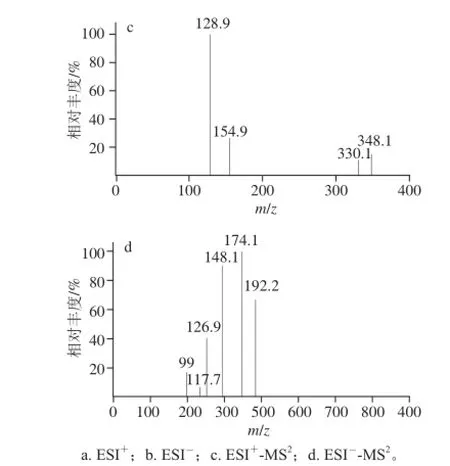
图3 CPPU半抗原的一级和二级质谱图Fig. 3 Mass spectrum and tandem mass spectrum of CPPU-COOH
对合成的半抗原进行质谱鉴定,一级质谱ESI+下出现m/z 348.1离子(图3a),ESI-下出现m/z 346.1离子(图3b),分别对应于加合质子准分子离子峰[M+H]+和[M-H]-,可以判断该物质的相对分子质量为347.1,与目标产物的理论相对分子质量(347.6)基本相符,这进一步验证了元素分析的结果,说明合成产物与目标产物不仅具有相同的最简式,而且相对分子质量也基本相同。再对照目标化合物的分子结构式,对合成产物的一级质谱及二级质谱出现的碎片离子做归属分析:一级质谱ESI-下出现的m/z 192.1(图3b)为目标化合物断裂酰胺键之后形成的N-(C6H4)(COC2H4COOH)碎片;二级质谱ESI+-MS2出现的m/z 128.9(图3c)为断裂酰胺键之后形成的NH2+(C5H3NCl)碎片;二级质谱ESI+-MS2出现m/z 126.9(图3d)为断裂酰胺键之后形成的N-(C5H3NCl)碎片。
2.1.3 核磁共振氢谱分析
为了进一步鉴定合成产物的分子结构式,对CPPU及纯化后的CPPU-COOH分别进行1H-NMR(600 MHz,DMSO)分析。由图4、5可知,CPPU共有10 个H,分别对应δ 9.179~9.405(2H,2NH)、δ 7.107~7.320(5H,苯环)、δ 7.436~8.209(3H,杂芳环)。而CPPU-COOH有14 个H,分别对应δ 9.389~9.469(2H,2NH)、δ 7.349~7.668(4H,苯环)、δ 7.967~8.212(3H,杂芳环)、δ 12.097(1H,COOH)、δ 2.573~3.334(4H,2CH2),其中苯环上有4 个H,分为两类,分别对应δ 7.362(1.84H)、δ 7.668(1.86H)。将两个核磁共振氢谱进行对照,可以清楚地看到,CPPU-COOH的1H-NMR谱图中保留了CPPU中苯环、酰胺基和氮杂环的氢谱信息,增加了δ 12.097(1H,COOH)峰和δ 2.573~3.334(4H,CH2CH2)峰,同时苯环上的H由5 个变成4 个,并且只分为两类,这说明在苯环上发生对位的单取代反应。由此可推测丁二酸酐开环与CPPU发生了苯环上的对位取代反应,形成一个含4 个C原子的取代基,同时末端的羰基转变成了羧基,为新化合物与蛋白质偶联创造了条件。
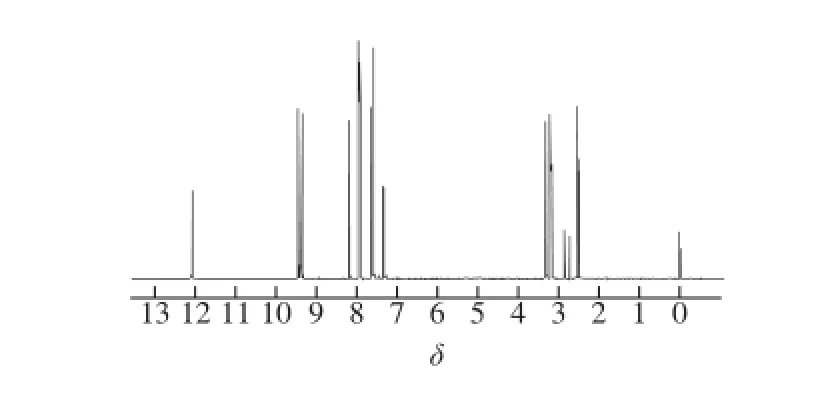
图5 CPPU-COOH的核磁共振图谱Fig. 51H-NMR spectrum of CPPU-COOH
由上述元素分析、质谱和核磁共振氢谱等技术手段的分析结果,可推断所合成的产物即为实验设计的CPPU-COOH目标物,该化合物保留了CPPU中苯环、杂环此类具有高免疫活性的特征结构[24],同时引入了一个含3 个C原子的连接臂和羧基活性基团,便于与载体蛋白偶联合成抗原,而合适的连接臂(3~6 个碳原子)的存在可以突出待测物分子的特征结构,使其不会被载体蛋白的三维结构掩盖,从而保证免疫抗体的合成成功[25-26]。
2.2 CPPU人工抗原的鉴定
2.2.1 紫外扫描光谱分析
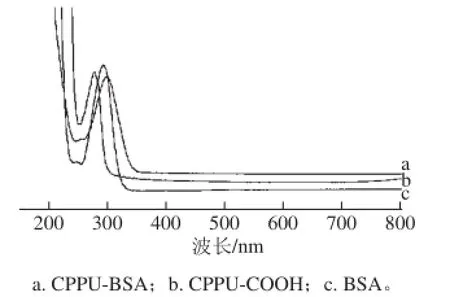
图6 人工免疫抗原紫外扫描光谱图Fig. 6 UV absorption spectrum of artificial immune antigen
按1.3.3节将CPPU-COOH分别与BSA和OVA进行偶联得到人工免疫抗原和人工包被原,对人工抗原、半抗原和载体蛋白分别进行紫外光谱扫描,结果见图6和图7。由图6可知,BSA在波长278 nm处有最大吸收峰,CPPUCOOH在298 nm波长处有最大吸收峰,而CPPU全抗原在309 nm波长处有最大吸收峰,说明产物与两种反应物相比,最大吸收峰位发生了一定的变化,表明CPPU-COOH与BSA可能发生了偶联反应。同样,由图7可知,OVA与也可能发生了偶联反应。
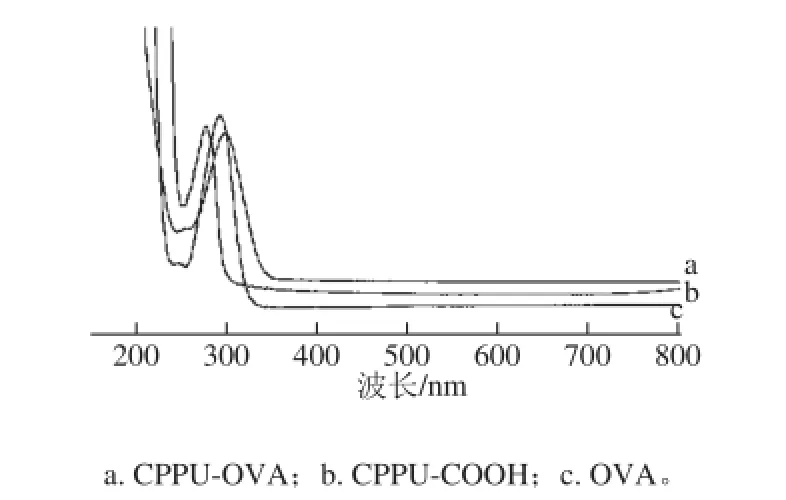
图7 人工包被抗原紫外扫描光谱图Fig. 7 UV absorption spectrum of artificial coating antigen
2.2.2 MALDI-TOF-MS测定全抗原和载体蛋白的相对分子质量
当载体蛋白偶联上半抗原分子后,其分子质量会发生改变,因此可通过MALDI-TOF-MS测定蛋白的相对分子质量(图8),来进一步验证载体蛋白是否与半抗原发生偶联,同时测定偶联比。
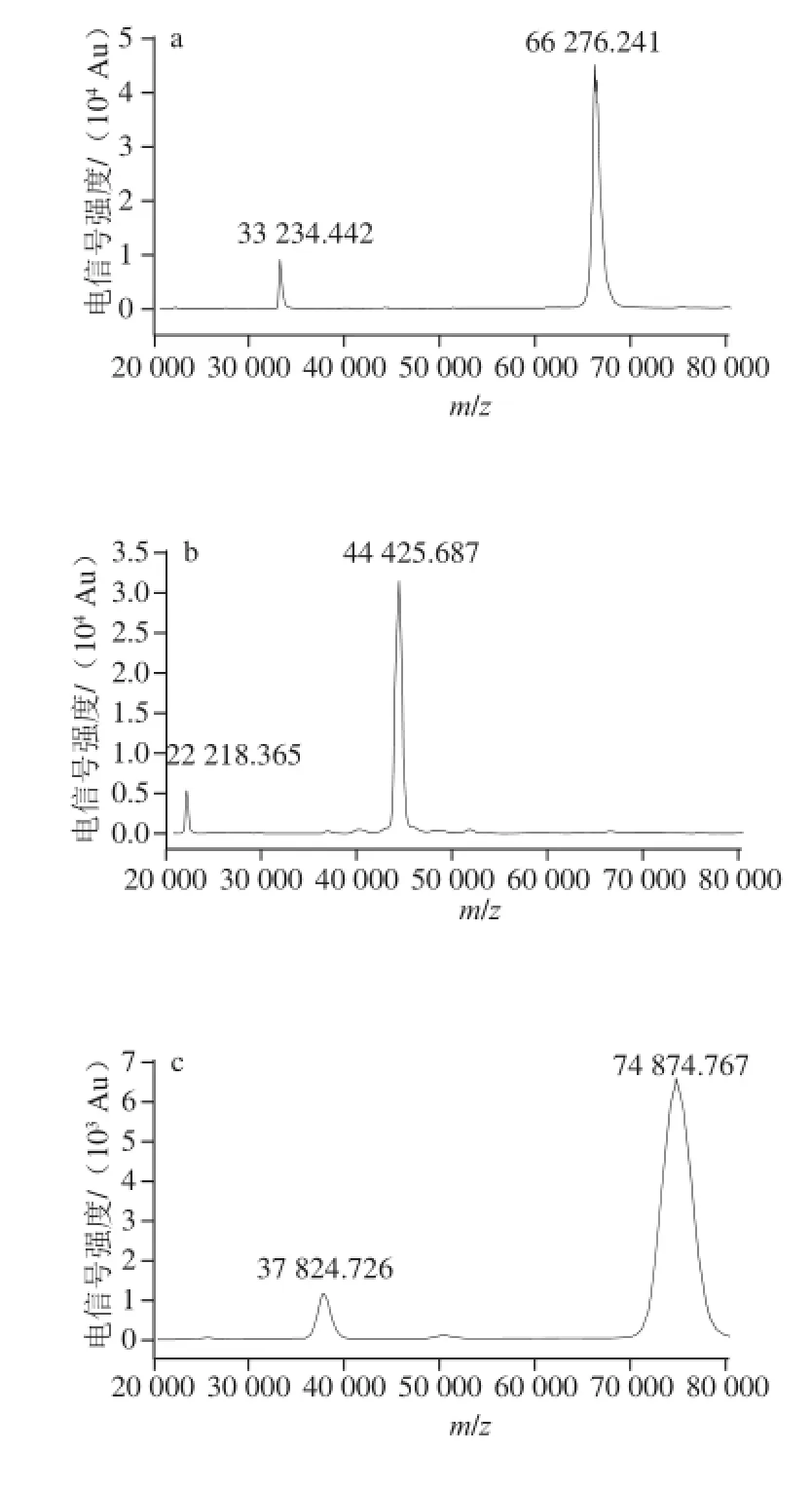
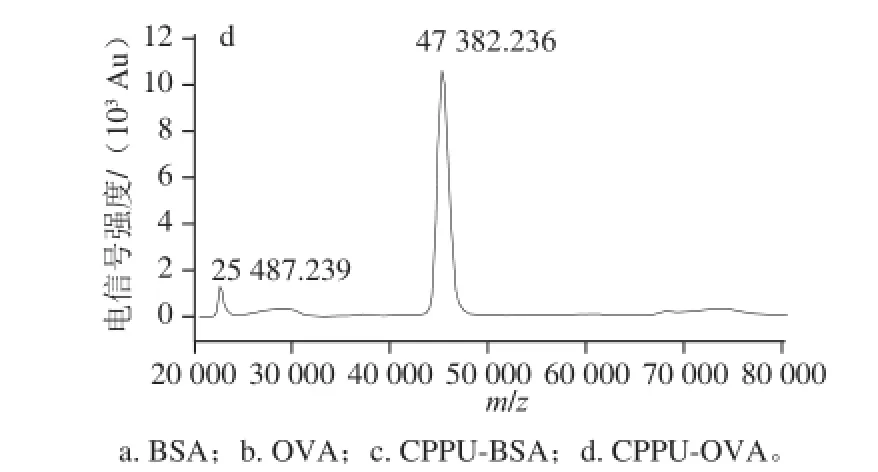
图8 载体蛋白和人工抗原的质谱图Fig. 8 Mass spectra of carrier proteins and artificial antigens
由MALDI-TOF-MS测定结果可知,载体蛋白BSA的单电荷离子峰为66 276.241(图8a),OVA的单电荷离子峰为44 425.687(图8b),全抗原CPPU-BSA的分子离子峰为74 874.767(图8c),CPPU-OVA的分子离子峰为47 382.236(图8d),这些数据很好地说明了半抗原小分子成功地与载体蛋白进行了偶联[27]。已知CPPU-COOH相对分子质量是347,可得出平均每个载体蛋白BSA分子上偶联的CPPU-COOH分子个数=(74 874.767-66 276.241)/347≈24.78 个。载体蛋白OVA分子上偶联的CPPU-COOH分子个数=(47 382.236-44 425.687)/347≈8.52 个。为获得相应的抗血清,合成的人工抗原一般要求小分子与载体蛋白的偶联比在1∶10~1∶25之间,方可有效地刺激机体产生免疫应答[28],另有文献报道每一载体上含有8~25 个半抗原能得到效价较高的抗体[29]。因此从偶联比结果来看,用本研究制备的CPPU免疫抗原(CPPU-BSA)免疫小鼠,有可能产生相应的应答。
3 结 论
本研究以CPPU和丁二酸酐为反应物,采用傅克反应制备CPPU-COOH,成功地在CPPU的苯环上引入一个含3 个碳原子的连接臂和活性基团羧基,既保留了CPPU的特征结构,又能够与载体蛋白偶联合成抗原,同时合适的连接臂可以很好地使小分子半抗原充分暴露在载体蛋白的表面,便于抗原递呈细胞对其的识别,产生免疫应答[26]。采用重结晶法对合成的CPPU-COOH进行了纯化,以避免杂质与载体蛋白偶联而影响免疫效果。在此基础上,采用EDC法制备了CPPU的免疫抗原及包被抗原。应用紫外光谱、质谱、核磁共振、元素分析等技术,对所制备的CPPU-COOH及其全抗原进行了结构鉴定。同时采用MALDI-TOF-MS分析技术,测得免疫原和包被原的偶联比分别为24.78∶1和8.52∶1,表明成功合成了CPPU人工抗原,为其抗体的制备和免疫法的构建提供了依据。
参考文献:
[1] 史晓梅, 金芬, 黄玉婷, 等. 水果中常用植物生长调节剂的研究进展[J]. 食品工业科技, 2012, 33(4): 417-422; 426. DOI:10.13386/ j.issn1002-0306.2012.04.009.
[2] 朱杰丽, 杨柳, 柴振林, 等. 国内外植物生长调节剂限量标准分析研究[J]. 生物灾害科学, 2013, 21(2): 232-236. DOI:10.3969/ j.issn.2095-3704.2013.02.025.
[3] VALVERDE A, AGUILERA A, FERRER C, et al. Analysis of forchlorfenuron in vegetables by LC/TOF-MS after extraction with the buffered QuEChERS method[J]. Journal of Agricultural and Food Chemistry, 2010, 58(5): 2818-2823. DOI:10.1021/jf904465s.
[4] 卫生部. 食品中农药最大残留限量: GB 2763—2014[S]. 北京: 中国标准出版社, 2014: 110-111.
[5] 罗伟强, 肖小华, 杜卓, 等. 整体柱固相萃取-高效液相色谱法在线分析水果中的氯吡脲[J]. 色谱, 2014, 30(4): 407-412. DOI:10.3724/ SP.J.1123.2013.11011.
[6] LIU Qiang, GONG Dong, PENG Xiang. Determination of forchlorfenuron dissipation and residue in cucumbers and red soil[J]. Journal of Northeast Agricultural University, 2010, 17(1): 27-31.
[7] CHRIS S, MICHAEL S, NARRONG C, et al. Collaborative validation of the QuEChERS procedure for the determination of pesticides in food by LC-MS/MS[J]. Journal of Agricultural & Food Chemistry, 2011, 59(12): 6383-6411. DOI:10.1021/jf201618q.
[8] TRAN K, EIDE D, NICKOLS M, et al. Finding of pesticides in fashionable fruit juices by LC-MS/MS and GC-MS/MS[J]. Food Chemistry, 2012, 134(4): 2398-2405. DOI:10.1016/ j.foodchem.2012.04.034.
[9] 冯翀. 食品中真菌毒素检测分析: 以酶联免疫吸附法(ELISA)为例[J].中国科技博览, 2011, 10(36): 264-265.
[10] 王升吉, 杨崇良, 尚佑芬, 等. 免疫分析法在农药残留检测中的应用及前景[J]. 山东农业科学, 2005, 27(4): 72-75.
[11] LEDOUX M. Analytical methods applied to the determination of pesticide residues in foods of animal origin. a review of the past two decades[J]. Journal of Chromatography A, 2011, 1218(8): 1021-1036. DOI:10.1016/j.chroma.2010.12.097.
[12] 陈婷. 酶联免疫分析法及其在兽药残留检测中的应用[J]. 福建畜牧兽医, 2008, 30(5): 30-32.
[13] 宋娟, 王榕妹, 王悦秋, 等. 半抗原的设计、修饰及人工抗原的制备[J]. 分析化学, 2010, 38(8): 1211-1218. DOI:10.3724/ SP.J.1096.2010.01211.
[14] 邓发亮, 刘晓云, 唐时幸, 等. 莱克多巴胺人工抗原的合成与鉴定[J].食品科学, 2013, 34(18): 146-149. DOI:10.7506/spkx1002-6630-201318029.
[15] TORRES O B, JALAH R, RICEK C, et al. Characterization and optimization of heroin hapten-BSA conjugates: method development for the synthesis of reproducible hapten-based vaccines[J]. Analytical & Bioanalytical Chemistry, 2014, 406(24): 5927-5937. DOI:10.1007/ s00216-014-8035-x.
[16] THYES M, LEHMANN H D, GRIES J, et al. 6-Aryl-4,5-dihydro-3(2H)-pyridazinones. A new class of compounds with platelet aggregation inhibiting and hypotensive activities[J]. Journal of Medicinal Chemistry, 1983, 26(6): 800-807. DOI:10.1021/ jm00360a004.
[17] 章杰兵, 柴晓云, 俞世冲, 等. 哒嗪酮类化合物的合成及其抗血小板聚集活性[J]. 第二军医大学学报, 2009, 30(7): 821-824. DOI:10.3724/SP.J.1008.2009.00821.
[18] 曾磊, 周常义, 苏国成, 等. 呋喃唑酮代谢物人工抗原的合成及半抗原偶联比的测定[J]. 安徽农业科学, 2013, 41(3): 961-962. DOI:10.13989/j.cnki.0517-6611.2013.03.176.v.
[19] NA Yu, SHENG Wei, YUAN Meng, et al. Enzyme-linked immunosorbent assay and immunochromatographic strip for rapid detection of atrazine in water samples[J]. Microchimica Acta, 2012, 177(1/2): 177-184. DOI:10.1007/s00604-012-0772-y.
[20] LI Qingxiao, ZHAO Mengshu, GEE S J, et al. Development of enzyme-linked immunosorbent assays for 4-nitrophenol and substituted 4-nitrophenols[J]. Journal of Agricultural and Food Chemistry, 1991, 39(9): 1685-1692. DOI:10.1021/jf00009a028.
[21] CAO Zhen, ZHAO Hongwei, CUI Yongliang, et al. Development of a sensitive monoclonal antibody-based enzyme-linked immunosorbent assay for the analysis of paclobutrazol residue in wheat kernel[J]. Journal of Agricultural and Food Chemistry, 2014, 62(8): 1826-1831. DOI:10.1021/jf404905w.
[22] 王莹, 王希春, 金福源, 等. 质谱法测定4 种真菌毒素与载体蛋白偶联物的结合比[J]. 食品科学, 2012, 33(2): 219-223.
[23] 齐小花, 王正方, 金泳, 等. 生物质谱法对人工抗原偶联比的快速测定[J]. 检验检疫科学, 2007, 1(增刊1): 56-57.
[24] 金茂俊, 王静, 杨丽华, 等. 化学发光免疫分析方法在食品安全检测中的研究进展[J]. 食品安全检测学报, 2014, 5(3): 840-845.
[25] 王建华, 张冲. 小分子抗原人工合成进展[J]. 应用化学, 2011, 28(4): 367-375.
[26] 晁博, 薛飞群. 小分子半抗原抗体制备技术的研究进展[J]. 中国兽医科学, 2006, 36(9): 757-762.
[27] ERLNGER B F. The preparation of antigenic hapten-carrier conjugates: a survey[J]. Methods in Enzymology, 1980, 70(1): 85-104.
[28] BYZOVAN A, ZVEREVA E A, ZHERDEV A V, et al. Rapid pretreatment-free immunochromatographic assay of chloramphenicol in milk[J]. Talanta, 2010, 81(3): 843-848. DOI:10.1016/ j.talanta.2010.01.025.
[29] 张蕾, 马凡舒, 闫喜军, 等. 单克隆抗体制备的关键因素[J]. 特产研究, 2015, 37(1): 69-71. DOI:10.3969/j.issn.1001-4721.2015.01.017.
Synthesis and Identification of Artificial Antigens of Forchlorfenuron
XIAO Shimei1, YAN Aiping2, XIAO Fang1, WAN Yiqun1,2, GUO Lan1,2,*
(1. College of Chemistry, Nanchang University, Nanchang 330031, China; 2. Center of Analysis and Testing, Nanchang University, Nanchang 330047, China)
This work aimed to develop an effective novel method to synthesize artificial antigens of forchlorfenuron (CPPU). Towards this goal, Friedel-Crafts reaction was used to modify the structure of forchlorfenuron with the catalysis of anhydrous aluminum chloride and the hapten was coupled with bovine serum albumin (BSA) and ovalbumin (OVA) by carbondiimine (EDC) method, respectively, to obtain forchlorfenuron immunogen and coating antigen. The molecular structure of the forchlorfenuron hapten was identified by elemental analysis, mass spectroscopy (MS) and nuclear magnetic resonance spectroscopy (1H-NMR). The artificial antigens were identified by UV spectroscopy and high performance matrix assisted laser desorption ionization time of flight mass spectroscopy (MALDI-TOF-MS). The experimental results showed that the artificial antigen of forchlorfenuron has been synthesized successfully and it can lay the foundation for the preparation of antibody and the development of immunoassays.
forchlorfenuron; hapten; artificial antigen; synthesis; identification
10.7506/spkx1002-6630-201621031
TS201.2
A
1002-6630(2016)21-0183-06
肖石妹, 鄢爱平, 肖芳, 等. 氯吡脲人工抗原的合成与鉴定[J]. 食品科学, 2016, 37(21): 183-188. DOI:10.7506/spkx1002-6630-201621031. http://www.spkx.net.cn
XIAO Shimei, YAN Aiping, XIAO Fang, et al. Synthesis and identification of artificial antigens of forchlorfenuron[J]. Food Science, 2016, 37(21): 183-188. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201621031. http://www.spkx.net.cn
2016-01-31
江西省科技支撑计划重大项目(20143ACG70005;20133ACG70002);国家自然科学基金地区科学基金项目(21465017)
肖石妹(1990—),女,硕士研究生,研究方向为食品质量与安全。E-mail:1959499683@qq.com
*通信作者:郭岚(1973—),女,研究员,博士,研究方向为食品质量与安全。E-mail:guolan@ncu.edu.cn
