某市再生水灌区水土环境中PPCPs污染特征分析
2016-12-01黄德亮何江涛何宝南中国地质大学北京水资源与环境学院水资源与环境工程北京市重点实验室北京100083
黄德亮,何江涛,杨 蕾,何宝南 (中国地质大学(北京)水资源与环境学院,水资源与环境工程北京市重点实验室,北京 100083)
某市再生水灌区水土环境中PPCPs污染特征分析
黄德亮,何江涛*,杨 蕾,何宝南 (中国地质大学(北京)水资源与环境学院,水资源与环境工程北京市重点实验室,北京 100083)
为初步了解再生水灌区土壤环境中药物与个人护理品(PPCPs)的污染特征,识别灌区地下水中PPCPs的主要来源,对某市东南郊Y灌区内的淸灌区、再生水灌区以及湿地三种类型的场地进行了精细剖面钻探工作,采集不同深度土壤、灌区地表水及成井地下水样品,分别对其进行了常规指标和15种PPCPs浓度的测试.结果表明,不同场地土壤中PPCPs含量分布存在差异,土壤剖面中PPCPs含量总体表现为再生水灌区>清灌区>湿地.土壤中PPCPs总浓度平均值为15.6μg/kg,主要以卡马西平CBZ、苯扎贝特BF、吉非罗齐GF、氯霉素CP、吲哚美辛IM为主.灌区地表水中 PPCPs总含量明显高于地下水,总浓度平均值分别为 272.5ng/L和 63.5ng/L,且地表水中,PPCPs含量呈现沿程递减现象.利用Multi-cell基本原理并结合推流的概念刻画PPCPs从地表穿透土壤包气带进入地下水的垂向输移过程,计算结果显示除卡马西平CBZ、甲芬那酸MA和萘啶酸NA外,其余9种PPCPs计算值和地下水中的实测值吻合良好,初步证实再生水是灌区地下水中PPCPs的主要来源.
药物及和人护理品(PPCPs);再生水灌区;折减系数;源识别
药物及个人护理品(PPCPs)作为人类的必需品,种类繁杂,包括各类抗生素、人工合成麝香、止痛药、降压药、避孕药、催眠药、减肥药、发胶、染发剂和杀菌剂等.1999年,Daughton等[1]对PPCPs环境污染与生态风险的综述研究逐渐引起人们对这类新型污染物的关注.随着环境分析技术的进步,地下水环境中PPCPs的检出成为最严重的环境问题之一[2],而再生水被认为是城市地下水中PPCPs等新型有机污染物的主要来源.在缺水的北方,城市污水的再生回用已经成为缓解水资源匮乏的重要途径[3],再生水被广泛应用于农业灌溉、景观用水和含水层补给[4].再生水回用虽能缓解一定的供水压力,但由于污水处理厂现有工艺的制约,对 PPCPs等不能有效去除,导致其最终进入环境介质,长期暴露对生物和人类健康造成潜在危害.景观用水[5]、海洋[6]、灌溉农田[7-8]、河流以及地下水[9-13]中已有不同程度PPCPs检出.考虑到再生水的利用对环境的影响日益严重,因此开展PPCPs在环境中运移方法分析以及污染来源解析具有重要意义.
本文对B市东南郊Y灌区内的淸灌区、再生水灌区以及湿地3种类型的场地进行了精细剖面钻探工作,采集不同深度土壤、灌区地表水及成井地下水样品,分析了 PPCPs的检出情况、含量水平和分布特征,结合场地钻孔土壤垂向剖面,初步探索PPCPs在‘地表水-土壤-地下水’的响应关系,运用 Multi-cell基本原理并结合推流的概念对包气带中 PPCPs污染进行量化,对再生水灌区土壤和地下水中 PPCPs来源进行识别.
1 材料与方法
1.1 研究区概况
再生水灌区位于某市东南郊区(如图1),该市位于山前冲积平原,西北地势高,主要为基岩,松散堆积物主要分布在东南地势低的山前平原.灌区耕种方式主要以传统玉米小麦轮种和蔬菜大棚种植为主,其中蔬菜大棚为井灌,传统农作物种植区为再生水灌溉.再生水来自灌区北侧4km处的河,经引水渠引入进行农田灌溉.河水主要来自于上游某污水处理厂处理后的再生水.湿地位于再生水灌区南部,面积约 0.07km2,湿地蓄水主要来源于农田灌溉后的余水.
1.2 样品采集
采用地质勘探冲击钻于2014年11月对再生水灌区进行垂向精细剖面钻探工作,共布置3个钻孔(钻孔分布见图1),钻孔深度12.5~15.0m不等,地下水位在8.9~11.4m.其中钻孔Y-1位于井灌区内,以场地地下水作为清灌区对照组;Y-2位于再生水灌区内,位于传统作物区;钻孔Y-3位于湿地内,为再生水补给湿地场地.共采集土壤样品43组,采样原则为:浅层加密采样,采样间距在0.2~0.5m;深层采样间距可适当加大,为在 1~2m,具体采样情况见表 1.土样均用锡箔纸避光保存于自封袋中,放入便携式冰箱冷藏.
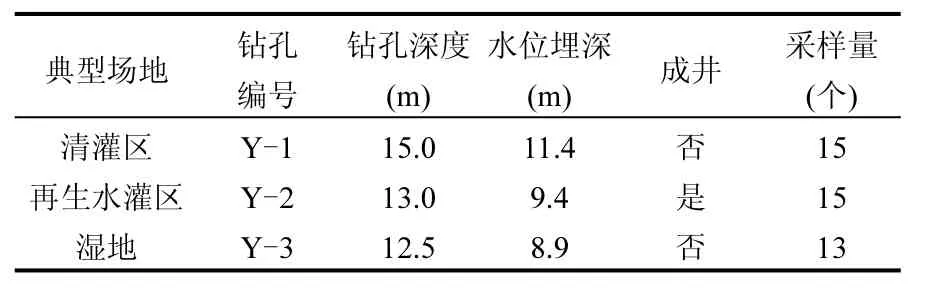
表1 研究区采样采集情况场地土样采集情况Table 1 Information on soil sampling sitesin study area
同期对灌区内灌溉用水进行沿程采样,并对Y-2钻孔成井地下水样品进行采集,地下水采用PVC贝勒管采样器(bailers tube)进行采集,地表水采用便携式手持取样泵采集.地表水采集按照上下游顺序,地表水 4个采样点.地表水采样点位一般应在水面0.5m以下,距河底0.5m以上,样品放在1L棕色瓶中;成井地下水采样前进行洗井,共采集水样2个,采样量为2L.所有样品暂存于便携式冷藏箱中,带回实验室后置于0~4℃冰箱保存.
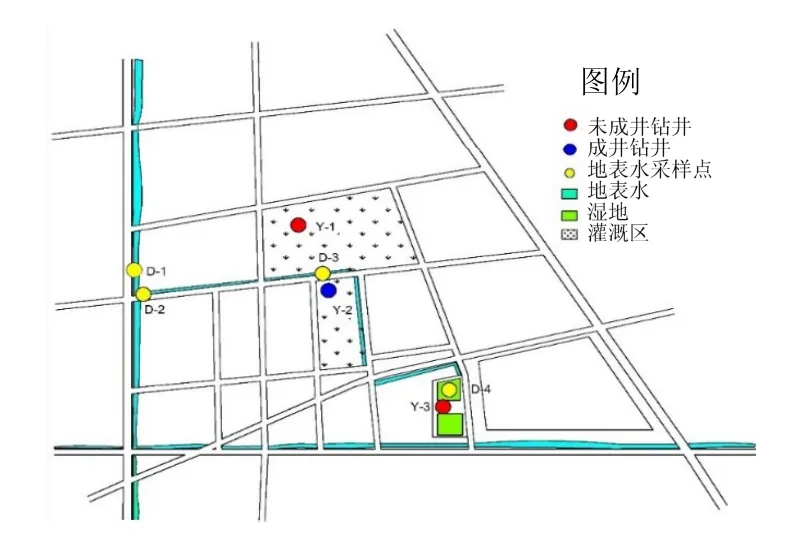
图1 研究区及采样点分布Fig.1 Study area and sampling sites
1.3 样品测试
本研究选用高效液相色谱—串联质谱法(HPLC-MS/MS),详见Dai的文章[2],优化了不同介质PPCPs前处理方法,建立了能同时、快速检测水、土样品中15种PPCPs的分析方法.15种药物标品均购自 Dr.Ehrenstorfer(德国),纯度>95%,相关理化性质参数如表2所示.所用试剂均为色谱级,超纯水由Milli-Q超纯水系统制得(Millipore,美国).
1.3.1 水样前处理用经在马弗炉中 450℃灼烧4h的直径为47mm的玻璃纤维滤纸进行水样过滤.取过滤后的水样加入 50ng D3—mecoprop和13C—phenacetin替代物,不调节pH值.先后用5mL甲醇、3×5mL超纯水依次通过小柱进行活化.大容量采样线与 HLB小柱相连,另一头浸入水样,调节固相萃取装置使得水样速率为5~10mL/min.后用5mL5%甲醇溶液(超纯水:甲醇=19:1,V:V)清洗柱子去除杂质,真空干燥1h.用4mL甲醇进行洗脱2次,洗脱液经平行蒸发浓缩,后用甲醇定容至1mL,经 0.22µm针头过滤器过滤并移入棕色进样瓶,于4℃冰箱保存待测.

表2 PPCPs理化性质Table 2 The physicochemical propertiesof PPCPs
空白加标回收率实验:向6组1L超纯水中分别加入25ng PPCPs混标和50ng上述替代物,操作步骤与水样一致,得到回收率为 95%~105%,RSD为3.5%;样品加标回收实验:分别向3组(每组6份)1L地表水样品和1L地下水样品中添加10、50和100ng低、中、高3个浓度梯度的PPCPs混标和50ng D3—mecoprop和13C—phenacetin替代物,与水样处理方法一致,样品加标回收率分别为:地表水为 70%~88%、86%~95%和 83%~101%,地下水为80%~98%、83%~95%和93%~105%.
1.3.2 土壤前处理将所取土样冻干研磨过60目筛后准确称取2.0g于15mL离心管中,加入50ng替代物,避光老化24h;加入8ml甲醇水提取液(甲醇:水=1:2,V:V,);经涡旋1min;超声15min浸提后,5000rpm离心10min;将上清液移入1L棕色样品瓶中.上述步骤重复 3次,3次提取上清液共30mL.加超纯水稀释定容至 500mL,后续步骤同上述水样处理过程.
样品加标回收率实验:取6组同一采样点土壤样品各2.0g,分别加入50ngPPCPs混标和50ng D3—mecoprop和13C—phenacetin替代物,后续处理步骤通土样,得到的样品加标回收率为:68%~118%,相对标准偏差RSD为8.5%;内标回收率为88%~99%.
1.3.3 质量控制为保证测试结果的准确性,选用以下质量保证与质量控制措施:
①每批样品测定前后,各测定一次标准曲线溶液,用于判断仪器响应变化,其相对变化不大于10%.每个样品添加替代物50ng,回收率为80%~98%;②每批样品均设置实验室空白和野外取样空白,要求空白值不得高于仪器最低检出限;③每批样品,每 10个设置一个平行样品,平行样品的相对误差小于30%;④每批样品,每10个设置一个样品加标,加标量为50ng,加标回收率为75%~110%.
2 结果与讨论
2.1 场地地表水及地下水中PPCPs含量分析
对场地再生水河道以及成井地下水取样分析,从图2(a)中可以发现,水样中PPCPs总浓度均超过50ng/L,地表水PPCPs总浓度均大于地下水,地表水与地下水中美托洛尔MTP无检出,此外地下水中普萘洛尔PPN、舒必利SP、甲氧苄啶TP、苯扎贝特BF、吉非罗齐GF、吲哚美辛IM均没有检出.根据地表水取水位置顺序发现,PPCPs浓度含量水平从上游到下游呈现递减的趋势,已有研究表明,PPCPs在随再生水流动的过程中,部分能够被光解、水解或者被悬浮颗粒物、河流沉积物吸附[14],从而 PPCPs沿程浓度呈降低趋势,图2(b)中对比发现,CF和DEET沿再生水河渠段含量呈上升趋势.咖啡因和避蚊胺作为中区兴奋药和杀虫剂在人类社会中使用十分广泛,人类直接或间接丢弃在水环境中的咖啡因会在水环境中长时间存在[6,15].场地只有一条河渠,不存在其他河道汇流,推测在人类活动对河渠段影响强烈,导致CF和DEET含量延程略微增高.进一步分析发现单个 PPCP浓度和组成在沿程地表水及场地成井地下水样品中也存在差异,CBZ在地表水中的最大检出浓度为21.6ng/L,而在#Y-2地下水中高达38.89ng/L,与此相同的还有NA;而CF在地表水中的浓度范围为 45.4~160ng/L,而在地下水中仅为 6.3ng/L,地表水中的浓度明显高于地下水,DEET、SP、TP、BF、DF、IM的检出情况也呈现出与 CF一致的特征;而检出浓度较低的PPN、CA、CP、GF、MA的地表水与地下水的含量并无明显变化.
目前,PPCPs在世界范围内已被广泛被检出,表3为本灌区检出PPCPs浓度与国内外其他地区对比,从表3可以发现,本研究区地下水与地表水中的PPCPs含量水平处于中等水平.
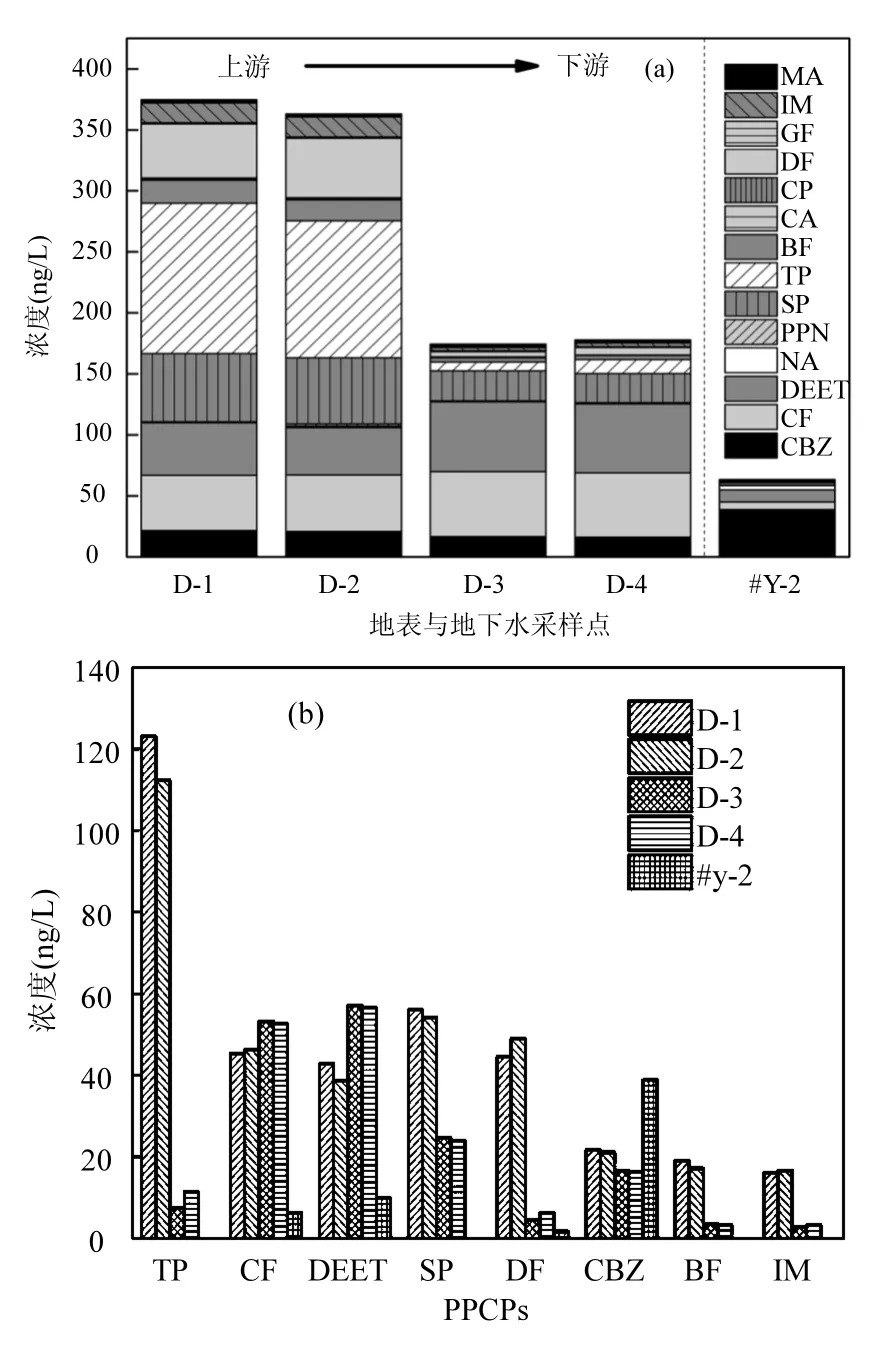
图2 研究区沿程水样PPCPs的浓度分布Fig.2 Concentrationsof PPCPs at different sitesin study area
2.2 土壤剖面 PPCPs的检出情况及含量分析
图3为对4个钻孔的59个土壤样品中目标污染物的检出率和含量进行的统计分析,PPCPs的检出情况存在较大的差异性.其中卡马西平CBZ和吉非罗齐GF的检出率最高,分别达到85%和79%,其次为氯霉素CP,检出率为65%,萘啶酸NA 和舒必利SP的检出率最低,仅为2%,仅次于检出率为5%的甲芬那酸MA和甲氧苄啶TP,而避蚊胺DEET、普萘洛尔PPN、氯贝酸CA均没有检出.而从检出浓度来看,15种 PPCPs 总含量的平均值为15.60ug/kg.以美托洛尔MTP的检出浓度最高,为63μg/kg,其次为氯霉素CP,其最大检出浓度为42.25μg/kg.单个PPCP在不同深度土层中的赋存浓度差异性较大,氯霉素 CP和卡马西平CBZ的平均检出浓度最高,分别为 2.52μg/kg和2.12μg/kg.其次为吉非罗齐GF,其平均检出浓度为1.55μg/kg,苯扎贝特BF为1.36μg/kg,而除了未检出的PPCPs,平均检出浓度最小的是舒必利SP,仅为0.19μg/kg.而从检出浓度的中位值进行分析,仅CBZ和GF的中位值为0.42ug/kg和0.27ug/kg外,其余PPCPs中位值均为0.

表3 国内外不同地区水体中PPCPss检出情况Table 3 Concentrations of PPCPs detected in water from different countries and regions in the world
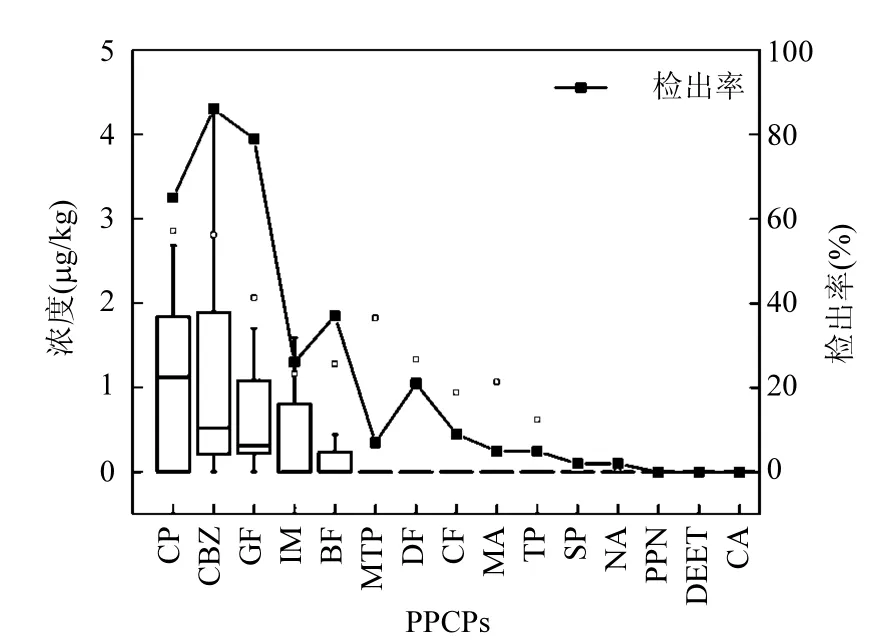
图3 土壤中15种PPCPs的检出率与含量特征Fig.3 Concentration and detection rate of 15selected PPCPs in soil
图4为对场地3个钻孔各深度土样中检出率高的5种PPCPs浓度分布特征进行的分析,从图4可以看出,土壤中PPCPs含量水平为再生水灌区>清灌区>湿地.其中土壤含量水平较高主要以卡马西平 CBZ、氯霉素CP为主,其平均值在灌区中Y-1为2.97ug/kg与3.10ug/kg,在Y-2为4.32ug/kg与3.36ug/kg.灌区土壤中PPCPs浓度分布差异明显,作为再生水灌溉的Y-2区中其5种典型PPCPs均有不同程度的检出,其中最大值相差不大.清灌区中除了卡马西平CBZ、氯霉素 CP,其他 3种PPCPs含量水平较低.研究表明,24h之内卡马西平最大去除率约为 24%,在污水中很难被去除[22],在地下水中卡马西平浓度降低的原因主要是由于稀释作用的影响[23].氯霉素可通过疏水相互作用而被土壤吸附,因为其较低的Kd值导致在土壤中表现为较低的被吸附能力和较高的迁移能力
[24].而湿地Y-3钻孔位于蓄水沟西南侧3m处,土壤中 PPCPs随深度分布均匀,推测该水沟作为直接污染源对Y-3剖面PPCPs的侧向输移产生重要影响.Y-1和Y-2钻孔都处于传统作物种植区,灌溉制度相同,都只能通过表层入渗方式进入地下水,Y-1为井水灌溉,灌溉用水差异明显.
2.3 土壤剖面中PPCPs垂向分布特征分析
Y-1和Y-2属于灌溉农田区,Y-3为湿地区,从图5可看出其总体含量呈表层高深层低分布.从含量上看灌溉农田的两个钻孔最高含量均有超过100μg/kg,含量主要分布在0~3m,3m以下含量几乎均小于检出限;湿地的钻孔含量相对较低且分布均匀,各层取样深度均没有超过10μg/kg, PPCPs含量分布与岩性介质没有明显的关系.
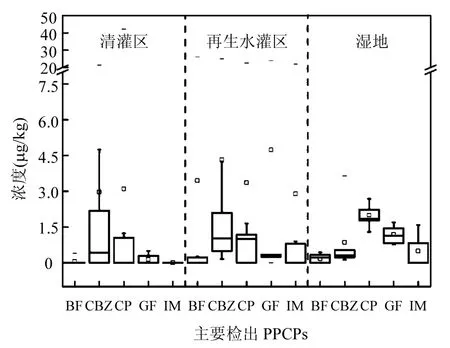
图4 研究区钻孔剖面典型PPCPs浓度箱形图Fig.4 Concentrations of selected PPCPsat typical contaminated site in study area
由于Y-1和Y-2场地为灌溉区,垂向灌溉水补给为主要入渗方式,而Y-3位于湿地内,存在一蓄水沟对其发生侧向补给,因此场地介质差异性导致垂向分布不一致,从图 5中可以发现,Y-1清灌区的PPCPs种类最少,仅有CBZ、CP和MTP的检出浓度较高,而Y-2和Y-3均检出较多种类的 PPCPs,可见场地灌溉水源的不同,导致下渗土壤中赋存 PPCPs种类的不同.Y-1与 Y-2土壤中最大含量深度分别位于2m 与 2.5m,推测在再生水非持续补给情况下,该层的包气带存在毛细管悬挂带可以截留PPCPs于土壤中,导致浓度在2m处浓度高于上表层,该现象与 Carmen[25]等研究的结论基本一致.Y-3湿地的PPCPs含量相对于灌区较低,随深度增加其浓度均有被检测,但总体上浓度有降低的趋势.
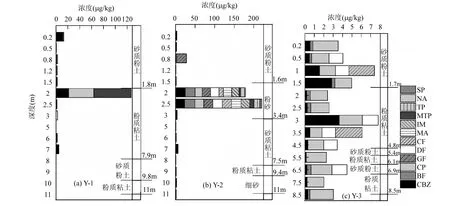
图5 研究区总PPCPs浓度垂向剖面图Fig.5 Verticaldistribution of total concentration of PPCPs in different profiles in study area
通过对比再生水与土壤中PPCPs的检出情况,可以发现,再生水中PPN、NA、CA、CP、GF本身浓度含量水平较低,对土壤以及地下水影响较小,TP、CF、SP、DF和DEET几种PPCPs在再生水中浓度含量远远高于土壤中检出浓度,在土壤中不容易吸附、溶解性好的物质在地下水中较易积累,推测土壤中低浓度低检出率与灌溉水源的初始浓度、理化性质有一定关系,表现为PPCPs溶解度大的越难被土壤中有机物吸附,反之越容易被吸附[26].不同性质的 PPCPs在环境中有着不同的迁移行为,导致空间分布出现差异性,PPCPs在环境中迁移转化规律需要进一步研究.
2.4 “地表源与地下水”之间响应关系
为探讨地表源与地下水之间PPCPs的响应关系,为源识别提供依据,本文利用Multi-cell基本原理并结合一维饱和推流的概念,主要考虑污染物在包气带介质中发生的吸附和降解作用,建立一个可以表征PPCPs在包气带中迁移时间、迁移距离及相应污染物浓度的过程单元模型.并对研究区Y-2进行公式试算,与实际土壤中和地下水中PPCPs浓度进行比对.
2.4.1 推导公式 PPCPs等在土壤中的吸附迁移过程非常复杂,主要受到污染物自身理化性质、土壤环境条件等因素的影响.从而导致PPCPs在土壤中的环境行为差异明显,其中吸附作用和降解作用是最主要的两个过程.在前期野外检测数据的基础上,选取再生水灌区Y-2钻孔,利用折减系数法对其包气带中PPCPs污染进行量化,充分考虑钻孔包气带岩性、污染物属性特征等差异对污染物衰减产生的影响.
假设污染物进入包气带介质过程中发生吸附反应和降解两个反应,依据质量守恒定理可得
式中:Min为在时间 t内进入单元体的溶质质量;Mout为在时间t内流出单元体的溶质质量;Ms为t时间内单元体增加的溶质质量;Md为在t时间内由于降解反应消耗的溶质质量.
假设在理想条件下,Y-2钻孔包气带介质是由均质介质构成的,溶质经过时间 t从地表随再生水下渗穿透包气带介质.包气带介质中溶质的吸附和解吸能够迅速的达到平衡,属于线性等温吸附.并且在包气带介质中发生的生物降解反应符合一级衰减动力学方程,可得式(2)
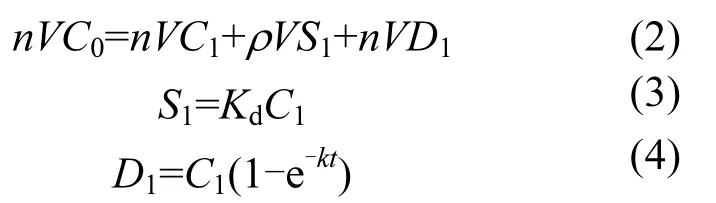
式中:n为土壤孔隙度;ρ为土壤介质容重;V为垂向单位土壤介质的体积;C0为初始时刻液相浓度;C1为时间t单元体的液相浓度;S1为时间t内单元的固相浓度;D1为时间t内单元体消耗的浓度;Kd为达到吸附平衡时固相和液相污染物的分配系数;k为降解速率常数.
将公式(3)和(4)带入公式(2)中求得系数 W,之后将W称之为折减系数

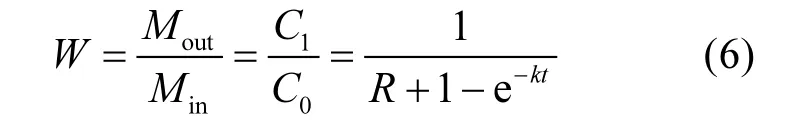
在此基础上,若得到PPCPs在包气带介质中的降解率,则可以根据在包气带介质中发生的吸附和降解反应时的原理将公式(4)简化为

式中:D1为时间t内单元体消耗的浓度;d为降解率常数.
从而折减系数W
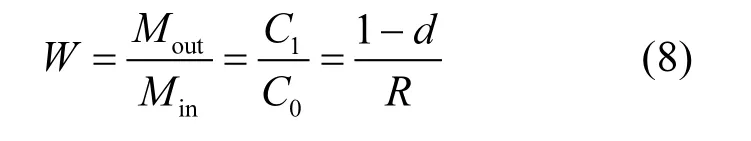
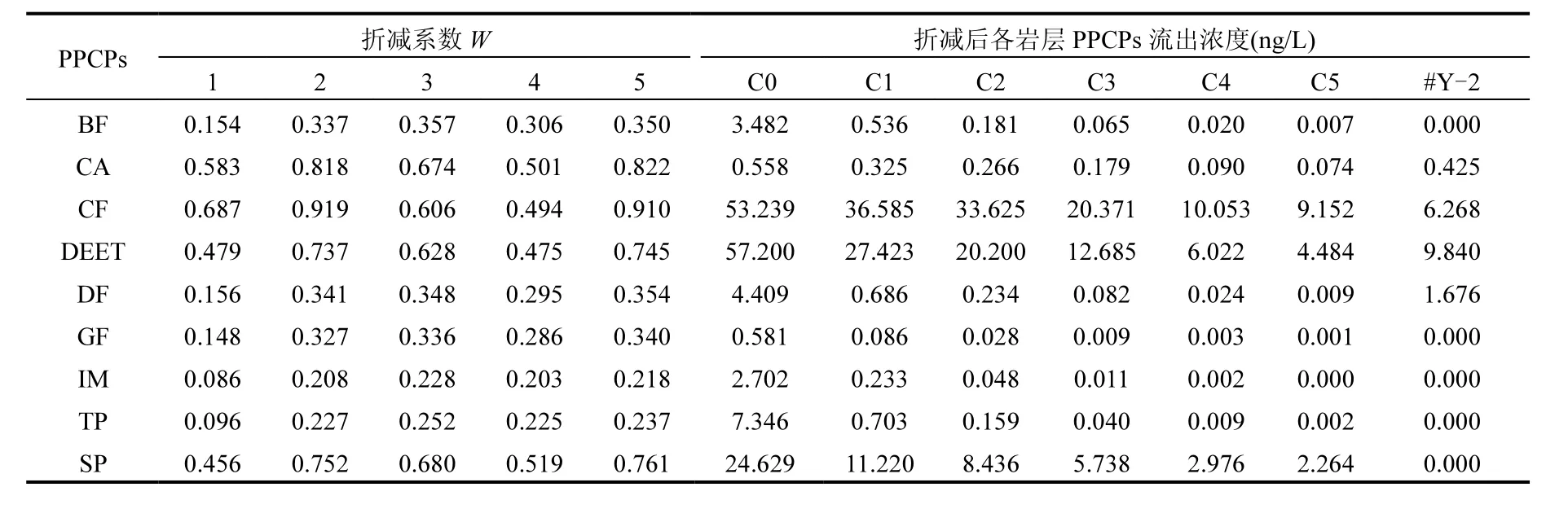
表4 15种PPCPs在Y-2土壤剖面包气带介质中的折减系数与折减浓度汇总Table 4 Reduction factor and reduction concentration of 15 selected PPCPs in aeration zone of Y-2soil profile
PPCPs折减浓度计算,将PPCPs地表排放量与每种包气带介质中的系数W相乘,扣除经过吸附作用和降解作用后流出的 PPCPs的液相浓度作为进入下一个均质部分的初始浓度进行计算,以此类推,最终从最后一个土壤介质类型中流出的液相浓度即为 PPCPs穿透整个包气带介质后的液相浓度.
2.4.2 计算结果与分析 按照上述计算公式,对再生水灌区内Y-2土壤剖面15种PPCPs在钻孔包气带介质中的折减系数进行计算.包气带介质的土壤容重和有机碳含量均为土样实测值,孔隙度n参考松散岩石孔隙度参考值赋值,渗透系数参考松散岩石渗透系数参考值赋值.分配系数Kd=Koc·foc,PPCPs的Koc值由EPI Suit 4.11 软件查得.如图5中所示,Y-2钻孔共有5层岩性,C1、C2、C3、C4、C5分别代表从浅层到深层的各个单元,选择地表水点D-3作为C0各PPCPs的初始浓度.
卡马西平等污染物在环境中较稳定,地下水浓度通常不会低于河流浓度[27-28],本研究中发现卡马西平CBZ、甲芬那酸MA和萘啶酸NA的地下水PPCPs浓度高于地表水,因此不适合该模型计算.氯霉素CP、美托洛尔MTP和普萘洛尔PPN的初始浓度为零,不予考虑.计算结果如表4所示,经过模型参数计算后,将最终流出包气带的PPCPs组分 C5和浓度与 Y-2成井地下水中PPCPs的检测浓度进行对比,可得到PPCPs从地表再生水穿透包气带介质进入地下水的响应关系.由表 4的计算结果与#Y-2地下水中 PPCPs的实测情况进行对比,如图 6所示,余下 9种PPCPs最终的折减浓度C5(即穿透包气带介质进入含水层的浓度)与实测地下水浓度与实测地下水浓度基本吻合,在最终的组分和浓度上显示良好的再生水地面源-地下水汇的响应关系,说明地下水中的PPCPs来源于再生水灌溉.

图6 最终单元流出的计算地下水浓度与地下水中PPCPs实际浓度对比图Fig.6 Comparison ofmeasured PPCPs concentrations in groundwater with calculated values
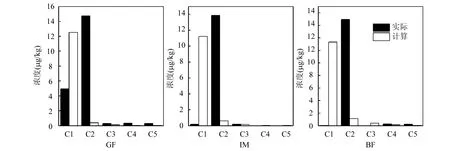
图7 3种典型PPCPs在Y-2土壤剖面包气带介质中实际含量与计算值Fig.7 Measuredand calculated concentrations for 3kinds of typical PPCPs in aeration zone of Y-2soil profile
将实际土壤中 PPCPs浓度与理论计算值进行对比.如图7所示,3种PPCPs的土壤中实际值与计算值在 C1砂质粉土、C2粉砂中相差明显,C2的实际值与C1的计算值相比大小相当,推测造成原因为采用高度概化的模型和一维饱和推流模式,模型计算公式以PPCPs的半衰期和在不同介质土壤中运移时间为计算参数,优先考虑降解,没有考虑地层因素,因此计算土壤中值吸附的浓度随之减小.而在实际环境中,PPCPs等污染物质在土壤介质中的迁移转化过程非常复杂,受到自身理化性质和环境的综合影响.折减系数法只能粗略地描述污染物只考虑吸附和降解作用时的衰减过程,但是从空间尺度上来说,仍有一定的指导意义.
3 结论
3.1 研究区再生水与地下水中总PPCPs浓度均超过 50ng/L.PPCP的浓度和组成在沿程地表水及场地成井地下水样品中存在差异,其中再生水中样品主要以咖啡因CF、避蚊胺DEET、舒必利SP和甲氧苄啶TP为主,地下水中主要以卡马西平CBZ、避蚊胺DEET为主.
3.2 研究区再生水灌区土壤中15种PPCPs总含量的平均值为 15.02ug/kg,不同场地和钻孔中PPCPs的赋存浓度和组成差异明显.灌溉区PPCPs组成主要有氯霉素CP、卡马西平CBZ、吉非罗齐GF吲哚美辛IM和苯扎贝特BF,PPCPs含量总体表现为再生水灌区>清灌区>湿地.
3.3 采用 Multi-cell基本原理并结合推流模型概念计算地表水源-土壤-地下水汇的PPCPs浓度衰减过程.其结果发现,除个别 PPCPs外,土壤中最终计算流出浓度与地下水响应较好,初步证实再生水是灌区地下水中PPCPs的主要来源.
[1] Daughton C G, Ternes T A. Pharmaceuticals and personal care products in the environment: Agents of subtle change? [J]. Environmental Health Perspectives, 1999,107:907-38.
[2] Dai G, Wang B, Huang J, et al. Occurrence and source apportionment of pharmaceuticals and personal care products in the Beiyun River of Beijing, China [J]. Chemosphere, 2015,119:1033-9.
[3] 甘一萍.北京城市污水资源化及中水回用发展现状 [J]. 城市管理与科技, 2003,(4):160-1.
[4] Xu J, Wu L, Chang A C. Degradation and adsorption of selected pharmaceuticals and personal care products (PPCPs) in agricultural soils [J]. Chemosphere, 2009,77(10):1299-305.
[5] Wang F H, Qiao M, Lv Z E, et al. Impact of reclaimed water irrigation on antibiotic resistance in public parks, Beijing, China[J]. Environ. Pollut., 2014,184:247-53.
[6] Weigel S, Kuhlmann J, Hühnerfuss H. Drugs and personal care products as ubiquitous pollutants: occurrence and distribution of clofibric acid, caffeine and DEET in the North Sea [J]. Science of the Total Environment, 2002,295(1—3):131-41.
[7] Ternes T A, Bonerz M, Herrmann N, et al. Irrigation of treated wastewater in Braunschweig, Germany: an option to remove pharmaceuticals and musk fragrances [J]. Chemosphere, 2007,66(5):894-904.
[8] Kinney C A, Furlong E T, Werner S L, et al. Presence and distribution of wastewater-derived pharmaceuticals in soil irrigated with reclaimed water [J]. Environmental Toxicology and Chemistry, 2006,25(2):317-26.
[9] Li Z, Xiang X, Li M, et al. Occurrence and risk assessment of pharmaceuticals and personal care products and endocrine disrupting chemicals in reclaimed water and receiving groundwater in China [J]. Ecotoxicology and Environmental Safety, 2015,119:74-80.
[10] Knee K L, Gossett R, Boehm A B, et al. Caffeine and agricultural pesticide concentrations in surface water and groundwater on the north shore of Kauai (Hawaii, USA) [J]. Marine Pollution Bulletin, 2010,60(8):1376-82.
[11] Peng X, Ou W, Wang C, et al. Occurrence and ecological potential of pharmaceuticals and personal care products in groundwater and reservoirs in the vicinity of municipal landfills in China [J]. Science of the Total Environment, 2014,490:889-98.
[12] Jurado A, Lopez-Serna R, Vazquez-Sune E, et al. Occurrence of carbamazepine and five metabolites in an urban aquifer [J]. Chemosphere, 2014,115:47-53.
[13] 王 丹,隋 倩,吕树光,等.黄浦江流域典型药物和个人护理品的含量及分布特征 [J]. 中国环境科学, 2014,34(7):1897-904.
[14] Liu J L, Wong M H. Pharmaceuticals and personal care products(PPCPs): a review on environmental contamination in China [J]. Environ. Int., 2013,59:208-24.
[15] Seiler R L, Zaugg S D, Thomas J M, et al. Caffeine and pharmaceuticals as indicators of waste water contamination in wells [J]. Ground Water, 1999,37(3):405-10.
[16] Del Rosario K L, Mitra S, Humphrey C P, et al. Detection of pharmaceuticals and other personal care products in groundwater beneath and adjacent to onsite wastewater treatment systems in a coastal plain shallow aquifer [J]. Science of the Total Environment, 2014,487:216-23.
[17] Fram M S, Belitz K. Occurrence and concentrations of pharmaceutical compounds in groundwater used for public drinking-water supply in California [J]. The Science of the TotalEnvironment, 2011,409(18):3409-17.
[18] Loos R, Locoro G, Comero S, et al. Pan-European survey on the occurrence of selected polar organic persistent pollutants in ground water [J]. Water Research, 2010,44(14):4115-26.
[19] Wiegel S, Aulinger A, Brockmeyer R, et al. Pharmaceuticals in the river Elbe and its tributaries [J]. Chemosphere,2004,57(2):107-26.
[20] Kim S D, Cho J, Kim I S, et al. Occurrence and removal of pharmaceuticals and endocrine disruptors in South Korean surface, drinking, and waste waters [J]. Water Research, 2007,41(5):1013-21.
[21] Teijon G, Candela L, Tamoh K, et al. Occurrence of emerging contaminants, priority substances (2008/105/CE) and heavy metals in treated wastewater and groundwater at Depurbaix facility (Barcelona, Spain) [J]. The Science of the Total Environment, 2010.
[22] 周海东,王奉飞,李 涵.PhACs在城市污水中迁移机理的研究[J]. 水资源与水工程学报, 2011(2):87-90.
[23] Clara M, Strenn B, Kreuzinger N. Carbamazepine as a possible anthropogenic marker in the aquatic environment: investigations on the behaviour of Carbamazepine in wastewater treatment and during groundwater infiltration [J]. Water Research, 2004,38(4):947-54.
[24] Pan M, Chu L M. Adsorption and degradation of five selected antibiotics in agricultural soil [J]. Science of the Total Environment, 2016,545/546:48-56.
[25] Corada-Fernández C, Jiménez-Martínez J, Candela L, et al. Occurrence and spatial distribution of emerging contaminants in the unsaturated zone. Case study: Guadalete River basin (Cadiz,Spain) [J]. Chemosphere, 2015,119:S131-S7.
[26] Karickhoff S W, Brown D S, Scott T A. Sorption of hydrophobic pollutants on natural sediments [J]. Water Research, 1979,13(3):241-8.
[27] Huntscha S, Rodriguez Velosa D M, Schroth M H, et al. Degradation of polar organic micropollutants during riverbank filtration: complementary results from spatiotemporal sampling and push-pull tests [J]. Environ. Sci. Technol., 2013,47(20):11512-21.
[28] Jurado A, Vàzquez-Suñé E, Carrera J, et al. Emerging organic contaminants in groundwater in Spain: A review of sources,recent occurrence and fate in a European context [J]. Science of the Total Environment, 2012,440:82-94.
致谢:感谢清华大学和环境保护部华南环境科学研究所对本研究的大力支持.
环境保护部发布五项污染物排放新标准
为贯彻落实国务院《大气污染防治行动计划》和《水污染防治行动计划》,通过制定、修订重点行业排放标准“倒逼”产业转型升级,环境保护部会同国家质检总局制定了《船舶发动机排气污染物排放限值及测量方法(中国第一、二阶段)》(GB 15097—2016)、《摩托车污染物排放限值及测量方法(中国第四阶段)》(GB 14622—2016)、《轻便摩托车污染物排放限值及测量方法(中国第四阶段)》(GB 18176—2016)、《轻型混合动力电动汽车污染物排放控制要求及测量方法》(GB 19755—2016)和《烧碱、聚氯乙烯工业污染物排放标准》(GB 15581—2016)等五项国家污染物排放标准.
摘自《中国环境报》
2016-08-31
Distribution characteristics of pharmaceuticals and personal care products in water and soil environment in reclaimed water irrigation area of a city.
HUANG De-liang, HE Jiang-tao*, YANG Lei, HE Bao-nan (Beijing Key Laboratory of Water Resources and Environmental Engineering, School of Water Resources and Environment, China University of Geosciences (Beijing), Beijing 10083, China). China Environmental Science, 2016,36(9):2614~2623
In order to preliminarily understand the distribution characteristics of pharmaceuticals and personal care products (PPCPs) in soil environment, and then identify the main source of PPCPs in groundwater in the farming area of southeast suburban of a city,drilled profiles in irrigation area, reclaimed water irrigation area, and wetland were investigated in detail. In each profile, samples of surface water, groundwater and soil samples from different depths were collected. The routine indexes and 15target PPCPs of all samples were analyzed. The analytical results indicated that there was an obvious difference in concentration levels of PPCPs in different areas. Generally, the concentrations of PPCPs in the soil profiles in reclaimed water irrigation area were the highest, and those in the wet lands were the lowest. The average total concentration of soil PPCPs was 15.6µg/kg. The detected PPCPs mainly includecarbamazepine, bezafibrate,gemifibrozil, chloramghenicol and indometacin. In the irrigation area, the average total concentrations of PPCPs in surface water and in groundwater were 272.5ng/L and 63.5ng/L, respectively. In surface water, there was a trend that the concentration of PPCPs decreased downwards. By using themixing Multi-cell principle and concept of Push flow, vertical transport process of PPCPs from soil surface to ground water was depicted. The calculated results of 9selected PPCPs (not includingcarbamazepine, mefenamicacidand nalidixic acid) in groundwateraccorded well with the measured values. This preliminarily indicated that the reclaimed water is the main source of PPCPs in groundwater in the irrigation area.
pharmaceuticals and personal care products (PPCPs);reclaimed irrigationarea;reduction factor;source identification
X52
A
1000-6923(2016)09-2614-10
2016-01-12
环保部公益科研专项(201309001-4);基本科研业务费(35832015023)
* 责任作者, 副教授, jthe@cugb.edu.cn
黄德亮(1991-),男,湖南醴陵人,硕士研究生,主要研究方向为地下水环境.
