三个基于Wells-Dawson型多酸的三核铜簇的合成、结构及性能
2016-11-28应俊宁亚莉侯雪田爱香
应俊 宁亚莉 侯雪 田爱香
(渤海大学化学系,锦州121013)
三个基于Wells-Dawson型多酸的三核铜簇的合成、结构及性能
应俊*宁亚莉侯雪田爱香
(渤海大学化学系,锦州121013)
在水热条件下,通过Wells-Dawson型多酸[As2W18O62]6-、氯化铜(CuCl2·2H2O)和5-(4-吡啶基)-1H-四氮唑(4-ptz)的反应,在同一反应釜中合成出2个结构完全不同的、都包含三核铜簇的多酸基化合物[Cu3(4-ptz)4(H2O)7(As2W18O62)]·42H2O(1)和[Cu3(4-ptz)5(H2O)5(As2W18O62)]·47H2O(2);当我们以另一种Wells-Dawson型多酸[P2W18O62]6-、氯化铜(CuCl2·2H2O)和5-(3-吡啶基)-1H-四氮唑(3-ptz)反应,获得了另一种多酸基三核铜簇化合物[Cu3(3-ptz)4(H2O)8(P2W18O62)]·33H2O(3)。X射线单晶衍射结果表明,化合物1为多酸单支撑三核铜簇的悬臂式结构,化合物2的多阴离子被三核铜簇交替连接形成一维链式结构,而化合物3为多阴离子和三核铜簇形成的孤立结构。吡啶-四氮唑类配体(3-ptz和4-ptz)是形成化合物1~3中三核铜簇的重要结构因素。同时,研究了3个化合物的电化学以及光催化性能。
Wells-Dawson型多酸;多核铜簇;水热合成;电化学;光催化
多金属氧酸盐,简称多酸,是距今发展近二百年的无机化学一个重要分支,在催化、电化学、磁性等领域有着广泛的应用[1-3]。到目前为止,多酸化学发展的方向除了继续探索、合成新型多酸以增加多酸种类以外,另一个重要方向就是多酸的修饰化学,即将过渡金属配合物片段引入多酸体系,对多酸分子进行修饰。所引入的过渡金属配合物片段在该类多酸基化合物中通常起到3种作用:配合物片段作为抗衡阳离子而游离于多酸分子之间,起到平衡电荷作用从而构筑零维结构[4];配合物通过连接多阴离子上的端氧或桥氧原子而共价嫁接到多酸表面,形成孤立的支撑结构[5];配合物片段可以作为连接体将多阴离子共价连接起来而构筑一维[6]、二维[7]以及三维框架结构[8]。被过渡金属配合物修饰的多酸种类,主要集中在Keggin型多酸[9],并获得了一系列高维、高连接多酸基化合物。和Keggin阴离子相比,对Wells-Dawson型多酸进行修饰的例子却相对较少[10-12]。因此,开展过渡金属配合物对Wells-Dawson型多酸的修饰成为多酸修饰化学一个吸引人且具有一定挑战性的方向。
作为多酸阴离子的修饰体,过渡金属配合物通常都是单核配合物,而多核金属簇对多酸的修饰实例相对较少[13]。并且在所报道的多酸基多核过渡金属配合物中,通常都集中在了多核银簇上,因为银离子的配位特性利于多核簇的形成[14]。但是,多核铜簇对多酸的修饰非常少见,只有刘术侠课题组[15]曾报道了一例基于Wells-Dawson多阴离子的七核铜簇化合物。要想成功制备该类多酸基多核铜簇化合物,合适的有机配体的选择是一个关键的合成因素。在本工作中,我们选择了吡啶-四氮唑类配体5-(4-吡啶基)-1H-四氮唑(4-ptz)和5-(3-吡啶基)-1H-四氮唑(3-ptz)作为有机组分,构筑多核铜簇(图1),从而达到对多酸的修饰作用。配体4-ptz和3-ptz中,四氮唑基团的4个给体N原子是连续的,利于铜原子的聚集;而吡啶基团则利于结构维度的拓展。
本工作中,我们选择(Wells-Dawson/铜/吡啶四氮唑)体系,在水热条件下成功获得了3个基于Wells-Dawson多酸的三核铜簇化合物[Cu3(4-ptz)4(H2O)7(As2W18O62)]·42H2O(1)、[Cu3(4-ptz)5(H2O)5(As2W18O62)]· 47H2O(2)和[Cu3(3-ptz)4(H2O)8(P2W18O62)]·33H2O(3)。其中,化合物1和2在同一反应釜中获得。我们表征了晶体结构,并研究了3个化合物的电化学以及光催化性能。
1 实验部分
1.1试剂与仪器
4-ptz和3-ptz按文献合成[16]。CuCl2·2H2O、H6[As2W18O62]和H6[P2W18O62]为国产分析纯试剂。红外光谱(IR)采用美国Nicolet公司Alpha-Centauri 560型FT-IR光谱仪(溴化钾压片),扫描范围400~4 000 cm-1。电化学测试采用CHI660电化学工作站,所用体系为常规三电极体系:工作电极为空白碳糊电极(CPE)和杂化材料本体修饰的碳糊电极,饱和甘汞电极(SCE)为参比电极,铂丝做对电极。紫外-可见光谱使用SP-1900 UV-Vis(日本)紫外可见分光光度计测定。晶体结构用德国布鲁克公司CCD面探X射线衍射仪测定。热重数据利用PYRIS DIAMOND TG/DTA热分析仪测定。X射线粉末衍射在Rigaku UltimaⅣ仪器上测定,Cu Kα射线(λ=0.154 056 nm),管电压和电流分别为40 kV和40 mA,测量角度范围为3.5°~40°;扫描速度为10°· min-1;步长为0.02°。
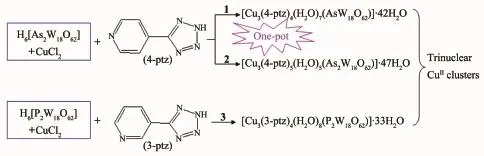
图1 3个化合物的合成路线示意图Fig.1Synthetic scheme for compounds 1~3
1.2化合物1~3的合成
化合物1和2的合成:将H6[As2W18O62](0.45 g,0.1 mmol)、CuCl2·2H2O(0.34 g,2.0 mmol)、4-ptz(0.06 g,0.4 mmol)和10 mL H2O混合,在搅拌条件下以1.0 mol·L-1HCl调节体系pH值至4.5。室温下剧烈搅拌1 h,然后将反应混合物置于20 mL内衬聚四氟乙烯的不锈钢反应釜中,放入160℃烘箱内,在自生压力条件下反应3 d后逐渐冷却到室温。经过滤、去离子水洗涤后于室温下晾干,得到蓝色块状晶体1和绿色块状晶体2,产率(以W元素计):30%(1)和35%(2)。C24H114N20O111Cu3As2W18(1)的元素分析计算值(实验值),%:C 4.71 (4.64),H 1.88(1.98),N 4.58(4.52)。C30H124N25O114Cu3As2W18(2)的元素分析计算值(实验值),%:C 5.71(5.75),H 1.98 (2.02),N 5.55(5.51)。
化合物3的合成与1、2相似,只是用H6[P2W18O62] (0.44 g,0.1 mmol)和3-ptz(0.05 g,0.3 mmol)分别替换H6[As2W18O62]和4-ptz,得到蓝色块状晶体3。产率(以W元素计):30%。C24H98N20O103Cu3P2W18(3)的元素分析计算值(实验值),%:C 4.91(4.95),H 1.68(1.63),N 4.77 (4.72)。
1.3晶体结构的测定
选取大小为0.16 mm×0.14 mm×0.12 mm(1)、0.24 mm×0.20 mm×0.18 mm(2)和0.26 mm×0.24 mm×0.20 mm(3)的单晶样品,置于Buker SMART-1000 CCD面探X射线单晶衍射仪进行数据收集,用Mo Kα射线(λ=0.071 073 nm),以ω扫描方式在293 K下收集衍射数据。所有数据经Lp因子校正,用直接法得到全部非氢原子坐标(SHELXS-97[17a]),有机基团上的氢原子坐标采用几何加氢的方法得到,用全矩阵最小二乘法精修结构(SHELXS-97[17b])。单晶解析揭示了化合物1~3中的结晶水高度无序,在此采用PLATON中的SQUEEZE程序将水分子除去[18]。所报道的结构为去除客体水分子的结构,并采用SQUEEZE程序中*.hkp文件精修。化合物1~3中结晶水分子数目通过热重及元素分析结果综合确定。这种方法是一种处理无序水的可靠方法,多见于文献[19]。晶体学数据见表1。
CCDC:1416806,1;1406807,2;1406808,3。
1.4化合物修饰碳糊电极(1-、2-、3-CPE)的制备
称取90 mg石墨粉和8 mg化合物1混合,在玛瑙研钵中研磨30 min,加入0.1 mL液体石蜡,用玻璃棒搅拌均匀。将所得混合物装入内径1.5 mm的玻璃管中,封装长度约0.8 cm,用铜棒从后面轻轻压实,并作为导电连线。所得碳糊电极的表面在称量纸上擦平。2-、3-CPE按类似方法制备。
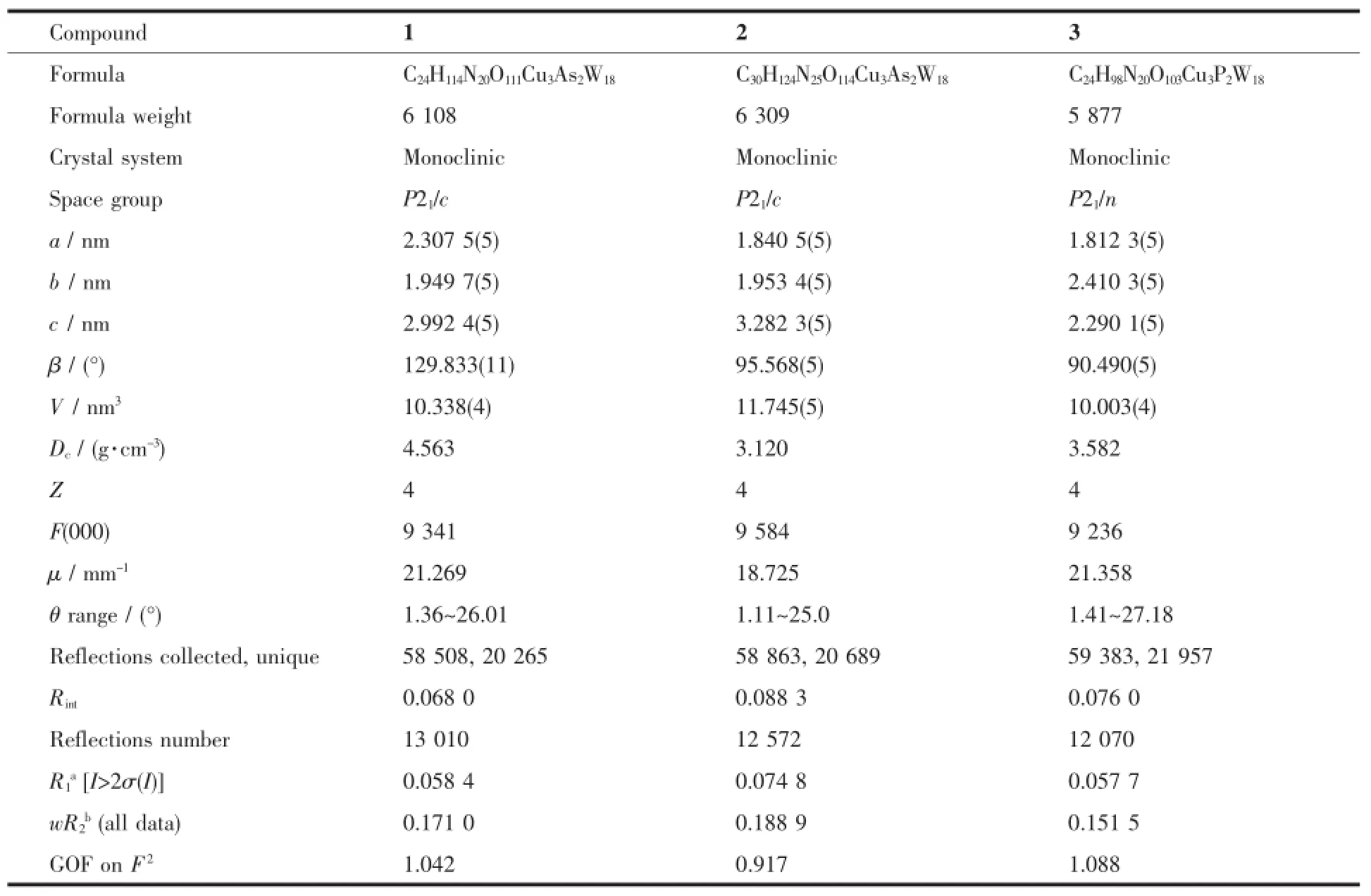
表1 化合物1~3的晶体学参数Table 1Crystal data and structure refinements for compounds 1~3
1.5光催化实验过程
将100 mg的化合物分散到250 mL 0.02 mol·L-1的有机染料(罗丹明B或亚甲基蓝)溶液中,在黑暗处机械搅拌10 min,得到悬浊液,并将该悬浊液置于汞灯下照射,并不停的进行搅拌。每隔相同时间段取一次样品,测试其吸收曲线。利用如下公式计算降解率(D):
D=(1-At/A0)×100%
A0:初始吸光度;At:t时刻吸光度。
2 结果与讨论
2.1晶体结构
2.1.1化合物1晶体结构
X射线晶体学研究表明化合物1的结构单元包含3个CuⅡ离子,4个4-ptz配体分子,7个配位水分子,1个[As2W18O62]6-(简写为As2W18)杂多阴离子和42个游离水分子,如图2a所示。As2W18杂多阴离子具有经典的Wells-Dawson结构[20]。As-O键长在0.162 7(13)~0.172 4(13)nm之间。W-O键长在较宽范围内变化:0.165 8(13)~0.238 9(12)nm。As-O键长和W-O键长与文献报道的As2W18化合物相一致。价键理论计算[21],所有的W都是+6氧化态,所有的Cu离子都是+2氧化态。有机配体4-ptz在化合物1和2中都为中性分子。
在化合物1中,存在3个晶体学独立的CuⅡ离子,都展示了六配位的扭曲八面体构型。Cu1与来自2个4-ptz配体的2个N原子(N3和N8)、3个水分子(O1W,O2W和O14W)和1个多酸端基氧原子O20配位;Cu2与来自4个4-ptz配体的4个N原子(N4,N9,N13和N8)和2个水分子(O3W,O14W)配位;而Cu3与 2个4-ptz配体的2个N原子(N14和N19)和4个水分子(O3W,O4W,O5W和O6W)进行配位。其中Cu-N键长在0.197 4(16)~0.202 6(17)nm范围内,而Cu-O键长在0.196 6(16)~0.256 6(15)nm范围。有机配体4-ptz展示了单一的配位模式,利用四氮唑顶端的2个N原子来固定CuⅡ离子,与水分子配合构筑了化合物1中的三核铜簇[Cu3(4-ptzH)4(H2O)7]6+,其中O3W和O14W作为水桥固定了三核铜簇(图2b)。As2W18多阴离子提供1个赤道位上的端基氧原子O20与该三核铜簇共价连接,形成了化合物1中多酸单支撑三核铜簇的悬臂式结构。

图2 (a)化合物1的单胞图;(b)化合物1中的三核铜簇Fig.2 (a)Unit of 1;(b)Tri-nuclear copper cluster of 1
2.1.2化合物2晶体结构
X射线晶体学研究表明化合物2的结构单元包含3个CuⅡ离子,5个4-ptz配体分子,5个配位水分子,1个As2W18和47个游离水分子,如图3a所示。价键计算[21]结果显示所有的W都是+6氧化态,所有的Cu离子都是+2氧化态。
在化合物2中,3个晶体学独立的CuⅡ离子同样展示了六配位的扭曲八面体构型。Cu1与来自2个4-ptz配体的2个N原子(N4和N8)、3个水分子(O1W,O4W和O5W)和1个多酸端基氧原子O33配位;Cu2与来自3个4-ptz配体的3个N原子(N13,N18和N233)、2个水分子(O2W和O3W)和多酸的1个端氧O12配位;而Cu3与4个4-ptz配体的4个N原子(N3,N9,N19和N24)和2个水分子(O3W和O4W)进行配位。Cu-N和Cu-O键长分别在0.198(2)~0.205 6(18)nm和0.194(2)~0.245 7(19)nm范围内。与1中4-ptz配位模式相同,化合物2中的部分配体利用四氮唑顶端的2个N原子与2个CuⅡ离子配位;而包含N13的配体4-ptz只提供1个四氮唑上的端N原子来连接1个CuⅡ离子(图3b)。CuⅡ离子与4-ptz的配位特点诱导了2中三核铜簇[Cu3(4-ptzH)5(H2O)5]6+的形成,其中O3W和O4W作为水桥。每个As2W18多阴离子提供2个赤道位上的端基氧原子O14与O33与两组三核铜簇共价连接,形成了化合物2中多酸与三核铜簇交替连接的一维链式结构(图3c)。

图3 (a)化合物2的单胞图;(b)化合物2中的三核铜簇;(c)2中多酸和三核铜簇交替连接形成的一维链结构Fig.3 (a)Unit of 2;(b)Tri-nuclear copper cluster of 2;(c)1D chain of 2 with anions and tri-nuclear clusters arranging alternately

图4 化合物3的2个孤立建筑单元:P2W18(a)与三核铜簇[Cu3Ⅱ(3-ptzH)4(H2O)8]6+(b)Fig.4Two discrete building blocks of 3:P2W18anion(a)and tri-nuclear cluster[Cu3Ⅱ(3-ptzH)4(H2O)8]6+(b)
2.1.3化合物3晶体结构
X射线晶体学研究表明化合物3的结构单元包含3个CuⅡ离子,4个3-ptz配体分子,8个配位水分子,1个[P2W18O62]6-(简写为P2W18)杂多阴离子和33个游离水分子。其中3-ptz为中性分子。化合物3是一个超分子结构,包含2个孤立建筑单元:P2W18和三核铜簇[Cu3(3-ptzH)4(H2O)8]6+(图4)。该三核铜簇里CuII离子的配位模式与1和2类似,同样是水分子作为桥来固定三核簇。多酸阴离子P2W18和孤立的三核铜簇之间存在丰富的氢键作用力而诱导了3中三维超分子结构的形成。
2.2红外光谱
化合物1和2的IR光谱分别在1 077、961、888、802 cm-1和1 090、962、912、790 cm-1处出现的特征峰可归结为化合物1和2中As2W18多阴离子ν(As-O),ν(W-Od)和ν(W-Ob/c-W)的吸收峰。在1 631~1 220 cm-1和1 636~1 162 cm-1范围内的谱带是1和2中4-ptz分子的特征振动吸收峰。化合物3的IR光谱在1 095,960,913和786 cm-1处出现的特征峰可归属为化合物3中P2W18多阴离子ν(P-O),ν(W-Od)和ν(W-Ob/c-W)的吸收峰。1 618~1 263 cm-1范围内的谱带是3中3-ptz分子的特征振动吸收峰。
2.3化合物1和2的X射线粉末衍射
化合物1和2同时在同一反应釜中获得,即使其颜色以及形状差别大而易于进行手工分离,我们也进行了化合物1和2的X射线粉末衍射来证实其纯度。图5展示了化合物1和2的X射线粉末衍射图。从图中可以看出,化合物1和2样品的X射线粉末衍射峰峰位与模拟衍射峰比较吻合,证实了用于测试的样品1和2具有较好相纯度。

图5 化合物1和2的模拟以及实验样品的粉末X射线衍射图Fig.5Simulativeand experimental powder X-ray diffraction patterns for complexes 1 and 2

图6 (a)3-CPE在0.1 mol·L-1H2SO4+0.5 mol·L-1Na2SO4水溶液中不同扫速下的循环伏安图;(b)3-CPE在加入不同浓度的的0.1 mol·L-1H2SO4+0.5 mol·L-1Na2SO4水溶液中的循环伏安图Fig.6 (a)Cyclic voltammograms of the 3-CPE in 0.1 mol·L-1H2SO4+0.5 mol·L-1Na2SO4aqueous solution at different scan rates; (b)Cyclic voltammograms of the 3-CPE in 0.1 mol·L-1H2SO4+0.5 mol·L-1Na2SO4aqueous solution containing NO2-
2.4电化学性能
化合物1~3的电化学性质相似(图S2,S3),我们以化合物3为例来研究其电化学性质。我们研究了化合物3修饰碳糊电极(3-CPE)在0.1 mol·L-1H2SO4+0.5 mol·L-1Na2SO4溶液中的电化学行为。由图6a中可以看到,在+600~-1 010 mV电位范围内,出现了1个不可逆的阳极峰Ⅰ和4对可逆的氧化还原峰Ⅱ-Ⅱ′、Ⅲ-Ⅲ′、Ⅳ-Ⅳ′和Ⅴ-Ⅴ′:阳极峰Ⅰ归属于铜中心的氧化,而可逆的氧化还原峰Ⅱ-Ⅱ′和Ⅲ-Ⅲ′归属于P2W18多阴离子W的2个连续的一电子氧化还原过程,Ⅳ-Ⅳ′和Ⅴ-Ⅴ′归属于W的2个连续的两电子氧化还原过程[22]。当扫速为120 mV·s-1时,这4对氧化还原峰的半波电位根据E1/2=(Epa+Epc)/2求出,分别是-38(Ⅱ-Ⅱ′)、-217(Ⅲ-Ⅲ′)、-506(Ⅳ-Ⅳ′)和-771(Ⅴ-Ⅴ′)mV。从图6a中我们可以观察到:随着扫速的提高(20~300 mV·s-1),阴极的峰电位向负方向移动,相应的阳极峰电位向正方向移动,并且阴极和阳极峰峰位差有所增加。
如图6b所示,3-CPE对亚硝酸根的还原具有良好的电催化活性。随着亚硝酸根的加入,4个还原峰电流都急剧增加,而相应的氧化峰电流都降低。因此我们可推知,P2W18多阴离子的1、2、4、6-电子还原物种都对亚硝酸根的还原有良好的电催化活性。
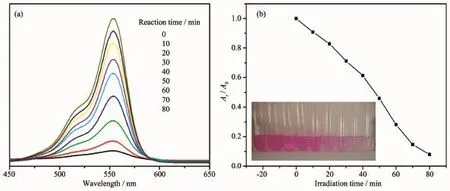
图7 (a)在紫外灯照射下,化合物3对RhB溶液光催化降解过程的吸收光谱;(b)RhB溶液的光催化降解率Fig.7(a)Absorption spectra of the RhB solution during the decomposition reaction under UV irradiation with the presence of compound 3;(b)Photocatalytic decomposition rates of RhB solutions under UV irradiation with the use of the title compound 3
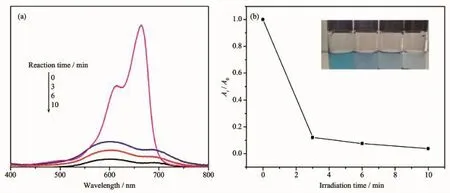
图8 (a)在紫外灯照射下,化合物3对MB溶液光催化降解过程的吸收光谱;(b)MB溶液的光催化降解率Fig.8(a)Absorption spectra of the MB solution during the decomposition reaction under UV irradiation with the presence of compound 3;(b)Photocatalytic decomposition rates of MB solutions under UV irradiation with the use of the title compound 3
2.5光催化性能
罗丹明B(RhB)和亚甲基蓝(MB)是两种经典的有机染料,我们研究了化合物1~3对RhB和MB的光催化降解性能,但只有化合物3的光催化效果明显,而1和2则几乎没有光催化效果。如图7所示,化合物3对RhB的催化降解率能达到92%左右,表明化合物3可作为一种出色的降解RhB的催化剂。同样将化合物3分散到MB溶液中,降解实验的吸收曲线如图8所示。从图中我们可以看出,化合物3对MB的催化降解速率很快,10 min时催化降解率已达到96%。多酸化合物对亚甲基蓝染料的降解能达到这样快速且高效的催化降解率并不多见,因此化合物3同样是降解MB的优良催化剂。
3 结论
在水热条件下,我们利用Wells-Dawson型多酸、氯化铜和2种吡啶-四氮唑类配体3-ptz和4-ptz,成功合成了3个多酸基化合物1~3。对As2W18/CuⅡ/4-ptz体系,同一反应釜中我们获得了2种类型的晶体:化合物1和2。对P2W18/CuⅡ/3-ptz体系,我们得到了化合物3。3个目标化合物都包含线型的三核铜簇,进一步证实了3-ptz和4-ptz配体选择的合理性。3个化合物为制备多核簇修饰的多酸基化合物提供了实验范例。
Supporting information is available at http://www.wjhxxb.cn
[1]Rubinstein A,Jiménez-Lozanao P,Carbó J J,et al.J.Am. Chem.Soc.,2014,136(31):10941-10948
[2]Shi D Y,He C,Qi B,et al.Chem.Sci.,2015,6(2):1035-1042
[3]Douvas A M,Makarona E,Glezos N.ACS Nano,2008,2(4): 733-742
[4]Schulz-Dobrick M,Jansen M.Inorg.Chem.,2007,46(11): 4380-4382
[5]Zhang H,Yu K,Wang C M,et al.Inorg.Chem.,2014,53(23): 12337-12347
[6]Zheng S T,Zhang J,Clemente-Juan J M,et al.Angew.Chem. Int.Ed.,2009,48(39):7176-7179
[7]Wang X L,Liu X J,Tian A X,et al.Dalton Trans.,2012,41(32):9587-9589
[8]Lü J,Lin J X,Zhao X L,et al.Chem.Comm.,2012,48(5): 669-671
[9]Pang H J,Ma H Y,Peng J,et al.CrystEngComm,2011,13 (23):7079-7085
[10]Wang X,Peng J,Liu M G,et al.CrystEngComm,2012,14 (9):3220-3226
[11]Sha J Q,Peng J,Lan Y Q,et al.Inorg.Chem.,2008,47(12): 5145-5153
[12]Tian A X,Ying J,Peng J,et al.Inorg.Chem.,2008,47(8): 3274-3283
[13]Wang X L,Wang Y F,Liu G C,et al.Dalton Trans.,2011, 40(36):9299-9305
[14]Wang X L,Li N,Tian A X,et al.Dalton Trans.,2013,42 (41):14856-14865
[15]Zhang C D,Liu S X,Sun C Y,et al.Cryst.Growth Des., 2009,9(8):3655-3660
[16]Demko Z P,Sharpless K B.J.Org.Chem.,2001,66(24): 7945-7950
[17](a)Sheldrick G M.Acta Crystallogr.Sect.A,2008,64(1):112-122
(b)Sheldrick G M.SHELXS-97,University of Göttingen,
Germany,1997.
[18]Spek A L.Acta Crystallogr.Sect.C:Struct.Chem.,2015,71: 9-18
[19]Tian A X,Ning Y L,Ying J,et al.CrystEngComm,2015,17 (29):5569-5578
[20]Yang Y,Liu S X,Li C C,et al.Inorg.Chem.Comm.,2012, 17:54-57
[21]Brown I D,Altermatt D.Acta Crystallogr.Sect.B:Struct. Sci.,1985,41(4):244-247
[22]Sadakane M,Steckhan E.Chem.Rev.,1998,98(1):219-237
Syntheses,Structures and Properties of Three Tri-nuclear Copper Clusters Based on Wells-Dawson Polyoxometalate
YING Jun*NING Ya-LiHOU XueTIAN Ai-Xiang
(Department of Chemistry,Bohai University,Jinzhou,Liaoning 121013,China)
Through using Wells-Dawson type anion[As2W18O62]6-,CuCl2·2H2O and 5-(4-pyridyl)-1H-tetrazole(4-ptz),two different POM-based compounds containing tri-nuclear copper clusters were synthesized in one-pot under hydrothermal conditions,namely[Cu3(4-ptz)4(H2O)7(As2W18O62)]·42H2O(1)and[Cu3(4-ptz)5(H2O)5(As2W18O62)] ·47H2O(2).When we used another Wells-Dawson anion[P2W18O62]6-,CuCl2·2H2O and 5-(3-pyridyl)-1H-tetrazole (3-ptz),another POM-based tri-nuclear copper cluster was also obtained,namely[Cu3(3-ptz)4(H2O)8(P2W18O62)]· 33H2O(3).Single crystal X-ray diffraction shows that compound 1 is a tri-nuclear copper cluster supporting pendent structure,and compound 2 is a one dimensional chain with anions and tri-nuclear copper clusters arranging alternately,while compound 3 is a discrete structure containing anions and tri-nuclear copper clusters.3-ptz and 4-ptz are important structural factors for constructing tri-nuclear copper clusters in compounds 1~3.The electrochemical and photocatalytic activities of the title compounds have been studied.CCDC:1416806,1; 1406807,2;1406808,3.
Wells-Dawson polyoxometalate;multi-nuclear copper cluster;hydrothermal synthesis;electrochemistry;photocatalysis
O614.121
A
1001-4861(2016)02-0267-08
10.11862/CJIC.2016.036
2015-09-15。收修改稿日期:2015-11-28。
国家自然科学基金(No.21571023)和辽宁省高等学校青年学者成长计划(No.LJQ2012097)资助项目。
*通信联系人。E-mail:ying@bhu.edu.cn
