由联苯-2,4,4′,6-四甲酸构筑的三维镉配位聚合物的合成、结构及与DNA作用
2016-11-28余玉叶沈伟吴小勇赵国良
余玉叶 沈伟 吴小勇 赵国良*,,2
(1浙江师范大学化学与生命科学学院,金华321004) (2浙江师范大学行知学院,金华321004) (3浙江金华职业技术学院,金华321017)
由联苯-2,4,4′,6-四甲酸构筑的三维镉配位聚合物的合成、结构及与DNA作用
余玉叶1,3沈伟1吴小勇1赵国良*,1,2
(1浙江师范大学化学与生命科学学院,金华321004) (2浙江师范大学行知学院,金华321004) (3浙江金华职业技术学院,金华321017)
在水热条件下,以联苯-2,4,4′,6-四甲酸(C16H10O12,H4bptc)为主配体、1,3-二(4-吡啶基)-丙烷(bpp)为辅助配体,与氯化镉(CdCl2·2.5H2O)反应合成了2个三维镉配位聚合物{[Cd2(bptc)(H2O)3]·H2O}n(1),{[Cd2(bptc)(bpp)·H2O]·2.25H2O}n(2)。用元素分析、红外光谱对配合物的组成及结构进行了表征,并通过X射线单晶衍射的方法测定了配合物的晶体结构。配合物1具有双核结构,2个中心离子Cd同为六配位,均形成略有畸变的八面体结构;而配合物2尽管也具有双核结构,但不同于1的是其中一个中心离子构成略显畸变的八面体几何结构,另一个却构成五角双锥结构。用溴化乙锭荧光光谱法测定了配体和配合物与DNA作用情况,结果表明配合物与DNA的作用强于配体。
联苯-2,4,4′,6-四甲酸;1,3-双(4-吡啶基)-丙烷;镉配位聚合物;DNA作用
0 引言
配位聚合物所涉及的学科领域广泛,对它进行系统深入的研究,不但对发展结构化学、合成化学和材料化学的基本概念及基础理论具有重要的学术意义;而且对于此类材料的开发应用也具有非常重要的现实意义。研究发现,由于此类化合物花样繁多,结构新颖,性能优异,在磁性[1-3],荧光[4-5],非线性光学[6-7],吸附[8-10]、催化[11-12]、分离[13]和生物制药[14-15]等诸多领域有着诱人的潜在应用,而倍受广大化学家和材料学家的极大关注和重视。然而,想要获得结构新颖、功能优异的配位聚合物,其关键之处在于中心金属离子和桥联配体的调控,即把中心金属离子作为节点,有机配体作为联结体,利用中心金属离子多变的几何结构和有机配体的对称性来构筑多样结构。通过这些特点的把握,人们可以根据自己的设计思路来合成具有各种各样的结构和功能的配位聚合物。
有机羧酸化合物因其配位模式的多样性及其与金属离子的强配位性,而成为配位化合物研究的首选配体。羧基不仅能以多种灵活的配位方式与金属离子配位,而且还可以与金属离子组合形成多核金属离子配合物或者次级结构单元(Secondary Building Units,SBUs),从而构筑结构更加新颖、性质更加独特的配位拓扑结构;除此之外,由于羧基可以全部或者部分去质子化,它可以作为氢键的供体或者受体,协同配位键和金属键等参与超分子的自组装。因此,用有机羧酸类作为配体构筑配位聚合物吸引了人们极大的研究兴趣。
近几十年来,各种羧酸及其相应配合物的合成和性质研究层出不穷,其中尤以多元芳香羧酸、联苯多元羧酸以及杂环多元羧酸最受青睐,因为它们易于金属离子形成双核或多核、具有三维网状结构配位聚合物[16-19]。本文以联苯-2,4,4′,6-四甲酸(H4bptc)为配体,合成了2种镉配位聚合物,用元素分析、红外光谱对配合物进行了表征,通过X射线单晶衍射方法测定了配合物的晶体结构。
1 实验部分
1.1试剂与仪器
H4bptc、1,3-二(4-吡啶基)-丙烷(bpp)、无水乙醇、氢氧化钠、氯化镉、丙酮、N,N-二甲基甲酰胺等试剂均为市售分析纯试剂,小牛胸腺DNA为生化试剂。
德国Bruker公司Smart APEXⅡ型X-射线单晶衍射仪;瑞士Bruker公司Avance 600 MHz核磁共振仪;德国Elementar公司Vario ELⅢ型元素分析;美国Nicolet公司NEXUS 670型傅立叶变换红外光谱仪(FTIR),KBr压片,测定范围为400~4 000 cm-1;美国Perkin Elmer公司的LS-55型荧光光谱仪。
1.2配合物的合成
1.2.1{[Cd2(bptc)(H2O)3]·H2O}n(1)的合成
将0.046 g CdCl2·2.5H2O(0.2 mmol),0.033 g H4bptc(0.1 mmol),0.016 g NaOH(0.4 mmol)和12 mL蒸馏水置于25 mL的聚四氟乙烯内衬的不锈钢反应釜中,在433 K下恒温晶化3 d后冷却至室温。过滤,得适合单晶测试的无色块状晶体,产率约为40%(以CdCl2·2.5H2O计)。元素分析按C16H14O12Cd2的计算值(%):C,30.84.11;H,2.26。实验值(%):C,30.98;H,2.17。IR(cm-1):3 374(w),1 601(m),1 532 (m),1 454(m),1 428(m),1 398(m),1 365(s),1 285(m),1 203(m),1 108(m),783(m),738(s),703(m)。
1.2.2{[Cd2(bptc)(bpp)·H2O]·2.25H2O}n(2)的合成
2的合成与1类似,只是同时加入了0.04 g bpp (0.2 mmol)辅助配体。无色块状晶体。产率约为37% (以CdCl2·2.5H2O计)。元素分析按C29H26.5N2O11.25Cd2的计算值(%):C,43.11;H,3.31;N,3.47。实验值(%):C,43.30;H,3.23;N,3.53。IR(cm-1):3 385(w),1 601 (m),1 587(m),1 534(s),1 459(m),1 426(s),1 382(m),1 364(s),1 209(m),1 104(m),782(m),758(s),734(s),701(m)。
1.3配合物与DNA作用的荧光光谱
将小牛胸腺DNA(ct-DNA)用0.1 mol·L-1的NaCl溶液配成200 μg·mL-1(cDNA=3.72×10-4mol·L-1),经纯度测定A260/A280=1.8~2.0,符合实验测试要求,置于4℃温度下保存,在4 d之内使用;Tris-HCl缓冲溶液(5 mmol·L-1Tris-HCl/50 mmol·L-1NaCl)按常规方法配制,其中Tris-HCl的浓度为0.0l mol·L-1,pH=7.40。
在10 mL比色管中加入1.0 mL 200 μg·mL-1的DNA溶液、1.0 mL 200 μg·mL-1EB溶液以及2.0 mL pH=7.40的Tris-HCl缓冲溶液,在室温下放置2 h。然后向混合溶液中依次加入不同量的浓度为5×10-4mol·L-1的化合物溶液,用Tris-HCl缓冲溶液定容,在4℃下反应4 h后,在美国Perkin Elmer公司的LS-55型荧光光谱仪上,激发波长λex为251 nm,扫描混合溶液在λem为520~700 nm范围的荧光光谱。
1.4晶体结构分析方法
选用晶体大小适宜的配合物单晶,在德国Bruker SMART APEXⅡCCD单晶衍射仪上上进行衍射实验。用辐射Mo Kα射线(λ=0.071 073 nm),在设定的2θ范围内收集衍射数据,衍射数据用程序SADABS[20]进行经验吸收校正,晶体结构用SHELXS-97[21]程序由直接法解出,对所有非氢原子坐标及其各向异性温度因子用SHELXL-97程序[22]进行全矩阵最小二乘法修正至收敛。除水上的氢原子外,其余氢原子均为理论加氢,水上的氢原子通过差值Fourier合成得到。主要晶体学数据列于表1,主要的键长和键角列于表2、表3。
CCDC:952960,1;952962,2。

表1 配合物的晶体学数据Table 1Crystallographic data for complexes

表2 配合物1的主要键长和键角Table 2Selected bond lengths(nm)and angles(°)of the complex 1

续表1

表3 配合物2的主要键长和键角Table 3Selected bond lengths(nm)and angles(°)of the complex 2
2 结果与讨论
2.1红外光谱分析
由2种配合物及配体H4bptc的FT-IR红外光谱可知,配合物在3 374 cm-1(1)和3 385 cm-1(2)处出现宽的吸收带,可归属于水分子的O-H伸缩振动。游离配体的羧基特征吸收峰出现在1 698 cm-1处,当形成配合物后,此处峰消失,出现了羧基的不对称伸缩振动和对称伸缩振动吸收峰。羧基的不对称伸缩振动νas(COO-)出现在1 601 cm-1处。1的对称伸缩振动分别出现在1 428、1 398和1 365 cm-1;2的对称伸缩振动则出现在1 426、1 382和1 364 cm-1。这不但说明羧基参与了配位,而且存在单齿、螯合、桥联多种配位方式[23]。而配合物2在1 587和758 cm-1处的吸收峰可归属为参与配位的bpp辅助配体中吡啶杂环[24-25]。这些均与单晶结构分析结果相吻合。
2.2晶体结构分析
2.2.1{[Cd2(bptc)(H2O)3]·H2O}n(1)的晶体结构
单晶X射线分析表明配合物1属于单斜晶系,空间群为P2/c,该配合物的不对称单元包含2个Cd离子,1个去质子化的配体bptc4-和4个水分子,其中3个为配位水分子,1个为游离水分子,如图1所示。配合物具有双核结构,Cd中心离子同为六配位,其中Cd(1)与配体bptc4-羧基上的4个氧原子和2个来自于配位水上的氧原子配位,形成一个略有畸变的八面体结构。Cd(2)与配体上的羧基5个氧原子和1个配位水上的氧原子配位,同样形成了略有畸变的八面体结构。4个氧原子O(1),O(2),O(3)#5,O(4W)在赤道平面上,O(2)-Cd(2)-O(3)#5,O(4W)-Cd(2)-O(3)#5,O(2)-Cd(2)-O(1),O(4W)-Cd(2)-O(1)键角之和为337.66°。O3,O2W占据轴向位置,O(4)#4-Cd(2)-O(5)#5键角为171.47(7)°。配合物中Cd-O的键长范围在0.221 8(2)~0.247 1(2)nm之间,与文献中报道的六配位的Cd羧酸配合物相类似[25-27]。值得注意的是配体bptc4-以单齿和螯合的形式参与配位,配合物的次级结构单元(SBU)是由相互对称的2个Cd离子和2个双齿桥式羧基构筑的一个八元环[Cd2(COO)2]2+。相邻的连续SBUs在ab面上构成了二维网状面(如图2)。配体的羧基氧原子又将这些二维平面串联成三维网络结构。
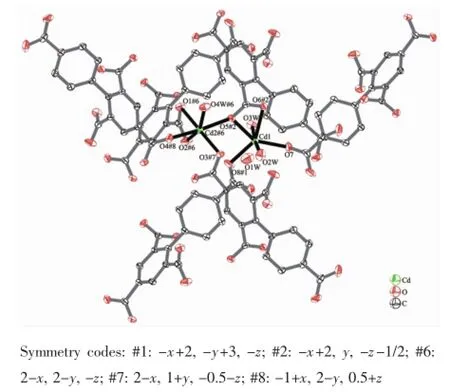
图1 配合物1的分子结构(椭球率50%)Fig.1Molecular structure of complex 1 with 50% probability ellipsoids
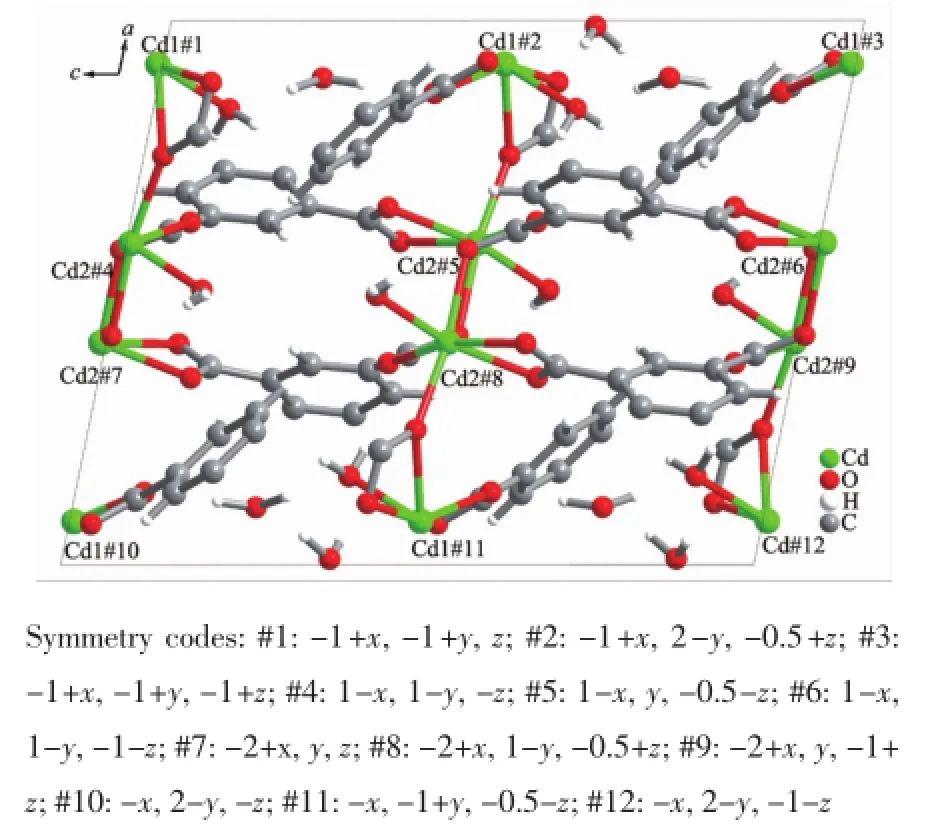
图2 配合物1的二维超分子结构Fig.22D supramolecular structure of complex 1
对配合物进行了拓扑分析,以双核Cd(1)组成的SBU周围连接有4个配体bptc4-,故该SBU可视为拓扑结构网络中的1个四连接点;而以双核Cd(2)组成的SBU周围连接有六个配体bptc4-,可看作六连接点;同一个配体bptc4-周围又连着5个相同的[Cd2(COO)2]2+,同样的可看作五连接点,因此该配合物具有(4,5,6)-连接拓扑结构(图3)。
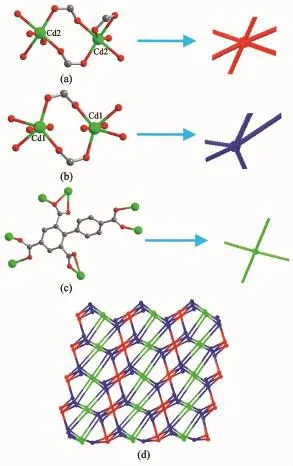
图3 (a)以双核Cd(2)为节点连接6个配体结构,(b)以配体为节点连有5个双核Cd单元,(c)以双核Cd(1)为节点连接4个配体结构,(d)配合物的(4,5,6)-连接拓扑Fig.3 (a)Linkage of{Cd(2)2}subunits 6-connected with six bptc4-ligands;(b)bptc4-ligand regarded as an organic 5-connected node linked with five{Cd2} subunits;(c)Linkage of{Cd(1)2}subunits 4-connected with four bptc4-ligands;(d)3D(4,5,6)-connected topological
2.2.2{[Cd2(bptc)(bpp)·H2O]·2.25H2O}n(2)的晶体结构
单晶结构分析表明,配合物2属于正交晶系,空间群为Pbcn;该配合物具有双核结构,其结构单元如图4所示,不对称单元中包含2个Cd离子,1个主配体bptc4-离子,1个辅助配体bpp分子,1个配位水和2.25个游离水分子。2个Cd离子的配位环境并不相同,Cd(1)分别与来自3个主配体bptc4-离子上的4个氧原子,1个辅助配体bpp分子上的氮原子,1个水分子上的氧原子配位,构成了一个略显畸变的八面体几何结构。其中N1,O1W原子位于竖轴方向,而O1,O5#1,O7#2,O1W原子占据赤道平面,Cd(1)与赤道平面的距离为0.018 14 nm,可以确定Cd(1)与O1,O5#1,O7#2,O1W共平面。Cd-O键长范围为0.219 4(6)~0.256 8(9)nm,Cd-N键长为0.226 9(11)nm,均与文献[28-29]报道的相接近。Cd(2)分别与来自4个配体bptc4-的6个氧原子和bpp分子上的1个氮原子配位,构成略有畸变的五角双锥构型(图5b),其中N(2)#3,O(8)#2位于轴向位置,而O(1),O(2),O(3)#4,O(4)#4,O(6)#1位于赤道平面,这5个原子与Cd(2)之间的夹角之和为359.2°,说明这些原子几乎在同一个平面上,Cd(2)与该平面之间的距离为0.015 70 nm。在配合物中,配体以螯合、螯合加桥的2种配位模式与Cd离子进行配位。

图4 配合物2的分子结构(椭球率30%)Fig.4Molecular structure of complex 2 with 30% probability ellipsoids

图5 (a)配合物2中Cd1的配位环境;(b)配合物2中Cd2的配位环境Fig.5(a)Cd1 coordination environment for complex 2; (b)Cd2 coordination environment for complex 2
为使结构更加清晰,我们对其结构进行拓扑分析,如图6所示。如果把双核金属簇[Cd2(COO-)2]2+看成一个次级结构单元(SBU)。同一个SBU又通过4个主配体bptc4-和2个辅助配体bpp连接相同的6个SBUs,可看作六接点,bptc4-配体和bpp为连接点的边。同一个配体连接4个SBUs,可看作四接点。拓扑软件OLEX分析表明该配合物具有(4,6)-接点拓扑结构。
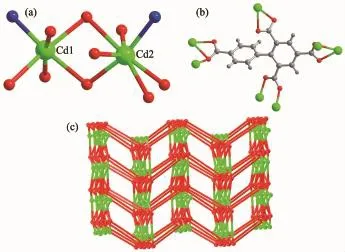
图6 (a)配合物的6连接点;(b)配合物的4接连点; (c)配合物的(4,6)-连接点拓扑结构Fig.6 (a)6-connected of complex;(b)4-connected of complex;(c)(4,6)-connected topological structure of complex
2.3与DNA作用的荧光光谱
图7为不同浓度的2种配合物和配体H4bptc对EB-DNA复合体系的荧光猝灭图,从图可看出,EB-DNA复合体系在592 nm处发出强烈的荧光,随着不同浓度的化合物的加入,EB-DNA复合体系的荧光发生了不同程度的猝灭,由此可以推测化合物均与DNA发生了不同程度的插入作用。为了较为定量地研究配合物与DNA的结合能力。根据Stem-Volmer公式求得配合物对EB-DNA体系的荧光淬灭常数[30]:I0/I=1+Ksqr,其中I0和I分别为EB-DNA复合体系和不同浓度的化合物加入EB-DNA复合体系后的荧光强度,r为化合物与DNA浓度之比,Ksq为线性Stem-Volmer淬灭常数(linear Stern-Volmer quench constant)。以I0/I对r作图(插图),直线的斜率即为Ksq。计算得出配体及2种配合物与DNA作用的结合常数Ksq分别对应为1.005,1.694,3.10,其大小定量地反应出配合物与DNA插入作用的能力;因此配合物的插入作用明显强于配体。加入辅助配体之后的配合物2,其作用力又强于不加辅助配体的配合物1,其原因是辅助配体的引入,增大了配合物的刚性平面,使得配合物2更有利于与DNA的结合。
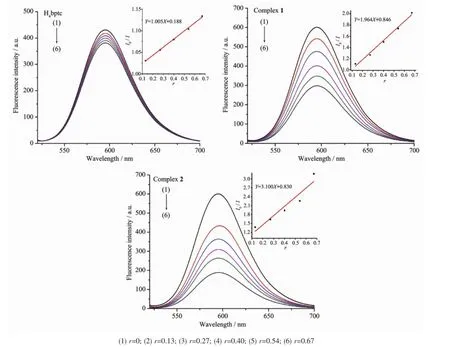
图7 配合物与配体对EB-DNA复合体系的荧光猝灭图Fig.7 Emission spectra of EB-DNA system in the absence and presence of complexes or ligand
3 结论
以联苯-2,4,4′,6-四甲酸为配体,合成了2种镉配位聚合物。用元素分析、红外光谱对配合物进行了表征,通过X射线单晶衍射的方法测定了配合物的晶体结构。配合物1具有(4,5,6)-连接拓扑结构。配合物2具有(4,6)-连接拓扑结构。根据配合物与DNA作用的结合常数大小比较,2种配合物与DNA都具有较强的插入作用,而且由于配合物2中有芳香平面辅助配体,其作用又强于配合物1。
[1]Chen P K,Che Y X,Zheng J M,et al.CrystEngComm,2010, 12:720-724
[2]Chang X H,Qin J H,Ma L F,et al.Cryst.Growth Des., 2012,12(6):4649-4657
[3]Mereacre V,Baniodeh A,Powell A K,et al.J.Am.Chem. Soc.,2011,133(6):15335-15337
[4]Guo H D,Guo X M,Zhang H J,et al.Cryst.Growth Des., 2009,9(3):1394-1401
[5]Zhao J,Wang X L,Shi X,et al.Inorg.Chem.,2011,50(11): 3198-3205
[6]Yu W H,Wang X Z,Ren X M,et al.Inorg.Chem.Commun., 2008,11:799-801
[7]Shan X C,Zhou Y F,Zhang H B,et al.Inorg.Chem.Commun., 2012,22:149-153
[8]Chen B L,Ockwig N W,Yaghi O M,et al.Angew.Chem. Int.Ed.,2005,44:4745-4749
[9]Choi H S,Suh M P.Angew.Chem.Int.Ed.,2009,48:6865-6869
[10]Lan A J,Li K H,Li J,et al.Inorg.Chem.,2009,48:7165-7173
[11]Kang J,Kim C,Kim Y,et al.Polyhedron,2012,42:282-290 [12]Li Q Y,Chen D Y,Yang G W,et al.J.Solid State Chem., 2012,190:196-201
[13]Semerci F,Soylu M S,Keskin S,et al.Polyhedron,2013,50:314-320
[14]Ma Z B,Moulton B.Coord.Chem.Rev.,2011,255:1623-1641
[15]Efthimiadou E K,Karaliota A,Psomas G.J.Inorg.Biochem., 2010,104:455-466
[16]Li B,Zang S Q,Ji C,et al.Cryst.Growth Des.,2012,12(3): 1443-1451
[17]Wang X L,Qin C,Wang E B,et al.Eur.J.Inorg.Chem., 2005(17):3418-3421
[18]Lin X,Jia J H,Zhao X B,et al.Angew.Chem.Int.Ed, 2006,45(44):7358-7364
[19]Liu T F,Lu J,Guo Z G,et al.Cryst.Growth Des.,2012,10 (4):1489-1491
[20]Scheldrick G M.SADABS,University of Göttingen,Göttingen, Germany,1996.
[21]Sheldrick G M.SHELXS 97,Program for the Solution of CrystalStructure,UniversityofGöttingen,Göttingen, Germany,1997.
[22]Sheldrick G M.SHELXS 97,Program for the Refinement of CrystalStructure,UniversityofGöttingen,Göttingen, Germany,1997.
[23]ZHU Zhi-Li(祝智力),FENG Yun-Long(冯云龙),LIN Hong (林鸿).J.Chin.Soc.Rare Earths(中国稀土学报),2005,23 (50):641-644
[24]Kazuo Nakamoto,Translated by HUANG De-Ru(黄德如), WANG Ren-Qing(汪仁庆).Infrared and Raman Spestra of Inorganic and Coordination Compounds(无机和配位化合物的红外和拉曼光谱).Bejing:Chemistry Industry Press, 1986.
[25]YU Yu-Ye(余玉叶),SHI Pei(石沛),SHENG Xiu-Dong(盛秀冬),et al.Chinese J.Inorg.Chem.(无机化学学报),2014,30 (10):2332-2340
[26]TAO Wu(陶武),LIU Jie-Min(刘杰民),SUN Chang-Yan(孙长艳),et al.Chinese J.Inorg.Chem.(无机化学学报),2011, 27(12):2419-2424
[27]Guo H D,Guo X M,Zhang H J,et al.Cryst.Growth Des., 2009,9(3):1394-1401
[28]Hao X R,Su Z M,Wang Y.et al.Acta Cryst.,2005,E61: m469-m471
[29]Liu G X,Zhu K,Ren X M,et al.Z.Anorg.Allg.Chem., 2009,635:156-164
[30]Lakowicz J R,Webber G.Biochemistry,1973,12(21):4161-4170
Syntheses,Structures and DNA-Binding of Cadmium Coordination Polymers with 3D Frameworks Constructed by Biphenyl-2,4,4′,6-tetracarboxylic Acid
YU Yu-Ye1,3SHEN Wei1WU Xiao-Yong1ZHAO Guo-Liang*,1,2
(1College of Chemistry and Life Science,Zhejiang Normal University,Jinhua,Zhejiang 321004,China) (2Xingzhi College,Zhejiang Normal University,Jinhua,Zhejiang 321004,China) (3Jinhua Polytechnic,Jinhua,Zhejiang 321017,China)
Two new cadmium coordination polymers,{[Cd2(bptc)(H2O)3]·H2O}n(1)and{[Cd2(bptc)(bpp)·H2O]· 2.25H2O}n(2),were synthesized under hydrothermal reactions by using biphenyl-2,4,4′,6-tetracarboxylic acid (H4bptc),CdCl2·2.5H2O and 1,3-di(4-pyridyl)propane(bpp).Both of them were characterized by elemental analysis, IR spectra,single crystal X-ray diffraction.Complex 1 is a binuclear structure with two six-coordinated Cd, both of which are distorted octahedral structures.The binuclear of Complex 2 is different.One Cdis distorted octahedral,and the other is seven-coordinated to form a pentagonal bipyramid.The interaction between two complexes,ligand and DNA was studied by EtBr fluorescence probe.Photoluminescence studies revealed that the interaction of complex 2 to the DNA is stronger than complex 1.CCDC:952960,1;952962,2.
biphenyl-2,4,4′,6-tetracarboxylic acid;cadmium coordination polymer;1,3-di(4-pyridyl)propane;DNA-binding
O614.24+2
A
1001-4861(2016)02-0259-08
10.11862/CJIC.2016.049
2015-08-12。收修改稿日期:2015-12-31。
浙江省自然科学基金(No.LY12B01003)资助项目。
*通信联系人。E-mail:sky53@zjnu.cn
