聚苯胺/聚吡咯⁃纳米二氧化硅复合薄膜的合成及防腐性能
2016-11-23李传宪石恩华
李传宪,石恩华,杨 爽,姚 博,杨 飞,燕 群
(中国石油大学(华东)储运与建筑工程学院,山东省油气储运安全省级重点实验室,青岛266580)
聚苯胺/聚吡咯⁃纳米二氧化硅复合薄膜的合成及防腐性能
李传宪,石恩华,杨 爽,姚 博,杨 飞,燕 群
(中国石油大学(华东)储运与建筑工程学院,山东省油气储运安全省级重点实验室,青岛266580)
采用循环伏安法(CV)在316不锈钢(316SS)表面聚合生成聚苯胺/聚吡咯⁃纳米二氧化硅(PAni/PPy⁃SiO2)共聚复合薄膜.通过电化学工作站、傅里叶变换红外光谱仪(FTIR)、X射线光电子能谱仪(XPS)和扫描电子显微镜(SEM)等考察了聚苯胺(PAni)、聚苯胺/聚吡咯(PAni/PPy)与PAni/PPy⁃SiO2薄膜的电化学聚合过程、分子结构和特征形貌;在3.5%(质量分数)NaCl水溶液中利用Tafel极化曲线和电化学阻抗谱(EIS)分别考察了PAni,PAni/PPy与PAni/PPy⁃SiO2薄膜对不锈钢的防腐性能.结果表明,通过电化学法可以在316不锈钢表面生成PAni/PPy⁃SiO2共聚复合薄膜;相对于PAni薄膜与PAni/PPy薄膜,PAni/PPy⁃SiO2薄膜有着更密实的表面结构,其对不锈钢的保护能力优于PAni/PPy薄膜和PAni薄膜,纳米SiO2的掺杂通过加强膜层的机械屏蔽作用并抑制腐蚀反应过程中电荷的传递,提高了薄膜的防腐能力.
聚苯胺;聚吡咯;二氧化硅;复合薄膜;防腐性能
金属腐蚀对经济生产造成巨大损害,为了提高金属使用寿命,减少因金属腐蚀引起的损失,开发新的防护材料势在必行[1].聚苯胺和聚吡咯等导电聚合物作为新型防护材料具有物理屏蔽性、传导静电性和缓蚀性等优点,已成为金属防腐领域的研究热点[2].DeBerry[3]利用电化学方法将聚苯胺(PAni)沉积于不锈钢上提高了不锈钢在酸性环境中的耐蚀性.Zhang等[4]用循环伏安法在1Cr18Ni9Ti不锈钢表面合成聚吡咯(PPy)膜层,通过在0.3 mol/L盐酸溶液中测试其阳极极化曲线,发现其腐蚀电位升高600 mV.
聚苯胺和聚吡咯可以通过电化学聚合法直接在金属电极表面沉积得到薄膜状态,直接用于金属防护.电化学聚合法可以有效避免大量使用挥发性有机溶剂,达到清洁生产的目的,不存在加工成膜困难的问题[5,6].徐慧等[7]采用电化学聚合法制备了耐防腐性能更好的聚苯胺/聚吡咯复合薄膜(PAni/PPy),但所制备的膜层易剥离,导致水分子和腐蚀性离子加速渗入[8].
将聚苯胺与无机物复合可增强防护效果[9~11].吕龙飞等[12]利用电化学方法通过加入TiO2粉末制备PAni/PPy/TiO2复合薄膜,发现其具有良好的防腐性能.刘万民等[13]采用循环伏安法分别制备了PAni⁃TiO2,PAni⁃SiO2,PAni⁃SiO2⁃TiO2涂层,其中单独掺入SiO2的效果最好.Grari等[14]通过超声分散SiO2粉末于水中制备得到聚吡咯⁃二氧化硅(PPy⁃SiO2)复合物,并用于金属防护领域.无机SiO2颗粒具有极高的化学稳定性与物理屏蔽性,可以与聚合物薄膜复合来提高薄膜的防腐性能,但常规分散法[15]在制备聚合物薄膜时不利于无机颗粒在体系中的分散.本文采用凝聚法[15]制备了纳米SiO2溶胶,并将其与含苯胺(Ani)和吡咯(Py)单体的电解液混合,提高了纳米SiO2的分散性;利用电化学合成法在316不锈钢(316SS)表面原位生成了聚苯胺/聚吡咯⁃纳米二氧化硅(PAni/PPy⁃SiO2)复合薄膜,考察了复合薄膜对不锈钢的防腐效果,探讨了纳米SiO2的加入对复合薄膜防腐性能的影响机理.
1 实验部分
1.1 试剂与仪器
苯胺,天津市光复科技发展有限公司;吡咯,天津博迪化工有限公司;硫酸,西陇化工有限公司;氯化钠、无水乙醇和正硅酸乙酯(TEOS),国药集团化学试剂有限公司.以上试剂均为分析纯.实验前分别对苯胺和吡咯进行减压蒸馏提纯.自制去离子水.
316不锈钢(316SS)电极购自上海楚兮实业有限公司,非工作区用聚四氟乙烯密封,工作区面积为1 cm2;NEXUS型傅里叶变换红外光谱仪(FTIR,美国Nicolet公司);Escalab 250Xi型X射线光电子能谱仪(XPS,美国Thermol Scientific公司);NoVaTM Nano SEM 430型冷场发射扫描电子显微镜(SEM,美国FEI公司);CHI604e电化学工作站(上海辰华公司),采用三电极系统:以带有鲁金毛细管的饱和甘汞电极(SCE)为参比电极,铂片电极为辅助电极,316不锈钢电极为工作电极,所测得的电位均相对于SCE.
1.2 实验过程
将316不锈钢电极工作区依次用600目、1000目和1200目的砂纸打磨至光亮,再依次用无水乙醇和去离子水清洗干净,自然晾干,备用.
1.2.1 PAni,PPy薄膜和PAni/PPy共聚薄膜的制备 将0.03 mol苯胺加入1 mol/L的硫酸溶液(将适量硫酸加入适量去离子水中,在300 r/min下搅拌10 min,并通入氮气15 min)中,在400 r/min下搅拌混合10min.于扫描速率50 mV/s下,在-0.45~1.25 V区间扫描5周,然后用无水乙醇和去离子水将所得工作电极清洗3次,在50℃下减压干燥24 h,备用.PPy薄膜和PAni/PPy共聚薄膜的制备方法同上(分别在0.03 mol吡咯的硫酸溶液和0.03 mol苯胺+0.006 mol吡咯的硫酸溶液中进行扫描).
1.2.2 PAni/PPy⁃SiO2复合薄膜的制备 纳米SiO2溶胶的制备:将适量TEOS加入1 mol/L的硫酸溶液中,在500 r/min下搅拌24 h直至TEOS充分水解,备用.
PAni/PPy⁃SiO2复合薄膜的制备:将0.03 mol苯胺和0.006 mol吡咯加入纳米SiO2溶胶中,在400 r/min转速下搅拌混合10 min;控制工作站扫描速率为50 mV/s,在-0.45~1.25 V区间扫描5周,使用无水乙醇和去离子水将所得工作电极清洗3次,在50℃下减压干燥24 h,备用;改变纳米SiO2与苯胺单体的摩尔比,制备摩尔比不同的复合薄膜,分别命名为PAni/PPy⁃SiO2(20∶1),PAni/PPy⁃SiO2(40∶3),PAni/PPy⁃SiO2(10∶1),PAni/PPy⁃SiO2(40∶5),PAni/PPy⁃SiO2(20∶3),括号中数值为SiO2与苯胺单体的摩尔比.
2 结果与讨论
2.1 制备过程分析
图1(A)~(D)分别是PAni,PPy,PAni/PPy和PAni/PPy⁃SiO2电化学合成过程的循环伏安曲线. 图1(A)在扫描范围内出现了聚苯胺从完全还原态到中间氧化态的氧化峰A和中间氧化态到完全氧化态的氧化峰B,A′和B′分别为其对应的还原峰[16].图1(B)中,第一周在-0.2 V处出现了由金属溶解电流引起的氧化峰,随后在0.95 V处出现的氧化峰为PPy成膜电流峰[17].第二周扫描时,由于不锈钢表面已经生成一层PPy膜,会抑制金属的溶解,并且PPy成膜电流峰值正移,电流减小,说明先形成的PPy膜对于后续的聚合具有催化作用[18].图1(C)中,第一周扫描时在-0.2 V处出现了由金属溶解电流引起的氧化峰;在1.0 V处出现与图1(B)相似的还原峰,但是峰值正移,且峰值电流有明显下降.说明先在不锈钢表面聚合的是PPy,但是聚合过程受到苯胺影响.从第二周开始没有出现与图1(A)和(B)相同的氧化还原峰,说明苯胺和吡咯已经发生共聚[7,12,19,20].图1(D)中各个氧化还原峰与图1(C)相比基本没有偏移,而氧化还原电流有所下降,这表明掺入的SiO2并没有与PAni或PPy发生化学反应,也没有改变PAni/PPy共聚时本身的成膜性质,而是降低了PAni/PPy薄膜的电荷传输能力.
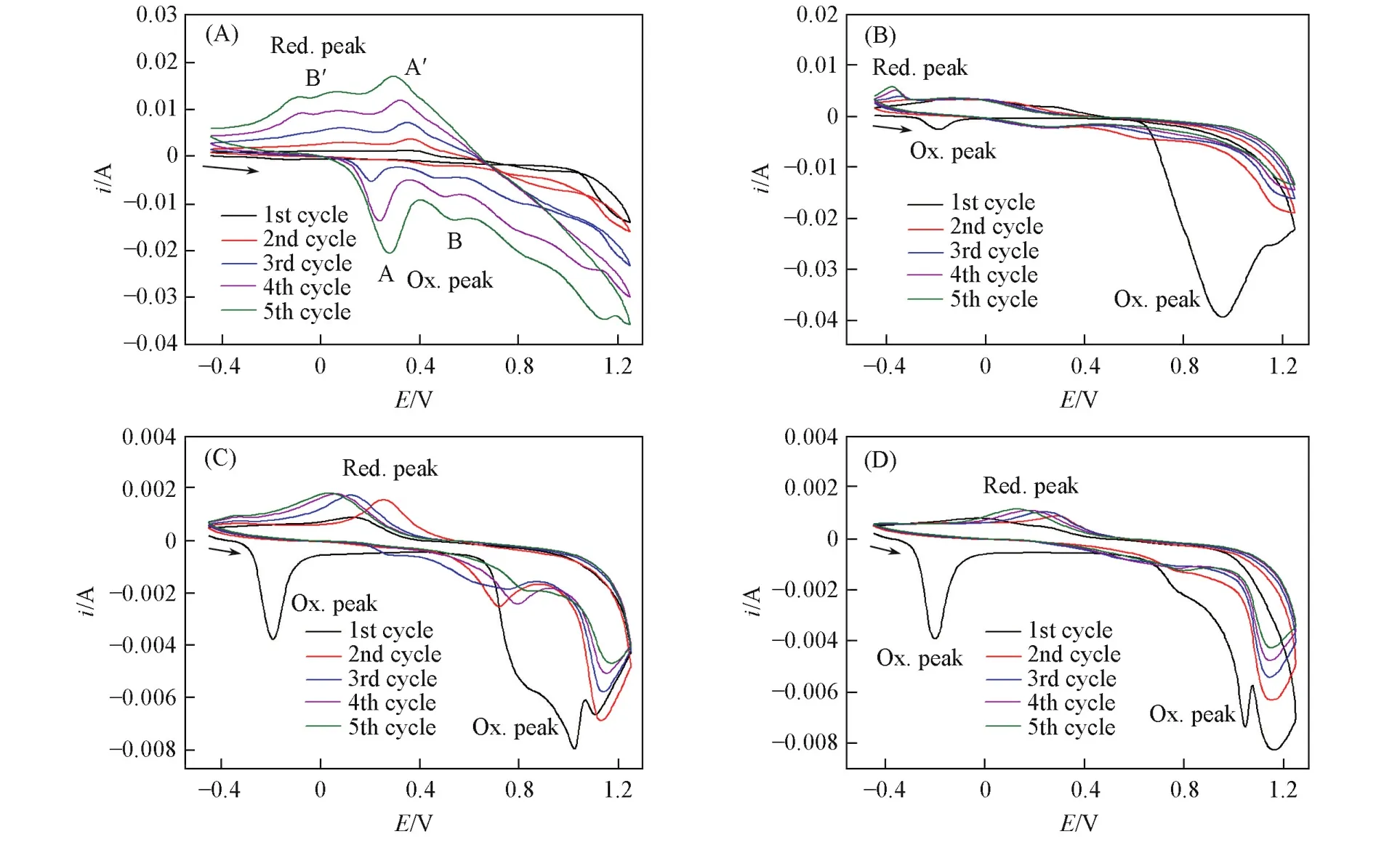
Fig.1 Cyclic voltammograms for PAni(A),PPy(B),PAni/PPy(C)and PAni/PPy⁃SiO2(D)
2.2 XPS分析
利用XPS谱对PAni、PPy和PAni/PPy薄膜进行了表征.由图2(A)可见,PAni中的N1s谱有3种类型:(醌亚胺),—NH—和—NH+,对应的结合能分别约为399.0,399.9和401.3 eV[21].由图2(B)可见,PPy中的N1s有2种类型:—NH—和N+,对应的结合能分别约为399.9和401.5 eV[22].图2(C)为PAni/PPy的N1sXPS谱图,图中出现了(醌亚胺),—NH—,—NH+和N+4种类型的峰.
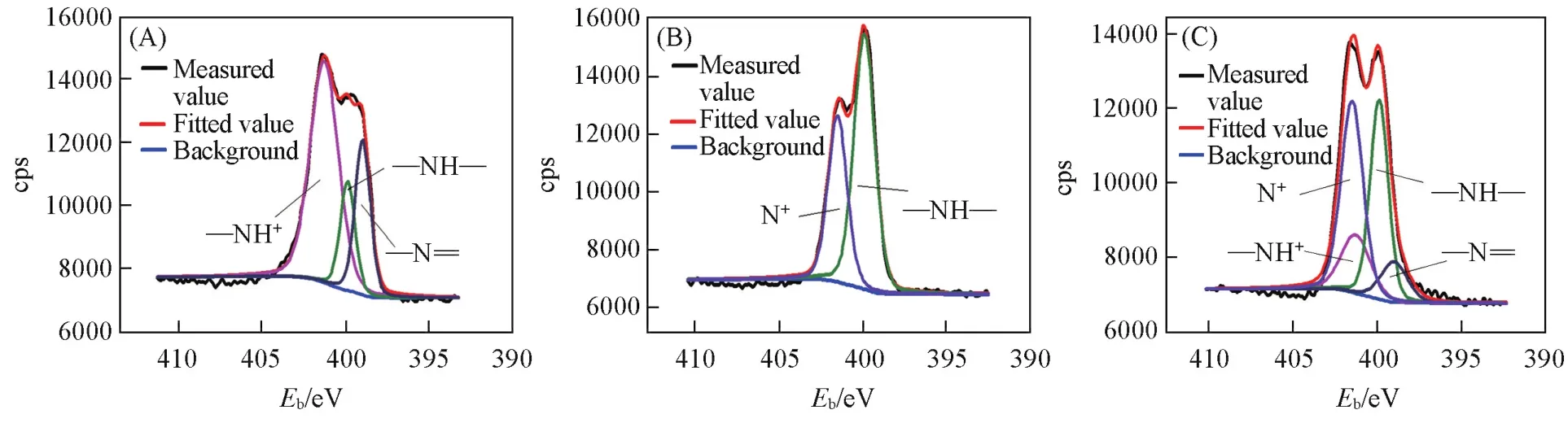
Fig.2 N1sXPS spectra of PAni(A),PPy(B)and PAni⁃PPy(C)
表1列出了图2中不同结合能对应N1s的分量.根据表中数据可看出,PAni/PPy中—NH+与的比值与PAni不同,且N+所占比例大于—NH—,与PPy中N+与—NH—的比例也明显不同,说明聚苯胺的分子结构发生了明显的改变,苯胺与吡咯发生了共聚[7,12,19,20].与—NH+结构的存在,以及体系内不成比例的N+/—NH—含量,说明仍有少量的PAni和PPy生成.

Table 1 Components of N1saccording to binding energy data from XPS
2.3 FTIR分析
PAni,PPy,PAni/PPy与PAni/PPy⁃SiO2薄膜的红外光谱图如图3所示.PAni的谱图(谱线a)在3450 cm-1处的吸收峰归属于N—H键的伸缩振动[23],在1560,1498 cm-1处分别是醌环和苯环的键的特征吸收峰,578, 614 cm-1处的吸收峰分别是键的伸缩振动和苯环对位取代峰.PPy的谱图(谱线b)在1060,1171和850 cm-1处的吸收峰分别为C—N键的特征吸收峰和吡咯环上的面内、面外弯曲振动吸收峰,886 cm-1处的吸收峰是吡咯环上C—H键面内弯曲变形振动和苯环对位取代振动的结果[24].PAni/PPy的谱图(谱线 c)出现了N—H键的吸收峰、醌环和苯环的键的特征吸收峰、键的伸缩振动和苯环对位取代峰;C—N吸收峰、吡咯环上的—H的面内和面外弯曲振动吸收峰、以及吡咯环上C—H键面内弯曲变形振动和苯环对位取代振动吸收峰,说明PAni/PPy薄膜中存在PAni 和PPy,这与XPS的分析结果一致.PAni/PPy⁃SiO2的谱图(谱线d)除了出现上述PAni/PPy的特征吸收峰外,1100 cm-1处的吸收峰是Si—O—Si结构反对称伸缩振动峰;780 cm-1处的吸收峰是Si—O对称伸缩振动吸收峰[25].红外分析结果表明,通过循环伏安法合成了PAni,PAni/PPy薄膜与PAni/PPy⁃SiO2复合薄膜.

Fig.3 FTIR spectra of PAni(a),PAni/PPy(b),PAni/PPy(c)and PAni/PPy⁃SiO2(d)membranes
2.4 CV分析

Fig.4 Cyclic voltammograms of PAni(A),PPy(B),PAni/PPy(C)and PAni/PPy⁃SiO 2(D)membranes in 1 mol/L H2SO4solution
在1 mol/L H2SO4溶液中分别对PAni,PPy,PAni/PPy和PAni/PPy⁃SiO2进行循环伏安扫描(CV),扫描范围-0.45~1.25 V,扫描速率50 mV/s,结果如图4所示.由图4(A)可以看出,PAni在1 mol/L
H2SO4溶液中的CV曲线与单体聚合时的CV曲线相比变化趋势相似,即在-0.2 V处还原峰增强,在0.6 V处还原峰减弱[26].图4(B)中,PPy的CV曲线与单体聚合时相比,同样是在-0.1 V处出现明显的还原峰.由图4(C)可以发现,PAni/PPy的CV曲线与单体聚合时的CV曲线相比,同样在0.2 V处出现明显的还原峰;与PAni和PPy的CV曲线有明显不同,说明二者在聚合过程中相互影响,发生了共聚[7,12,19,20].图4(D)中,PAni/PPy⁃SiO2的CV曲线与单体聚合时相比,同样也在0.2 V处出现明显的还原峰,说明SiO2并未与苯胺或吡咯单体发生化学反应.
2.5 SEM分析
图5为电沉积在316不锈钢表面的PAni和PAni/PPy薄膜和不同SiO2加入量的PAni/PPy⁃SiO2复合薄膜的SEM照片.由图5(A)~(C)可见,PAni薄膜表面颗粒为束棒状,结构较松散,且尺寸较大[27];PPy薄膜表面颗粒为不规则球状簇集,结构较紧凑,且尺寸相对较小;Ani和Py共聚后,合成的PAni/PPy聚合物薄膜表面突起状颗粒较少,结构明显更加平滑.由图5(D)~(F)可见,体系中含有纳米SiO2溶胶时,纳米SiO2颗粒参与聚合物成膜过程,由于SiO2的表面能极低[28],在金属表面吸附能力高于Ani和Py,所以SiO2会先吸附于金属表面并提供微小的晶核,使得电化学生成的聚合物分子附着于晶核的表面,在聚合物表面形成乳突,增加复合薄膜的致密度;但是随着SiO2加入量的增加,SiO2颗粒会在聚合物薄膜上发生团聚,使乳突的粒径增大,反而降低了PAni/PPy⁃SiO2复合薄膜的致密度.

Fig.5 SEM images of PAni(A),PPy(B),PAni/PPy(C)and PAni/PPy⁃SiO2(D—F)with different SiO2contents
2.6 防腐性能分析
2.6.1 Tafel极化曲线 将316不锈钢裸钢和分别电沉积有PAni,PAni/PPy,PAni/PPy⁃SiO2薄膜的316不锈钢电极浸润在3.5%(质量分数)NaCl溶液中,测试其浸泡初期的Tafel极化曲线,结果如图6所示.同时测试浸泡初期薄膜中不同SiO2含量对其防腐性能的影响,结果如图7所示.表2列出了根据Tafel曲线得到的自腐蚀电压(Ecorr)和自腐蚀电流(icorr).
由表2的Ecorr和icorr值可知,316不锈钢表面上电沉积PAni,PAni/PPy,PAni/PPy⁃SiO2薄膜后,Ecorr较裸钢都有了明显提高,其中PAni/PPy⁃SiO2>PAni/PPy>PAni.PAni/PPy⁃SiO2薄膜的Ecorr最高,icorr最小,说明PAni/PPy⁃SiO2薄膜的防腐性能最好,由于薄膜干燥过程中存在硅羟基缩水反应,使SiO2形成了“硅网络结构”[29],增强了薄膜的致密程度,又因为SiO2具有良好的物理屏蔽性,所以水分子在PAni/PPy⁃SiO2复合薄膜上具有更低的渗透率,从而加强了聚合物薄膜对腐蚀介质的机械屏蔽作用[30].
由表2可知,在一定范围内,随着复合薄膜中SiO2含量的增加,自腐蚀电流呈现出先减小后增大
的趋势,自腐蚀电压呈现出先增大后减小的趋势.当苯胺与纳米SiO2的摩尔比为10∶1时,薄膜表现出最佳的防腐性能,对应的腐蚀电位和腐蚀电流分别为0.122 V和2.748×10-6A/cm2,说明在一定范围内,随着SiO2加入量的增加,复合薄膜的防腐性能增强;但是SiO2加入量超过一定范围后,复合薄膜的防腐性能开始下降,这是因为大量SiO2掺杂在复合薄膜中后,在金属表面发生团聚,产生的乳突颗粒粒径不均一,影响了复合薄膜的致密性,导致腐蚀介质进入金属基体表面发生腐蚀反应,从而降低了复合薄膜对腐蚀介质的机械屏蔽作用[21].

Fig.6 Tafel curves for bare 316SS(a),316SS/PAni(b),316SS/PAni/PPy(c),316SS/PAni/PPy⁃SiO2(20∶1)(d)electrodes in 3.5%(mass fraction)NaCl solution

Fig.7 Tafel curves for 316SS/PAni/PPy⁃SiO2electrodes with different SiO2contents in 3.5%NaCl solution

Table 2 Ecorrand icorrin accordance with Tafel curves of differentmembranes on 316SS

Fig.8 EIS spectra for bare 316SS(a),316SS/PAni (b),316SS/PAni/PPy(c),316SS/PAni/PPy⁃SiO2(20∶1)(d)electrodes in 3.5% NaCl solution

Fig.9 EIS spectra for 316SS/PAni/PPy⁃SiO2electrodes with different SiO2contents in 3.5%NaCl solution
2.6.2 EIS测试 图8为316不锈钢裸钢和分别电沉积有PAni,PAni/PPy,PAni/PPy⁃SiO2薄膜的316
不锈钢电极在3.5%NaCl溶液中浸泡初期的电化学阻抗谱(Nyquist曲线);同时测试了浸泡初期不同纳米SiO2含量的PAni/PPy⁃SiO2薄膜的Nyquist曲线,如图9所示.
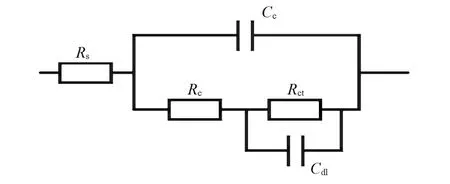
Fig.10 Equivalent circuit of 316SSmembrane
利用Z⁃view软件对图8和图9的EIS数据进行电路拟合,阻抗谱中出现2个时间常数,但薄膜表面尚未形成宏观小孔.高频段对应的时间常数来自于薄膜电容Cc及薄膜电阻Rc的贡献[31],与低频段对应的时间常数来自于薄膜界面双电层电容Cdl及薄膜传荷电阻Rct的贡献[32].图10为EIS等效电路模拟图(其中,Rs为溶液电阻,Rc为薄膜电阻,Cc为薄膜电容;Rct为传荷电阻,Cdl为界面双电层电容).由于电极过程中代表纯电容性质特性的部分偏离纯电容,所以用常相位角元件CPE代替纯电容元件
C[33],n为弥散指数.对图8和图9分析出的拟合原件参数见表3.

Table 3 EIS fitting parameters of differentmembranes on 316SS
电化学阻抗技术是衡量薄膜耐腐蚀性能的有效手段,Nyquist图中圆弧半径越大说明薄膜阻抗值越大,抗腐蚀能力越强.由图8可知,薄膜抗腐蚀能力的顺序为PAni/PPy⁃SiO2>PAni/PPy>PAni,且均优于裸钢.PAni/PPy⁃SiO2复合薄膜圆弧的半径最大,说明SiO2的加入使腐蚀介质(如Cl-)穿过薄膜到金属表面变得更加困难[34].由表3可知,PAni/PPy⁃SiO2的薄膜电阻为202.3Ω·cm2,高于PAni/PPy的薄膜电阻169.2Ω·cm2,这是因为二氧化硅具有极低的电导率,使PAni/PPy⁃SiO2薄膜电阻较高,较高的薄膜电阻有利于提高对金属的防护效果[35].同时,PAni/PPy⁃SiO2(20∶1)的薄膜电容为2.0994×10-4F/cm2,明显低于PAni/PPy的薄膜电容2.7486×10-4F/cm2,而薄膜电容与水分子在薄膜中的渗透程度有关,加入SiO2后形成的“硅网络结构”增加膜层的致密程度[29],降低了PAni/PPy⁃SiO2薄膜电容,较低的薄膜电容意味着水分子难以在薄膜中扩散.PAni/PPy⁃SiO2(20∶1)的传荷电阻为1512.8Ω·cm2,明显高于PAni和PAni/PPy薄膜,说明SiO2的加入可以抑制金属表面腐蚀过程中的电荷传输,提高复合薄膜的传荷电阻.
由图9可知,薄膜的抗腐蚀能力顺序为PAni/PPy⁃SiO2(10∶1)>PAni/PPy⁃SiO2(40∶5)>PAni/PPy⁃SiO2(40∶3)>PAni/PPy⁃SiO2(20∶3)>PAni/PPy⁃SiO2(20∶1),可见,在一定范围内,随着纳米SiO2加入量的增加,复合薄膜的防腐性能增强,但SiO2加入量超过一定范围后,防腐性能开始下降.这一测试结果和Tafel极化曲线的测试结果一致.由表3可知,在一定范围内,随着复合薄膜中SiO2加入量的增加,薄膜电阻和传荷电阻均先增大后减小,薄膜电容先减小后增大,说明在一定范围内随着SiO2的加入量的增大,PAni/PPy⁃SiO2复合薄膜的防腐性能先增强后下降.
3 结 论
通过循环伏安法制备了PAni/PPy⁃SiO2复合薄膜,薄膜中引入纳米SiO2颗粒会在表面形成乳突,强化薄膜的机械屏蔽作用.PAni/PPy⁃SiO2复合薄膜中SiO2的量在一定范围内(苯胺与纳米SiO2的摩尔比不超过10∶1)时能较好抑制电荷传递,使薄膜对金属的保护能力优于PAni/PPy薄膜和PAni薄膜;当SiO2的掺入量过大时,颗粒会在金属表面团聚,降低膜层的致密程度,使得复合薄膜对金属的防护能力下降.
[1] Chen S.G.,Zhao W.Y.,Corros.Sci.Prot.Technol.,2009,21(3),269(陈世刚,赵文元.腐蚀科学与防护技术,2009,21(3),269)
[2] Slimane A.B.,Connan C.,Vaulay M.J.,Chehimi M.M.,J.Colloids Surf.A,2009,332(2),157—163
[3] DeBerry D.W.,J.Electrochem.Soc.,1985,132(5),1022—1026
[4] Zhang T.,Zeng C.L.,J.Electrochim.Acta,2005,50(24),4721—4727
[5] Mollahosseini A.,Noroozian E.,J.Synth.Met.,2009,159(13),1247—1254
[6] Long J.M.,Wang S.L.,Wang J.,J.Mater.Prot.,2003,36(12),23—26(龙晋明,王少龙,王静.材料保护,2003,36(12),23—26)
[7] Xu H.,Wang X.Y.,Liu X.Y.,Corros.Sci.Prot.Technol.,2012,3(2),127—131(徐慧,王新颖,刘小育.腐蚀科学与防护技术,2012,3(2),127—131)
[8] Li Q.Q.,Huang J.H.,Liu S.Q.,Guan L.X.,Huang K.L.,J.Acta Chim.Sin.(Engl.Ed.),2008,66(5),571—575(李倩倩,黄健涵,刘素琴,关鲁雄,黄可龙.化学学报,2008,66(5),571—575)
[9] Olad A.,Barati M.,Shirmohammadi H.,J.Prog.Org.Coat.,2011,72(4),599—604
[10] Jia Y.F.,Liu C.H.,Liao Z.J.,Wang F.,Ye S.T.,Ban G.D.,Ding Y.D.,Lin R.,J.Surf.Technol.,2016,45(3),164—168(贾艺凡,刘朝辉,廖梓珺,王飞,叶圣天,班国东,丁逸栋,林锐.表面技术,2016,45(3),164—168)
[11] Redondo M.I.,Breslin C.B.,J.Corros.Sci.,2007,49(4),1765—1776
[12] Lv L.F.,Preparation,Characterization and Anti⁃corrosion Performance ofAniline⁃pyrrole CopolymerCompositeMaterials,Jiangsu University of Science and Technology,Zhenjiang,2014(吕龙飞.苯胺⁃吡咯共聚物复合材料的制备、表征及其防腐蚀性能,镇江:江苏科技大学,2014)
[13] Liu W.M.,He Y.J.,Li Z.T.,J.Surf.Technol.,2010,39(3),58—60(刘万民,何拥军,李芝坛.表面技术,2010,39(3),58—60)
[14] Grari O.,Dhouibi L.,Lallemand F.,Buron C.C.,Taouil A.E.,Hihn J.Y.,J.Ultrason.Sonochem.,2015,22,220—226
[15] Chen Z.Q.,Wang G.X.,Xu G.Y.,Colloid and Interface Chemistry,Higher Education Press,Beijing,2001,101—105(陈宗淇,王光信,徐桂英.胶体与界面化学.北京:高等教育出版社,2001,101—115)
[16] Stilwell D.E.,Park S.M.,J.Electrochem.Soc.,1988,135(10),2491—2496
[17] Tüken T.,Arslan G.,YazıcıB.,Erbil M.,J.Prog.Org.Coat.,2004,49(2),153—159
[18] LiM.C.,Zhu W.X.,Zhu J.N.,MoW.M.,Chem.J.Chinese Universities,2012,33(1),128—132(李美超,朱婉霞,朱静娜,莫卫民.高等学校化学学报,2012,33(1),128—132)
[19] Lv L.F.,Lin S.L.,Chen C.X.,Wen D.,Li X.S.,J.Surf.Technol.,2013,42(4),110—114(吕龙飞,林生岭,陈传祥,文丹,李潇霜.表面技术,2013,42(4),110—114)
[20] Xiong D.B.,Yang C.M.,Chin.J.Appl.Chem.,2009,26(9),1054—1059(熊冬柏,杨春明.应用化学,2009,26(9),1054—1059)
[21] Han M.G.,Cho S.K.,Oh S.G.,Im S.S.,J.Synth.Met.,2002,126(1),53—60
[22] Kang E.T.,Neoh K.G.,Zhang X.,Zhang X.,Tan K.L.,Liaw D.J.,J.Surf.Interface Anal.,1996,24(1),51—58
[23] KalendováA.,VeselýD.,Kohl M.,Stejskal J.,J.Prog.Org.Coat.,2015,78,1—20
[24] Sheng N.,Lei Y.H.,Hyonoo A.,Ueda M.,Ohtsuka T.,J.Prog.Org.Coat.,2014,77(11),1724—1734
[25] Huang H.,Wu J.,Lin X.,Li L.,Shang S.M.,Yuen M.C.,Yan G.P.,J.Carbohydr.Polym.,2013,95(1),72—76
[26] Chen Z.P.,Chu D.B.,Chen J.H.,Guo J.H.,Yin X.J.,Wu H.Z.,Acta Polym.Sin.,1900,1(6),536—540(陈忠平,褚道葆,陈君华,过家好,伊晓娟,吴何珍,高分子学报,1900,1(6),536—540)
[27] Wang H.Z.,LiuW.H.,Li J.,Yao S.W.,ZhangW.G.,Chem.J.ChineseUniversities,2012,33(2),421—425(王宏智,刘炜洪,李剑,姚素薇,张卫国.高等学校化学学报,2012,33(2),421—425)
[28] Luo Z.H.,He T.Y.,Lin C.G.,Dai L.Z.,J.Polym.Bull.,2007,9,9—13(罗正鸿,何腾云,蔺存国,戴李宗.高分子通报,2007,9,9—13)
[29] Jeong A.Y.,Koo S.M.,Kim D.P.,J.Sol⁃Gel Sci.Technol.,2000,19(1—3),483—487
[30] Cook A.,Gabriel A.,Siew D.,Laycock N.,J.Curr.Appl.Phys.,2004,4(2—4),133—136
[31] Zhang J.Q.,Cao C.N.,Corros.Prot.,1998,8,32—36(张鉴清,曹楚南.腐蚀与防护,1998,8,32—36)
[32] ZhangW.,Wang J.,Zhao Z.Y.,Liu X.Q.,J.Chin.Soc.Corros.Prot.,2011,5,36—45(张伟,王佳,赵增元,刘学庆.中国腐蚀与防护学报,2011,5,36—45)
[33] Cao C.N.,Electrochemistry ofCorrosion(3rd Edition),Chemical Industry Press,Beijing,2008,175—179(曹楚南.腐蚀电化学原理(第三版).北京:化学工业出版社,2008,175—179)
[34] Sathiyanarayanan S.,Azim S.S.,Venkatachari G.,J.Synth.Met.,2007,157(18),751—757
[35] Lasia A.,Modern Aspects of Electrochemistry,Springer,New York,2002,143—248
Synthesis and Anti⁃corrosion Properties of Polyaniline/Polypyrrole⁃nano Silicon Dioxide Composite Membrane†
LIChuanxian,SHIEnhua,YANG Shuang,YAO Bo,YANG Fei∗,YAN Qun
(College of Pipeline and Civil Engineering,China University ofPetroleum(East China),Shandong Key Laboratory ofOil&Gas Storage and Transport Safety Engineering,Qingdao 266580,China)
In this article,polyaniline/polypyrrole⁃nanosilicon dioxide(PAni/PPy⁃SiO2)compositemembrane was prepared by cyclic voltammetry(CV)method on the surface of 316 stainless steel(316SS).The electro⁃chemical polymerization process,structural and morphological characteristics of polyaniline(PAni),polyani⁃line/polypyrrole(PAni/PPy)and PAni/PPy⁃SiO2membraneswere investigated by cyclic voltammetry(CV),Fourier transform infrared spectroscopy(FTIR),X⁃ray photoelectron spectroscopy(XPS)and scanning elec⁃tron microscopy(SEM),respectively.The antiseptic properties of PAni,PAni/PPy and PAni/PPy⁃SiO2mem⁃branes to stainless steelwere studied by the Tafel polarization curve and electrochemical impedance spectrosco⁃py(EIS)in 3.5%(mass fraction)NaCl aqueous solution.The results show that PAni/PPy⁃SiO2composite membrane can form on the surface of 316 stainless steel by electrochemical process.Compared with PAni and PAni/PPymembranes,PAni/PPy⁃SiO2compositemembrane has tighter surface structure.The metal protec⁃tion ability of PAni/PPy⁃SiO2is better than those of PAni/PPy and PAnimembranes.The anti⁃corrosion abili⁃ty ofmembrane is improved because of the strengtheningmechanical shielding effect ofmembrane with nano SiO2and the inhibition of charge transfer during the corrosion reaction process.
Polyaniline;Polypyrrole;Silica;Compositemembrane;Anti⁃corrosion performance
O646;TG178
A
10.7503/cjcu20160390
(Ed.:S,Z,M)
†Supported by the Fundamental Research Funds for the Central Universities,China(Nos.15CX06072A,15CX06066A).
2016⁃05⁃30.
日期:2016⁃10⁃20.
中央高校基本科研业务费专项资金(批准号:15CX06072A,15CX06066A)资助.
联系人简介:杨 飞,男,博士,副教授,主要从事油气储运安全技术研究.E⁃mail:yf9712220@sina.com
