新型异烟酸类蚜虫报警信息素类似物的设计、合成及生物活性
2016-11-23秦耀果张景朋宋敦伦2段红霞蒋标标杨新玲
秦耀果,张景朋,宋敦伦2,段红霞,凌 云,蒋标标,王 迪,杨新玲
(1.中国农业大学理学院应用化学系,2.植物保护学院昆虫学系,北京100193)
新型异烟酸类蚜虫报警信息素类似物的设计、合成及生物活性
秦耀果1,张景朋1,宋敦伦2,段红霞1,凌 云1,蒋标标1,王 迪1,杨新玲1
(1.中国农业大学理学院应用化学系,2.植物保护学院昆虫学系,北京100193)
以蚜虫报警信息素[(E)⁃β⁃farnesene,EBF]为先导,通过活性亚结构拼接和生物电子等排原理,设计合成了一系列结构新颖的异烟酸类EBF类似物.以香叶醇为原料,经4步反应制得20个目标化合物(19个未见文献报道),其结构经1H NMR,13CNMR,IR及HRMS确证.初步生物活性测定结果表明,所有化合物对桃蚜有驱避活性和杀死活性,其中化合物7d,8f和8n表现出较好的桃蚜驱避活性,对桃蚜的驱避率分别为62.6%,62.0%和61.0%;化合物8a,8b和8d对桃蚜的致死率分别为73.6%,81.1%和70.2%.初步构效关系分析发现,酯基的引入对桃蚜的驱避活性有利;酰胺基的引入对杀蚜活性有利;N烷基取代的链长及支链数量影响驱避活性.
异烟酸;蚜虫报警信息素;类似物;生物活性
蚜虫给农业生产带来严重危害[1],是最主要的农业害虫之一[2].目前,蚜虫的防治过度依赖于传统农药,从而导致蚜虫的抗药性不断增加及对天敌、蜜蜂等非靶标生物不安全等严峻问题[3].因此,当今对蚜虫的防治应遵从生态友好的理念,从传统的“杀灭”转向科学的“调控”[4].利用蚜虫报警信息素控制蚜虫是一种有发展前景的策略,可以减少用药量及抗性产生,利于生态保护[5,6].
蚜虫报警信息素(Aphid alarm pheromone)是蚜虫受到外界干扰时从腹管分泌的油状液体,起到警示其它蚜虫迅速逃离的作用[7].这种油状液体的主要成分为(E)⁃β⁃farnesene(EBF,图1)[8,9].除具有报警活性外,EBF在高剂量时对蚜虫有毒杀作用[10],与商品化杀虫剂混用防治蚜虫可以起到增效作用[11].但由于其结构中存在共轭双键,使EBF易挥发、易氧化而不稳定,很难在实际中应用.因此,研究者为改善其稳定性对其进行结构改造,合成了一些具有一定报警活性和稳定性的EBF类似物[12~15].
Fig.1 Structure of(E)⁃β⁃farnesene
将杂环基团引入EBF活性骨架中替代不稳定的共轭双键,可能会发现活性与稳定性兼备的新型蚜虫控制剂先导化合物,为EBF的结构改造及活性研究提供了新思路.本研究组[16,17]前期引入噻唑、吡唑等杂环替代EBF中不稳定的共轭双键,设计合成了具有一定杀蚜活性与稳定性的化合物,具有较好的发展前景.
许多含吡啶基团的化合物表现出优异的杀蚜活性[18~21],如吡虫啉、吡蚜酮和氟啶虫酰胺等.含吡啶基团的异烟酸是重要的农用和医用中间体,很多含异烟酸结构的化合物具有优异的杀虫活性[18]和抗菌活性[22].
本文以生态友好为前提开展EBF的结构改造及生物活性研究.通过活性亚结构拼接,将异烟酸结构引入到EBF骨架结构中替代不稳定的共轭双键,同时利用生物电子等排原理将9号碳上的CH2以O,NH或N—R替代,设计合成了20个异烟酸酯或酰胺类的EBF类似物;对目标产物进行了蚜虫驱
避及杀蚜活性测定,并对其构效关系进行了初步分析.期望发现具有良好驱避活性或杀蚜活性的蚜虫控制剂先导化合物,并探索酯基、酰胺或N取代酰胺对活性的影响.目标化合物的设计策略及合成路线如Scheme 1所示.
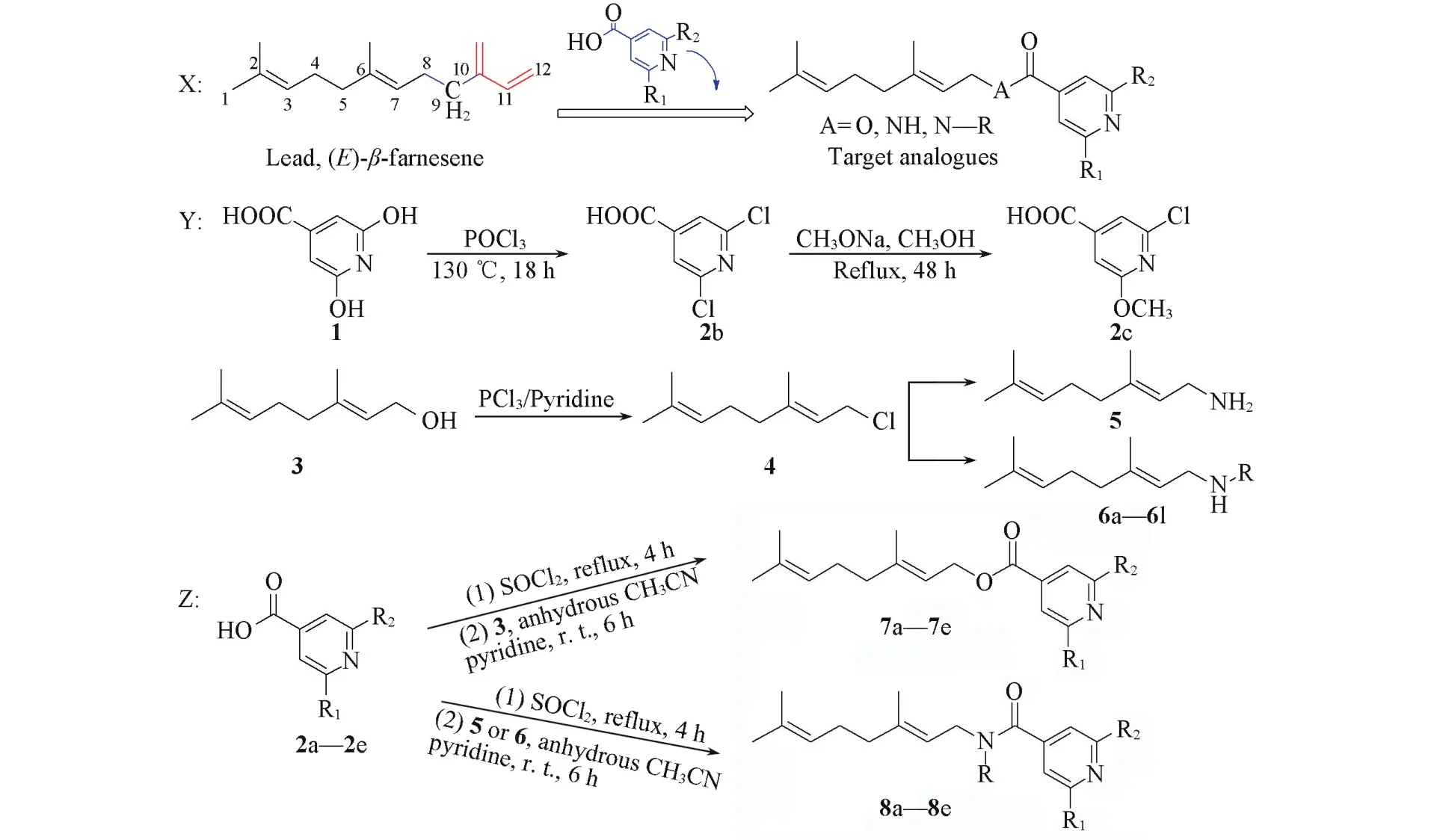
Scheme 1 Design strategy(X),general synthetic route of intermediates(Y)and target com pounds(Z)
1 实验部分
1.1 试剂与仪器
所用试剂均为国产分析纯或化学纯;二氯亚砜(SOCl2)、三氯氧磷(POCl3)、四甲基氯化铵(C4H12ClN)、氢氧化锂单水合物(LiOH·H2O)、异烟酸(2a)、2⁃氯异烟酸(2d)和2⁃甲氧基异烟酸(2e)等试剂均购于北京偶合科技有限公司;所用溶剂购于国药集团化学试剂北京有限公司,使用前均经无水处理;H型柱层析硅胶(青岛海洋化工厂).
Cole⁃Parmer熔点仪(美国Cole⁃Parmer仪器公司);Bruker DPX 300 MHz核磁共振仪(以TMS为内标,CDCl3为溶剂,德国Bruker公司);APEXⅣ型傅里叶变换高分辨质谱仪(德国Bruker公司).
1.2 中间体的制备
1.2.1 2⁃氯⁃6⁃甲氧基吡啶⁃4⁃羧酸(2c)的制备 中间体2a,2d和2e为市售产品;2b和2c由合成得到. 2,6⁃二氯异烟酸(2b)参照文献[23]方法合成,得到灰白色固体,m.p.208~210℃(文献值[24]:208~210℃),产率75.5%.2,6⁃二氯异烟酸2b与甲醇钠回流反应6 h后,将产物酸化得到2⁃氯⁃6⁃甲氧基异烟酸(2c),白色固体,m.p.212~213℃(文献值[25]:213~215℃),产率93.5%.
1.2.2 香叶基氯(4)的制备 以香叶醇(3)和三氯化磷为原料,无水吡啶为缚酸剂,参照文献[26]方
法合成中间体香叶基氯(4),得浅黄色液体,直接用于下一步的合成.
1.2.3 香叶基胺(5)的制备 以香叶基氯(4)和邻苯二甲酰亚胺钾盐为起始原料,参照文献[26]方法合成中间体香叶基胺5,得黄色液体,产率25.2%(文献值[26]:26.4%).
排放有害气体是化学制版的主要危害,无害化处理也是利用化学反应来进行。如含盐酸气体,一般利用氢氧化钠洗涤处理成为氯化钠;含氨废气通过稀硫酸处理得到硫酸铵等。
1.2.4 N⁃取代⁃香叶基胺(6)的制备 参照文献[26]方法合成化合物6,以N⁃甲基⁃香叶基胺为例,将甲胺甲醇(质量分数37%)室温下与香叶基氯(4)反应8 h,减压脱除溶剂,经柱层析分离得浅黄色液体,产率46.5%(文献值[26]:46.5%).中间体4~6的质谱数据列于表1.

Table 1 MS data of intermediates 4—6∗
1.3 目标物的制备
1.3.1 目标化合物7和8的制备 以(E)⁃3,7⁃二甲基⁃2,6⁃辛二烯基吡啶羧酸酯(7a)为例.将异烟酸(2.0 g,0.016 mol)、二氯亚砜(5.80 g,0.049 mol)和50 mL甲苯依次加入到100 mL三口瓶中,回流反应4 h.常压蒸馏,加入50 mL无水乙腈,滴加香叶醇(3,2.50 g,0.016 mol)和2 mL吡啶,常温下反应6 h.脱除溶剂,经柱层析纯化[V(石油醚)∶V(乙酸乙酯)=50∶1],得黄色液体3.56 g,产率85.9%.
目标化合物7和8的理化性质、高分辨质谱及红外光谱数据见表2,核磁共振数据见表3.

Table 2 Appearance,yields,HRMS and IR data of target compounds 7 and 8a
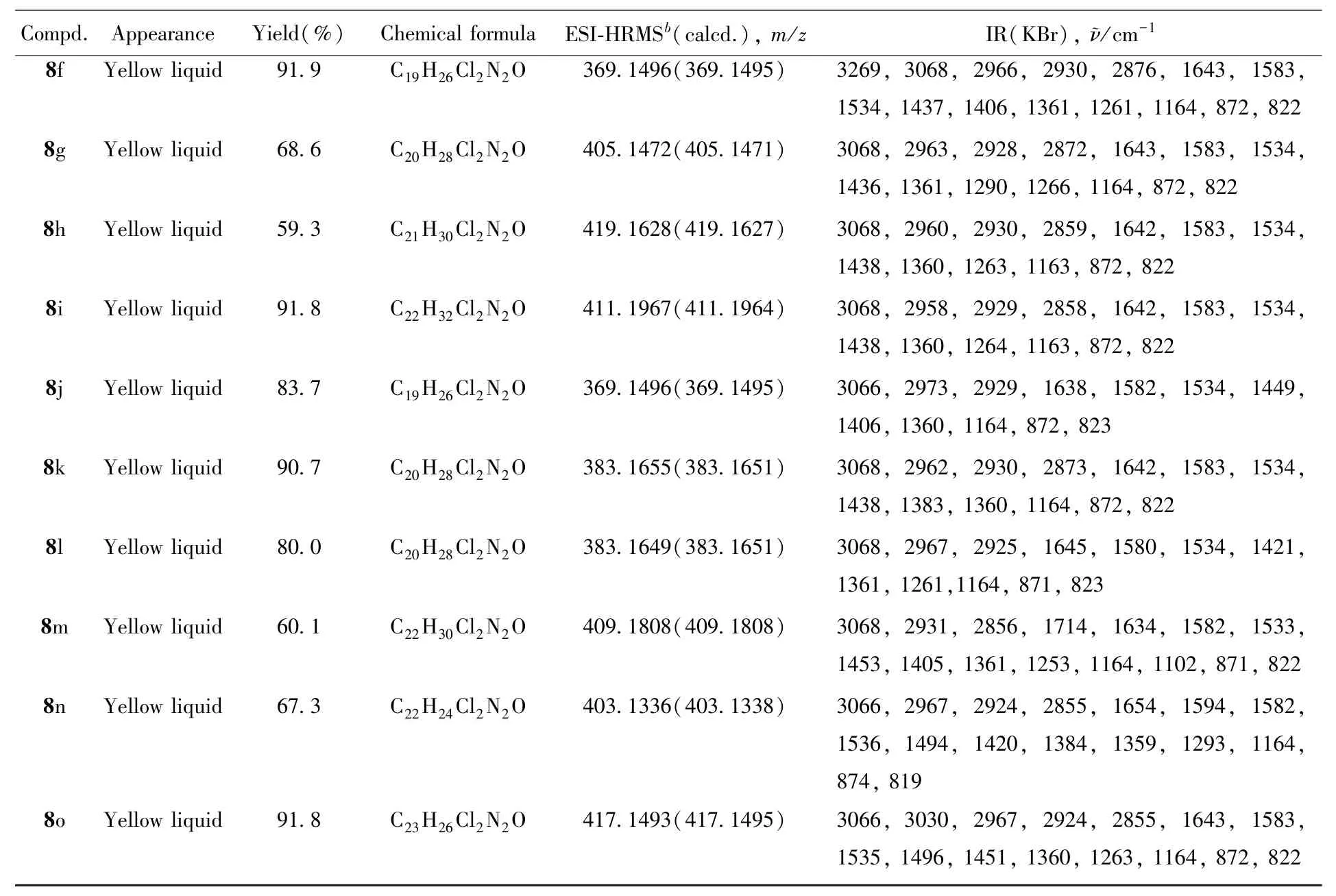
Continued

Table 31H NMR and13C NMR data of target compounds 7 and 8∗

Continued

Continued
1.4 目标化合物的生物活性测试
1.4.1 目标化合物的驱避活性测试 参照文献[17]方法,选择桃蚜(Myzus persicae)为供试昆虫,以先导EBF作为对照药,采用T管法测定了目标化合物的驱避活性,测试结果见表4.
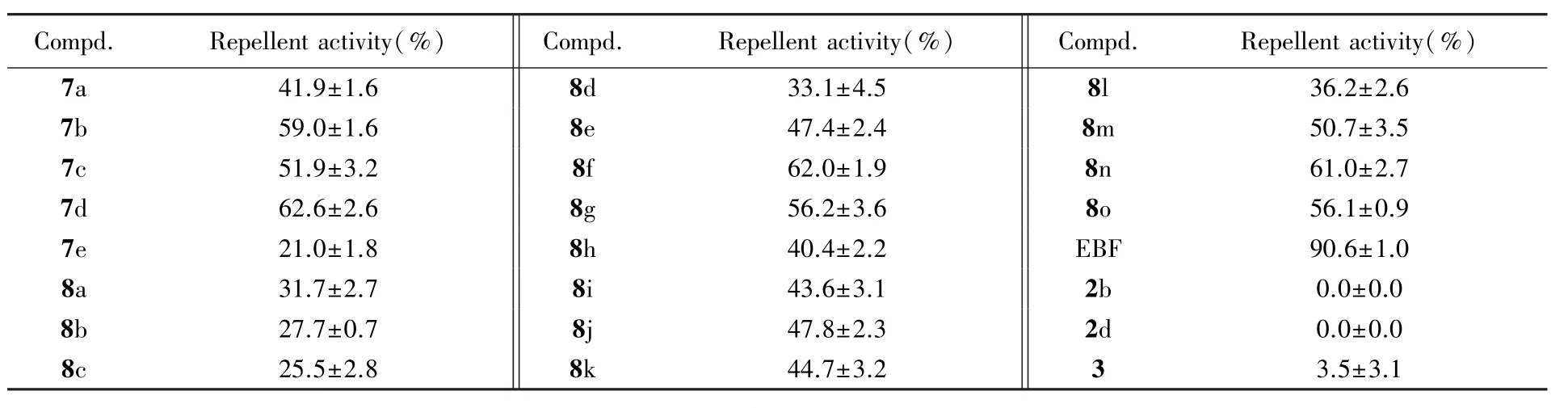
Table 4 Repellent activity of the target compounds against Myzus persicae(5μg)
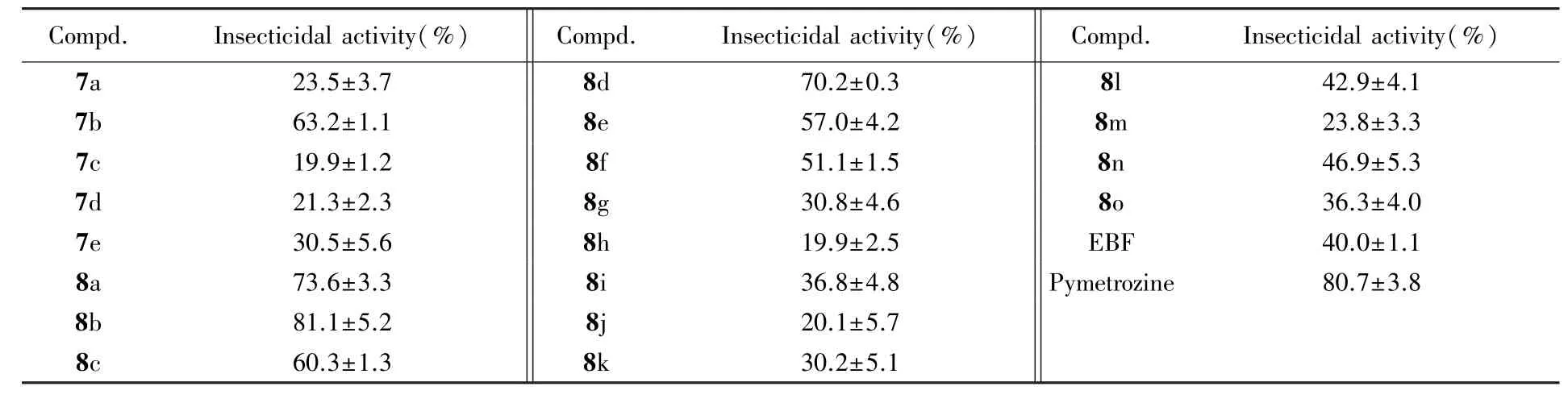
Table 5 Insecticidal activity of the target com pounds against Myzus persicae(300μg/m L)
2 结果与讨论
2.1 目标化合物的合成
中间体2,6⁃二氯异烟酸(2b)由2,6⁃二羟基异烟酸与三氯氧磷经亲核取代反应制得,另一中间体2c由中间体2b与甲醇钠通过置换反应制得.含酯基目标化合物(7a~7e)以香叶醇(3)为起始原料,与(取代)异烟酸2a~2e发生亲核取代反应制得.合成含酰胺基目标化合物(8a~8c)时,首先由香叶醇经亲核取代反应制得香叶基氯(4);香叶基氯再与邻苯二甲酰亚胺钾盐发生取代反应生成香叶基胺(5);最后,中间体5与2a~2c反应制得目标化合物.N取代酰胺基目标化合物(8d~8o)则由香叶基氯与甲胺、乙胺等对应伯胺反应制得相应中间体N⁃取代香叶基胺(6),然后化合物6与化合物2b发生亲核取代反应,即可制得目标化合物8d~8o.其中,在制备中间体2b的过程中,因反应物三氯氧磷遇潮湿空气易发生水解,故反应溶剂应经过严格的无水处理.以二氯亚砜为氯化剂,通过常规方法可高收率获得目标物.
2.2 目标化合物的结构表征
目标化合物的结构均通过1H NMR,13C NMR,IR及HRMS表征.酯基和酰胺基的EBF类似物以代表性化合物7d的结构表征为例.在化合物7d的1H NMR谱中,吡啶环上的6位H在δ8.53处呈2个双重峰,偶合常数分别为5.1和0.7 Hz,吡啶环上的另外2个H均为四重峰,分别位于δ7.89和7.78处.香叶基链上的H分别位于δ5.42~5.48和5.04~5.13处,均为多重峰.与酯基相连的2个 CH2位于δ4.89和4.86处,均为1个尖锐的单峰.香叶基链上2个相连的CH2位于δ2.02~2.19处,为多重峰.香叶基链上的3个CH3分别位于δ1.78,1.68和1.61处,均呈单峰.在化合物7d的IR谱中,3060与2970 cm-1附近为不饱和碳的C—H伸缩振动吸收峰;2920与2860 cm-1附近为饱和碳链CH2的C—H伸缩振动吸收峰;1730 cm-1附近为C的伸缩振动吸收峰—尖峰,强度最大,而1590与760 cm-1附近为吡啶环的伸缩振动吸收峰,强度中等;1460 cm-1附近为CH2的C—H弯曲振动吸收峰.
N烷基取代的EBF类似物在1H NMR和13C NMR谱中均出现了异常裂分.以代表性化合物8d的结构表征为例:在其常温1H NMR谱中,吡啶环上的2个H呈单峰,位于δ7.26处.C3和C7上2个H分别位于δ5.18~5.21和5.07~5.13处,均为多重峰.C8上2个H位于δ4.14和3.76处,呈2个双峰. C16上3个H位于δ3.04和2.85处,呈2个单峰.C4和C5上4个H位于δ2.03~2.10处,为多重峰. C1,C17和C18上3个CH3分别位于δ1.74,1.69,1.62和1.52处,呈4个单峰.以上C3,C7,C8和C16上的H发生了不规则裂分,可能是由N—CH3基团的N—C键自由旋转引起的构象转换所致.因此,采用变温核磁手段对化合物8d的结构进一步确证,图2(A)为化合物8d在相同浓度下于常温(25℃)和变温(100℃)下的1H NMR对比谱图.在变温1H NMR(300 MHz,CDCl3)谱图中,C3,C7,C8和C16上的质子“异常裂分”现象消失,可能是由于该类化合物在高能量下构象快速转换,以一种构象存在.在化合物8d的常温13C NMR(75 MHz,CDCl3)谱中,碳原子在谱图中成对出现,如C10 (δ165.66,165.20),C11(δ150.49,150.43),C6(δ141.13,140.59),C2(δ131.48,131.20),C3 (δ123.37,123.11),C7(δ117.69,117.51),C5(δ39.15,39.00)和C17(δ15.82,15.71),推测也是
由N—CH3基团的N—C键自由旋转引起的构象转换所致.因此,采用变温核磁手段对化合物8d的13C NMR进一步研究,图2(B)为化合物8d在相同浓度下于常温(25℃)和变温(100℃)下的13C NMR谱图.在变温13C NMR谱图中,成对出现的谱线消失,证明了推测的正确性.

Fig.21H NMR(A)and13C NMR spectra(B)of compound 8d at 25(a)and 100℃(b)
2.3 目标化合物的生物活性及构效关系
驱避活性和杀蚜活性测定均依据标准方法进行,对二者独立测定,二者无相互负面影响.驱避活性测定结果(表4)表明,在5μg用量下,所有目标化合物对桃蚜均有驱避活性.其中,化合物7d,8f 和8n的驱避活性较好,驱避率分别为62.6%,62.0%和61.0%;化合物7e,8b和8c对桃蚜的驱避活性较低,仅有约20%的驱避活性;反应物2,6⁃二氯异烟酸(2b),2⁃氯异烟酸(2d)和香叶醇(3)均未表现出驱避活性,而对应的目标物7b和7d均有驱避活性,推测EBF的骨架结构对驱避活性起重要作用.初步构效关系分析表明,当R1与R2相同时,A为酯基时化合物的驱避活性明显优于A为酰胺基时的活性,如7a>8a,7b>8b,7c>8c;且吡啶环2位为吸电子基的化合物7d活性优于给电子基7e的活性;N原子上的取代基为直链烷基时,碳链长度对活性有影响,3个碳原子对活性最有利,呈现出C3>C4>C2>C5≈C6>C1的规律;N原子上取代烷基支链的数量也对活性有一定影响,表现为支链越多对活性越不利,如8l<8k<8g,8j<8f.
杀蚜活性测定结果表明,在300μg/mL浓度下目标化合物对桃蚜均表现出杀死活性.其中,化合物7b,8a~8f的杀蚜活性优于先导化合物EBF,化合物8i,8l,8n和8o与EBF的杀蚜活性相当,化合物8b与吡蚜酮杀蚜活性相当.对目标化合物的结构活性进一步分析发现:当R1与R2相同时,A为酰
胺时的化合物的杀蚜活性明显优于A为酯基时的活性,如化合物8a,8b和8c的杀蚜活性明显高于化合物7a,7b和7c;N⁃取代烷基化合物的活性比相应的酰胺基化合物的活性有所下降;N原子上烷基链的长度对杀蚜活性有影响,表现为随着碳链的增长,杀蚜活性有所降低;N原子上为6个直链碳取代的化合物的活性优于六元饱和环状化合物的活性,如8i>8m.
3 结 论
以蚜虫报警信息素活性成分EBF为先导,利用活性亚结构拼接和生物电子等排原理,以香叶醇和2,6⁃二羟基异烟酸为起始原料,经取代、酰化等反应,将异烟酸结构引入EBF以取代不稳定的共轭双键,设计合成了一系列新型含异烟酸结构的EBF类似物.初步生物活性测定结果表明,目标化合物均有一定的蚜虫驱避活性及杀蚜活性.初步构效关系分析发现,酯基的引入对桃蚜的驱避活性有利,酰胺基的引入则对杀蚜活性有利;N上的烷基取代的链长、支链数量或芳香性影响驱避活性,表现为3个碳原子对活性最有利,支链越多对活性越不利.本文为进一步的结构优化提供了依据,对新型蚜虫控制剂的创制工作具有一定的指导意义.
[1] Yang Y.,Liu Y.X.,Song H.J.,Li Y.Q.,Wang Q.M.,Bioorg.Med.Chem.,2016,24(3),391—402
[2] Yang X.L.,HuangW.Y.,Ling Y.,Kan W.,Fang Y.L.,Zhang Z.N.,Chem.J.Chinese Universities,2004,25(9),1657—1661(杨新玲,黄文耀,凌云,阚伟,方宇凌,张钟宁.高等学校化学学报,2004,25(9),1657—1661)
[3] David P.,Environ.Dev.Sustain.,2005,7(2),229—252
[4] Huang W.Y.,Yang X.L.,Zhang Z.N.,Chemistry Bulletin,2002,3,157—161(黄文耀,杨新玲,张钟宁.化学通报,2002,3,157—161)
[5] Zhang Z.N.,Liu X.,Mei X.Q.,Animal Bulletin,1993,10,1—3(张钟宁,刘珣,梅雪琴.动物学集刊,1993,10,1—3)
[6] Yan F.M.,Chen J.L.,Tang Q.B.,Plant Protection,2013,39(5),9—15(闫凤鸣,陈巨莲,汤清波.植物保护,2013,39(5),9—15)
[7] Kislow C.J.,Edward L.J.,Nature,1972,235(5333),108—109
[8] BowersW.S.,Nault L.R.,Webb R.E.,Dutky S.R.,Science,1972,175(4026),1121—1122
[9] Edwards L.J.,Siddall J.B.,Dunham L.L.,Uden P.,Kislow C.J.,Nature,1973,241(5385),126—127
[10] Van O.A.M.,Gut J.,Harrewijn P.,Piron P.G.M.,Acta Phytopathol.Entomol.Hung.,1990,25(1—4),331—342
[11] CuiL.L.,Dong J.,Francis F.,Liu Y.J.,Heuskin S.,Lognay G.,Chen J.L.,Bragard C.,Tooker J.F.,Liu Y.,Crop Protection,2012,35,91—96
[12] Nishino C.,BowersW.S.,Montgomery M.E.,Nault L.R.,Appl.Entomol.Zool.,1976,11(4),340—343
[13] Dawson G.W.,Gibson R.W.,Griffiths D.C.,Pickett J.A.,Rice A.D.,Woodcock C.M.,J.Chem.Ecol.,1982,8(11),1377—1388
[14] Li Z.M.,Wang T.S.,Me E.Y.,Chen X.R.,Zhu L.H.,Wang S.H.,Acta Chemical Sinica,1987,45,1124—1128(李正名,王天生,么恩云,陈学仁,朱兰蕙,王素华.化学学报,1987,45,1124—1128)
[15] Zhang Z.N.,Liu X.,Pickett J.,Acta Entomol.Sinica,1988,31(4),435—438(张钟宁,刘珣,Pickett John.昆虫学报,1988,31 (4),435—438)
[16] Sun Y.F.,Li Y.Q.,Ling Y.,Yu H.L.,Yang S.X.,Yang X.L.,Chin.J.Org.Chem.,2011,31(9),1425—1432(孙玉凤,李永强,凌云,宇红莲,杨绍祥,杨新玲.有机化学,2011,31(9),1425—1432)
[17] Qin Y.G.,Qu Y.Y.,Zhang J.P.,Tan X.Q.,Song L.F.,LiW.H.,Song D.L.,Yang X.L.,Chin.J.Org.Chem.,2015,35(2),455—461(秦耀果,曲焱焱,张景朋,谭晓庆,宋丽芳,李文浩,宋敦伦,杨新玲.有机化学,2015,35(2),455—461)
[18] Song B.A.,Jin L.H.,New Heterocyclic Pesticide,Chemical Industry Press,Beijing,2010,118—128(宋宝安,金林红.新杂环农药,北京:化学工业出版社,2010,118—128)
[19] Zhang Y.,Wang B.L.,Zhan Y.Z.,Zhang L.Y.,Li Y.H.,Li Z.M.,Chem.J.Chinese Universities,2016,37(6),1100—1107(张燕,王宝雷,詹益周,张丽媛,李永红.李正名.高等学校化学学报,2016,37(6),1100—1107)
[20] Gao Y.,Wang B.W.,Gao S.,Zhang R.H.,Yang C.Y.,Sun Z.,Liu Z.H.,Chem.Res.Chinese Universities,2016,32(4),594—599
[21] Tian Z.Z.,Zhang D.,Guo B.,Tian G.,Liu X.X.,Yue H.J.,Chem.Res.Chinese Universities,2015,31(2),249—252
[22] Wang H.S.,Huai Q.Y.,Nat.Prod.Res.Dev.,2013,25(2),237—240(王华森,怀其勇.天然产物研究与开发,2013,25(2),237—240)
[23] Wild N.,Groth U.,Eur.J.Org.Chem.,2003,2003(22),4445—4449
[24] PeterW.,John P.M.,Org.Lett.,2008,10(19),4383—4386
[25] Maciej A.,Srinivasa R.A.,Rajarathnam E.R.,Tetrahedron,2002,58(34),6951—6963
[26] Sun L.,Synthesis Process and Structure Optimization of EBF Analogue CAU⁃1204,China Agricultural University,Beijing,2013(孙亮. EBF类似物CAU⁃1204的合成工艺及结构优化研究.北京:中国农业大学,2013)
[27] Ravikumar P.C.,Yao L.H.,Fleming F.F.,J.Org.Chem.,2009,74(19),7294—7299
Design,Synthesis and Biological Activity of Novel Aphid Alarm Pheromone Analogues Containing Isonicotinic Acid†
QIN Yaoguo1,ZHANG Jingpeng1,SONG Dunlun2,DUAN Hongxia1,LING Yun1,JIANG Biaobiao1,WANG Di1,YANG Xinling1∗
(1.Department of Applied Chemistry,College of Science,2.Department of Entomology,College of Plant Protection,China Agricultural University,Beijing 100193,China)
A series of new aphid alarm pheromone[(E)⁃β⁃farnesene,EBF]analogues containing isonicotinic acid was designed based on the principles of connecting sub⁃structure and bioisosterism.With EBF as a lead compound,20 EBF analogueswere prepared via four steps starting from geraniol.Their structures were con⁃firmed by1H NMR,13C NMR,IR and HRMS.The preliminary bioassay suggested that all the analogues showed repellent and aphicidal activities against Myzus persicae(Sulzer).Among them,compounds 7d,8f and
Isonicotinic acid;Aphid alarm pheromone;Analogue;Biological activity
O626
A
10.7503/cjcu20160434
(Ed.:P,H,N,K)
†Supported by the National Natural Science Foundation of China(No.21132003)and the Special Fund for Agro⁃scientific Research in the Public Interest,China(No.201203022).
2016⁃06⁃15.
日期:2016⁃10⁃18.
国家自然科学基金(批准号:21132003)和公益性行业(农业)科研专项(批准号:201203022)资助.
联系人简介:杨新玲,女,博士,教授,博士生导师,主要从事新农药分子设计与创制方面的研究.E⁃mail:yangxl@cau.edu.cn
8n showed good repellent activity with the repellent rate of 62.6%,62.0%and 61.0%respectively;and the analogues 8a,8b and 8d exhibited better aphicidalmortality of 73.6%,81.1%and 70.2%than lead EBF. The primary structure⁃activity relationship(SAR)analysis indicated that introducing of ester group was favora⁃ble to repellent activity while introducing amide was conducive to aphicidal activity.Moreover,N⁃substituted carbon chain length,number of branched chain as well as aromaticity played roles in repellent activity.This study provides useful clues for further development of novel aphid control agent.
