甘精胰岛素联合阿卡波糖对2型糖尿病患者胰岛功能的影响
2016-11-22苏建军林瑞典厦门市第五医院厦门361101
苏建军 林瑞典(厦门市第五医院厦门361101)
甘精胰岛素联合阿卡波糖对2型糖尿病患者胰岛功能的影响
苏建军林瑞典(厦门市第五医院厦门361101)
目的:研究甘精胰岛素联合阿卡波糖对2型糖尿病患者胰岛功能的影响。方法:以我院2014年7月~2015年6月接诊的102例2型糖尿病患者为研究对象,根据数字随机分组的方式分为比较组和实验组;比较组运用阿卡波糖片联合普通胰岛素诊治,实验组在比较组的基础上将普通胰岛素改为甘精胰岛素治疗,对比两组治疗前后各种参数变动情况。结果:治疗前两组参数检测区别不大,差异无统计学意义(P>0.05),治疗后实验组各种参数明显好于比较组,差异具有统计学意义(P<0.05)。讨论:使用甘精胰岛素结合阿卡波糖治疗2型糖尿病效果明显,能有效改善患者的氧化应激功能,提高对胰岛素的敏感性,减少低血糖不良反应,能够在较短时间内有效控制血糖。
甘精胰岛素 阿卡波糖 2型糖尿病
糖尿病是我国较为多见的慢性疾病,发病人群以中老年为主,糖尿病患者早期症状以多饮、多尿、多食、体重减轻为主,糖尿病对人体健康危害极大,严重情况可导致患者早逝。伴随我国人口老龄化程度增加,糖尿病的发病率逐年增长且日益呈现年轻化态势,数据发现,在我国糖尿病患病基数极多,以30岁以上人群为主。90%以上的患者为2型糖尿病[1]。糖尿病主要是对人体大血管和微型血管造成伤害,同时引发一连串的并发症对人体健康造成威胁,由于该病发病机理较为复杂,临床医学目前仍然无法完全阐明,需要进一步从遗传、病理、代谢等多方面进行研究。在临床治疗过程中,以快速把控血糖含量,降低高血糖对靶细胞的伤害,保持胰岛素持续分泌为治疗目的。
甘精胰岛素在中性pH液中溶解度低,是一种全新的人胰岛素类似物,已经广泛运用于1、2型糖尿病治疗。阿卡波糖通过抑制小肠的α葡萄糖苷酶发挥作用,主要是限制食物的多糖分解,控制餐后血糖含量,避免糖尿病患者血糖出现快速波动,一般情况下多为单用。但有相关学者研究发现[2],使用甘精胰岛素联合阿卡波糖治疗2型糖尿病血糖控制极佳,但并没有探究其作用机理。因此,本次研究主要观察甘精胰岛素联合阿卡波糖治疗2型糖尿病的临床疗效,并重点探究对胰岛功能的影响。
1 资料与方法
1.1一般资料:本文以我院2014年7月~2015年6月接诊的102例2型糖尿病患者为研究对象,按照数字随机分组方式分成比较组和实验组,其中男性56例,女性46例,患者年龄31~55岁,平均年龄(34.1±2.1)岁,均符合《中国慢性疾病防治基层医生诊疗手册(糖尿病分册)》临床诊断标准[1]。全部患者排除心脏功能、肾功能、肺部功能问题无其他并发症状,在治疗前分别检测患者空腹、餐后血糖含量和糖化血红蛋白含量;三酰甘油及总胆固醇数值无明显差异,两组一般资料无区别,差异不具有统计学意义(P>0.05)。
1.2治疗方法:两组均进行限制饮食及合理运动治疗。比较组采用常规方法治疗,口服阿卡波糖片,一日三次,每次剂量为50mg,与三餐主食一同服用,且在三餐主食前皮下注射普通胰岛素,每次剂量为0.15U/kg,结合血糖变化情况进行药物用量调整,保持空腹状态下血糖含量为4.4~7.0mmol/L,餐后2h血糖含量控制在8~10mmol/L之间。实验组在比较组的基础上,把皮下注射普通胰岛素更换为皮下注射甘精胰岛素,于患者每天睡前注射一次,每次剂量为0.2U/kg,同时结合血糖变化情况进行药物用量调整。
1.3胰岛功能观察指标估算方法:在治疗前后监测患者空腹状态下胰岛素(FINS)含量与空腹血糖(FBG),通过科学计算方式估算出Homa-IR和Homa-β数据,估算公式参照参考文献[4]。
1.4效果评定:医护人员要在治疗前治疗后,分别记录患者血糖参数变动情况,准确记录平均达标使用时间,并记录患者每天低血糖次数,计算出周低血糖次数和月低血糖次数,并记录好胰岛素使用量,做好平均值计算。另外,要密切观察患者是否出现头晕、呕吐、皮肤瘙痒等不良症状,一旦患者出现不良症状及时做好记录,并及时通报医生进行治疗。
1.5统计学方法:本次研究使用的是全新SPSS18.0软件,计量资料用均数±标准差(±s)表示,组间比较用t检验,数据对比用X2检验,P<0.05表示差异具有统计学意义。
2 结果
2.1两组治疗前后Homa-IR与Homa-β对比:根据检测数据发现,在治疗之前实验组和比较组Homa-IR和Homa-β数据区别不大,而在治疗后实验组Homa-IR要远远低于比较组,Homa-β则明显高于比较组,差异具有统计学意义(P<0.05)。
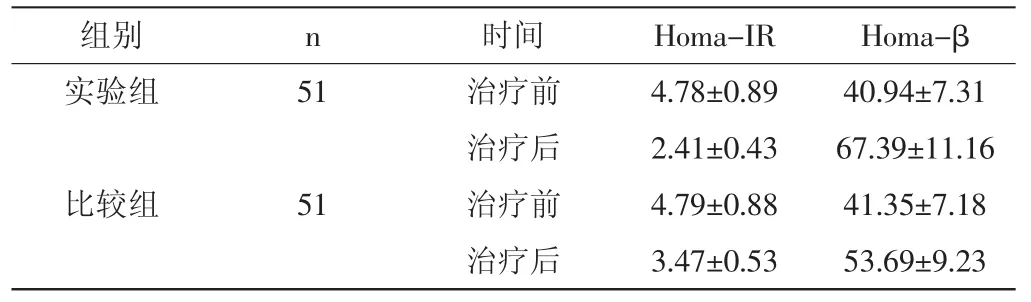
表1 两组Homa-IR与Homa-β治疗前后对比
2.2治疗前后两组血糖把控情况比对:在治疗三个月过程中,实验组血糖达标平均时间(7.11±1.25)d,低血糖平均次数(0.41± 0.10)次,平均胰岛素使用量(19.25±4.33)U/d,比较组血糖平均达标时间(9.31±2.15)d,平均低血糖次数(1.17±0.03)次,平均胰岛素使用量(26.36±6.2)U/d,两组比较差异具有统计学意义(P<0.05)。数据如表2所示:
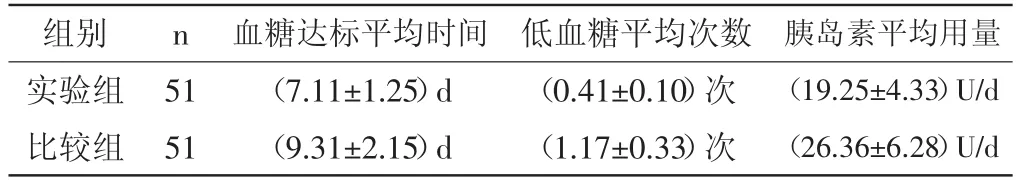
表2 治疗后两组血糖把控情况对比
3 讨论
目前,糖尿病在我国有着极大的基数人群,是临床中较为多见的一种疾病,早期糖尿病患者若得到有效治疗,病情可得到控制,反之则可能造成患者死亡,仅在中国,糖尿病患病人数约为1030万,每年约有100万人死亡,主要原因是病情恶化,同时引发并发症。更令人担忧的是,这种死亡年龄正逐渐趋向年轻化。胰岛素分泌障碍是引发高血糖2型糖尿病的主要原因,阿卡波糖是一种全新的口服降血糖药物,作用机理是利用a-糖苷酶抑制剂,减缓肠胃对葡萄糖吸收转化,起到饭后降血糖和降血浆胰岛浓度的效果。甘精胰岛素是借助基因重组技术生产的新型人胰岛素药物,通过皮下注射24h后可释放出胰岛素,从而有效把控血糖含量,使血糖含量处于正常区间。一般情况下,餐后血糖含量会有所增高,仅仅使用阿卡波糖并不能起到降血糖效果,若为了避免饭后血糖含量升高而使用甘精胰岛素,又可能引发低血糖,所以在临床治疗中应联合使用。通过研究数据发现[5],实验组每日胰岛素平均用量明显少于比较组,低血糖发生次数明显少于比较组,表明阿卡波糖与甘精胰岛素联合使用安全可靠。相关研究发现[6],氧化应激素是造成胰岛素抵抗和胰岛素细胞死亡的重要原因。相关学者研究还发现,高血糖是造成炎性IL-6分泌的直接原因,进而造成氧化应激情况发生,氧化应激的出现造成胰岛功能受损。本次研究数据结果显示,实验组血糖达标时间明显少于比较组,对血糖达标时间的控制可有效改善氧化应激失衡,与相关学者结论相符。需要说明的是,两组治疗过程当中,都没有出现头晕目眩、呕吐、皮肤瘙痒等不良反应。过去数年研究发现,通过降低人体血糖,改善早期胰岛素β细胞的分泌情况,维护胰岛素β的主要功能,是治疗糖尿病的主要方法。过去对糖尿病的治疗仍然以控制血糖为主,然而现在研究已经表明[7],在单纯降糖治疗的基础上进行胰岛素β细胞功能的维护可有效降低糖尿病并发症的发生率。而在2型糖尿病的早期阶段,胰岛素β细胞受损是可以避免的,细胞处在葡萄糖失去敏锐性过程中,要严格控制血糖保护胰岛素β细胞,使其功能尽快得到恢复,进而规避糖尿病并发症。
Homa-IR特指靶细胞对胰岛素抵抗程度,值越大表明抵抗能力越强,而Homa-β评估胰岛β细胞的功能性,值越大表明功能越强。在治疗前两组Homa-IR和Homa-β数据区别不大,而在治疗后两组Homa-IR和Homa-β数据差异具有统计学意义(P<0.05)。在治疗三个月过程中,根据统计数据发现,比较组血糖平均达标时间为(9.31±2.15)d,平均低血糖次数为(1.17± 0.03)次,平均胰岛素使用量为(26.36±6.2)U/d,实验组血糖平均达标时间为(7.11±1.25)d,低血糖平均次数为(0.41±0.10)次,平均胰岛素使用量为(19.25±4.33)U/d,两组比较差异具有统计学意义(P<0.05)。本次研究发现,实验组在减少2型糖尿病患者Homa-IR增长和Homa-β方面要明显好于比较组,与相关学术观点一致,表明实验组可提升患者对胰岛素的敏锐性,进而改善胰岛细胞功能。
综合而言,本次研究数据结果表明,甘精胰岛素联合阿卡波糖能有效改善2型糖尿病患者氧化应激情况,提升患者对胰岛素的敏锐性,提高胰岛功能,低血糖症出现次数少,能在短时间内安全有效控制患者血糖含量,能够有效改善糖尿病患者生存环境,对延长患者生存时间意义重大。
[1]纪立农,陈莉明,郭晓蕙,等.中国慢性疾病防治基层医生诊疗手册(糖尿病分册)2015年版[J].中国糖尿病杂志,2015,07(8):12-13
[2]王筱景,阮凌燕,周小爱.甘精胰岛素联用阿卡波糖治疗老年糖尿病患者的临床疗效及安全性评价[J].中国临床药理学杂志,2014,11(10):225-226.
[3]王敏.阿卡波糖联合诺和锐30治疗2型糖尿病血糖控制欠佳患者的疗效观察[J].现代药物与临床,2014,7(8):23-25.
[4]戴红,赵跃萍,于津,等.阿卡波糖对糖耐量减低患者血清C-反应蛋白和血脂水平的影响[J].解放军医药杂志,2014,1(1):88-89.
[5]杨青,高宁,刘芳芳,等.阿卡波糖对2型糖尿病患者血清nesfatin-1水平及糖脂代谢的影响[J].山东大学学报(医学版),2013,4(5):99-100.
[6]王平,祝开思.动态监测甘精胰岛素与预混胰岛素治疗期间老年2型糖尿病患者血糖漂移和低血糖发生率[J].中国糖尿病杂志,2010,1(2):8-9.
[7]李凡.甘精胰岛素合用口服降糖药治疗老年2型糖尿病的疗效分析[J].中国现代药物应用,2016,5(4):23-25.
R 587.1
B
1672-8351(2016)11-0019-02
