胆宁片预防性治疗复发性高甘油三脂血症性胰腺炎合并脂肪肝22例临床分析
2016-11-19盛潇磊袁睿蔺汝云
盛潇磊 袁睿 蔺汝云
摘要:目的近年来高脂血症性急性胰腺炎(HLAP)的发病率明显升高,其特征之一是复发率极高。该研究拟通过口服胆宁片观察对HLAP的影响。方法2010年1月—201.4年9月笔者所在医院的复发性高脂血症性胰腺炎住院患者共45例,予以胆宁片口服,随访观察患者有无复发高脂血症性胰腺炎,血清甘油三酯水平变化,血清谷丙转氨酶、谷草转氨酶,以及脂肪肝影像学评分变化。结果胆宁片显著地减低了患者血清甘油三酯的水平,降低了肝酶学指标,大大改善了脂肪肝的B超评分,也明显减少了复发性高脂血症性胰腺炎的复发率。结论胆宁片对于预防性治疗高脂血症性胰腺炎疗效肯定有效,值得进一步研究推广。
关键词:高脂血症性胰腺炎;胆宁片;甘油三酯
中图分类号:R576文献标志码:B文章编号:1007-2349(201.6)04-0085-03
近些年来,随着人们生活水平的提高及饮食结构的改变,高脂血症性急性胰腺炎(hyperlipidemic acute pancreatitis,HLAP)的发病率明显升高,高脂血症(hyperlipidemia,HL)特别是高甘油三酯血症(hypertriglyceridemia,HTG)已成为除胆源性及酒精性因素外AP发病的重要病因[1]。
HLAP发病机制仍不十分清楚,目前认可的主要有:HTG使胰腺血液处于高凝状态导致血栓形成,血清脂质颗粒聚集堵塞胰腺微血管导致胰腺微循环障碍;胰腺及胰周高浓度甘油三酯(triglyceride,TG)被水解成游离脂肪酸(free fatty acid,FFA),诱发酸中毒,激活胰蛋白酶酶原,加重胰腺自身消化,形成恶性循环;FFA对胰腺腺泡及毛细血管内皮细胞产生直接细胞毒性作用,通过炎症介质及细胞因子等生物学作用加重胰腺缺血及坏死[2,3]。而在AP动物模型实验中也证实FFA及TG可导致胰腺水肿及缺血[4,5]。
考虑到HLAP与高血脂的相关性,且易于复发,临床预后不佳。而胆宁片临床上明确可以降血脂、而且可以护肝、护胰。本研究拟通过胆宁片的口服治疗,观察对于复发性HLAP的疗效,对血清甘油三酯的浓度、脂肪肝的疗效,希望为复发性HLAP的预防提供一种新的临床治疗选择。
1资料与方法
1.1一般资料患者选自本院2010年1月—201.4年9月复发性高脂血症性胰腺炎患者,平均为住院期间证实存在脂肪肝,共45例。其中男31例,平均年龄(4943±1.689)岁;女1.4例,平均年龄(55.10±1.798)岁。起病时血清甘油三酯(1.822±673)mmol/L,按照CT评分分级标准及201.2亚特兰大最新诊断标准均为非重症胰腺炎(NSAP)[6]。
1.2治疗方法
1.2.1研究方法所有患者入院后根据“中国急性胰腺炎诊治指南”接受规范治疗[7];包括严格禁食,必要的胃肠减压,早期体液复苏,肠外营养,质子泵抑制剂(proton pump inhibitor,PPI)抑制胃酸分泌,抗生素,胰液胰酶抑制剂抑制胰液分泌和胰酶活性,必要早期肠内营养。患者平均住院时间为(101.1± 626)d,出院时血清甘油三脂为391±075mmol/L,复查CT或是B超均未见胰腺假性囊肿、脓肿等并发症。所有出院患者均要求低脂饮食,门诊随访。随访患者分2组:A组:胆宁治疗组23例,其中男1.6例,女7例,患者出院后予以胆宁片4片,tid,口服3月;B组:空白对照组22例,其中男1.5例,女6例。随访半年,观察患者有无复发高脂血症性胰腺炎,血清甘油三酯水平变化,血清谷丙转氨酶、谷草转氨酶,以及脂肪肝影像学评分的在胆宁片治疗前后的变化。
1.2.2统计学处理方法采用SPSS1.20统计软件,计量数据用均数±标准差[HTSS](x[TX-3/8]±s)表示,组间比较t检验,治疗前后使用配对t检测,P<005为差异有统计学意义。
2结果
2.1胆宁片对预防复发性HLAP的疗效胆宁治疗组患者随访半年仅有2例(870%)发作一次HLAP,再次入院治疗;而空白对照组患者共有8例再次发作HLAP入院,平均发生HLAP为(1.50±076)次,胆宁片可以明显减低复发性HLAP的发生率(P<005)。
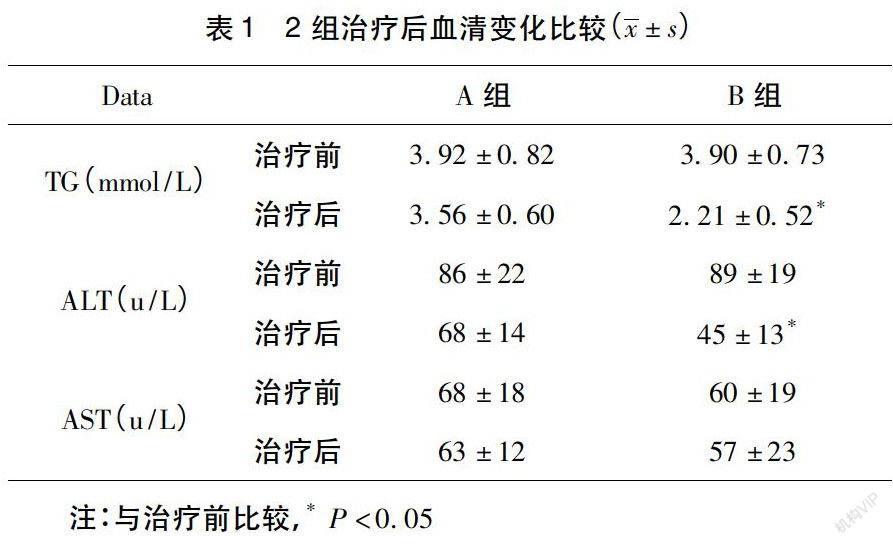
2.2.2组治疗后血清变化比较见表1。
2.3胆宁片对脂肪肝影像学评分变化脂肪肝按照轻中重度的分级,分别记为1、2、3分。胆宁片治疗组的评分分别为(1.8±03),降为(08±03),效果显著,差异具有统计学意义(P<005)。而空白对照组的评分为(1.7±05),随访终点时为(1.5±04),差异无统计学意义(P>005)。
3讨论
HLAP临床主要表现为无其他原因的血清高TG >1000mg/dL(1.1.3mmol/L)或乳糜血伴血清甘油三酯>500 mg/dL(565mmol/L)[7],血及尿淀粉酶升高可不明显,常合并脂肪肝、糖尿病、肥胖等,易复发;大多数人认为HLAP的结局与NHLAP无差别[8],但HL是否加重AP病情仍然存在争议。Balachandra等[9]在研究43例AP患者病因分析中得出HTG与重症急性胰腺炎(severe acute pancreatitis,SAP)(APACHE II score ≥8分)的病情及并发症无明显相关性。相反的,Lloret Linares等[10]研究证实HLAP患者病情的严重程度(需要重症监护,CRP>1.50mg/L,或Balthazar CT分级大于C级)高于NHLAP患者,但是疾病的严重程度与血清TG水平没有明显关系。Baranyai 等[11]研究证实相比于NHLAP,HLAP病情更为严重,更易发生坏死,败血症等并发症,住院天数明显延长。相关动物模型实验[12]的组织学结果也提示HTG可加重AP的病程。总结以上实验结果提示相比于NHLAP,HLAP病情要更为严重,治疗上更为困难[13]。因此,临床上对于 HLAP的预防与诊治显得尤为重要。
中药治疗急性胰腺炎已经有大量的临床研究数据证实其疗效确切,其具有通里攻下,消痞除满之功效,同时还具有清热解毒、活血凉血等功用。在急性胰腺炎的早期病程中可以排除胃肠积滞,清除肠道内的细菌和内毒素,保护肠道的机械和免疫屏障,减轻SIRS,减少MODS发生。“胆宁片”由大黄、虎杖、青皮、白茅根、陈皮、郁金、山楂等组成,起到疏肝利胆,清热通下的功用。方中大黄有通下的作用,虎杖、青皮、白茅根、陈皮、郁金清热泻火,诸药合用共奏疏肝泻火通便之效。2007年Liu[14]曾经通过高效液谱仪(HPLC)偶联电喷雾串联质谱等方法对胆宁片的有效成分进行了分析,发现8种高效生物活性物质,分别为:橙皮素、金丝桃苷、白藜芦醇、川陈皮素、姜黄素、大黄素、大黄酚、大黄素甲醚。
临床上对于慢性胆囊炎胆囊结石、便秘、脂肪肝、高脂血症等疗效较为显著。2004年Fan[15]采用胆宁片治疗232例非酒精性脂肪肝的多中心临床研究发现,临床短疗程胆宁片治疗非酒精性脂肪肝疗效明确,对于血脂、ALT水平、血脂水平、脂肪肝有效率为858%、782%、396%及34%的缓解率;2005年的一项多中心随机双盲实验发现[16],相对于熊去氧胆酸的对照组而言,胆宁片对于非酒精性脂肪肝疗效更为明确,可以缓解乏力、纳差、肝功能、血脂及肝组织学病变;201.2年Ding[17]通过建立淤胆性肝损伤的大鼠模型,研究发现胆宁片具有显著的剂量依赖性的护肝效应,推测其中的机制是减轻了肝内中性粒细胞浸润及氧化应激。201.4年Ding[18]进一步实验研究发现,胆宁片能够显著减弱多重耐药相关蛋白2(Mrp2)的有效胞内移位,上调肝内代谢酶的mRNA 及蛋白的表达,如细胞色素P450 2b1(Cyp2b1)、尿苷二磷酸葡糖醛酸转移酶1A1(Ugt1a1))、胆盐转运因子(Bsep)等,结论指出胆宁片能够通过调节肝内代谢酶及转运因子的表达从而促进了胆盐及胆色素的排泄。
结合上述研究,笔者推测通过胆宁片可以降低复发性高脂血症性胰腺炎患者的血脂水平,改善脂肪肝脂肪胰腺的组织学病变程度,从而以减低复发性高脂血症性胰腺炎的复发率。临床实验结果证实了笔者的推论,相对于空白对照组而言,胆宁片治疗组不但显著地减低了血清甘油三酯的水平,降低了肝酶学指标,大大改善了脂肪肝的B超评分,3月的短程胆宁片的口服治疗也明显减少了复发性高脂血症性胰腺炎的复发率,疗效明显。当然,该研究病例数较少,有待进一步深入的基础实验及临床研究来证实及推广。[HJ22mm]
参考文献:
[1]YIN G,HU G,CANG X,et alC-reactive protein:rethinking its role in evaluating the severity of hyperlipidemic acute pancreatitis[J]Pancreas,201.4,43(8):1.323-8
[2]HAVEL R JPathogenesis,differentiation and management of hypertriglyceridemia[J]Adv Intern Med,1.969,1.5(1.1.7):54
[3]GAN S I,EDWARDS A L,SYMONDS C J,et alHypertriglyceridemia-induced pancreatitis:A case-based review[J]World J Gastroenterol,2006,1.2(44):71.97-202
[4]SAHARIA P,MARGOLIS S,ZUIDEMA G D,et alAcute pancreatitis with hyperlipemia:studies with an isolated perfused canine pancreas[J]Surgery,1.977,82(1):60-7
[5]KIMURA W,MOSSNER JRole of hypertriglyceridemia in the pathogenesis of experimental acute pancreatitis in rats[J]Int J Pancreatol,1.996,20(3):1.77-84
[6]BANKS P A,BOLLEN T L,DERVENIS C,et alClassification of acute pancreatitis-201.2:revision of the Atlanta classification and definitions by international consensus[J]Gut,201.3,62(1):102-1.1
[7]WANG X P,LI Z S,YUAN Y Z,et alChinese guidelines for daignosis and treatment of acute pancreatitis(201.3,Shanghai)[J]Chinese Journal of Pancreatology,201.3,1.3(2):73-8
[8]FORTSON M R,FREEDMAN S N,WEBSTER P D,3RDClinical assessment of hyperlipidemic pancreatitis[J]Am J Gastroenterol,1.995,90(1.2):21.34-9
[9]BALACHANDRA S,VIRLOS I T,KING N K,et alHyperlipidaemia and outcome in acute pancreatitis[J]Int J Clin Pract,2006,60(2):1.56-9
[FL)][HJ23mm][SD1,1][FQ(1.93/4。1.75mm,X,DY-W][SQ+1mm][CD=1.75mm][FL(K8mm]
[10]LLORET LINARES C,PELLETIER A L,CZERNICHOW S,et alAcute pancreatitis in a cohort of 1.29 patients referred for severe hypertriglyceridemia[J]Pancreas,2008,37(1):1.3-8
[11]BARANYAI T,TERZIN V,VAJDA A,et alHypertriglyceridemia causes more severe course of acute pancreatitis[J]Clin Lipidol,201.2,7(6):731-6
[12]HOFBAUER B,FRIESS H,WEBER A,et alHyperlipaemia intensifies the course of acute oedematous and acute necrotising pancreatitis in the rat[J]Gut,1.996,38(5):753-8
[13]EWALD N,HARDT P D,KLOER H USevere hypertriglyceridemia and pancreatitis:presentation and management[J]Curr Opin Lipidol,2009,20(6):497-504
[14]LIU R,ZHANG J,LIANG M,et alSimultaneous analysis of eight bioactive compounds in Danning tablet by HPLC-ESI-MS and HPLC-UV[J]J Pharm Biomed Anal,2007,43(3):1007-1.2
[15]FAN J G,SHANGHAI MULTICENTER CLINICAL COOPERATIVEGROUP OF DANNING PIAN TEvaluating the efficacy and safety of Danning Pian in the short-term treatment of patients with non-alcoholic fatty liver disease:a multicenter clinical trial[J]Hepatobiliary Pancreat Dis Int,2004,3(3):375-80
[16]JI G,FAN J G,CHEN J J[Clinical study on treatment of non-alcoholic fatty liver of damp-heat syndrome type by danning tablet][J]Zhongguo Zhong Xi Yi Jie He Za Zhi,2005,25(6):485-8
[17]DING L L,ZHANG B F,DOU W,et alProtective effect of Danning tablet on acute livery injury with cholestasis induced by alpha-naphthylisothiocyanate in rats[J]J Ethnopharmacol,201.2,1.40(2):222-9
[18]DING L,ZHANG B,ZHAN C,et alDanning tablets attenuates alpha-naphthylisothiocyanate-induced cholestasis by modulating the expression of transporters and metabolic enzymes[J]BMC Complement Altern Med,201.4,1.4(2):49
