纳米混悬剂中稳定剂的研究进展*
2016-11-19毛坤军王雪婷黄道明叶颖俊
黄 平,毛坤军,王雪婷,黄道明,叶颖俊
(1 江西医学高等专科学校药学系,江西 上饶 334000; 2 上饶市食品药品检验所,江西 上饶 334000)
纳米混悬剂中稳定剂的研究进展*
黄 平1,毛坤军1,王雪婷1,黄道明2,叶颖俊1
(1 江西医学高等专科学校药学系,江西 上饶 334000; 2 上饶市食品药品检验所,江西 上饶 334000)
纳米混悬剂作为一种新的制剂技术,在提高难溶性药物的溶出度和生物利用度等方面发挥了重要作用。本文对纳米混悬剂的物理稳定性问题、稳定剂的种类、作用机理等方面进行了综述,这为选择合适的稳定剂,制备稳定性好、生物利用度高的纳米混悬剂提供了参考价值。纳米混悬剂的物理稳定性研究是一个复杂且艰辛的过程,相信在不久的将来,随着微粒稳定理论研究的深入和稳定剂高通量筛选方法的建立,纳米混悬剂的物理稳定性的难题一定能够迎刃而解。
纳米混悬剂;物理稳定性;稳定剂;难溶性药物
纳米混悬剂(nanosuspension,NS)通常是指纯药物以晶态或无定形形式,在稳定剂的稳定下分散在液体中的亚微米胶体分散体系[1]。纳米混悬剂可解决多数难溶性药物的溶解度和溶出度问题,提高药物的生物利用度,降低药物的毒副作用,特别适用于生物药剂学分类系统第Ⅱ类和第Ⅳ类药物。由于中药有效成分或部位给药剂量相对较大,与其他新型药物传递技术如脂质体、环糊精包合物、固体分散体等相比,纳米混悬剂具有更高的载药量,更适合作为改善难溶性中药成分的溶解度和生物利用度的新型给药系统。该制剂既可以作为最终剂型应用,也可以作为一种中间剂型,进一步加工成口服制剂、注射剂以及适合其他给药途径(经皮[2]、眼部[3]、鼻腔[4]等)的最终制剂。近些年来,有关纳米药物晶体的研究得到了国内外药学工作者的广泛关注,并取得了令人瞩目的成就,至今FDA已批准多个产品上市(表1)[5]。药物的纳米混悬剂很不稳定,这这往往限制了纳米混悬剂的发展和应用。因此,制备过程中需加入一定量合适的稳定剂,避免纳米混悬剂不稳定现象的发生。
1 纳米混悬剂稳定性存在的问题
1.1 沉降
纳米混悬剂由药物、分散介质(通常为水)和稳定剂组成。微粒在分散介质中的沉降速度可用Stokes公式来描述:
V=2r2(ρ1-ρ2) g/(9η)
由Stokes公式可知降低混悬剂沉降速度主要方法是:减小微粒半径;减小固体微粒与分散介质间的密度差;增加分散介质的黏度。第一种方法可以通过制备出细小粒径的微粒而实现。后两种方法则需通过向混悬剂中加入适当稳定剂加以实现。
1.2 聚集
纳米粒的粒径小,布朗运动强烈,微粒在介质中保持聚集稳定性的主要作用是,静电排斥作用和空间稳定作用。这两种作用可以通过加入离子或非离子稳定剂来实现。

表1 目前已上市的产品
1.3 晶体生长
纳米混悬剂中的药物微粒大小不一,在静置时,微粒的粒径大小和分布将不断变化,这一规律可用Ostwald-Freundlich方程进行描述:
log(S2/S1)=2σM(1/r2-1/r1)/ρRT
由此可知,若r2
1.4 晶形转化
药物之间的晶型不同,其理化性质会有所不同。在某些条件下,药物晶型之间可以发生转化。药物的稳定性、溶出度和生物利用度,以及其安全性和有效性都会受到晶型的影响。纳米混悬剂主要是无定型态和结晶态之间的转化,稳定剂将会影响其转化。
2 稳定剂种类
在纳米混悬剂制备和储存过程中为避免颗粒聚集和沉降,稳定剂是必不可少的。稳定剂分为传统稳定剂和新型稳定剂。
2.1 传统稳定剂
传统稳定剂包括聚合物、离子型表面活性剂和非离子型表面活性剂。聚合物包括聚维酮、羟丙基甲基纤维素、羟丙基纤维素、TPGS、聚乙二醇、聚乙烯醇、微晶纤维素等。离子型表面活性剂包括十二烷基硫酸钠、硫酸月桂酯钠(SLS)、poly(ethylene imine) (PEI)、壳聚糖等。非离子表面活性剂包括吐温、泊洛沙姆、PEO-PPO-PEO等。
2.2 新型稳定剂
新型稳定剂主要有食物蛋白、水溶性糖类和黏土。食物蛋白相对于传统稳定剂更安全,常用食物蛋白有大豆蛋白(SPI)、乳清蛋白(WPI)、β-乳球蛋白(β-lg)。食物蛋白变性后具有更好的稳定效果[6]。水溶性糖类主要包括甘露醇、乳糖和海藻糖,在固化过程中能有效抑制药物纳米粒的聚集。黏土主要使用蒙脱土(montmorillonite),其具有较好的吸附性和流变学性质并且能控制药物的释放。Dong等[7]研究表明以蒙脱土为稳定剂能够有效抑制非洛贝特纳米粒聚集,固化后纳米粒仍然具有较高的溶出度。
3 稳定剂作用原理
不同稳定剂具有不同的作用原理,离子型稳定剂通过静电排斥稳定纳米混悬剂,非离子型稳定剂通过空间阻力稳定混悬剂。
3.1 静电排斥作用
在以水为介质的纳米混悬液中,微粒间的作用力可以用经典的DLVO(Derjaguin-Landau-Verwey-Overbeek)理论来加以描述。DLVO理论认为,在介质中,微粒间的作用力可分为静电斥力和范德华力。稳定剂吸附在纳米混悬剂颗粒的表面,部分吸附的分子链继续热运动通过排斥力阻碍纳米粒子聚集。当吸附完全时,形成氢键和静电作用,进一步稳定纳米混悬剂。Heather等[8]考察了多种离子盐对纳米混悬剂Zeta电位的影响,得出结论,对于溶解度大于10 μmol/L或logP小于3.5的阳离子,由于其不能有效吸附到聚合物微粒表面,因此不能给予纳米微粒表面足够的电荷。当只有静电排斥作用的情况下,纳米混悬剂的双电层切平面处的电位(ζ)绝对值大于30 mV才能维持其稳定。
3.2 空间稳定作用
作为稳定剂,既要和混悬剂中的微粒有很强的亲和力,以便能牢固地吸附在微粒表面上;又要与溶剂有良好的亲合性,以便形成厚的吸附层,从空间上阻碍微粒的相互接近,保护微粒不聚集。
一般来说,相对分子质量越大,稳定剂在微粒表面上形成的吸附层越厚,稳定效果越好。高分子浓度的影响比较复杂,吸附的高分子要能盖住微粒表面才能起到稳定、保护作用,但更多的高分子却不能增加其稳定作用;在优良溶剂中,和不良溶剂中,高分子的稳定作用差异很大[9]。
非离子型表面活性剂通过吸附在药物颗粒表面,使颗粒之间产生空间位阻,从而促进立体稳定性。同时,其亲水部分延伸到大量的分散介质中,形成较厚的水化膜,增强空间稳定作用。
Deng等[10]研究了Pluronic F127对紫杉醇纳米混悬液的稳定作用机制。通过解吸附实验表明,不同浓度时的稳定剂对药物晶体的吸附能力不一样。当稳定剂的浓度低于临界胶束浓度(CMC)时,其与纳米晶体表面具有较高的亲和力;当其浓度高于CMC时,其与药物晶体的亲和力下降,引起制剂不稳定。
4 稳定剂选择
为了克服纳米粒间的相互吸引力及减少微粒相互之间碰撞的机会,需要在微粒间增加排斥力,通常使用适量的稳定剂来达到抑制纳米微粒的成长速率。一般可选择离子型和非离子型表面活性剂,离子型表面活性剂可使纳米微粒间产生静电排斥;非离子型表面活性剂则使纳米微粒间产生立体排斥。研究显示,合用两种类型表面活性剂可以使制剂具有更好的长期稳定性[11]。
Lee等[12]考察了稳定剂对不同难溶性药物纳米混悬剂的稳定作用,实验结果表明,稳定剂和药物具有相似的高分子量、低溶解度、高熔点、高表面能易成功制备纳米混悬剂。Verma等[13]利用原子显微镜(AFM)观察聚合物吸附在药物表面的形态学特征,以此方法来选择制备稳定纳米混悬剂合适的稳定剂。Maya等[14]考察6种不同性质的药物(分子量、熔点、溶解度、油水分配系数、酸电离常数、焓、形态)和2种稳定剂(离子型、非离子型)对形成纳米混悬剂稳定性的影响,研究表明,具有较高焓和疏水性的药物最易形成稳定的纳米混悬剂(图1),同时为不同性质的药物选择合适稳定剂提高参考依据。

图1 根据药物性质选择稳定剂
Yue等[15]用10种稳定剂在3种浓度条件下与8种药物作用,采用高压均质法制备纳米混悬剂,考察稳定剂的黏度和浓度对纳米混悬剂的形成过程的影响。研究发现,低粘度稳定剂(如TW80、P188、TPGS等)在纳米分散过程中稳定作用比高粘度稳定剂(如HPMC、PVPK30、MC等)好,但在固化过程中较高粘度稳定剂差。增加稳定剂浓度,纳米分散、固化过程稳定效果都有所增加。在纳米分散与固化过程中,高浓度TPGS稳定效果最好。如图2所示,对于具有较高的内聚能(>30 kJ/g)和润湿常数(> 0.15)的药物,可以选取任何表面活性剂和聚合物;对于具有较高润湿常数(> 0.15)和较低内聚能(> 30 kJ/g)的药物,可以选取高粘度的表面活性剂;对于具有较低内聚能(< 25 kJ/g)和润湿常数(< 0.05)的药物,难以找到合适的稳定剂制成稳定的纳米混悬剂。目前主要通过“trial and error”方法选择稳定剂[14],关于稳定剂如何选择的研究较少,这些研究为稳定剂的选择提供了一定的参考价值。
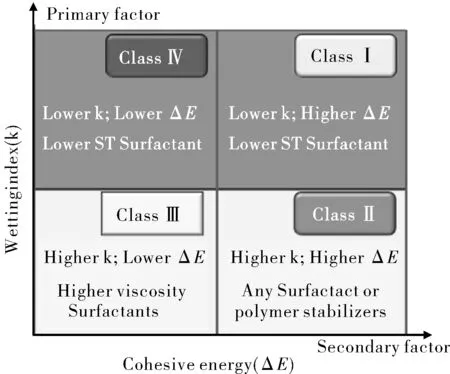
图2 根据药物和稳定剂性质制定纳米混悬剂设计策略
5 结 论
随着纳米混悬剂制剂技术在研究、应用及产业化方面的不断推进和深入,纳米混悬剂将一直是一个研究重点,但物理稳定性问题是其瓶颈。影响其物理稳定性的因素一般有剂型、分散介质、给药途径、生产技术和药物自身性质等。加入合适的稳定剂是解决纳米混悬剂物理稳定最常见的方法,但稳定剂的选择是一个艰辛且很复杂的过程。缺乏对纳米混悬剂内在分子间相互作用基础的理论研究;稳定剂筛选过程复杂且会出现无效筛选的现象。
目前稳定剂的筛选工作主要包括稳定剂的单独使用和联合使用两种,此过程需筛选大量有效候选稳定剂,难度较高。故深入了解药物纳米粒间的作用机制并掌握高通量筛选技术将有利于稳定剂的高效筛选。本文通过讨论纳米混悬剂的物理稳定性问题、稳定剂的种类、作用机理和选择,为制备稳定性好、生物利用度高的纳米混悬剂的研究提供参考。
[1] Sahilhusen I J, Alpesh D P, Mukesh R P. Recent Survey on Nanosuspension: A Patent Overview[J]. Recent patents on drug delivery & formulation, 2015, 9(1): 432-441.
[2] Hill A, Geiβler S, Meyring M, et al. In vitro-in vivo evaluation of nanosuspension release from subcutaneously implantable osmotic pumps[J]. Int J Pharm, 2013, 415(1-2): 57-66.
[3] Khan M S, Vishakante G D, Bathool A. Development and characterization of pilocarpine loaded Eudragit nanosuspensions for ocular drugdelivery[J]. J Biomed Nanotechnol, 2013, 9(1): 124-31.
[4] Bhavna M S, Ali R, Bhatnagar A, et al. Donepezil nanosuspension intended for nose to brain targeting: In vitro and in vivo safety evaluation[J]. Int J Biol Macromol, 2014, 67: 418-25.[5] Chin W W L, Parmentier J, Widzinski M, et al. A brief literature and patent review of nanosuspensions to a final drugproduct[J]. J Pharm Sci, 2014, 103: 2980-2999.
[6] He W, Lu Y, Qi J P, et al. Food proteins as novel nanosuspension stabilizers for poorly water-soluble drugs[J]. Int J Pharm, 2013, 441:269-278.
[7] Dong Y C, Ng W K, Hu J, et al. Clay as a matrix former for spray drying of drug nanosuspensions[J]. Int J Pharm, 2014, 465: 83-89.
[8] Owen H, Graham S, Werling J O, et al. Anion effects on electrostatic charging of sterically stabilized, water insoluble drug particles[J]. Int J Pharm, 2009, 368 (1-2): 154-159.
[9] 谢向阳, 陈晨, 廖祥茹, 等. 纳米混悬剂的物理稳定性研究进展[J]. 国际药学研究杂志, 2011, 38(5):369-374.
[10]Deng Z, Xu S, Li S. Understanding a relaxation behavior in a nanoparticle suspension for drug delivery applications[J]. Int J Pharm, 2008, 351: 236-243.
[11]Vijay A, Meenakshi B. Stability Issues Related to Nanosuspensions: A Review. Pharmaceutical Nanotechnology[J]. 2013, 1(2): 104-113.
[12]Lee J, Choi J Y, Park C H. Characteristics of polymers enabling nano-communiotion of water-insoluble drugs[J]. Int J Pharm, 2008, 355: 28-336.
[13]Verma S, Huey B D, Burgess D J. Scanning probe microscopy method for nanosuspension stabilizer selection[J]. Langmuir, 2009, 25: 12481-12487.
[14]George M, Ghosh I. Identifying the correlation between drug/stabilizer properties and critical quality attributes (CQAs) of nanosuspension formulation prepared by wet media milling technology[J]. Eur J Pharm Sci, 2013, 48: 142-152.
[15]Yue P F, Li Y, Wan J, et al. Study on formability of solid nanosuspensions during nanodispersion and solidification: I. Novel role of stabilizer/drug property[J]. Int J Pharm, 2013, 454: 269-277.
Research Progress on Stabilizers Nanosuspensions*
HUANGPing1,MAOKun-jun1,WANGXue-ting1,HUANGDao-ming2,YEYing-jun1
(1 Department of Pharmacy, Jiangxi Medicine College, Jiangxi Shangrao 334000; 2 Food and Drug Inspection of Shangrao, Jiangxi Shangrao 334000, China)
As a new preparation technique, nanosuspensions play an important role on improving the dissolution and bioavailability of poorly soluble drug. The research progress on physical stability of nanosuspensions, the types of stabilizers and the mechanism of action were discussed, which could provide reference value for selecting the appropriate stabilizers to prepare nanosuspensions with good stability and high bioavailability. The physical stability of nanosuspensions is a complex and difficult process, but in the near future, with the deepening of the particle stability theory research and the establishment of the stabilizer high-throughput screening method, the physical stability of nanosuspensions will be solved.
nanosuspension; physical stability; stabilizer; poorly soluble drug
上饶市科技局科技指导计划项目(20162CZD12)。
黄平(1988-),女,讲师,主要从事药物新剂型研究。
叶颖俊(1973),男,副教授,从事药学、药理方面的研究。
R944.9
A
1001-9677(2016)020-0007-04
