原癌基因C-met在食管鳞癌中的表达与预后相关性研究①
2016-11-18朱晓峰张浩业窦鹏挥邹志田
朱晓峰,张浩业,乔 峰,窦鹏挥,邹志田
(佳木斯大学附属第一医院胸外科,黑龙江 佳木斯 154003)
原癌基因C-met在食管鳞癌中的表达与预后相关性研究①
朱晓峰,张浩业,乔 峰,窦鹏挥,邹志田
(佳木斯大学附属第一医院胸外科,黑龙江 佳木斯 154003)
目的:探讨C-met基因mRNA阳性表达与食管鳞癌复发、转移及预后的相关性。方法:应用RT-PCR技术检测50例食管鳞癌组织和20例癌旁正常食管组织中C-met mRNA的表达情况,统计学分析C-met mRNA表达与临床病理资料、复发转移及预后的相关性。结果:C-met mRNA在食管鳞癌组织中阳性表达率明显高于癌旁正常食管组织(P<0.01);C-met mRNA阳性表达率与癌组织浸润深度(P<0.05)、淋巴结转移(P<0.01)和TNM(P<0.01)分期有关,而与患者年龄、性别、病变长度和癌组织分化程度无关;C-met mRNA阳性表达者与阴性表达者在术后5年内发生复发、转移的例数分别为16例(59.3%)和5例(21.7%),差异有统计学意义(P<0.01);C-met mRNA阳性表达者的5年生存率为25.9%,明显低于阴性表达者的60.9%(P<0.01);COX回归多因素分析提示C-met mRNA阳性表达是影响食管鳞癌患者预后的独立危险因素(HR=6.026,P=0.005)。结论:C-met mRNA的检测对判断食管鳞癌的复发、转移及预后有重要临床意义。
食管;鳞状细胞癌;逆转录-聚合酶链反应;C-met基因;预后
食管癌是我国最常见的恶性肿瘤之一,手术目前是其主要的治疗方法,然而即使临床分期较低的食管癌患者,手术后仍然有20%~30%的复发率,这提示食管癌患者的预后在很大程度上取决于其内在的生物学行为,尤其是基因表达失调对于肿瘤本身的生长、增殖以及侵袭、转移起着至关重要的作用。C-met是一种由C-met原癌基因编码的蛋白产物,为肝细胞生长因子受体,具有酪氨酸激酶活性,与多种癌基因产物和调节蛋白相关,参与细胞信息传导、细胞骨架重排的调控,是细胞增殖、分化和运动的重要因素。目前研究表明[1],C-met与多种恶性肿瘤的发生和转移密切相关,许多肿瘤病人在其肿瘤的发生和转移过程中均有C-met的过度表达和基因扩增。当前国内外关于食管鳞癌C-met表达情况的研究报道较少,所以本研究通过逆转录-聚合酶链反应(RT-PCR)技术检测了50例食管鳞癌组织和20例癌旁正常食管组织中C-met mRNA的表达,并分析C-met mRNA的表达与临床病理资料之间的关系,判断其与食管鳞癌术后复发、转移及预后的相关性。
1 材料与方法
1.1 材料
50例食管鳞癌手术标本及20例癌旁正常食管组织标本来自于佳木斯大学附属第一医院胸外科2008-11~2010-12手术病例,其中男40例,女10例,年龄35~71岁,中位年龄52.6岁。50例肿瘤组织中,11例低分化,25例中分化,14例高分化,23例有淋巴结转移。肿瘤部位中段24例,下段26例。肿瘤大小≤5cm 28例,>5cm 22例。根据国际抗癌联盟(UICC)1997年修订的食管癌临床分期标准,Ⅱa期27例,Ⅱb+III期23例,食管上段、T4及M1(Ⅳ期)病人不包括在手术范围内。胸腹部淋巴结清扫范围参照美国癌症联合委员会(American Joint Committee on Cancer,AJCC)食管癌淋巴结分布图,淋巴结清扫数目8~24枚,平均9.8枚。所有患者术中肉眼大体判断均达RO切除,术后病理诊断食管鳞癌,食管上、下切缘均无肿瘤细胞残留。相应的癌旁正常食管组织标本为术中采集距离食管癌组织至少5cm以上的正常食管组织。所有患者术前未行放疗、化疗等治疗,手术标本取材后马上放入液氮罐中保存。
1.2 主要试剂及药品
总RNA提取试剂盒(Trizo Rragent,Gibcobrl公司),RT-PCR试剂盒(Takara公司),DNA分子量标准(北京中山公司),其它试剂均为国产优质分析纯。
1.3 RT-PCR实验方法和结果判定
按照Trizol的说明书,首先应用Trizol一步法分别提取食管鳞癌和癌旁正常食管组织中的总RNA,然后用紫外分光光度计测定纯度并定量。从总RNA 中取0.5μg 用于合成cDNA第一链。逆转录反应体系中加入以下试剂:MgCl22μL、10×RNA buffer 1μL、Rnase Free dH2O 3.75μL、 dNTP1μL、 Rnase Inhibitor 0.25μL、 Rnase Transcriptase 0.5μL和 Random 9mers 0.5μL样品1μL。逆转录反应条件:30℃ 10min、42℃ 30min、99℃ 5min、5℃ 10min。根据GenBank提供的C-met和内参照β-actin的mRNA序列,应用Oligo5.0软件自行设计引物。设计引物序列由上海科华生物公司合成。C-met上游引物:5'-TTCACCGCGGAAACACCCATC -3';下游引物:5'-GTCTTCCAGCCAGGCCCAGT -3'。预计扩增片段C-met140bp。β-actin上游引物,5'-GGCATCCTCACCCTGAAGTA -3',下游引物,5'-CCATCTCTTGCTCGAAGTCC -3'。预计扩增片段为496 bp。C-met特异性引物稀释终浓度为20pmol/μL,内参照β-actin特异性引物稀释终浓度为10pmol/μL。取2.5μL cDNA用于PCR扩增,在反应体系中加入以下试剂:5×RNA buffer 2.5μL、灭菌 ddH2O 7.16μL、 TaqHs 0.04μL和C-met的上、下游引物各0.15μL或者β-actin的上、下游引物各0.15μL。C-met基因的逆转录扩增反应条件:95℃ 2min变性、95℃ 1min、58℃ 1min、72℃ 1min、一共30个循环,最后72℃延伸7min。取2μLPCR产物与2μL Lodding Buffer混合,进行8%的聚丙烯酰胺凝胶电泳,100V/1.5h,电泳结束后,凝胶成像仪成像分析,计算目的基因mRNA的相对含量。应用100bp梯度的Makers(中山公司)为分子量大小对照,确定电泳条带。
1.4 随访
对患者定期随访,记录肿瘤复发或转移的时间,死于肿瘤复发或转移的患者纳入生存分析。随访截止日期为2015年12月底,术后中位随访时间为40.7个月(22~62个月)。所有患者都进行随访,随访率100%,随访通过门诊复查及电话进行。
1.5 统计学方法
采用SPSS13.0软件进行统计分析,两样本率的比较用皮尔逊卡方检验法,Kaplan-Meier寿命表法进行生存分析,Log-rank检验判断生存差异性,采用COX回归多因素分析法判定独立的预后因素。P<0.05为差异有统计学意义。
2 结果
2.1 食管鳞癌组织和癌旁正常食管组织中C-met mRNA及β-actin mRNA的表达
依据C-met mRNA和β-actin mRNA条带灰度值比较分析结果,50例食管鳞癌组织中有27例C-met mRNA阳性表达(阳性率为54.0%);而20例癌旁正常组织仅有1例C-met mRNA阳性表达(阳性率为5.0%)。50例食管鳞癌组织和20例癌旁正常组织均有β-actin mRNA表达,见图1。
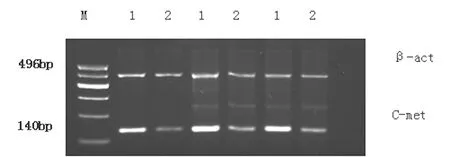
1:食管鳞癌组织;2:癌旁正常食管组织;M:DNA分子量标准基因产物:C-met mRNA 140bp,β-actin mRNA 496bp
2.2 C-met mRNA表达情况与临床病理资料的关系
在食管鳞癌组织中,C-met的表达与患者年龄、性别、病变长度和癌组织分化程度无关,而与癌组织浸润深度、淋巴结转移和TNM分期有关,见表1。

表1 C-met mRNA在食管鳞癌中的表达与临床病理资料的关系
2.3 C-met mRNA表达情况与食管鳞癌术后复发、转移的相关性
术后随访出现复发、转移的患者共21例,复发转移率为42.0%。C-met mRNA阳性表达者有复发、转移的为16例(59.3%),阴性表达者中为5例(21.7%),二者比较差异有统计学意义(P<0.01)。
2.4 C-met mRNA表达情况与食管鳞癌预后的相关性
应用Kaplan-Meier生存曲线对50例患者进行术后随访,结果显示所有患者的5年生存率为42.0%。C-met mRNA阳性表达者5年生存率为25.9%,C-met mRNA阴性表达者5年生存率为60.9%,log-rank检验显示二者差异具有统计学意义(P<0.01)。COX回归多因素分析显示淋巴结转移(HR=4.896,P=0.008)和C-met mRNA表达(HR=6.026,P=0.005)是影响食管鳞癌患者预后的独立危险因素。
3 讨论
C-met基因位于人类第七号染色体长臂(7q31),大小约超过110kbp,包含21个外显子。它的启动子区域包含许多的调控序列,有AP1、AP2、NF-KB和HGF基因等。C-met基因编码蛋白产物是先合成170kD的单链前体物,进而切割和重排成50kD的α亚基和145kD的β亚基,然后两亚基再以二硫键相连形成190kD的异二聚体。α亚基和β亚基的胞外区是配体识别部位,可识别并结合HGF,而胞内部位具有酪氨酸激酶活性,是多种信号分子相互作用的结合部位。作为肝细胞生长因子(HGF)唯一受体蛋白,C-met受体被HGF激活后发生自体磷酸化,其酪氨酸激酶活性增强,导致多种底物蛋白的酪氨酸磷酸化,这些中间底物的激活扩大了HGF的生物学活性,如促进细胞增殖、运动等[2]。
目前认为C-met促进肿瘤进展的机制主要有以下几点:①C-met通过上调环氧合酶COX-2的基因表达和增加前列腺素(PG)的合成,从而促进食管癌的发展和转移[3]。②C-met诱导基质降解酶的产生,通过破坏基底膜和增加蛋白水解来促进肿瘤的侵袭和转移[4]。③在食管恶性肿瘤的生长和增殖过程中新生血管的形成是不可或缺的[5],同时也是肿瘤侵袭转移的必要条件,而HGF是一种促血管生长因子,它与内皮细胞表达的C-met受体特异性结合,能够激活血管内皮细胞,引起血管内皮细胞的增殖和迁移,从而参与肿瘤新生血管的形成[6]。
最近的研究表明在正常细胞中C-met的表达和在肿瘤细胞中有着明显的区别。在正常细胞中,原癌基因C-met mRNA呈低表达或不表达,虽然在组织器官切除或损伤后,C-met的表达有一过性的增加,但表达水平很快恢复到正常,证明正常细胞可以通过减少C-met的表达来控制它对HGF的反应。在许多恶性肿瘤细胞中,可以观察到C-met的持续、过度表达,常常伴随高水平的自体磷酸化,这通常是由于基因的扩增所致。C-met的过度表达可见于人的肝癌、肺癌、胃癌、胰腺癌、甲状腺癌、结肠癌和脑胶质瘤,C-met的过度表达提示肿瘤预后差[7,8]。
本研究利用RT-PCR技术,以β-actin为内参照,检测了食管鳞癌组织和癌旁正常食管组织中C-met mRNA的表达情况,结果提示C-met mRNA在癌旁正常食管组织中低表达,而在食管鳞癌组织中呈高表达(P<0.01)。本实验的研究结果还发现,C-met mRNA的表达与癌组织浸润深度、淋巴结转移和TNM分期有关,浸润深度越深C-met mRNA阳性表达率越高(P<0.05),有淋巴结转移患者C-met mRNA阳性表达率显著高于无淋巴结转移患者(P<0.01),表明C-met mRNA基因的表达与癌组织浸润深度、淋巴结转移呈正相关,而与患者年龄、性别、病变长度和癌组织分化程度无关(P>0.05),更进一步说明食管鳞癌中C-met的过度表达能促进肿瘤细胞的扩散和转移,提示C-met的过度表达与食管鳞癌的不良病理参数密切相关,肿瘤预后差。
本研究还发现,C-met mRNA阳性表达者复发、转移率为59.3%,明显高于阴性表达者的21.7%。50例食管鳞癌患者总的5年生存率为42.0%,C-met mRNA阳性表达患者的5年生存率为25.9%,明显低于阴性表达患者的60.9%。COX回归多因素分析显示,淋巴结转移和C-met mRNA表达是影响食管鳞癌患者预后的独立危险因素。
目前以HGF-C-met信号通路为靶点的抑制剂、拮抗剂和反义核苷酸治疗在多项实验研究中已经取得了可喜的成果。许多能够阻断HGF-C-met信号转呈途径的化合物已经被发现,其中的典型代表是格尔德霉素类药物(GA)。由于GA能降低C-met受体的表达,而且具有降低HGF诱导的uPA的表达的作用,因此在抑制肿瘤转移方面有很大临床意义。HGF拮抗剂NK4由HGFɑ链N末端的发夹样结构和4个Kringle区结构所组成,能够和C-met相结合,竞争性地抑制HGF和C-met的相互作用,影响HGF-C-met信号通路,进而抑制HGF诱导的肿瘤细胞侵袭转移过程。多项体外实验显示NK4可抑制HGF诱导的包括人结肠癌、胆囊癌、乳腺癌、胰腺癌、宫颈癌、胆管癌和前列腺癌等细胞的运动和侵袭。有国内学者采用脂质体法合成的C-met反义寡核苷酸链,将构建的C-met反义质粒及U1SnRNA/核酸/反义C-met复合体分别转染肝癌SF7721细胞,来封闭C-met信号转呈,探讨C-met信号转呈阻滞对肝癌生长和转移的影响。结果显示C-met反义寡核苷酸链能抑制肝癌SF7721细胞的增殖,C-met反义质粒及U1SnRNA/核酸/反义C-met复合体质粒转染后细胞表达受体C-met的量均显著减少,而且转染后细胞增殖速度明显减慢,侵袭运动能力减弱。体内实验也发现细胞转染后裸鼠体内生成肿瘤速度较慢,进而证明阻断HGF-C-met的信号传导能够降低肿瘤生长甚至转移的能力。国外学者也应用C-met反义寡核苷酸/U6表达质粒治疗非小细胞肺癌,同样观察到伴有C-met蛋白表达下调的对肿瘤的抑制作用[9,10]。
C-met基因在食管鳞癌中表达的研究较少,它在食管鳞癌发生、发展中的作用机制尚不完全清楚,但是C-met mRNA在食管鳞癌中呈现高表达而且与肿瘤侵袭、复发及转移密切相关,所以研究其结构、功能和作用机制对判断食管鳞癌的复发、转移、预后及以后的治疗有重要临床意义,HGF-C-met信号通路有望成为未来生物治疗的靶点。
[1]Fieten H,Spee B,Ijzer J,et al.Expression of hepatocyte growth factor and the proto-oncogenic receptor c-Met in canine osteosarcoma[J].Vet Pathol,2009,46(5):869-877
[2]Nakamura T,Nishizava T,HagiyaM,et al.Molecular cloningand expression of human hepatocyte growth factor[J].Nature,1989,342(6248):440-443
[3]Chen JH,Liu TY,Wu CW,et al.Nonsteroidal anti-inflammatory drugs for treatment of advanced gastric cancer:cyclooxygenase-2 is involved in hepatocyte growth factor mediated tumor development and progression[J].Medical Hypothesis,2001,57(4):503
[4]Kermorgant S,Aparicio T,Dessirier V,et al.Hepatocyte growth factor induces colonic cancer cell invasiveness via enhanced motility and protease overproduction.Evidence for PI3 kinase and PKC involvement[J].Carcinogenesis,2001,22(7):1035
[5]Inoue T,Kataoka H,Goto K,et al.Activation of c-met (hepatocyte growth factor receptor) in human gastric cancer tissue[J].Cancer Sci,2004,95(10):803
[6]Dong G,Lee TL,Yeh NT,et al.Metastatic squamous cell carcinoma cells that overexpress c-met exhibit enhanced angiogenesis factor expression,scattering and metastasis in response to hepatocyte growth factor[J].Oncogene,2004,23(37):6199
[7]邹志田.C-met基因与COX-2基因在食管鳞癌中的表达及其临床意义[J].黑龙江医药科学,2012,35(5):74-76
[8]Kong DS,Song SY,Kim DH,et al.Prognostic significance of C-met express in glioblastomas[J].Cancer,2009,115(1):140-148
[9]朱晓峰,王林,戚家峰,等.食管鳞癌患者术前血清HGF、VEGF-C的表达及临床意义[J].黑龙江医药科学,2011,34(1):69
[10]Stabile LP,Lyker JS,AuangL,et al.Inhibition ofhuman non-small cell lung tumors by a c-Met antisense/U6 expression plasmid strategy[J].Gene Ther,2004,11(3):325-335
黑龙江省卫生厅科研项目,编号:2012-187。
朱晓峰(1970~)男,黑龙江佳木斯人,博士,主任医师,硕士研究生导师。
邹志田(1962~)男,黑龙江佳木斯人,博士,主任医师,硕士研究生导师。E-mail:zxf700105@sina.com。
R735.1
A
1008-0104(2016)05-0001-04
2016-04-09)
