放大内镜结合窄带成像技术评估早期食管癌浸润深度价值的Meta分析*
2016-11-15李婷园张烁
李婷园,张烁
(浙江中医药大学附属第一医院 消化科,浙江 杭州 310000)
论 著
放大内镜结合窄带成像技术评估早期食管癌浸润深度价值的Meta分析*
李婷园,张烁
(浙江中医药大学附属第一医院 消化科,浙江 杭州 310000)
目的 系统评价放大内镜结合窄带成像技术(ME-NBI)对评估早期食管癌浸润深度的临床价值。方法 计算机检索Embase、Pubmed、Web of Science、Cochrane Library、CBM、CNKI、万方及维普数据库,检索年限从建库至2016年2月,全面收集有关ME-NBI评估食管癌浸润深度相关的研究。根据纳入标准筛选文献,并按诊断试验评价标准(QUADAS)系统评价文献质量并提取数据,采用Stata 12.0版软件进行Meta分析。结果 最终纳入6篇文献,提取出7组数据,包括319例患者的366例病变进行合并分析。ME-NBI评估早期食管癌的敏感度(Se)为93.8%[95%可信区间(95%CI):0.886~0.967)],特异度(Sp)为75.2%(95%CI:0.658~0.827),阳性似然比(LR+)3.779(95%CI:2.685~5.318),阴性似然比(LR-)0.083(95%CI:0.044~0.155),综合受试者工作特征曲线(SROC)下面积(AUC)0.80(95%CI:0.770~0.840),诊断比值比(DOR)45.658(95%CI:21.006~99.240)。结论 ME-NBI对评估早期食管癌浸润深度的诊断准确性较高,可作为临床术前诊断黏膜内癌的有效工具,对指导临床选择合理的手术方式和治疗手段具有重要意义。
放大内镜;窄带成像;早期食管癌;浸润深度
食管癌主要流行于发展中国家,是世界上最常见的恶性肿瘤之一,其死亡率位居所有癌症的第7位[1]。我国亦是食管癌高发国家,每年新发病例数超过22万例,死亡约20万例[2]。超过90.0%的食管癌患者确诊时已进展至中晚期[3],总体预后较差。因此,早期发现和正确治疗是提高我国食管癌治疗效果的突破点。对于早期食管癌,侵犯的深度及淋巴结的转移是临床治疗方案选择的重要参考标准,并对预后的评价有重要意义。而侵犯深度又与淋巴结转移存在密切联系,文献显示黏膜内癌的淋巴结转移率为0.0%~8.0%,侵及黏膜下的淋巴结转移率为11.0%~54.0%[4-5]。
消化道内镜近年来发展迅速,放大内镜结合窄带成像技术(magnifying endoscopy with narrow band imaging,ME-NBI)在判断食管癌浸润深度方面的技术也日趋成熟。ME-NBI可以清楚观察到黏膜的微细结构特征,通过对食管上皮内乳头状毛细血管襻(intraepithelial papillary capillary loop,IPCL)[6]的观察来判断食管早癌侵犯深度。本研究通过应用循证医学Meta分析的方法,全面收集国内外有关ME-NBI评估早期食管癌浸润深度准确性的相关研究,评价MENBI临床应用价值并为其临床早期诊治食管癌提供科学依据。
1 资料与方法
1.1 检索策略
计算机检索Embase、Pubmed、Web of Science和Cochrane Library 4个外文数据库,以及CBM、CNKI、万方和维普中文数据库,检索年限均从建库起至2016年2月,并对已检索文献中提供的参考文献进行再次检索以获取补充资料。文献限于国内外已发表的中文及英文研究。文献检索策略采用主题词和自由词结合的原则,英文检索词包括:esophageal cancer,narrow band imaging,depth,staging,mucosal,submucosal;中文检索词包括:食管、窄带内镜、浸润深度和分期等。
1.2 纳入与排除标准
1.2.1 文献纳入标准
①研究类型:有关ME-NBI对早期食管癌浸润深度评估准确性的相关随机或非随机研究,包括前瞻性研究及回顾性研究;②所有研究对象均进行了ME-NBI检查及病理诊断;③以INOUE分类[6]为ME-NBI诊断食管浸润深度的分类标准;④所有研究的金标准均为内镜手术术后或外科手术术后的病理组织学诊断;⑤纳入研究临床数据资料(四格表)完整,能提取真阳性、假阳性、真阴性和假阴性值。
1.2.2 文献排除标准
①文摘、综述、讲座和书信类;②数据资料有误或数据不完整无法获取诊断四格表资料;③纳入研究样本量小于35例;④未标明诊断标准或诊断标准不符的文献;⑤未获取全文。
1.3 数据提取和质量评价
由两位研究者分别独立提取文献信息,其中包括研究作者、发表年限、地区、样本量、性别、年龄和金标准等,并对文献进行质量评价,如存在争议,通过与第三方讨论解决分歧。运用诊断试验评价标准(quality assessment of diagnostic accuracy studies,QUADAS)[7]对纳入文献质量进行评价。该工具为一问卷式调查表,由14个条目构成,每一条目按“是”、“否”及“不清楚”进行分级。
1.4 数据分析
采用Stata 12.0版本软件的计算纳入研究敏感度(sensitivity,Se)、特异度(specificity,Sp)、阳性似然比(positive likelihood ratio,LR+)、阴性似然比(negative likelihood ratio,LR-)、诊断比值比(diagnostic odds ratio,DOR)及其95%可信区间(coincidence interval,95%CI),并进行合并受试者工作特征曲线(summary receiver operating characteristic curve,SROC)分析,并计算曲线下面积(area under the curve,AUC),AUC值越接近1.00,说明诊断的准确性越高,一般而言,AUC在0.50~0.70之间表示诊断价值较低,在0.70~0.90之间诊断价值中等,在0.90以上认为诊断价值较高,用Deek漏斗图判断发表偏倚,Cochran's Q及I2评估异质性[8]。
2 结果
2.1 入选文献结果
据本研究检索策略,最初检索到相关文献106篇,经过阅读文题及摘要后,排除不符合纳入标准的文献后,初步纳入文献15篇,仔细查阅全文后,其中4篇文献的研究目的与本研究不符,3篇文献ME-NBI下诊断浸润深度未用INOUE分类,2篇文献未分离黏膜内癌与黏膜下癌的数据。最终纳入6篇文献[9-14],其中一篇可提取两组数据,纳入的文献年限在2004年-2014年,其中日本的研究3篇,中国的研究2篇,韩国的研究1篇,包括319例患者,366处病变,见表1。根据QUADAS工具对所纳入的6篇研究进行质量评分,2篇9分,3篇10分,1篇11分,见表2。
2.2 Meta分析结果
最终纳入6篇文献,提取7组数据,包含319例患者的366例病灶,进行了Meta分析。对这7组数据进行异质性检验,Q =1.514,P =0.235,I2=0.00,提示异质性低,SROC曲线图上未呈“肩臂状”分布,提示无阈值效应。Deek漏斗图显示直线斜率接近0,P >0.1,表示漏斗图较对称,不存在发表偏倚[8](图1)。Se为93.8%(95%CI:0.886~0.967)(图2);Sp为75.2%(95%CI:0.658~0.827)( 图3);LR+及LR-分别为3.779(95%CI:2.685~5.318),0.083(95%CI:0.044~0.155),DOR为45.658(95%CI:21.006~99.240),曲线下面积AUC为0.80(95%CI:0.770~0.840)(图4)。
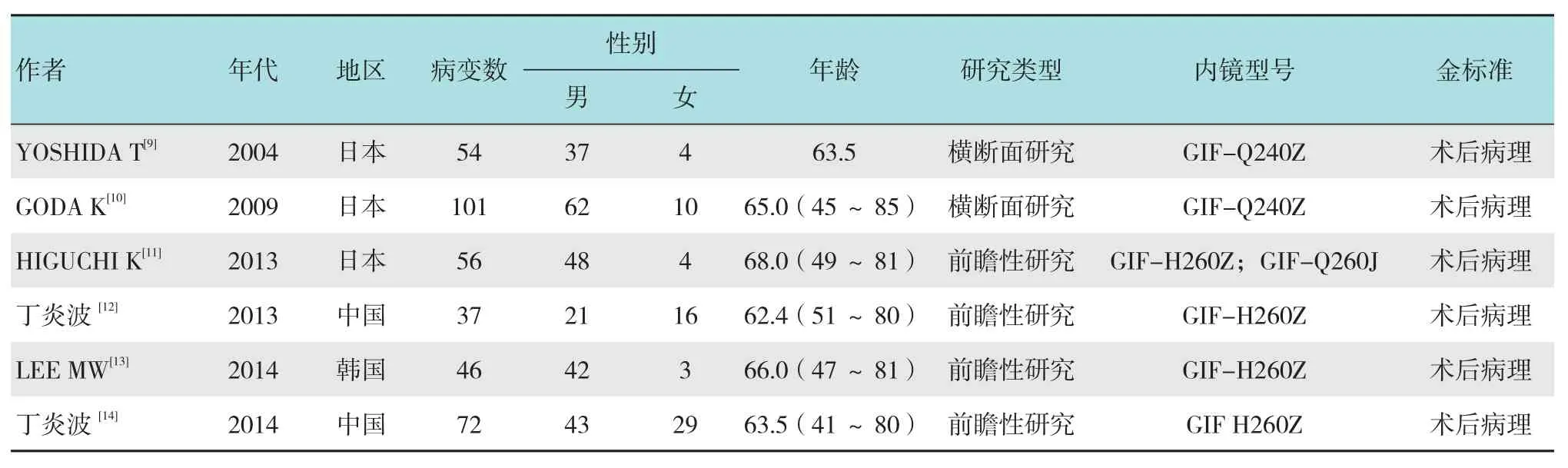
表1 纳入Meta分析各文献的一般情况
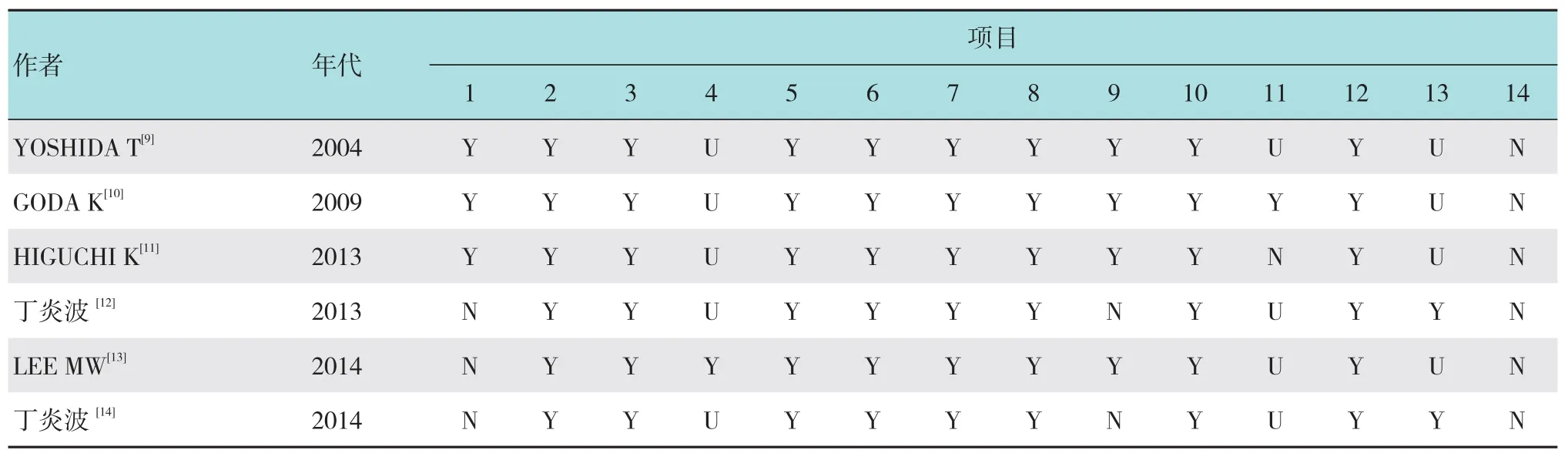
表2 QUADAS工具评价文献质量结果

图1 Deek漏斗图

图2 Se森林图

图3 Sp森林图
3 讨论
早期食管癌定义为仅局限于黏膜和黏膜下层的肿瘤,不伴淋巴结转移和远处转移,包括黏膜内癌和黏膜下癌,其治疗方法包括内镜下切除和外科手术。内镜治疗主要为内镜下黏膜切除(endoscopic mucosal resection,EMR)和内镜下黏膜剥离术(endoscopic submucosal dissection,ESD),黏膜内癌为其治疗适应证[15]。而且,与传统外科手术相比,内镜下切除具有创伤小、并发症少、恢复快和费用低等优点,且两者疗效相当[16]。因此,准确判断浸润深度对于选择合理治疗方案至关重要,并影响患者预后生存期及生活质量。影像学CT及磁共振成像(magnetic resonance imaging,MRI)对周围淋巴结浸润及远处转移情况的判定具有一定的优势,但较难判断肿瘤浸润深度;食道钡餐检查对早期食管癌的诊断准确性低于胃镜,也很难准确判断肿瘤浸润深度。对于白光内镜,EBI等[17]的多中心前瞻性研究认为,其对诊断肿瘤位置及大小较为准确,但对于浸润深度的判断则与镜下分型有重要关系,对于平坦型(0~Ⅱ型)的准确性较其他型稍高,准确率约为71.4%。而临床上较常用的超声内镜,一篇Meta分析[18]纳入了19项回顾性研究,包含1 019例行EMR、ESD及外科手术的患者,分析得出超声内镜判断黏膜内癌敏感度约为85.0%。
窄带成像技术(narrow band imaging,NBI)是一种新的内镜技术,不同于传统内镜采用白色的照明光,它通过特殊的滤光器窄化内镜光源光谱,将白光波长窄化为415 nm的蓝光、540 nm的绿光以及605 nm的红光,达到特殊的光学染色效果,而血液对蓝光的吸收较强,且早期食管癌伴有上皮内毛细血管的扩张和增生,故病变部位在NBI下可与周围正常黏膜形成鲜明的对比,同时放大内镜(magnifying endoscopy,ME)可将图像放大至最适合操作者观察的倍数,检查者可更细致地观察IPCL的形态变化,从而评估病变的浸润深度。
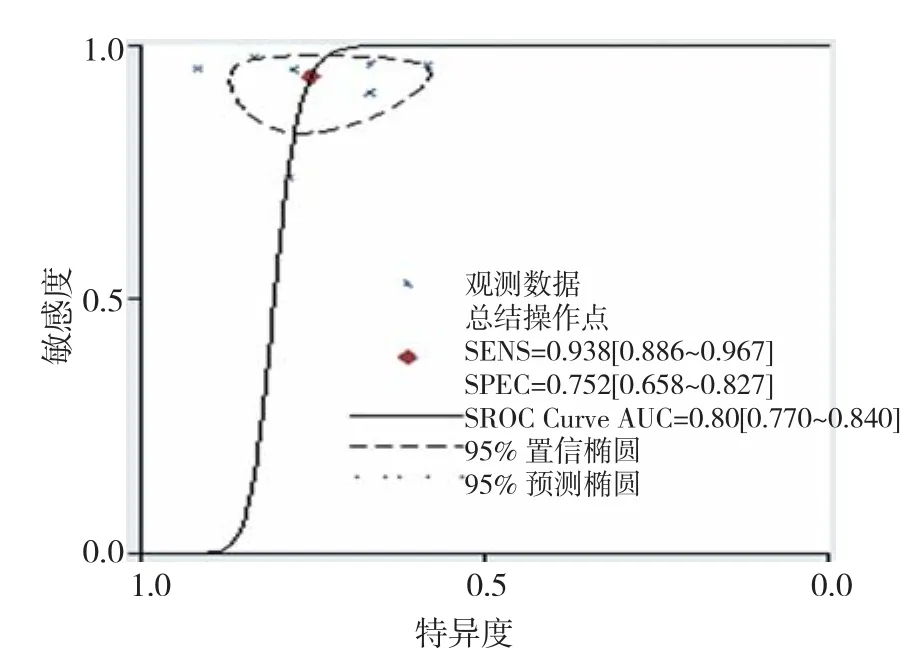
图4 SROC
本研究通过采用诊断试验的系统评价方法对ME-NBI在评估早期食管癌浸润深度的诊断准确性价值进行了分析。此次Meta分析总共纳入6篇文献,7组数据,共有366处病变对象,Meta分析结果显示:异质性指标Q =1.514,P =0.235>0.05,同时I2为0.0%,表示各个研究是同质来源。SROC曲线下面积AUC为0.80(95%CI:0.770~0.840),曲线下面积越大,诊断价值越高。Se为93.8%(95%CI:0.886~0.967),Sp为75.2%(95%CI:0.658~0.827)、LR+为3.779(95%CI:2.685~ 5.318)、LR-为 0.083(95%CI:0.044~0.155)。LR+为真阳性率与假阳性率之比,比值越高,说明诊断价值越高。相反,LR-为真阴性率与假阴性率之比,比值越小,试验结果的价值越高。DOR用来说明某种试验阳性结果的机会是阴性结果的倍数。对于黏膜内癌,LR+远高于LR-。这就意味着,ME-NBI在明确黏膜内癌浸润深度具有高度可信性。这也给选择治疗方式提供了可靠的依据。
本研究亦存在不足之处:①研究纳入的文献仅为英文和中文,可能遗漏使用其他语言撰写的研究;②纳入研究的地区主要为中日韩3国,大多数患者在亚洲。因此,报告的结果可能并不适用于其他地区;③病变最常见的特点,如大小和位置在2篇中文研究中无法明确提取;④最终只有6篇文献纳入,原始文献数量较少。
综上所述,ME-NBI对早期食管癌浸润深度的诊断具有较高的敏感性和特异性,且其具有操作方便,可重复性高的特点,故可作为临床术前诊断食管浸润深度的有效工具。
[1] SIIEGEL R, NAISHADHAM D, JEMAET A, et al. Cancer statistics, 2013[J]. CA Cancer J Clin, 2013, 63(1): 11-30.
[2] JEMAL A, BRAY F, MELISSA M, et al. Global cancer statistics[J]. CA Cancer J Clin, 2011, 61(2): 69-90.
[3] MERKOW R P, BILIMORA K Y, KESWANI R N, et al. Treatment trends, risk of lymphnode metastasis, and outcomes for localized esophageal cancer[J]. J Natl Cancer Inst, 2014, 106(7): 766-776.
[4] BOLLSCHWEILER E, BALDUS SE, SCHRDERC W, et al. High rate of lymph-node metastasis in submucosal esophageal squamous-cell carcinomas and adenocarcinomas[J]. Endoscopy,2006, 38(2): 149-156.
[5] TACHIBANA M, HIRAHARA N, KINUGASA S, et al. Clinicopathologic features of superfi cial esophageal cancer: results of consecutive 100 patients[J]. Ann Surg Oncol, 2008, 15(1): 104-116.
[6] INOUE H, KUMAGAI Y, YOSHIDA T, et al. High-magnifi cation endoscopic diagnosis of the superfi cial esophageal cancer[J]. Dig Endosc, 2000, 12(1): 32-35.
[7] WHITING P, RUTJES A W, REITSMA J B, et al. The development of QUADAS: a tool for the quality assessment of studies of diagnostic accuracy included in systematic reviews[J]. BMC Med Res Methodol, 2003, 3(1): 1-13.
[8] PETITTI D B. Approaches to heterogeneity in meta-analysis[J]. Statstics in Medicine, 2001, 20(23): 3625-3633.
[9] YOSHIDA T, INOUE H, USUI S, et al. Narrow-band imaging system with magnifying endoscopy for superficial esophageal lesions[J]. Gastrointestinal Endoscopy, 2004, 59(2): 288-295.
[10] GODA K, TAJIRI H, IKEGAMI M, et al. Magnifying endoscopy with narrow band imaging for predicting the invasion depth of superfi cial esophageal squamous cell carcinoma[J]. Diseases of the Esophagus, 2009, 22(5): 453-460.
[11] HIGUCHI K, TANABE S, MIZUTOMO A, et al. A phase II study of endoscopic submucosal dissection for superfi cial esophageal neoplasms[J]. Gastrointestinal Endoscopy, 2013, 78(5): 704-710.
[12] 丁炎波, 陈炳芳, 王莉, 等. 窄带成像放大内镜在早期食管癌术前评估中的应用价值[J].右江医学, 2013, 41(6): 852-853.
[13] LEE M W, KIM G H, IB H, et al. Predicting the invasion depth of esophageal squamous cell carcinoma: comparison of endoscopic ultrasonography and magnifying endoscopy[J]. Scandinavian Journal of Gastroenterology, 2014, 49(7): 853-861.
[14] 丁炎波, 陈炳芳, 陈建平, 等. 三种方法预测食管早癌及高级别上皮内瘤变浸润深度的对比观察[J]. 中华消化内镜杂志,2014, 31(11): 665-667.
[15] JES. Japanese classification of esophageal cancer, 10th edition:part I[J]. Esophagus, 2009, 6(1): 1-25.
[16] CULLOCH P, WARD J, TEKKIS P, et al. Mortality and morbidity in gastrooesophageal cancer surgery: initial results of ASCOT multicentre prospective cohort study[J]. BMJ, 2003, 327(7425):1192-1197.
[17] EBI M, SHIMURA T, YAMADA T, et al. Multicenter, prospective trial of white-light imagine alone versus white-light imagine followed by magnifying endoscopy with narrow-band imaging for the real-time imaging and diagnosis of invasion depth in superficial esophageal suquamous cell carcionoma[J]. Gastrointest Endosc, 2015, 81(6): 1355-1361.
[18] THOSANI N, SINGH H, KAPADIA A, et al. Diagnostic accuracy of EUS indifferentiating mucosal versus submucosal invasion of superficial esophageal cancers: a systematic review and metaanalysis[J]. Gastrointest Endosc, 2012, 75(2): 242-253.
(吴静 编辑)
Accuracy of magnifying endoscopy with narrow-band imaging for detecting early esophageal cancer invasion depth: a meta-analysis*
Ting-yuan Li, Shuo Zhang
(Department of Gastroenterology, the First Affi liated Hospital of Zhejiang Chinese Medical University,Hangzhou, Zhejiang 310000, China)
Objective To evaluate the accuracy of magnifying endoscopy with narrow-band imaging (MENBI) for detecting early esophageal cancer invasion depth. Methods We searched Embase, Pubmed, Web of Science,Cochrane Library, CBM, CNKI, Wanfang and VIP databases from inception to Feb.2016. Domestic articles related to the accuracy of ME-NBI detecting the early esophageal cancer invasion depth were collected comprehensively. The quality of the papers was evaluated by quality assessment of diagnostic accuracy studies (QUADAS). Data analysis was conducted by Stata 12.0 software. Results Seven group data from six studies including 319 patients with 366 lesions met the inclusion criteria. The pooled sensitivity, specificity, positive likelihood ratio, negative likelihood ratio, SROC area under the curve and DOR were 93.8 % (95 % CI: 0.886~0.967), 75.2 % (95 % CI: 0.658~0.827),3.779 (95 % CI: 2.685~5.318), 0.083 (95 % CI: 0.044~0.155), 0.80 (95 % CI: 0.770~0.840) and 45.658 (95 % CI:21.006~99.240). Conclusions The results suggest that ME-NBI may be an effective tool for detecting invasion depth of early esophageal cancer, which plays an important role in clinical selection of surgical approach and treatment.
magnifying endoscopy; narrow band imaging; early esophageal cancer; invasion depth
R735.1
A
10.3969/j.issn.1007-1989.2016.09.001
1007-1989(2016)09-0001-05
2016-03-25
浙江省医药卫生平台计划(No:2015RCA020)
张烁,E-mail:zhangshuotcm@163.com;Tel:13957192066
