甲状腺结节与甲状腺癌的临床评估和处理
2016-11-09黎丹凤张进安
黎丹凤+张进安
摘 要 成人甲状腺结节的发病率相当高,其中大多数为良性病变,无需特殊处理,而恶性病变占5%~15%,需要及时处理。鉴于良恶性甲状腺结节对患者生存质量的影响有显著差异,且临床处理方法不同,所以鉴别结节的良、恶性非常重要。一般可通过病史、体格检查、影像学、核素扫描、细针穿刺、实验室检查等几方面评估甲状腺结节性质。对于分化型甲状腺癌需采取手术、同位素、甲状腺激素抑制治疗等综合手段,预后良好。
关键词 甲状腺结节 分化型甲状腺癌 超声 治疗
中图分类号:R736.1/R581.3 文献标志码:A 文章编号:1006-1533(2016)20-0003-05
Clinical evaluation and management of thyroid nodule and carcinoma
LI Danfeng, ZHANG Jinan
(Department of Endocrinology, Jinshan Hospital affiliated to Fudan University , Shanghai 201508, China)
ABSTRACT Incidence of thyroid nodule is quite high in adults. Most of thyroid lesions are benign and need no special treatment. The malignant lesions are accounted for 5%-15% and active treatment is warranted. Because the impact on the quality of life is significant difference between benign and malignant thyroid nodules as well as different clinical management, the differentiation of benign from malignant nodules is very important. The evaluation of thyroid nodules can be conducted by medical history, physical examination, imaging and nuclide scan, fine needle puncture, laboratory examination,etc. The combined therapy including surgery, isotope and thyroid hormone suppression can be adopted in the treatment of patients with differentiated thyroid cancer, which results in good prognosis.
KEY WORDS thyroid nodule; sonography; differentiated thyroid carcinoma; treatment
甲状腺结节是指甲状腺细胞在局部异常生长所引起的散在病变[1]。甲状腺结节的病因复杂,有炎症、自身免疫性疾病、退行性变或肿瘤等。随着超声技术的发展以及甲状腺检查普及,甲状腺结节的检出率越来越高,达20%~76%[2],其中5%~15%为恶性[3]。由于良、恶性甲状腺结节对患者的生存质量影响不同,故治疗方法亦差别很大,恶性肿瘤需要积极处理,包括手术治疗,而良性结节则以保守治疗为主,不会给患者带来创伤和心理负担。因此,准确评估甲状腺结节的性质,尤其是良、恶性,对于正确治疗具有重要临床意义。
1 甲状腺结节的鉴别诊断
详细的病史采集和全面的体格检查是评估甲状腺结节性质的基础。首先是病史询问,如心悸、多汗、易怒为毒性甲状腺肿的症状;局部疼痛、发热是亚急性甲状腺炎(亚甲炎)的症状;是否存在上呼吸道感染等诱因,对甲状腺功能亢进(甲亢)、亚甲炎的鉴别诊断有指导意义。大多数甲状腺结节患者无临床症状,常通过健康体检或影像学检查发现,下述几方面的病史可以为鉴别甲状腺结节的良、恶性提供一定的线索[4]:儿童期有头颈部放射线照射史或放射性尘埃接触史及全身放射治疗史者的甲状腺癌的发生率明显升高;有分化型甲状腺癌(DTC)、甲状腺髓样癌(MTC)或多发性内分泌腺瘤病2型(MEN2型)、家族性多发性息肉病、某些甲状腺癌综合征家族史者的甲状腺结节为恶性的可能性较大;结节生长迅速应考虑恶性可能;甲状腺结节伴持续性声音嘶哑、发音困难、呼吸困难、吞咽困难,并可排除声带病变(炎症、息肉等)后考虑为恶性。女性甲状腺结节发病率虽高于男性,但男性甲状腺癌的发病率比女性高2~3倍。恶性甲状腺结节一般为单发结节,触诊质地硬且不均匀,形态不规则,边界不清,固定,无触痛,常伴局部淋巴结肿大或有周围组织结构如气管、喉返神经、颈交感神经、颈丛等受侵表现。慢性甲状腺炎、伴有钙化或囊内出血的甲状腺结节或甲状腺良性肿瘤有时也可表现为单发质硬肿块,仅靠体检难以与甲状腺癌鉴别,需要靠辅助检查进行判断。
2 辅助检查在甲状腺结节诊断中的价值
2.1 甲状腺超声检查
高分辨率超声检查是评估甲状腺结节的首选方法[5]。对触诊怀疑或其他影像学检查发现的甲状腺结节均需行颈部B超检查,确定甲状腺结节的大小、数量、位置、质地(实性或囊性)、形状、边界、包膜、钙化、血供及与周围组织的关系等情况,同时评估颈部区域有无淋巴结和淋巴结大小、形态和结构特点。不同性质结节的声像特点不同,多发的高回声或等回声结节,边缘整齐,有完整包膜,纯囊性结节,由多个小囊泡占据5 0 %以上结节体积、呈海绵状改变的结节考虑为良性。恶性结节常表现为内回声不均匀的单发结节,结节纵径大于横径,结节形态和边缘不规则、晕圈缺如,结节内血供丰富,微小钙化、针尖样弥散分布或簇状分布的钙化,周围组织受侵犯可出现蟹足样改变或有肿大淋巴结。亚甲炎结节常表现为单侧低回声,且边界不清。桥本甲状腺炎B超征象为甲状腺肿大,弥漫性密度减低或小的低密度结节与线样密度增高相间排列。
2.2 放射性核素扫描
放射性核素131I或99mTc扫描适用于评估直径>1 cm的甲状腺结节。甲状腺癌一般呈“冷结节”,但并非所有的“冷结节”均为恶性,其中10%~15%为恶性,“冷结节”也可见于甲状腺囊肿、腺瘤、结节性甲状腺肿或甲状腺炎。“热结节”绝大部分为良性,一般是高功能腺瘤或结节性甲状腺肿。放射性核素扫描因可记录甲状腺结节的功能状态,曾作为甲状腺结节的首选检查,但其在诊断直径<1.0 cm的结节及甲状腺外周和峡部结节时有局限性,故近年来首选地位逐渐被B超及细针穿刺活检(fine needle aspiration biopsy,FNAB)所取代。
2.3 影像学在甲状腺结节评估中的作用
CT和磁共振成像(MRI)在鉴别良、恶性甲状腺结节方面并不优于超声[6],2-18F-2-脱氧-D-葡萄糖(18F-FDG)正电子发射断层显像(PET)能反映甲状腺结节摄取和代谢葡萄糖的状态,但并非所有的甲状腺恶性结节都能在18F-FDG PET中表现为阳性,而某些良性结节也会摄取18F-FDG[7],因此,单纯依靠18F-FDG PET不能准确鉴别甲状腺结节的良恶性。所以一般不建议将CT、MRI和18F-FDG PET 作为评估甲状腺结节的常规检查。
2.4 FNAB在甲状腺结节评估中的作用
FNAB是诊断甲状腺癌敏感度和特异度最高的方法,术前通过FNAB诊断甲状腺癌的敏感度为83%(65%~98%),特异度为92%(72%~100%),阳性预测率为75%(50%~96%),假阴性率为5%(1%~11%),假阳性率为5%(0~7%)[8]。FNAB不能区分甲状腺滤泡状癌和滤泡细胞腺瘤。该检查有助于减少不必要的甲状腺结节手术,并帮助确定恰当的手术方案。凡直径>1 c m的甲状腺结节,均可考虑FNAB检查。但在下述情况时FNAB不作为常规:经甲状腺核素显像证实为有自主摄取功能的“热结节”;超声提示为纯囊性结节;根据超声影像已高度怀疑为恶性结节。直径<1 c m的甲状腺结节常规不考虑行F N B A,但以下可考虑行超声引导下F N B A[9]:超声提示结节有恶性征象;伴颈部淋巴结超声影像异常;童年期有颈部放射线照射史或辐射污染接触史;有甲状腺癌或甲状腺癌综合征的病史或家族史;18F-FDG PET检查阳性;伴有血清降钙素水平异常升高。FNAB不但可诊断结节性质,还可对恶性肿瘤进一步分类,从而决定治疗方案。但FNAB在鉴别甲状腺滤泡状癌和滤泡细胞腺瘤时有困难,此时测定血促甲状腺激素(TSH)或检查穿刺标本中甲状腺癌分子标志物对诊断有帮助。
2.5 实验室检查
测定血FT3、FT4、TSH及相关抗体水平可了解甲状腺功能状态。研究显示,甲状腺结节患者伴有TSH 水平低于正常值者,其结节为恶性的比例低于伴有TSH水平正常或升高者[10]。血中甲状腺过氧化物酶抗体(TPOAb)、甲状腺球蛋白抗体(TgAb)滴度明显升高者考虑为慢性淋巴细胞性甲状腺炎。甲状腺球蛋白(Tg)由甲状腺滤泡上皮细胞分泌,多种甲状腺疾病均可引起血清Tg水平升高,包括分化型甲状腺癌、甲状腺肿、甲状腺组织炎症或损伤、甲亢等,因此,血清Tg不能鉴别甲状腺结节的良恶性。降钙素由甲状腺滤泡旁细胞(C细胞)分泌,当其大幅度升高时(>100 pg/ml)对MTC有诊断价值[11]。
3 甲状腺结节的处理
3.1 良性甲状腺结节的处理
多数良性甲状腺结节仅需定期随访,无需特殊治疗。少数情况下,可选择手术治疗、TSH抑制治疗、放射性碘即131I治疗。
出现以下情况可考虑手术[12]:出现与结节明显相关的局部压迫症状;合并甲亢,内科治疗无效;肿物位于胸骨后或纵隔内;结节进行性生长,临床考虑有恶变倾向或合并甲状腺癌高危因素。因外观或思想顾虑过重影响正常生活而要求手术者,可作为手术的相对适应证。此类手术在彻底切除甲状腺结节的同时,尽量保留正常甲状腺组织,由于切除部分或全部甲状腺组织,患者术后有可能发生不同程度的甲状腺功能减退(甲减),伴有高滴度TPOAb和(或)TgAb者更易发生甲减。术后需定期监测甲状腺功能,如监测中发现甲减,要及时给予左旋甲状腺素(L-T4)替代治疗。
在碘缺乏地区,TSH抑制治疗可能有助于缩小结节、预防新结节出现或缩小结节性甲状腺肿的体积。在非缺碘地区,TSH抑制治疗虽也可能缩小结节,但其长期疗效不确切,停药后可能出现结节再生长。不建议常规使用TSH抑制疗法治疗良性甲状腺结节;可在小结节性甲状腺肿的年轻患者中考虑采用;如要使用,目标为TSH部分抑制(TSH控制于正常范围下限,即0.4~0.6 mU/L)。
131I主要用于治疗有自主摄取功能并伴有甲亢的良性甲状腺结节。131I治疗后2~3个月,有自主功能的结节可逐渐缩小,甲状腺体积平均减少40%;伴有甲亢者在结节缩小的同时,甲亢症状、体征和相关并发症可逐渐改善,甲状腺功能指标可逐渐恢复正常。如131I治疗4~6个月后甲亢仍未缓解、结节无缩小,应结合患者的临床表现、相关实验室检查和甲状腺核素显像复查结果,考虑再次给予131I治疗或采取其他治疗方法[13]。131I治疗后,约10%的患者于5年内发生甲减,随时间延长甲减发生率逐渐增加。因此,建议治疗后每年至少检测1次甲状腺功能,如监测中发现甲减,要及时给予 L-T4替代治疗。对于出现压迫症状或位于胸骨后的甲状腺结节,不推荐131I治疗。妊娠期或哺乳期是131I治疗的绝对禁忌证。
3.2 儿童甲状腺结节的处理
儿童甲状腺结节的治疗与成年患者基本相同。手术是儿童甲状腺恶性、可疑恶性结节的主要治疗手段。在儿童甲状腺结节中,恶性结节的比例高于成人,可高达20%左右[14],恶性结节通常为多病灶,且伴有淋巴结转移,甚至远处转移的概率更高[15],因此,较大比例的分化型甲状腺癌患儿治疗上宜选择全或近全甲状腺切除术,术后进行131I治疗。甲状腺结节患儿如有MTC或MEN2型家族史,建议进行RET基因突变检测[16],突变阳性者,MTC发病率显著增高,此类患者应行预防性全甲状腺切除,切除的年龄视MTC发病风险高低(根据RET基因突变位点评估)而定。
3.3 孕妇甲状腺结节的处理
已知妊娠是甲状腺结节进展的危险因素,但尚无证据表明L-T4可以阻止甲状腺结节生长,因此不建议孕期补充L-T4治疗甲状腺结节。如证实孕期甲状腺结节为良性时,无需手术治疗,只有当良性结节压迫气管、食管或生长迅速时,才可考虑手术治疗。在妊娠早期发现经FNAB证实的乳头状甲状腺癌时,孕妇应定期接受超声监测,如肿瘤在妊娠期的前24周体积增大明显(体积增加50%,直径增加20%),应立即行手术治疗。若肿瘤在妊娠中期保持稳定,或在妊娠中、后期才诊断出肿瘤,手术应在分娩后实施,但应考虑立即给予甲状腺激素抑制治疗[17],L-T4治疗的目标应保持TSH在0.1~1.5 mU/L。对于可疑恶性的甲状腺结节,可以延期至产后行手术治疗,对预后并无不利影响,不提倡L-T4抑制治疗。
对于已手术的甲状腺癌孕妇,孕期TSH的控制目标应根据不同情况决定。在甲状腺癌未能完全控制的孕妇,血清TSH应保持低于0.1 mU/L;在甲状腺癌已得到控制但仍有高风险孕妇,TSH水平应抑制在0.1~0.5 mU/L;在甲状腺癌已得到控制并属于低风险孕妇,TSH应保持在正常低值范围(0.3~1.5 mU/L)。对于大部分手术后服用L-T4的孕妇,在妊娠前3个月L-T4的剂量平均增加9%,妊娠4~6个月增加21%,妊娠7~9个月增加26%,怀孕后应尽快检测甲状腺功能。每4周检测1次甲状腺功能,调整L-T4的剂量。
3.4 DTC的治疗
DTC的治疗需采用综合手段,包括手术治疗、术后131I治疗和TSH抑制治疗。其中,手术治疗最为重要,直接影响本病的后续治疗和随访,并与预后密切相关。手术方案应根据肿瘤大小、有无侵犯周围组织、患者性别和年龄、家族史和既往史、各种术式的利弊和患者意愿合理制定,并细化外科处理原则。根据中央区淋巴结转移数目、患者年龄等决定颈部淋巴结清扫范围。
手术治疗分全/近全甲状腺切除术和甲状腺腺叶+峡部切除术。①全/近全甲状腺切除术的适应证包括:童年期有头颈部放射线照射史或放射性尘埃接触史;原发灶最大直径>4 cm;多癌灶,尤其是双侧癌灶;不良的病理亚型,如甲状腺乳头状癌的高细胞型、柱状细胞型、弥漫硬化型、实体亚型,甲状腺滤泡状癌的广泛浸润型,低分化型甲状腺癌;已有远处转移,需行术后131I治疗;伴有双侧颈部淋巴结转移;伴有腺外侵犯(如气管、食管、颈动脉或纵隔侵犯等)。全/近全甲状腺切除术的相对适应证为:肿瘤最大直径1~4 cm,伴有甲状腺癌高危因素或合并对侧甲状腺结节。②甲状腺腺叶+峡部切除术的适应证为:局限于一侧腺叶内的单发DTC,并且肿瘤原发灶≤1 cm、复发危险度低、无童年期头颈部放射线接触史、无颈部淋巴结转移和远处转移、对侧腺叶内无结节。甲状腺腺叶+峡部切除术的相对适应证为:局限于一侧腺叶内的单发DTC,并且肿瘤原发灶≤4 cm、复发危险度低、对侧腺叶内无结节;微小浸润型甲状腺滤泡状癌 。
131I是DTC术后治疗的重要手段之一。131I治疗包含两个层次:一是采用131I清除DTC术后残留的甲状腺组织(简称131I清甲);二是采用131I清除手术不能切除的DTC转移灶(简称131I清灶)。
对DTC术后患者进行实时评估,根据TNM分期,选择性实施131I清甲治疗。总体来说,除癌灶<1 cm且无腺外浸润、无淋巴结和远处转移外,均可考虑131I清甲治疗。妊娠期、哺乳期、计划短期(6个月)内妊娠者和无法依从辐射防护指导者,禁忌进行131I清甲治疗。
目前首次清甲治疗多采用固定剂量,即3.7 GBq(100 mCi)的131I。在部分患者中(尤其是低、中危患者),较低剂量的131I(30~75 mCi)也能有效完成清甲治疗,但单次治疗成功率可能偏低。对于合并肾功能异常者,首次清甲治疗剂量要酌减。儿童DTC患者需根据体重或体表面积调整清甲治疗剂量[18]。下述情况可直接应用 3.7~7.4 GBq(100~200 mCi)131I:残留较多手术不能切除的DTC病灶;伴发颈部淋巴结或远处转移,但无法手术或患者拒绝手术;不明原因的血清Tg水平明显升高。此时,清甲治疗同时兼顾清灶目的。
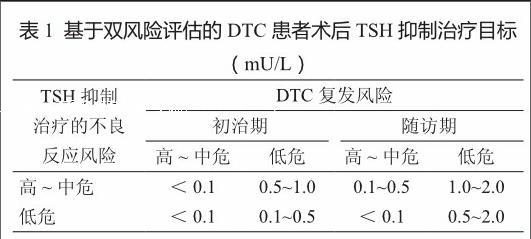
DTC患者术后应及时给予TSH抑制治疗,并持续5~10年。5~10年后无病生存者,可仅进行甲状腺激素替代治疗。TSH抑制治疗是指手术后应用甲状腺激素将TSH抑制在正常低限或低限以下、甚至检测不到的程度,一方面补充DTC患者所缺乏的甲状腺激素,另一方面抑制DTC细胞生长[19]。TSH抑制治疗用药首选L-T4口服制剂。甲状腺片中甲状腺激素的剂量和T3/T4的比例不稳定,可能带来TSH波动,因此不建议在长期抑制治疗中作为首选。TSH抑制水平与DTC的复发、转移和癌症相关死亡关系密切,特别对高危DTC者,这种关联性更加明确。某些低分化DTC的生长和增殖并非依赖于TSH,对此类患者,即使将TSH抑制至较低水平,仍难以减缓病情进展[20]。近年来,TSH抑制治疗的理念发生了转变,提倡兼顾DTC患者的肿瘤复发危险度和TSH抑制治疗的不良反应风险,制定了TSH抑制治疗的目标(表1)。
参考文献
[1] Schlumberger M. Non toxic goiter and thyroid neoplasia[M]// Kronenberg HM, Melmed S, Larsen PR, et al. WilliamsTextbook of Endocrinology. Philadelphia: WB Saunders, 2003: 457-490.
[2] Gharib H, Papini E, Paschke R, et al. American Association of Clinical Endocrinologists, Associazione Medici Endocrinologi, And European Thyroid Association medical guidelines for clinical practice for the diagnosis and management of thyroid nodules executive summary of recommendations[J]. Endocr Pract, 2010, 16(3): 468-475.
[3] American Thyroid Association (ATA) Guidelines Taskforce on Thyroid Nodules and Differentiated Thyroid Cancer, Cooper DS, Doherty G, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer[J]. Thyroid, 2009, 19(11): 1167-1214.
[4] Hegedüs L. Clinical practice. The thyroid nodule[J]. N Engl J Med, 2004, 351(17): 1764-1771.
[5] Baskin HJ. Thyroid ultrasound and ultrasound-guided FNA biopsy[M]. Boston: Kluwer Academic Publishers, 2000: 71-86.
[6] Shetty SK, Maher MM, Hahn PF, et al. Significance of incidental thyroid lesions detected on CT: correlation among CT, sonography,and pathology[J]. Am J Roentgenol, 2006, 187(5): 1349-1356.
[7] 关志伟, 徐白萱, 陈英茂, 等. 大规模人群FDG PET/CT意外发现甲状腺高代谢结节的回顾性分析[J]. 中华核医学与分子影像杂志, 2012, 32(1): 32-35.
[8] Noguchi S, Yamashita H, Uchino S, et al. Papillary microcarcinoma[J]. World J Surg, 2008, 32(5): 747-753.
[9] Carmeci C, Jeffrey RB, McDougall IR, et al. Ultrasoundguided fine-needle aspiration biopsy of thyroid masses[J]. Thyroid, 1998, 8(4): 283-289.
[10] Fiore E, Vitti P. Serum TSH and risk of papillary thyroid cancer in nodular thyroid disease[J]. J Clin Endocrinol Metab, 2012, 97(4): 1134-1145.
[11] Gagel RF, Hoff AO, Cote GJ. Medullary thyroid carcinoma[M]// Braverman LE, Utiger RD, eds. Werner and Ingbars the thyroid. Lippincott Williams and Wilkins, Philadelphia, 2005: 967-988.
[12] Hegedüs L. Clinical practice. The thyroid nodule[J]. N Engl J Med, 2004, 351(17): 1764-1771.
[13] Ross DS. Radioiodine therapy for hyperthyroidism[J]. N Engl J Med, 2011, 364(6): 542-550.
[14] Raab SS, Silverman JF, Elsheikh TM, et al. Pediatric thyroid nodules: disease demographics and clinical management as determined by fine needle aspiration biopsy[J]. Pediatrics, 1995, 95(1): 46-49.
[15] Rachmiel M, Charron M, Gupta A, et al. Evidence-based review of treatment and follow up of pediatric patients with differentiated thyroid carcinoma[J]. J Pediatr Endocrinol Metab, 2006, 19(12): 1377-1393.
[16] American Thyroid Association Guidelines Task Force, Kloos RT, Eng C, et al. Medullary thyroid cancer: management guidelines of the American Thyroid Association[J]. Thyroid, 2009, 19(6): 565-612.
[17] American Thyroid Association (ATA) Guidelines Taskforce on Thyroid Nodules and Differentiated Thyroid Cancer, Cooper DS, Doherty GM, et al. Revised American Thyroid Association management guidelines for patients with thyroid nodules and differentiated thyroid cancer[J]. Thyroid, 2009, 19(11): 1167-1214.
[18] Jarzab B, Handkiewicz-Junak D, Wloch J. Juvenile differentiated thyroid carcinoma and the role of radioiodine in its treatment: a qualitative review[J]. Endocr Relat Cancer, 2005, 12(4): 773-803.
[19] Brabant G. Thyrotropin suppressive therapy in thyroid carcinoma: what are the targets?[J]. J Clin Endocrinol Metab, 2008, 93(4): 1167-1169.
[20] Biondi B, Filetti S, Schlumberger M. Thyroid-hormone therapy and thyroid cancer: a reassessment[J]. Nat Clin Pract Endocrinol Metab, 2005, 1(1): 32-40.
