苯甲羟肟酸浮选黑钨矿体系中铅离子的活化作用机理
2016-11-01高玉德钟传刚邱显扬冯其明
高玉德,钟传刚,邱显扬 ,冯其明,万 丽
苯甲羟肟酸浮选黑钨矿体系中铅离子的活化作用机理
高玉德1, 3,钟传刚1, 2, 3, 4,邱显扬1, 3,冯其明4,万 丽1
(1. 广州有色金属研究院,广州 510651;2. 万宝矿产有限公司,北京 100053;3. 稀有金属分离与综合利用国家重点实验室,广州 510651;4. 中南大学资源加工与生物工程学院,长沙 410083)
通过浮选实验、吸附量测定、红外光谱分析、XPS测试和浮选溶液化学计算研究Pb2+活化苯甲羟肟酸浮选黑钨矿作用机理。结果表明:Pb2+可明显活化苯甲羟肟酸浮选黑钨矿,pH值为6~10时,黑钨矿都保持较好的可浮性,pH值为9时浮选回收率最高;Pb2+促进苯甲羟肟酸在黑钨矿表面的吸附,且很好地符合Freundlich吸附等温方程;黑钨矿表面主要活性质点为Mn2+;pH值为9时Mn2+的主要存在形式是界面氢氧化锰沉淀,苯甲羟肟酸与之发生“O,O”螯合生成羟肟酸金属盐。
苯甲羟肟酸;黑钨矿;铅离子;浮选;活化机理
氧化矿浮选作业中,通常需要加入某种特定的金属离子,以获得良好的作业指标,关于其活化矿物浮选机理一直是矿物加工学者的研究重点[1−4]。早在1965年,FUERSTENAU等[5]研究了不同金属离子活化黄药浮选石英的机理,发现最佳活化pH值与金属离子−羟基络合物生成量最大的pH值相一致,由此提出金属离子其活化作用的主要成分是一羟基络合物。考虑到金属羟基络合物生成量最大的pH值往往对应氢氧化物沉淀的pH值,且产生的pH值范围窄,组分含量较低,达不到浮选有效浓度,加之金属离子在界面区域的性质与其在溶液中的性质存在较大的差异性,ANANTHAPADMANABHAN等[6]、胡岳华等[7]提出金属氢氧化物表面沉淀物是金属离子在矿物表面吸附并起浮选活化作用的有效成分。
生产实践表明Pb2+是黑钨矿[8]、白钨矿[9]、锡石[10]等多种氧化矿浮选的有效活化剂,其活化机理一直是研究的热点。与白钨矿、锡石相比,黑钨矿表面存在着Fe2+、Mn2+两种阳离子,经Pb2+作用后,表面性质同时存在着3种阳离子质点,且三者均可能与捕收剂反应,其活化黑钨矿的浮选机理会更加复杂。
苯甲羟肟酸(以下简称BHA)作为黑钨矿浮选新型螯合高效捕收剂,浮选过程中必须添加Pb2+才能起到良好的效果[11]。而关于Pb2+活化BHA浮选黑钨矿机理,迄今没有文献系统地报道其活化机理。本文作者通过研究Pb2+对黑钨矿可浮性及BHA在黑钨矿表面吸附行为的影响,运用红外光谱和XPS等分析手段,综合考虑界面区域内金属离子的特殊性质,较为系统地研究了Pb2+活化苯甲羟肟酸浮选黑钨矿作用机理。
1 实验
1.1 实验原料
黑钨矿取自江西西华山钨矿,人工挑出大块黑钨矿,并使用瓷磨机磨至约43 µm,反复淘洗、干式磁选得到黑钨矿单矿物,经化学分析含WO371.64%、Mn 8.24%、Fe 12.92%。
苯甲羟肟酸取自中南大学化工冶金研究所,纯度>90%,为白色晶体,分子结构式见图1。实验所用硝酸铅、氯化铁、硫酸亚铁、氯化锰以及pH调整剂(盐酸、氢氧化钠)等试剂为分析纯。实验所用水为一次蒸馏水。

图1 苯甲羟肟酸分子结构式
1.2 浮选实验
浮选实验是在容积为40 mL的XFG型挂槽式浮选机上进行,每次实验矿量为2.00 g,浮选温度为15 ℃,浮选实验流程图见图2。使用PHS-3C型精密pH计测pH值后开始浮选,浮选时间为5 min,浮选过程采用人工刮泡。浮选结束后浮选精矿(泡沫产品)与尾矿(槽底产品)分别过滤、烘干、称量,采用式(1)计算回收率。
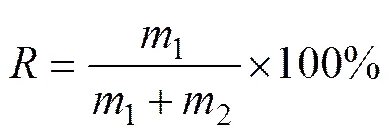
式中:1为泡沫产品质量,g;2为槽底产品质量,g;为回收率,%。

图2 浮选实验流程图
1.3 吸附量测试
吸附量测试是在岛津UV2600/2700型紫外可见分光光度计上进行。根据陈远道等[12]的研究,BHA在0.1mol/L HCL介质中,在紫外可见光区存在着明显吸收峰。本实验中通过全波谱扫描,确定波长为228.4nm时,BHA浓度与吸光度存在着良好的线性关系,符合朗伯−比尔定律,所得线性方程为
=0.06369+0.06254,2=0.99915 (2)
式中:为吸光度,%;为BHA浓度,mg/L。
实验步骤为称取1g黑钨矿单矿物倒入锥形瓶中,加入适量蒸馏水、pH调整剂以及浮选药剂,在SHZ−82型气浴恒温振荡器振荡8h,使其吸附达到平衡,用PHS-3C型精密pH计测定pH后将矿浆离心15min,离心机转速为8000 r/min,抽取上层清液,在0.1mol/L HCL介质中进行吸光度测试,根据式(2)计算出残余浓度。根据式(3)计算药剂在矿物表面的吸附量:

式中:为药剂的吸附量,mg/g;0为BHA初始浓度,mg/L;为BHA残余浓度,mg/L;为药剂溶液的体积,mL;为矿物的重量,g。
1.4 红外光谱测试与光电子能谱测试(XPS)
使用玛瑙研磨将矿物磨至2 µm以下。称取2 g矿物加入浮选槽中,调节pH后加入适量金属离子及BHA,搅拌过程中通过滴加pH调整剂使矿浆pH始终保持在pH=9左右,搅拌30 min后过滤,并用相同pH值的蒸馏水冲洗矿物两次,所得样品用真空干燥箱烘干,烘箱温度25 ℃,烘干后送红外光谱测试。制取羟肟酸金属盐的方法为称取适量金属盐,溶解于BHA溶液中,调节pH=9,此时溶液中析出沉淀,过滤、洗涤、真空干燥。红外光谱在Nicolet FTIR-740 型傅里叶变换红外光谱仪上采用溴化钾压片法进行红外测试,波数范围为4000~400 cm−1。
光电子能谱测试所用矿样为浮选矿样(43 µm以下),称取2 g矿样加入浮选槽中,调节pH后按浮选实验流程加入药剂,作用时间延长至30 min,搅拌过程中维持矿浆pH为pH=9±0.3,然后将矿浆倒入离心管中,离心两次,离心机转速为3500 r/min,每次离心时间为15 min,离心结束后过滤,使用相同pH的蒸馏水冲洗两次,所得矿样用真空干燥箱烘干,烘箱温度25 ℃,烘干后送光电子能谱测试。仪器型号为K-Alpha 1063,采用铝K微聚集单色器做X射线源,工作电压12 kV,分析室真空度为1×10−7Pa,仪器分辨率为0.5 eV,误差范围在±0.2 eV。
2 结果与讨论
2.1 实验结果
图3所示为矿浆pH值与矿物回收率的关系。从图3可以看出,不添加金属离子,黑钨矿几乎不能被BHA浮选,Fe3+、Fe2+、Mn2+等对BHA浮选黑钨矿的影响有限,唯独Pb2+能明显活化黑钨矿浮选,当pH值为6~10时,黑钨矿都保持了较好的可浮性,最高浮选回收率达95.58%。

图3 矿浆pH值与黑钨矿浮选回收率的关系
2.2 活化机理
2.2.1 药剂在矿物表面的吸附
图4所示为BHA在矿物表面的吸附量与pH值的关系。从图4可以看出,Pb2+对BHA在矿物表面的吸附有明显的影响:不添加Pb2+,BHA在黑钨矿表面吸附量少,此时矿物可浮性、疏水性差,与浮选实验结果一致;加入1×10−4mol/L Pb2+,BHA在矿物表面的吸附量急剧增加,在pH为6~10,BHA在矿物表面的吸附量均较大,与浮选最佳浮选pH区间吻合,并且吸附量在pH=9附近达到最大值。

图4 BHA在矿物的吸附量与pH值的关系
图5所示为对数坐标下,pH=9时BHA在黑钨矿表面的吸附等温线。从图5可以看出,对数坐标下,BHA在黑钨矿表面的吸附量与BHA浓度呈线性关系,符合Freundlich吸附方程,吸附方程为:
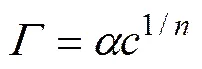
式中:、为常数,分别为在对数坐标下的截距和斜率的倒数。本次实验中测得、分别为6.33×10−4、0.732。

图5 BHA在矿物表面的吸附等温线
根据FUERSTENAU等[13]、胡岳华等[14]的研究,当药剂在矿物表面的吸附符合Freundlich吸附方程时,药剂通常在矿物表面发生了分子−离子共吸附,呈不均匀的多层分布。
2.2.2 红外光谱测试
图6所示为BHA的红外光谱图。图6中3293.8 cm−1是N—H和O—H伸缩振动峰相互叠加的结果,是羟肟酸的特征峰。3062.4 cm−1是N—H基伸缩振动峰,1608.3 cm−1是C=N伸缩振动吸收峰,也可认为是羰基的C=O伸缩振动吸收峰。由于共轭效应,在1571.1 cm−1、1490.7 cm−1、1456.0 cm−1出现苯环骨架特征峰。1074.1 cm−1、1045.2 cm−1、1022.1 cm−1为 N—O振动分裂的3个吸收峰,1162.9 cm−1为C—N伸缩振动峰[15]。

图6 BHA的红外光谱
图7所示为苯甲羟肟酸铅盐、铁盐、锰盐的红外光谱。

图7 羟肟酸金属盐的红外光谱
盐类的红外光谱特征峰主要是酸根的特征,金属离子质量大小只能使波峰的波数有所偏移[16]。图7所示为Pb(BHA)2的红外光谱。在图7中,C=O的吸收峰从1608.3 cm−1移到1598.8 cm−1,苯环骨架振动的3个峰分别在1561.8 cm−1、1483.0 cm−1、1436.7 cm−1,C—N振动峰由1162.9 cm−1移至1153.3 cm−1。与羟肟酸铅盐的红外光谱图类似,羟肟酸铁盐、锰盐的红外光谱图中这些官能团的振动峰发生不同程度偏移。这就表明,当羟肟酸在矿物表面吸附时,3种金属阳离子质点均可作为活性质点与之反应。
图8所示为黑钨矿被Pb2+和BHA处理前后的红外光谱。
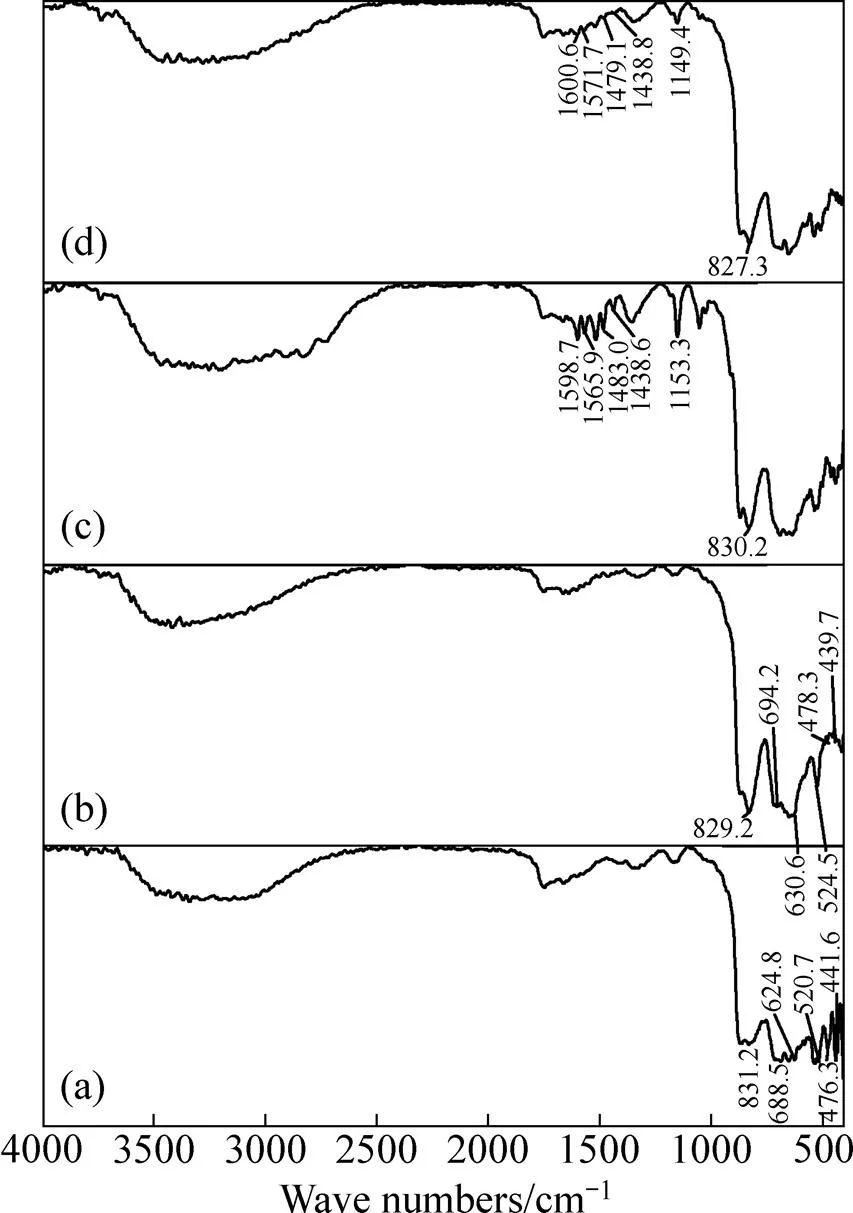
图8 黑钨矿与药剂作用前后的红外光谱
图8(a)所示为黑钨矿红外光谱,在831.2 cm−1有一个强而宽,尖而明显的吸收峰,这是黑钨矿中[WO6]聚合八面体特征吸收峰,688.5 cm−1、624.8 cm−1、520.7 cm−1、476.3 cm−1、441.6 cm−1等强度不等的吸收峰是Fe2+与Mn2+呈类质同象共同参与的振动吸收峰[17];黑钨矿被Pb2+处理后的红外光谱(见图8(b))基本上没有改变,[WO6]聚合八面体特征吸收峰在829.2 cm−1;黑钨矿被Pb2+和BHA共同处理后的红外光谱(见图8(c))可以看作是黑钨矿的红外光谱图与羟肟酸金属盐的红外光谱图的叠加,830.2 cm−1是黑钨矿[WO6]聚合八面体特征吸收峰,C=O的吸收峰在1598.7 cm−1,苯环骨架振动的3个峰分别在1565.9 cm−1、1483.0 cm−1、1438.6 cm−1,C—N的吸收峰1153.3 cm−1,这表明BHA在矿物表面发生了化学吸附,生成了羟肟酸金属盐,但由于羟肟酸金属盐的特征吸收峰相差不大,因而不能根据红外结果判断矿物表面的活性质点。黑钨矿被BHA处理后的红外光谱(见图8(d))也存在着C=O、苯环、C—N的吸收峰,但这些吸收峰强度低,不明显,表明不添加Pb2+时BHA在矿物表面的吸附强度较弱。
2.2.3 黑钨矿表面活性质点
已有关于黑钨矿表面与药剂作用的活性质点的研究,研究者们得出了不同的结论。胡岳华等[14]通过红外分析及溶液化学分析认为黑钨矿表面Mn的活性较高,而叶志平[18]通过量子化学计算,从配合物的晶体场稳定化能论证黑钨矿表面的Fe2+能与羟肟酸形成更稳定的产物,是与苯甲羟肟酸作用的主要活性组分。本文作者采用XPS测试技术,通过比较与药剂作用前后黑钨矿表面原子的电子结合能的变化来讨论黑钨矿表面活性质点,测试结果分别见表1~3。

表1 BHA作用前后黑钨矿表面W4f、Pb4f、Fe2p、Mn2p、O1s结合能的变化

表2 Pb2+和 BHA作用前后黑钨矿表面W4f、Pb4f、Fe2p、Mn2p、O1s结合能变化

表3 与黑钨矿作用前后BHA的O1s、N1s结合能的变化
从表1可以看出,经BHA作用后,黑钨矿表面Pb、Mn、Fe等原子的电子结合能变化极小,表明BHA在黑钨矿表面的作用不够强烈,不足以改变原子的化学环境,这是与红外结果相符的。从表2可以看出,Pb2+作用后,黑钨矿表面W、Pb原子的电子结合能位移相对较小(仪器误差为0.2 eV),Mn2p的结合能向高能量方向移0.68 eV,Fe2p的结合能向低结合能方向移0.2 eV,二者价电子位移显著,表明Mn、Fe的化学环境发生了改变,这正是Pb2+在黑钨矿表面化学吸附的结果;矿物经Pb2++BHA处理后,与单独被Pb2+作用相比,Mn2p结合能比作用铅向低结合能方向分别移动1.05 eV,结合能变化显著,而Fe2p、Pb4f电子结合能偏移极小,仅为−0.02 eV、0.01 eV,这表明此时与BHA作用的矿物表面活性质点主要为Mn质点。从表3可以看出,无论黑钨矿是否预先用Pb2+处理与否,BHA与之作用后,N1s、O1s电子结合能均发生偏移,但N1s电子结合能偏移均小于0.2 eV,O1s电子结合能偏移更为明显,远大于0.2 eV,这表明BHA与矿物表面阳离子质点发生“O,O”螯合,生成稳定的五元环螯合物,这与已有的研究是相符的[19]。
2.2.4 浮选溶液化学研究
图9所示为1×10−4mol/L Mn2+的水解组分的浓度对数图。

图9 锰离子水解组分的浓度对数图(Mn2+浓度为1×10−3 mol/L)
从图9中可以看出,当pH=9.73左右时,溶液中开始析出氢氧化锰沉淀。但是,在界面区域,由于电场的存在,介质的介电常数远低于溶液的介电常数,金属离子在溶液中和界面区域形成的氢氧化物沉淀的条件存在区别,相应的溶度积数据也不一样。根据王淀佐等[20]的研究,氢氧化锰在界面区域的浓度积将小于其在溶液中的溶度积,二者之间的关系为:

因而,根据溶液化学计算,在不考虑界面区域金属离子浓度与溶液中金属浓度间的差异的前提下(界面金属离子的浓度远大于溶液中金属离子的浓度,这也会导致在更低的pH时析出沉淀)界面区域内析出氢氧化锰沉淀的pH=8.91。因此,在pH=9时,在黑钨矿表面已经析出氢氧化锰沉淀。
3 结论
1) Pb2+可明显活化黑钨矿浮选,Pb2+用量为1×10−4mol/L,BHA用量100 mg/L时,黑钨矿在pH为6~10范围内都保持了很好的可浮性,pH=9时浮选回收率最高,达95.58%。
2) Pb2+化学吸附于矿物表面,促进了BHA在矿物表面的吸附,符合Freundlich吸附方程,表明BHA在矿物表面发生了分子—离子共吸附,主要为化学吸附,形成不均匀多层吸附。
3) XPS测试结果表明,Pb2+主要通过改变Mn、Fe等原子的化学环境,提高二者与BHA反应的活性来活化黑钨矿浮选,矿物表面Mn质点是主要活性质点,溶液化学计算表明活性组分为表面氢氧化锰沉淀,BHA主要与之发生“O,O”螯合,生成稳定的五元环螯合物。
REFERENCES
[1] 朱阳戈, 张国范, 冯其明, 卢毅屏,欧乐明. 微细粒钛铁矿的自载体浮选[J]. 中国有色金属学报, 2009, 19(3): 554−560.ZHU Yang-ge, ZHANG Guo-fan, FENG Qi-ming, LU Yi-ping, OU Le-ming. Autogenous-carrier flotation of fine ilmenite[J]. The Chinese Journal of Nonferrous Metals, 2009, 19(3): 554−560.
[2] 曹 钊, 张亚辉, 孙传尧, 曹永丹. 铜镍硫化矿浮选中Cu(Ⅱ)和Ni(Ⅱ)离子对蛇纹石的活化机理[J]. 中国有色金属学报, 2014, 24(2): 506−510. CAO Zhao, ZHANG Ya-hui, SUN Chuan-yao, CAO Yong-dan. Activation mechanism of serpentine by Cu(Ⅱ) and Ni(Ⅱ) ions in copper-nickel sulfide ore flotation[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(2): 506−510.
[3] ZHANG Jie, WANG Wei-qing, LIU Jing, HUANG Yang, FENG Qi-ming, ZHAO Hong. Fe (III) as an activator for the flotation of spodumene, albite, and quartz minerals[J]. Minerals Engineering, 2014, 61: 16−22.
[4] 冯其明, 赵岩森, 张国范. 油酸钠在赤铁矿及磷灰石表面的吸附机理[J]. 中国有色金属学报, 2012, 22(10): 2902−2907.FENG Qiming, ZHAO Yansen, ZHANG Guofan [J]. The Chinese Journal of Nonferrous Metals, 2012, 22(10): 2902−2907.
[5] FUERSTENAU M C, MILLER J D, PRAY R E, PERINNE B F. Metal ion activation in xanthate flotation of quartz[J]. Trans SME/AIME, 1965, 232: 359−364.
[6] ANANTHAPADMANABHAN K P, SOMASUNDARAN P. Surface precipitation of inorganics and surfactants and its role in adsorption and flotation[J]. Colloids and Surfaces, 1985(13): 151−167.
[7] 胡岳华, 王淀佐. 金属离子在氧化物矿物/水界面的吸附及浮选活化机理[J]. 中南矿冶学院学报, 1987, 18(5): 501-508, 590−591. HU Yue-hua, WANG Dian-zuo. Mechanism of adsorption and activation flotation of metallic ion on oxide mineral-water interface[J]. Journal of Central South Institute of Mining and Metallurgy, 1987, 18(5): 501-508, 590−591.
[8] Meng Qing-you, Feng Qi-ming, Shi Qing, OU Le-ming. Studies on interaction mechanism of fine wolframite with octyl hydroxamic acid[J]. Minerals Engineering, 2015, 79: 133−138.
[9] 高玉德, 邱显扬, 韩兆元. 羟肟酸浮选白钨矿的机理[J]. 中国有色金属学报, 2015, 25(5): 1339−1344.GAO Yu-de, QIU Xian-yang, HAN Zhao-yuan. Flotation mechanism of scheelite with hydroxamic acid[J]. The Chinese Journal of Nonferrous Metals, 2015, 25(5): 1339−1344.
[10] LI Fang-xu, ZHONG Hong, ZHAO Gang, WANG Shuai, LIU Guang-yi. Flotation performances and adsorption mechanism of-hydroxyoctyl phosphinic acid to cassiterite[J]. Applied Surface Science, 2015, 353: 856−864.
[11] 黄建平, 钟 宏, 邱显杨, 王 帅, 赵 刚, 高玉德, 戴子林, 刘广义. 环己甲基羟肟酸对黑钨矿的浮选行为与吸附机理[J]. 中国有色金属学报, 2013, 23(7): 2033−2039.HUANG Jian-ping, ZHONG Hong, QIU Xian-yang, WANG Shuai, ZHAO Gang, GAO Yu-de, DAI Zi-lin, LIU Guang-yi. Flotation behavior and adsorption mechanism of cyclohexyl hydroxamic acid to wolframite[J]. The Chinese Journal of Nonferrous Metals, 2013, 23(7): 2033−2039.
[12] 陈远道, 刘国全, 何旭元,胡 霞. 水溶液中苯甲羟肟酸含量的紫外光度测定法[J]. 湖南文理学院学报(自然科学版), 2008(2): 46−48. CHEN Yuan-dao, LIU Guo-quan, HE Xun-yuan, HU Xia.Determination of benzohydroxamic acid by ultraviolet spectrophotometry in aqueous solution[J]. Journal of Hunan University of Arts and Science (Science and Technology), 2008(2): 46−48.
[13] FUERSTENAU D W, PRADIP. Mineral flotation with hydroxamate collectors[M]. London: I.M.M, 1984: 161−168.
[14] HU Yue-hua, WANG Dian-zuo, XU Zheng-he. A study of interactions and flotation of wolframite with octyl hydroxamate[J]. Minerals Engineering, 1997, 10(6): 623−633.
[15] 付广钦. 细粒级黑钨矿的浮选工艺及浮选药剂的研究[D]. 长沙: 中南大学, 2010: 59−62.FU Guang-qin. Study on flotation process and reagent of fine wolframite[D]. Changsha: Central South University, 2010: 59−62.
[16] 赵景云, 朱建光. BHA浮选硫酸铅试验[J]. 有色金属(选矿部分), 1992(1): 26−29.ZHAO Jing-yun, ZHU Jian-guang. Flotation test of lead sulfate with BHA as collector[J]. Nonferrous Metals (Mineral Processing), 1992(1): 26−29.
[17] 周佩玲. 赣南钨矿床中黑钨矿和白钨矿的红外光谱[J]. 矿物学报,1984(4): 12−20.ZHOU Pei-ling. Infrared spectra of wolframite and scheelite from tungsten ore deposits in southern Ganzhou in Jiangxi province[J]. Acta Mineralogica Sinica, 1984(4): 12−20.
[18] 叶志平. 苯甲羟肟酸对黑钨矿的捕收机理探讨[J]. 有色金属(选矿部分), 2000(5): 35−39. YE Zhi-ping. The mechanism of benzohydroxamic acid as collector of wolframite[J]. Nonferrous Metals (Mieral Processing), 2000(5): 35−39.
[19] 唐 清, 钟 宏, 王 帅, 彭 静. 羟肟酸类化合物的合成与应用研究进展[J]. 化工进展, 2014, 33(3): 703−709.TANG Qing, ZHONG Hong, WANG Shuai, PENG Jing. Research progress on the synthesis and application of hydroxamic acid compounds[J]. Chemical Industry and Engineering Progress, 2014, 33(3): 703−709.
[20] 王淀佐,胡岳华. 浮选溶液化学[M]. 长沙: 湖南科学技术出版社, 1988: 141−143.WANG Dian-zuo, HU Yue-hua. Solution chemistry of flotation[M]. Changsha: Hunan Press of Science and Technology, 1988: 141−143.
Activation mechanism of Pb2+in flotation of wolframite with benzohydroxamic acid as collector
GAO Yu-de1, 3, ZHONG Chuan-gang1, 2, 3, 4, QIU Xian-yang1, 3, FENG Qi-ming4, WAN Li1
(1. Guangzhou Research Institute of Non-ferrous Metals, Guangzhou 510651, China;2. Wanbao Mining Limited, Beijing 100053, China;3. State Key Laboratory of Rare Metals Separation and Comprehensive Utilization, Guangzhou 510651, China;4. School of Resources Processing and Bioengineering, Central South University, Changsha 410083, China)
The activation mechanism of Pb2+in flotation of wolframite with benzohydroxamic acid as collector was studied through flotation test, adsorptive capacity, IR spectroscopy, XPS study and flotation chemistry calculation. The results show that Pb2+can increase the floatability of wolframite and the optimum pH region is 6−10, the floatation recovery rate reaches maximum when pH=9; the adsorption test shows Pb2+can promote the adsorption of benzohydroxamic acid onto the surface of wolframite, and the adsorption isotherm obeys Freundlich equation quite well; tthe result of XPS study shows the main activity of species is Mn2+, and the floatation chemistry reveals the majority of Mn2+exists as surface manganese hydroxide; two oxygen atoms from hydroxamate anion chelate manganese hydroxide on the surface of wolframite and form five- chain complex.
benzohydroxamic acid; wolframite; Pb2+; flotation; activation mechanism
Project(2010CB735500) supported by the Major State Basic Research Development Program of China; Project(2011A080403007) supported by Major Science and Technology Program of Guangdong Province, China
2015-07-09; Accepted date:2016-04-08
GAO Yu-de; Tel: +86-13826287656; E-mail: ydgao948@163.com
1004-0609(2016)-09-1999-08
TD923;TD952
A
国家重点基础研究发展计划资助项目(2010CB735500);广东省重大科技专项(2011A080403007)
2015-07-09;
2016-04-08
高玉德,教授级高级工程师;电话:13826287656;E-mail:ydgao948@163.com
(编辑 王 超)
