疏基乙酸改性花生壳对铜、锌、铅的吸附性能研究
2016-10-31黄冬兰王超凡
黄冬兰,王 齐,王超凡
(韶关学院化学与环境工程学院,广东韶关 512005)
疏基乙酸改性花生壳对铜、锌、铅的吸附性能研究
黄冬兰,王齐,王超凡
(韶关学院化学与环境工程学院,广东韶关 512005)
以废弃花生壳(PS)为原料,利用疏基乙酸对其进行改性制得新型的花生壳生物吸附剂(MPS),研究其对重金属离子Cu2+、Zn2+、Pb2+的吸附性能,并考察了溶液pH、吸附温度、吸附时间和金属离子初始浓度对MPS吸附性能的影响。通过测定化学需氧量(COD)、傅里叶红外光谱图(FTIR)和扫描电镜(SEM)对改性前后花生壳粉进行结构表征。结果表明,Cu2+、Zn2+、Pb2+在改性花生壳上的吸附速率快,40 min基本达到吸附平衡,吸附过程均符合准二级动力学方程。MPS对Cu2+、Zn2+、Pb2+的吸附等温线用Langmuir方程拟合的相关系数分别为0.9724,0.9733和0.9501,优于Freundlich方程的拟合结果,表明吸附均为单分子层吸附。MPS对Cu2+、Zn2+、Pb2+的饱和吸附量分别为37.88、44.84、125.0 mg/g,均高于未改性花生壳。改性后的花生壳生物吸附剂对于Cu2+、Zn2+、Pb2+的吸附可以再生重复使用至少10次。因此,巯基乙酸改性制得的花生壳吸附剂对铜、锌、铅有良好的吸附性能。
改性花生壳,吸附,重金属,解吸附
当前,重金属离子是主要的污染物之一,它不仅不利于水生生物的生长,还会通过生物链富集进入人体,进而严重威胁人体健康,因此,重金属废水的处理已引起全世界的普遍重视。去除水中重金属离子的方法有很多,传统的方法主要有化学沉淀法、离子交换法、电解法、膜分离法等[1]。离子交换法、电解法和膜分离法处理成本高,沉淀法虽然成本较低但会产生二次污染。近年来,农林废弃物作为吸附剂去除水中重金属广泛引起了研究者的关注,香蕉皮、稻壳、竹粉和白果壳等农林废弃物经过化学改性可制得吸附性能良好的生物吸附剂[2-5]。
花生是我国主要油料作物和经济作物之一,截至2013年,花生的种植面积达到4632.99千公顷,总产达1697.22万吨[6]。FAOSTAT(粮农组织总的统计数据库)显示,中国是世界上最大的花生生产国和消费国[6]。花生在加工过程中每年产生大量的花生壳,但花生壳一般仅用作燃料或直接作废物处理,利用率较低且造成环境污染。花生壳富含木质素、半纤维素和纤维素,三者约占花生壳质量的75%~80%[7],这些成分含有大量的羧基、羟基、氨基等活性基团,可以通过离子交换、螯合等方式吸附重金属离子,故对重金属离子具有很好的吸附潜能。但天然花生壳的功能团含量较少,吸附能力有限,必须通过化学改性来增加吸附金属离子能力强的活性基团,如羧基、羟基、酚羟基等,以提高其吸附能力[8]。本文以花生壳粉为原料,利用疏基乙酸对花生壳进行改性制得新型花生壳生物吸附剂(MPS),并研究其对重金属离子Cu2+、Zn2+、Pb2+的吸附性能。同时考察溶液pH、吸附温度、吸附时间和金属初始浓度等因素对吸附过程的影响,分析生物吸附动力学和等温方程,期望为改性花生壳生物吸附剂在工业废水处理中的应用提供理论依据。
1 材料与方法
1.1材料与仪器
试剂:Cu、Zn、Pb标准储备液(1 g/L)购自北京有色金属研究总院;HCl、乙醇、NaOH和巯基乙酸等均为分析纯,实验用水为超纯水。
实验用花生壳在韶关市曲江区马坝镇石堡村采摘新鲜花生,去花生米后,将花生壳置于清水中浸泡24 h,除去花生壳表面的灰土浮尘,再用蒸馏水多次冲洗至干净后,将其放在烘箱中于70 ℃烘干至恒重,粉碎过筛后过得100目筛,得到花生壳样品(PS)。
Nicolet iS10傅里叶变换红外光谱仪赛默飞世尔科技有限公司;AA-7000原子吸收分光光度计岛津国际贸易有限公司;JSM-6360LV 扫描电镜仪日本电子株式会社;恒温振荡器金坛市晶玻实验仪器厂;pHS-3C酸度计上海精密科学仪器有限公司;DFT-50中药粉碎机温岭市林大机械有限公司;LD-UPW超纯水机砾鼎水处理设备有限公司。
1.2改性花生壳生物吸附剂的制备
改性花生壳生物吸附剂的制备参照文献[9],取50 g粉碎后的花生壳(PS)于烧杯,加入250 mL无水乙醇和250 mL质量分数为1%的NaOH溶液,在室温下浸泡24 h,抽滤并用超纯水洗至pH接近中性,将乙醇-氢氧化钠改性的花生壳置于70 ℃左右的鼓风干燥箱中烘24 h,再取30 g乙醇-NaOH预处理的花生壳于烧杯中,用体积分数为1%的巯基乙酸1000 mL浸泡搅拌24 h,然后用超纯水洗至中性,抽滤,将疏基乙酸改性的花生壳于70 ℃左右的干燥箱中烘24 h。粉碎机粉碎后过100目筛,所得花生壳吸附剂简写为MPS。
1.3吸附实验
在水浴恒温振荡器中进行静态吸附实验[9]。分别在100 mL具塞锥形瓶中加入一定量的改性花生壳生物吸附剂及Cu2+、Zn2+、Pb2+标准溶液,调节溶液pH,密封瓶口以防实验过程中瓶内液体飞溅出来而使体积发生变化。将锥形瓶放入一定温度的水浴恒温振荡器中振荡吸附一定时间后过滤、定容。用火焰原子吸收分光光度计测定滤液中金属离子的平衡质量浓度。吸附量(q)和吸附率(Ra)计算式如下:
式(1)
式(2)
式中:V表示溶液体积(mL);ρ0和ρe分别表示Cu2+、Zn2+、Pb2+的初始质量浓度和平衡质量浓度(mg·L-1);m表示所用生物吸附剂的质量(mg)。
1.4数据处理
1.4.1吸附动力学计算方法在吸附动力学的研究中,通常用准二级动力学方程对实验数据进行模拟,分析重金属离子浓度随吸附时间的变化关系。若吸附过程遵循二级动力学方程,则其吸附速率被化学吸附所控制[10]。二级动力学方程[11]为:
式(3)
式中:qe-平衡时的吸附量,mg/g;qt-吸附时间为tmin时生物吸附剂对金属离子的吸附量,mg·g-1;k2-准二级动力学方程的速率常数,其单位为g·mg-1·min-1。
1.4.2等温吸附的计算方法在等温条件下,常用Langmuir[12]和Freundlich[13]方程表征吸附剂表面的吸附现象以及吸附量与溶液平衡浓度的关系。若吸附过程符合Langmuir等温吸附方程,则该吸附过程为单分子层吸附;反之,若吸附过程符合Freundlich等温吸附方程,则该吸附过程为多分子层吸附[14]。Langmui和Freundlich方程表达式如式(4)和式(5):
式(4)
式中:Ce-吸附平衡时溶液中剩余的金属离子的浓度,mg/L;qe-吸附平衡时吸附剂对金属离子的吸附量,mg/g;qm-吸附剂的最大理论吸附量,mg/g;b-Langmuir常数,L/mg。
式(5)
式中:KF-与吸附能有关的常数;n-与反应键能有关的常数。
2 结果与讨论
2.1化学需氧量
化学需氧量的测定参照国标GB11914-89[15]。步骤如下:在最佳吸附条件下,分别采用未改性花生壳PS和巯基改性花生壳MPS处理相同水样,过滤,参照国标GB11914-89中的重铬酸钾法测定水样的COD。测定结果如表1所示,改性后的花生壳吸附各金属离子溶液后的溶液与未改性的相比,COD明显降低,从而说明用改性的花生壳吸附各金属离子溶液后的溶液不会产生二次污染。
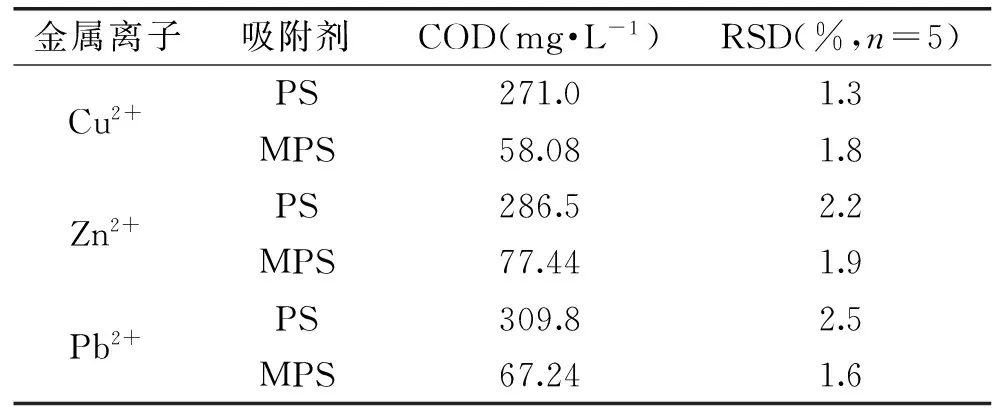
表1 改性前后溶液的COD(mg O2/L)
2.2改性前后花生壳的红外光谱比较
PS和MPS的红外光谱图如图1所示。PS主要成分有木质素、半纤维素和纤维素等。参考文献[16-19],对PS的光谱特征峰进行归属分析,3384 cm-1宽强峰为羟基(-OH)的伸缩振动吸收峰,2929 cm-1为甲基和亚甲基中C-H伸缩振动峰,1735 cm-1为羧基(-COOH)、酮羰基(-C=O)和酯羰基(-COOCH3)中C=O的伸缩振动峰,1635 cm-1和1424 cm-1为共轭羰基C=O的伸缩振动峰,1373 cm-1是C-H弯曲振动峰,1264 cm-1为脂肪酸族振动峰可能来自于羧酸和酚类化合物中C=O键的变形振动和-OH键的伸缩振动,1102、1056、1032 cm-1等则为糖苷类的C-O的伸缩振动峰。

图1 PS(a)和MPS(b)的红外光谱图Fig.1 FTIR spectra of PS(a)and MPS(b)
比较MPS和PS的红外光谱图可发现,天然花生壳经巯基乙酸改性后,结构发生了变化,譬如,天然花生壳的1735 cm-1羰基C=O峰经巯基乙酸改性后消失了,1635 cm-1共轭羰基C=O峰减弱且蓝移到了1646 cm-1波长处,1264 cm-1附近的脂肪酸振动峰蓝移到了1267 cm-1处,并在1229 cm-1处出现了明显的小峰,说明花生壳上的羟基与巯基乙酸发生反应生成了酯。MPS中1229、1157 cm-1分别为C=S和S-C-S的伸缩振动峰。进一步通过元素分析比较MPS和PS中硫的含量,发现PS为0.42%,而MPS为0.72%,这说明-SH已成功接到花生壳表面。
2.3扫描电镜分析
图2为PS和MPS的扫描电镜图。从图中可以看出:经巯基乙酸改性后的MPS的表面比未改性的PS变得更为粗糙、疏松、多孔,使得更多的活性官能团暴露在吸附剂表面,更有利于吸附过程的进行。

图2 PS(a)和MPS(b)的SEM图(×200)Fig.2 SEM images of PS(a)and MPS(b)(×200)
2.4溶液中初始pH对吸附效果的影响
图3所示为pH对MPS吸附Cu2+、Zn2+、Pb2+的影响。从图中可看出,Cu2+、Zn2+、Pb2+溶液的吸附率受pH的影响大,在pH为2.5时,Cu2+、Zn2+、Pb2+的溶液的吸附率均很低;pH<5.0时,随着pH的增加,吸附率也随着增大;当pH>5.0时,吸附趋于平衡,Cu2+、Zn2+、Pb2+最大吸附率分别为98.49%、98.49%、97.56%。这可能是因为当溶液pH较低时,溶液中的H+浓度较高,会与金属离子存在竞争吸附从而降低了对金属离子的吸附[20];而当pH较高时,溶液中OH-的浓度随之增加,金属离子将与OH-生成沉淀,这就会使吸附效果减弱。为了避免因pH太高使得各金属离子变成沉淀,因此实验pH确定为5.0。

图3 溶液中pH对MPS吸附离子的影响Fig.3 Effect of pH value on adsorption of heavy metals on MPS注:C(Cu2+)=50 mg/L,C(Zn2+)=25 mg/L,C(Pb2+)=150 mg/L,吸附剂量:0.05 g/10 mL,温度:30 ℃,时间:2 h。
2.5吸附温度对吸附效果的影响
图4所示为温度对MPH吸附Cu2+、Zn2+、Pb2+的影响。从图4可看出,温度对MPS吸附Pb2+溶液的吸附性能影响很小,在30~90 ℃温度范围内,吸附率均在95%以上,说明MPS吸附过程可能为化学吸附;而MPS对Cu2+的吸附率随着温度升高略有降低;但温度对MPS吸附Zn2+溶液的吸附性能影响较大,在30~90 ℃温度范围内,其吸附率从95.55%降为82.59%。这说明MPS对Cu2+、Zn2+的吸附可能是一种放热反应。因此,确定此后实验在30 ℃下进行。

图4 吸附温度对MPS吸附的影响Fig.4 Effect of temperature on adsorption of heavy metals on MPS注:C(C2+)=50 mg/L,C(Zn2+)=25 mg/L,C(Pb2+)=150 mg/L,吸附剂量:0.05 g/10 mL,pH=5.0,时间:2 h。
2.6吸附动力学
图5所示为30 ℃条件下吸附时间对MPS吸附Cu2+、Zn2+、Pb2+的影响。可以看出,MPS对Cu2+、Zn2+、Pb2+的吸附,在0~20 min内,吸附速率很快;随着时间增加,吸附率增大,在40 min时,吸附基本达到平衡,因此吸附时间为40 min。按式3对图6数据进行准二级动力学的模拟,结果如图6和表2所示。从表2实验的结果可以看出,各种金属的准二级动力学参数中的相关系数均为1,且qe理论值与实验值相差很小,这说明了吸附过程符合准二级动力学反应机理,且吸附速率受化学吸附所控制。

表2 MPS对Cu2+、Zn2+和Pb2+准二级动力学参数
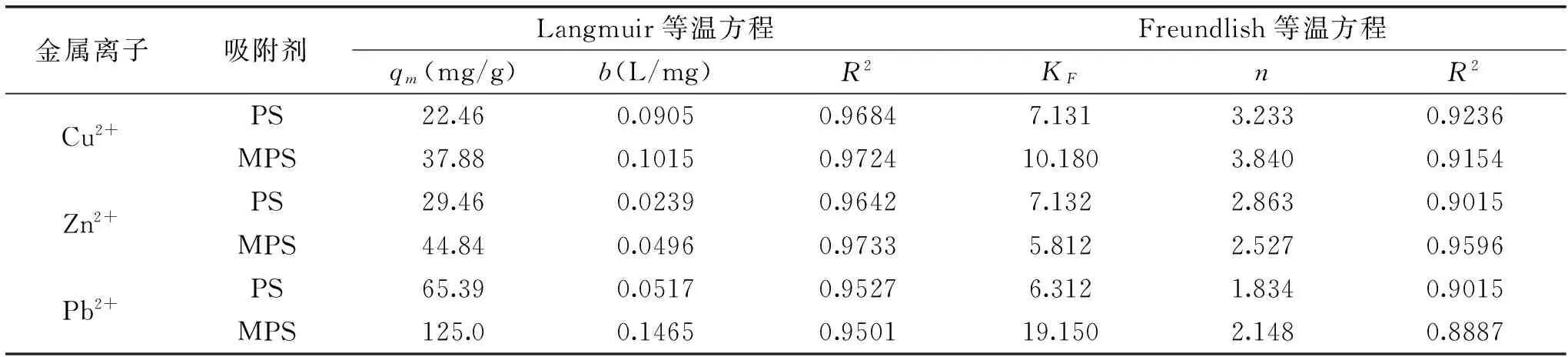
表3 PS和MPS吸附重金属的等温线参数

图5 时间对MPS吸附离子的影响Fig.5 Effect of time on adsorption of heavy metals on MPS注:C(Cu2+)=50 mg/L,C(Zn2+)=25 mg/L,C(Pb2+)=150 mg/L,吸附剂量:0.05 g/10 mL,温度:30 ℃,pH=5.0。

图6 MPS吸附重金属离子的准二级动力学图Fig.6 Pseudo-second-order plot
2.7吸附等温线
图7所示为MPS对Cu2+、Zn2+、Pb2+的吸附等温线。从图7可以看出,平衡吸附量是随着金属离子浓度的增大而增加。采用Langmuir(式4)和Freundlich(式5)吸附等温式对数据进行拟合,拟合结果的相关参数见表3。相比之下,Langmuir等温方程拟合线性关系更好,表明吸附过程均属于单分子层吸附。从表3还可看出,MPS对Cu2+、Zn2+、Pb2+的最大吸附容量分别为37.88、44.84、125.0 mg/g,高于PS对Cu2+、Zn2+、Pb2+的最大吸附容量22.46、29.46和65.39 mg/g,说明改性后的花生壳对金属离子的结合性增强。

表5 MPS对实际废水中Cu2+、Pb2+、Zn2+的去除结果

图7 MPS吸附各重金属离子的吸附等温线Fig.7 Adsorption isotherm of Cu2+,Zn2+and Pb2+ on MPS注:吸附剂量:0.05 g/10 mL,pH=5.0,温度:30 ℃,时间:40 min。
与其他农林废弃物生物吸附剂相比(见表4),MPS对重金属离子的吸附能力更强。MPS对Cu2+、Zn2+、Pb2+的吸附机理可用下式表示:
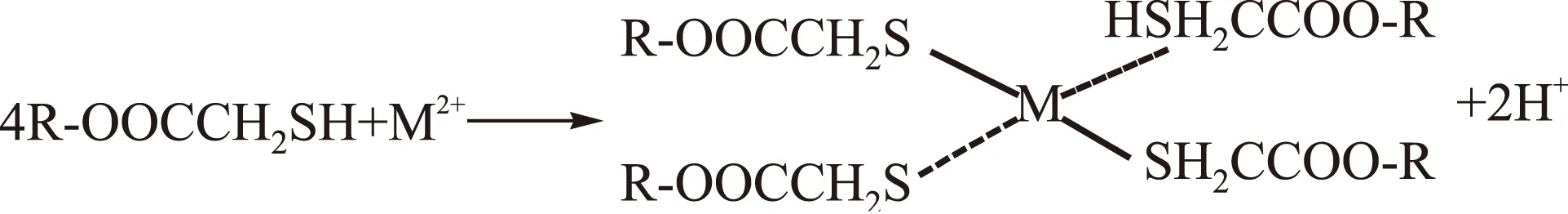
表4 不同吸附剂吸附能力的比较

吸附剂qm(mg/g)Cu2+Zn2+Pb2+文献稻谷壳10.908.1458.1[21]玉米淀粉8.586.8628.8[22]野燕麦22.9023.40111[23]玉米芯35.4610.2134.13[24]甜菜渣21.1617.7873.76[25]PS22.4629.4665.39本文MPS37.8844.84125.0本文
2.8吸附解吸附实验
为了实现改性花生壳重复利用,并且不造成改性花生壳的浪费和环境污染,用盐酸把所吸附的离子解析出来,就是用盐酸的H+把金属离子置换出来,把解析烘干的MPS对各金属离子再次吸附。从图8所示,经过10次吸附循环后,MPS对Cu2+、Zn2+、Pb2+的吸附率一直维持在94%、88%、94%以上,说明该生物吸附剂再生性能好,至少可重复使用10次。

图8 改性花生壳吸附对各重金属的循环吸附实验Fig.8 Adsorption-desorption cycles for MPS注:pH5.0, CCu(II)=50 mg/L,CZn(II)=25 mg/L,CPb(II)=150 mg/L,biosorbent dosage:0.05 g/10 mL,温度:30 ℃,吸附时间:40 min,解析时间:3 h。
2.9实际废水吸附实验
为了更好突显改性花生壳对各重金属的吸附效果,取韶关地区某冶炼厂的废水,用改性的花生壳对该废水进行吸附,加入吸附剂0.1 g,调节pH为5.0左右,于30 ℃下恒温振荡40 min,测定吸附后废水中Cu2+、Pb2+、Zn2+主要金属离子的含量。吸附后,废水中Cu2+、Pb2+、Zn2+的浓度均符合国家污水排放标准,结果见表5。
3 结论
以废弃花生壳为原料,利用疏基乙酸对花生壳进行改性,制成新型的吸附剂MPS,并研究了其对Cu2+、Zn2+、Pb2+的吸附特性。红外光谱和扫描电镜表征结果表明花生壳经巯基乙酸改性后比表面积增大,有效官能团增加,吸附性能增强。吸附实验结果表明,Cu2+、Zn2+、Pb2+在MPS的吸附过程可用准二级吸附动力学模型描述(R2=1)。在最优条件下,MPS对Cu2+、Zn2+、Pb2+的最大吸附容量分别为37.88、44.84、125.0 mg/g,高于PS对Cu2+、Zn2+、Pb2+的最大吸附容量22.46、29.46、65.39 mg/g。且吸附过程符合Langmuir等温方程,为单分子层吸附。改性花生壳对各重金属离子吸附均为化学吸附。该研究对丢弃的花生壳的有效综合利用与对含重金属的废水处理研究有参考的价值。
[1]佟玉衡,实用废水处理技术[M].北京:化学工业出版社,1998.
[2]Liu Z N,Liu Y M,Chen L,et al. Performance study of heavy metal ion adsorption onto microwave-activated banana peel[J]. Desalination and Water Treatment,2014,52:7117-7124.
[3]Yadav D,Kapur M,Kumar P,et al. Adsorptive removal of phosphate from aqueous solution using rice husk and fruit juice residue[J]. Process Safety Environmental protection,2015,(94):402-409.
[4]Alidoust D,Kawahigashi M,Yoshiwa S J,et al. Mechanism ofcadmium biosorption from aqueous solutions using calcined oyster shells[J].Journal of Environmental Management,2015,150:103-110.
[5]苏鹃,伍钧,杨刚,等. 改性白果壳对水溶液总重金属镉的吸附研究[J]. 农业环境科学学报,2014,33(6):1218-1225.
[6]张怡. 中国花生生产布局变化研究[D].北京:中国农业大学,2015.
[7]俞力家,李强,王天贵. 花生壳粉末活性炭成型工艺研究[J]. 化学工程师,2010,182(11):13-14,33.
[8]黄翔,宗浩,陈文祥,等. 花生壳对水溶液中铜离子的吸附特性[J]. 四川师范大学学报,2007,30(3):380-383.
[9]郭学益,梁莎,冯宁川,等. 巯基乙酸改性橘子皮对Cu2+的吸附性能[J]. 环境科学学报,2009,29(9):1905-1910.
[10]郭学益,梁莎,肖彩梅,等.MgCl2改性柑橘皮对水溶液中重金属离子的吸附性能[J].中国有色金属学报,2011,21(9):2270-2276.
[11]Ho Y S,Mckay G. The Kinetics of sorption of basic dyes from aqueous solution by sphagnum moss peat[J].Can J Chem Eng,1998,76(4):822-827.
[12]Langmuir I. The adsorption of gases on plane surfaces of glass,mica and platinum[J].Journal of American Chemistry Society,1981,40(9):1361-1403.
[13]Freunlich H M F. Uber die adsorption in Losungen[J]. Z Phys Chem,1906,57:385-470.
[14]孟启,舒斌斌,周峰,等.胺化聚苯乙烯树脂的制备及吸附对硝基酚[J]. 化工进展,2015,34(6):1714-1719.
[15]GB 11914-89,化学需氧量的测定-COD标准测定法[S].
[16]刘文霞,李佳昕,王俊丽,等. 改性泡桐树叶吸附剂对水中铅和镉的吸附特性[J]. 农业环境科学学报,2014,33(6):1226-1232.
[17]郭学益,肖彩梅,梁莎,等. 改性柿子粉吸附剂对Cd2+的吸附性能[J]. 中南大学学报,2012,43(2):412-416.
[18]苏鹃,伍钧,杨刚,等. 改性白果壳对水溶液总重金属镉的吸附研究[J]. 农业环境科学学报,2014,33(6):1218-1225.
[19]彭小明,傅大放,秦庆东. 竹炭表面改性对两种抗生素吸附性能的影响[J]. 东南大学学报,2014,44(6):1271-1276.
[20]Khormaei M,Nasemejad B,Edrisi M. Copper biosorption from aqueous solutions by sour orange residues[J]. Journal of Hazardous Materials,2007,149(2):269-274.
[21]Krishnani K K,Meng X,Christodoulatos C,et al. Biosorption mechanism of nine different heavy metals onto biomatrix from rice husk[J]. Journal of Hazardous Materials,2008,153(3):1222-1234.
[22]Kweon D K,Choi J K,Kim E K,et al. Adsorption of divalent metal ions by succinylated and oxidized corn starches[J]. Carbohydrate Polymer,2001,46(2):171-177.
[23]Areco M M,Saleh-Medina L,Trinelli M A,et al. Adsorption of Cu(II),Zn(II),Cd(II)and Pb(II)by dead Avena fatuabiomass and the effect of these metals on their growth[J]. Colloids and Surfaces B,2013,(110):305-312.
[24]Vaughan T,Seo C W,Marshall W E. Removal of selected metal ions from aqueous solution using modified cornbobs[J]. Bioresource Technology,2001,78(2):133-139.
[25]Reddad Z,Gernte C,Andres Y,et al. Adsorption of several metal ions onto a low-cost bisorbent:kinetic and equilibrium studies[J]. Environmental Science and Technology,2002,36(9):2067-2073.
Adsorption properties of Cu2+,Zn2+and Pb2+by mercapto-acetic acid modified peanut shell
HUANG Dong-lan,WANG Qi,WANG Chao-fan
(College of Chemistry and Environmental Engineering,Shaoguan University,Shaoguan 512005,China)
The peanut shell powder(PS)was used as raw material to prepare peanut shell biosorbent MPS by chemical modification with mercapto-acetic acid(C2H4O2S). The adsorption behavior of Cu2+,Zn2+and Pb2+in aqueous solution on MPS was investigated. The effects of solution pH,adsorption temperature,adsorption time and metal ion concentration were considered. In addition,the biosorbent was characterized by measuring Chemical Oxygen Demand(COD),Fourier transform infrared spectroscopy(FTIR)and scanning electron microscope(SEM).The results showed that the adsorption of Cu2+,Zn2+and Pb2+on MPS were rapid and can attain equilibrium with 40 min. Moreover,the dynamic adsorption data could be well fitted by pseudo-second order kinetics. The isothermal adsorption of Cu2+,Zn2+and Pb2+can well described by Langmuir models,and the correlation coefficients obtained from the Langmuir equations were 0.9724,0.9733 and 0.9501. Furthermore,the maximum adsorption capacities of Cu2+,Zn2+and Pb2+by MPS were 37.88,44.84,125.0 mg/g,respectively,which were higher than that of PS. The MPS could be recycled for ten times when it was used to adsorb Cu2+,Zn2+and Pb2+. Consequently,the adsorption properties of modified peanut shell biosorbent(MPS)for Cu2+,Zn2+and Pb2+were favorable.
modified peanut shell;adsorption;heavy metals;desorption
2016-03-01
黄冬兰(1983-),女,硕士,讲师,研究方向:从事环境分析化学研究,E-mail:lantern1227@163.com。
广东省教育厅特色创新项目(自然科学类)(2014KTSCX169);韶关学院校级科研项目(S201501028);2014年广东省大学生创新创业立项项目(201410576051)资助。
TS255
A
1002-0306(2016)17-0075-06
10.13386/j.issn1002-0306.2016.17.006
