替莫唑胺用于恶性神经胶质瘤术后化学治疗35例及安全性评价
2016-10-29任明亮王旭辉徐伦山
梁 鸿,任明亮,王旭辉,徐伦山
(中国人民解放军第三军医大学大坪医院野战外科研究所神经外科,重庆400042)
替莫唑胺用于恶性神经胶质瘤术后化学治疗35例及安全性评价
梁鸿,任明亮,王旭辉,徐伦山
(中国人民解放军第三军医大学大坪医院野战外科研究所神经外科,重庆400042)
目的观察替莫唑胺用于人恶性神经胶质瘤术后辅助化学治疗的疗效及安全性评估。方法选取2013年1月至2016年1月确诊为人恶性神经胶质瘤的患者35例,采用替莫唑胺进行化学治疗(简称化疗)并进行随访,记录比较临床疗效、治疗期间患者生存质量评分、不良反应发生情况。结果35例患者治疗结束后的客观有效率(ORR)和疾病控制率(DCR)分别为57.15%和80.01%;治疗前生存质量评分为(30.67±8.03)分,显著低于治疗后的(83.46±11.7)分;不良反应有厌食、便秘等消化道症状13例(37.14%),白细胞减少4例(11.43%),假性进展1例(2.86%)。结论替莫唑胺治疗恶性神经胶质瘤具有较好临床疗效,且不良反应少,患者生活质量可明显提高,是较为理想的恶性神经胶质瘤术后辅助化疗药物。
替莫唑胺;恶性神经胶质瘤;疗效;安全性
神经胶质瘤在颅肿瘤中最多见,肿瘤体积逐渐增大,形成颅内占位病变,使组织水肿加重,当超过代偿限度时即产生颅内压增高的一系列体征;当颅内压等于动脉压时,脑血流停止,血压下降,患者死亡[1]。目前,神经胶质瘤仍以手术治疗为主,但肿瘤往往呈浸润性生长,与脑组织无明显边界,除早期肿瘤小且位于适当位置外,一般主张综合治疗,即术后辅助以放射治疗、化学治疗(简称化疗)。替莫唑胺(TMZ)是一种新型的二代烷化剂-咪唑四嗪类衍生物,口服后会迅速吸收,生物利用度高,近100%,且具有广谱抗肿瘤活性;可不经过肝脏代谢,广泛分布于全身,可透过血脑屏障,顺利进入脑脊液,在中枢神经系统达到有效的药物浓度[2]。基于此,笔者将替莫唑胺用于恶性神经胶质瘤患者术后的辅助化疗,观察其疗效和不良反应发生情况,现报道如下。
1 资料与方法
1.1一般资料
选取2013年1月至2016年1月确诊为人恶性神经胶质瘤的患者35例,均经开颅术后病理证实为恶性神经胶质瘤。其中,患者男25例,女10例;年龄15~80岁,中位年龄47.5岁;肿瘤病理分型为胶质母细胞瘤20例,间变型星形细胞瘤9例,间变性少突胶质细胞瘤4例,间变型管膜瘤1例,髓母细胞瘤1例;肿瘤部位为大脑半球浅表22例,岛叶8例,丘脑3例,脑干2例。所有患者一般资料比较,无显著性差异(P>0.05),具有可比性。
1.2方法
所有患者空腹口服替莫唑胺胶囊(商品名蒂清,江苏天士力帝益药业有限公司,国药准字H20040637,规格为每粒50 mg)150~200 mg/(m2·d),连续5 d,28 d为1个疗程,治疗5个疗程。对患者治疗前、治疗结束时、治疗结束后3个月时行增强CT或MRI检查,以观察患者客观有效率(ORR)和疾病控制率(DCR)、治疗期间患者生存质量评分、不良反应发生情况等为指标。
1.3观察指标及疗效判定标准
完全缓解:肿瘤体积缩减完全消失且维持4周以上;部分缓解:肿瘤最大径及最大垂直径相乘,体积减少50%以上且无新病灶出现,维持4周以上;稳定:病灶两径相乘,出现新病灶或体积增大25%以上或减小50%以下;进展:出现新病灶或肿瘤两径相乘,体积增大25%以上。以完全缓解+部分缓解为客观有效,以完全缓解+部分缓解+稳定为疾病控制。化疗前、化疗结束后3个月复查CT或MRI以评估疗效。治疗期间采用生存质量评分表对患者生存质量进行评价。
1.4统计学处理
采用Ridit分析对患者疗效进行分析,采用卡方检验对ORR和DCR进行分析,生存期采用秩和检验进行分析。P<0.05表示差异具有统计学意义。
2 结果
2.1临床疗效
治疗结束时,35例患者中,完全缓解12例,部分缓解8例,稳定8例,进展7例,ORR和DCR分别为57.15%和80.01%,见表1和图1。

表135 例患者临床疗效结果[例(%),n=35]
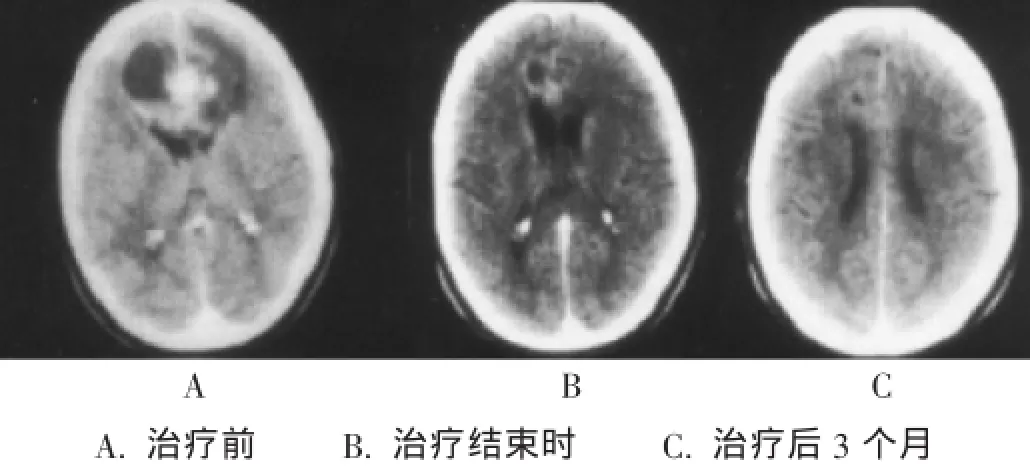
图1 典型患者头颅MRI检查结果比较
2.2生存质量评分
35例患者治疗前生存质量评分为(30.67±8.03)分,治疗后为(83.46±11.7)分,两者比较,差异有统计学意义(P<0.05)。
2.3不良反应发生情况
35例患者中,在化疗期间有13例出现厌食、便秘等消化道症状(37.14%),4例白细胞减少(11.43%),1例假性进展(2.86%)。发生不良反应的患者均为胶质母细胞瘤患者,期间患者出现头痛等颅内压增高的表现,在给予间断脱水、激素等对症治疗以后症状减弱。
3 讨论
恶性神经胶质瘤是中枢神经系统最常见的原发性肿瘤,患者死亡率高,且大多数肿瘤在初次诊断时就已发生广泛浸润。目前,手术切除仍是治疗的首选方式,在全切肿瘤术后辅助放射治疗(简称放疗)和化疗能改善患者症状并延长生存期[3]。Stupp等[4]的研究表明,巩固化疗方案在替莫唑胺同期放化疗后治疗新诊断胶质母细胞瘤(GBM)的2年生存率高达31%,明显高于其他治疗方案的8%~12%,也提及了替莫唑胺治疗GBM的相对较为安全,患者耐受性也较好。
替莫唑胺属于新型烷化剂,抗瘤谱广,不良反应轻微,能透过血脑屏障,可口服,是一种较为理想的、使用方便的中枢神经系统恶性肿瘤化疗药物,也是化疗药物出现的20多年来,唯一被随机、多中心临床Ⅲ期研究证实的化疗加放疗较单独放疗可延长GBM患者总生存期的药物[5]。本研究结果显示,治疗结束时,35例患者的客观有效率和疾病控制率分别为57.15%和80.01%,与相关报道一致[6-9];患者治疗前生存质量评分为(30.67±8.03)分,治疗结束后生存质量评分为(83.46± 11.7)分,两者比较差异有统计学意义(P<0.05)。在化疗期间,有13例患者出现厌食、便秘等消化道症状(37.14%),4例白细胞减少(11.43%),1例假性进展(2.86%),还有胶质母细胞瘤患者在治疗期间出现头痛等颅内压增高的表现,在给予间断脱水、激素等对症治疗以后症状减弱[10-15]。
综上所述,替莫唑胺用于人恶性神经胶质瘤术后辅助化学治疗,能有效控制肿瘤的生长,可以显著提高患者的生活质量,且不良反应较轻微,值得临床推广,但替莫唑胺能有效抑制神经胶质瘤的分子水平检测尚需进一步研究。
[1]Aoki T,Matsutani M,Hashimoto N.Management of glioblastoma[J].Expert Opin.Pharmacother,2007,8(18):3 103-3 135.
[2]Ashby L,Ryken T,La Rocca R.Treatment of brain tumors[J].N Engl J Med,2005,352(21):2 340-2 343.
[3]Soffietti R,Trevisan E,Ruda R.New chemotherapy options for the treatment of malignant gliomas[J].Anticancer Drugs,2007,18(7):620-629.
[4]Stupp R,den Bent MJV,Mason WP,et al.Radiotherapy plus concomitant and adjuvant temozolomide for glioblastoma[J].N Engl J Med,2005,350(11):977-986.
[5]Diserens AC,Hegi ME,Gorlia T,et al.MGMT gene silencing and benefit from temozolomide I n glioblastoma[J].N Engl J Med,2005,342(10):977-983.
[6]Mutter N.Temozolomide:a milestone in neuro-oncology and beyond[J].ExpertRevAnticancerTher,2006,7(8):1188-1202.
[7]Platten M,Weller M.New(alternative)temozolomide regimens for the treatment of glioma[J].Neuro Oncol,2009,10(3):66-75.
[8]张俊平,塞克,魏大年,等.替莫唑胺治疗国人恶性脑胶质瘤:31例临床疗效分析[J].中国新药与临床杂志,2007,26(7):534-538.
[9]王增光,杨树源,杨学军,等.恶性胶质瘤患者应用替莫唑胺治疗的临床研究[J].天津医药,2008,36(7):481-483.
[10]林宁,张占英.应用替莫唑胺治疗颅内肿瘤的疗效观察[J].中国临床神经外科杂志,2008,13(2):108-109.
[11]Rich JN,Reardon DA.Diagnosis and treatment of high-grade astrocytoma[J].Neurol Clin,2007,25(4):1 100-1 127.
[12]Falcone C,Filippini G,Boiardi A,et al.Prognostic factors for survival in 676 consecutive patients with newly diagnosed primary glioblastoma[J].Neuro Oncol,2008,10(11):99-103.
[13]Taal W,Brandsma D,Stalpers L,et al.Clinical features,mechanisms,and management of pseudoprogression in malignant gliomas[J].Lancet Oncol,2008,9(5):443-452.
[14]Mrugala MM,Chamberlain MC.Mechanisms of disease:temozolomide and glioblastoma-look to the future[J].Nat Clin Pract Oncol,2008,11(8):352-369.
[15]Diserens AC,Hegi ME,Gorlia T,et al.MGMT gene silencing and benefit from temozolomide in glioblastoma[J].N Engl J Med,2005,314(11):978-1 023.
Temozolomide Used for Chemotherapy after Malignant Glioma Operation in 35 Cases and Its Safety Evaluation
Liang Hong,Ren Mingliang,Wang Xuhui,Xu Lunshan
(Department of Neurosurgery,Teaching and Research Section of Surgery,Daping Hospital and Research Institute of Surgery,Third Military Medical University,Chongqing,China400042)
ObjectiveTo evaluate the efficacy and safety of temozolomide(TMZ)used for chemotherapy in the treatment of human malignant gliomas.Methods35 cases of postoperative pathologically confirmed malignant glioma patients from January 2013 to January 2016 were seleceted and given chemotherapy with TMZ.All cases were followed up to compare the clinical efficacy,quality of life scores during treatment,and the occurrence of adverse reactions.ResultsAt the end of the full course of TMZ treatment,the overall response rate of the 35 cases was 57.15%and disease control rate was 80.01%.Pre-treatment quality of life score was(30.67± 8.03)points,which was significantly lower than that(83.46±11.7)points after treatment;adverse reactions included 13 cases of anorexia,constipation and other gastrointestinal symptoms(37.14%),4 cases of leukopenia(11.43%),and 1 case of pseudo-progress(2.86%).ConclusionTreatment of malignant gliomas with TMZ has better clinical efficacy and less adverse reactions.It is well tolerated and is an ideal drug for postoperative adjuvant chemotherapy for malignant glioma
temozolomide;malignant gliomas;efficacy;safety
R969.4;R979.1
A
1006-4931(2016)13-0046-03
梁鸿(1982-),男,硕士研究生,主治医师,研究方向为神经胶质瘤的治疗,(电子信箱) 15909399027@163.com;徐伦山(1972-),男,博士研究生,主任医师,本文通讯作者,研究方向为神经胶质瘤及功能性神经外科,(电子信箱)xulunshan@sina.com。
2016-03-22)
