小剂量糖皮质激素与N-乙酰半胱氨酸联用对特发性肺纤维化的有效性和安全性
2016-10-29艾学才
艾学才
(湖北省武汉市江夏区纸坊街社区卫生服务中心,湖北武汉430200)
小剂量糖皮质激素与N-乙酰半胱氨酸联用对特发性肺纤维化的有效性和安全性
艾学才
(湖北省武汉市江夏区纸坊街社区卫生服务中心,湖北武汉430200)
目的探讨小剂量糖皮质激素(GC)联合N-乙酰半胱氨酸(NAC)对特发性肺纤维化(IPF)的有效性和安全性。方法选取2013年5月至2015年4月确诊的IPF患者72例,随机分为对照组和观察组,各36例。对照组给予常规剂量(≥80 mg/d)注射用甲泼尼龙琥珀酸钠联合NAC(60 mg,3次/日)治疗;观察组给予治疗小剂量(<80 mg/d)注射用甲泼尼龙琥珀酸钠联合NAC治疗。统计并比较两组治疗前后肺功能指标[用力肺活量/预计值(FVC%pred)、单位肺泡容积的一氧化碳弥散量/预计值(DLCO/VA%pred)和1秒用力呼气量/预计值(FEV1%pred)]、Brog呼吸困难评分、CAT生活质量评分和运动耐力试验及不良反应发生情况。结果治疗前,两组患者FVC%pred,DLCO/VA%pred,FEV1%pred,Brog评分,CAT评分和运动耐力试验结果相比,差异无统计学意义(P>0.05);治疗后,观察组FVC%pred,DLCO/VA%pred,FEV1%pred分别为(73.4±9.5),(81.2±12.8)和(64.6±14.8),明显高于对照组的(67.1±9.2),(72.5±8.3)和(61.1±10.4)(P<0.05);治疗第3个月,观察组Brog呼吸困难评分明显低于对照组,CAT生活质量评分和运动耐力试验均明显高于对照组(P<0.05);两组血压升高、腰背疼痛、血糖升高等反应发生率相比,差异无统计学意义(P>0.05)。结论小剂量GC联合NAC治疗IPF能明显改善患者肺功能和生活质量,值得临床推广。
糖皮质激素;N-乙酰半胱氨酸;特发性肺纤维化;临床疗效
特发性肺纤维化(IPF)是一组具有相似临床表现、X线胸部摄片改变及肺功能损害的异质性疾病的总称,肺间质纤维化是以肺泡间质炎细胞浸润、纤维母细胞增生和肺泡间质纤维结缔组织沉积为特征的免疫介导的、进行性慢性炎症性疾病。目前,IPF的治疗包括应用糖皮质激素(GC)、免疫抑制剂、细胞毒药物和抗纤维化药物,但此类药物存在特异性差等缺点,且单用GC疗效欠佳。N-乙酰半胱氨酸(NAC)是目前最具活力的抗氧化药物,在体内可直接清除自由基、过氧化氢以及次氯酸[1-3],从而保护肺组织损伤。GC联合NAC治疗IPF效果更佳,但尚缺乏关于剂量的研究。笔者对36例确诊为IPF的患者采用小剂量(<80 mg/d)甲强龙联合NAC治疗,疗效满意,现报道如下。
1 资料与方法
1.1一般资料
纳入标准:符合IPF诊断标准,并胸部摄片和肺部高分辨CT等影像学检查确认;对治疗药物无过敏;病历资料完全,且随访无脱落,知情受试。
排除标准:已确定为某种风湿免疫性疾病所致的肺纤维化;存在或合并肺部及其他部位感染;合并严重骨质疏松、消化性溃疡。
病例选择与分组:选择2013年5月至2015年4月在本院接受治疗的IPF患者72例,均经确诊,符合IPF诊断标准[4]。将患者按随机数字表法分为两组,各36例。观察组中,男28例,女8例;年龄45~59岁,平均(54.5±7.2)岁。对照组中,男29例,女7例;年龄46~61岁,平均(55.2±6.8)岁。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性。
1.2方法
两组患者均口服乙酰半胱氨酸片(海南赞邦制药有限公司,国药准字H20080326,规格为每片0.6 g),每次600 mg,3次/日。观察组在此基础上予注射用甲泼尼龙琥珀酸钠(国药集团容生制药有限公司,国药准字H20030727,规格为每支40 mg)<80 mg/d,静脉注射,可根据疗效判定标准予以减半,直至减至口服甲泼尼龙片维持剂量20 mg/d。对照组予注射用甲泼尼龙琥珀酸钠80~120 mg/d,静脉注射,根据疗效判定标准予以减半,直至减至口服甲泼尼龙片维持剂量20 mg/d。两组疗程均为3个月。
1.3观察指标及疗效判定标准
统计并比较两组治疗前后肺功能指标,包括用力肺活量/预计值(FVC%pred)、单位肺泡容积的一氧化碳弥散量/预计值(DLCO/VA%pred)和1秒用力呼气量/预计值(FEV1%pred)、Brog呼吸困难评分、CAT生活质量评分和运动耐力试验。观察患者不良反应发生情况。运动耐力试验:采用6 min步行试验,即患者在事先标好距离的病房走廊内以最大能力和速度往返行走6 min,测量行走距离。Brog呼吸困难评分量表:0~10分表示从无到非常严重。
1.4统计学处理
采用SPSS 19.0进行统计学分析,计量资料以X±s表示,行t检验;计数资料以百分比表示,行卡方检验。P<0.05为差异有统计学意义。
2 结果
2.1肺功能指标
两组患者治疗前FVC%pred,DLCO/VA%pred,FEV1%pred相比,差异无统计学意义(P>0.05);治疗后,观察组FVC%pred,DLCO/VA%pred,FEV1%pred均明显高于对照组(P<0.05)。见表1。
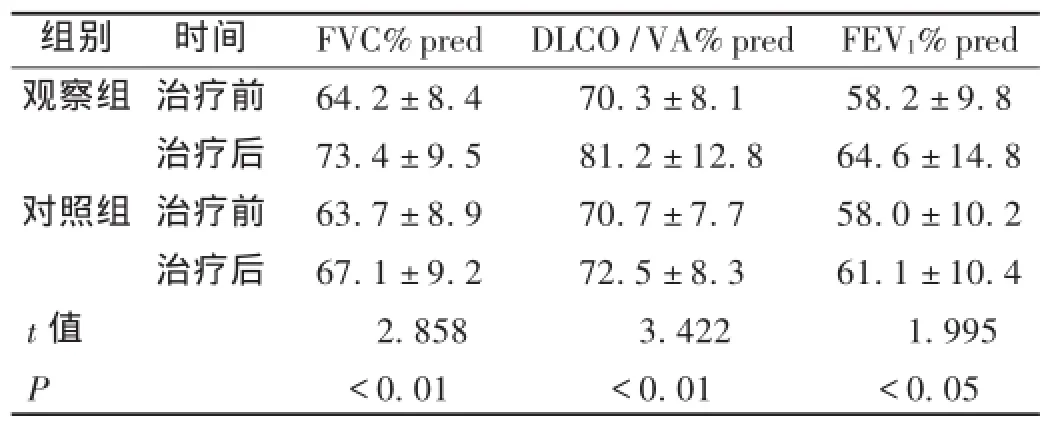
表1 两组患者FVC%pred,DLCO/VA%pred,FEV1%pred比较(X±s,n=36)
2.2量表评分和运动耐力试验
两组患者治疗前Brog呼吸困难评分、CAT生活质量评分和运动耐力试验相比,差异无统计学意义(P>0.05);治疗第3个月,观察组Brog呼吸困难评分明显低于对照组,CAT生活质量评分和运动耐力试验均明显高于对照组(P<0.05)。见表2。
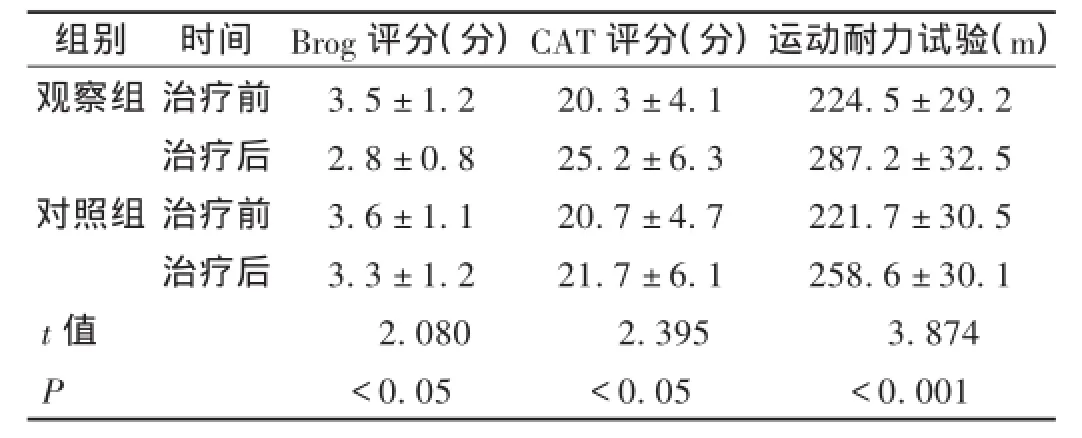
表2 两组患者Brog呼吸困难评分、CAT生活质量评分和运动耐力试验比较(X±s,n=36)
2.3不良反应发生情况
两组患者血压升高、腰背疼痛、血糖升高等不良反应发生率相比,差异无统计学意义(P>0.05)。见表3。
3 讨论
IPF是一组病因各异,表现相似的疾病谱,随着对其发病机制的深入认识和理解及相关其他学科的发展,人们致力于从各个角度寻找有效的治疗药物和方法[4-5]。
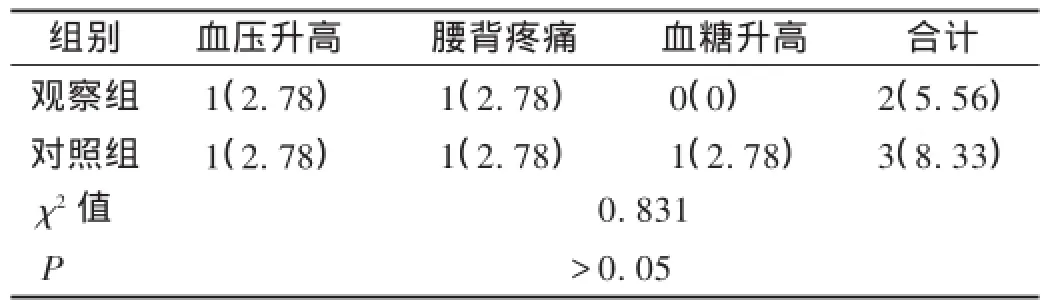
表3 两组患者不良反应发生情况比较[例(%),n=36]
NAC是目前最具活力的抗氧化药物,在体内可直接清除自由基、过氧化氢以及次氯酸,从而保护肺组织损伤。GC为治疗IPF的经典临床用药,较常使用的有甲泼尼龙,多数医师主张早用。有研究认为,GC治疗IPF的主要机制为抑制炎性反应、免疫反应[6],减少成纤维细胞(FB)的增生[7-8],阻断FB的细胞周期,但对其的凋亡无促进作用,部分患者单用GC能改善肺功能[9-10]。鉴于GC的作用机制,仍作为IPF的首选治疗方法[11-12]。但经反复临床研究后,GC单独治疗IPF的疗效有限,因此应与其他药物联合使用。前期许多研究表明,NAC可以通过抑制干扰素-γ(IFN-γ)、白细胞介素(IL)-1β、肿瘤坏死因子-α(TNF-α)及内毒素所致细胞核因子NF-κB信号转导途径[13],下调转化生长因子、IL-6和IL-8的表达,抑制炎性反应。NAC作为一种抗氧化剂,具有清除自由基及多种炎症细胞释放活性氧,加强细胞在缺血缺氧状态下的抗氧化能力,可保护细胞不受损伤。经自由基清除剂NAC治疗后[14],可能减轻炎性细胞释放氧自由基等有害因子对肺部的损伤。
本研究结果显示,采用小剂量GC联合NAC治疗IPF,患者的肺功能改善更明显,且呼吸困难改善情况及生活质量的提升也更加显著,表明低剂量的GC对IPF的治疗疗效更佳。
在使用GC治疗的过程中,不良反应的发生严重影响患者的生存质量及治疗进度[15]。本研究结果显示,小剂量GC联合NAC与常规剂量GC联合NAC相比,血压升高、腰背疼痛、血糖升高等不良反应发生率相当,故总体上低剂量GC方案与高剂量方案治疗IPF,患者的耐受性相当。
综上所述,小剂量GC联合NAC治疗IPF能明显改善患者肺功能和生活质量,值得临床推广。
[1]Richeldi L,du Bois RM,Raghu G,et al.Efficacy and safety of nintedanib in idiopathic pulmonary fibrosis[J].New England Journal of Medicine,2014,370(22):2 071-2 082.
[2]Morawiec E,Tillie-Leblond I,Pansini V,et al.Exacerbations of idiopathic pulmonary fibrosis treated with corticosteroids and cyclophosphamide pulses[J].European Respiratory Journal,2011,38(6):1 487-1 489.
[3]张海英.小剂量糖皮质激素联合N-乙酰半胱氨酸治疗特发性肺纤维化的临床研究[J].临床肺科杂志,2014,19(1):48-50.
[4]王传海,李承红,孔彬,等.N-乙酰半胱氨酸辅治特发性肺纤维化的临床疗效观察[J].疑难病杂志,2015,14(2):129-131.
[5]Le Saux CJ,Davy P,Brampton C,et al.A novel telomerase activator suppresses lung damage in a murine model of idiopathic pulmonary fibrosis[J].PloS one,2013,8(3):e58 423.
[6]佘巍巍,杨新官.糖皮质激素治疗与特发性肺纤维化患者生存期的相关性[J].中国老年学杂志,2010,30(21):3 173-3 174.
[7]Rafii R,Juarez MM,Albertson TE,et al.A review of current and novel therapies for idiopathic pulmonary fibrosis[J].Journal of Thoracic Disease,2013,5(1):48.
[8]张坚,黄慧,陆志伟,等.特发性肺纤维化患者生存预后因素的回顾性分析[J].中华结核和呼吸杂志,2011,34(3):174-178.
[9]Xue J,Kass DJ,Bon J,et al.Plasma B lymphocyte stimulator and B cell differentiation in idiopathic pulmonary fibrosis patients[J]. The Journal of Immunology,2013,191(5):2 089-2 095.
[10]黄振杰,汤艳,郑金旭,等.布地奈德吸入联合N-乙酰半胱氨酸治疗特发性肺纤维化[J].临床肺科杂志,2010,15(12):1 755-1 757.
[11]Mermigkis C,Mermigkis D,Varouchakis G,et al.CPAP treatment in patients with idiopathic pulmonary fibrosis and obstructive sleep apnea-therapeutic difficulties and dilemmas[J].Sleep and Breathing,2012,16(1):1-3.
[12]Hu C,Wang Y,Fan Y,et al.Lipidomics Revealed Idiopathic Pulmonary Fibrosis-Induced Hepatic Lipid Disorders Corrected with Treatment of Baicalin in a Murine Model[J].The AAPS Journal,2015,17(3):711-722.
[13]孙英坤,赵琦,邵玉霞,等.N-乙酰半胱氨酸治疗特发性肺纤维化的临床分析[J].哈尔滨医科大学学报,2012,46(5):465-467.
[14]Kahloon RA,Xue J,Bhargava A,et al.Patients with idiopathic pulmonary fibrosis with antibodies to heat shock protein 70 have poor prognoses[J].American Journal of Respiratory and Critical Care Medicine,2013,187(7):768-775.
[15]陆建华,高静珍.乙酰半胱氨酸联合糖皮质激素治疗特发性肺纤维化中一氧化氮水平变化的研究[J].中国实验诊断学,2013,17(9):1 692-1 693.
Effectiveness and Safety of Low Dose Glucocorticoid Combined with N-acetylcysteine in Treatment Idiopathic Pulmonary Fibrosis
Ai Xuecai
(Jiangxia District Zhifang Street Community Health Service Center,Wuhan,Hubei,China430200)
ObjectiveTo explore the efficacy and safety of low dose glucocorticoid(GC)combined with N-acetylcysteine(NAC)in the treatment of idiopathic pulmonary fibrosis(IPF).Methods72 patients diagnosed with IPF from May 2013 to April 2015 were randomly divided into the control group and the observation grou,36 cases in each group.The control group was given conventional dose(equal to or more than 80 mg)methylprednisolone combined with NAC treatment;the observation group was given treatment of small dose(<80 mg/d)methylprednisolone combined with NAC treatment.Pulmonary function indicators[forced vital capacity/expected value(FVC%pred),the volume of carbon monoxide diffusing capacity per unit(DLCO/VA%pred)and forced expiratory volume/estimated value(FEV1%pred)],Brog dyspnea score,CAT quality of life score and exercise endurance test and adverse reactions occurred were recorded and compared in the two groups before and after the treatment.ResultsThe difference of FVC%pred,DLCO/VA%pred,FEV1%pred,Brog score,CAT score and exercise tolerance test results in the two groups before treatment not statistically significant(P>0.05);after treatment,FVC%pred,DLCO/VA%pred,FEV1%pred were(73.4±9.5),(81.2±12.8)and(64.6±14.8)in the observation group,which were higher than(67.1±9.2),(72.5±8.3)and(61.1±10.4)in the control group(P<0.05);after 3 months of treatment,Brog dyspnea scores in observation group were significantly lower than the control group,while CAT score and exercise tolerance test scores were significantly higher(P<0.05);the difference of adverse reactions incidence such as high blood pressure,low back pain,elevated blood glucose was not statistically significant(P>0.05).ConclusionLow dose of GC combined with NAC in treatment of IPF can significantly improve the patients'lung function and quality of life,which is worthy of clinical promotior.
glucocorticoid;N-acetylcysteine;idiopathic pulmonary fibrosis;clinical efficacy
R969.4;R977.1+1
A
1006-4931(2016)13-0019-03
艾学才(1968-),男,汉族,湖北武汉人,硕士研究生,副主任医师,研究方向为呼吸内科疾病,(电话)027-87953738。
2016-01-06)
