多巴胺脂质体经鼻给药治疗帕金森氏病的研究
2016-10-27赵丽妮叶梦于洋王俊平
赵丽妮 叶梦 于洋 王俊平
(沈阳医学院药理学教研室 辽宁沈阳 110034)
多巴胺脂质体经鼻给药治疗帕金森氏病的研究
赵丽妮 叶梦 于洋 王俊平
(沈阳医学院药理学教研室 辽宁沈阳 110034)
目的: 研制多巴胺脂质体,用于治疗帕金森氏病。方法: 用大豆卵磷脂和油酸制备多巴胺脂质体;采用昆明种小白鼠,腹腔注射1-甲基-4-苯基-1,2,3,6-四氢吡啶(MPTP)建立帕金森氏病动物模型,用于评价多巴胺脂质体经鼻给药的治疗帕金森氏病的疗效。结果:多巴胺脂质体的平均粒径为20-120nm, Zeta电位为-25.6mV,对多巴胺的包封率为(98.2±1.6)%(n =3);经鼻给药,多巴胺脂质体具有显著的抗帕金森氏病作用(p<0.05)。结论: 采用大豆卵磷脂、油酸可以制备出多巴胺脂质体,经鼻给药用于治疗帕金森氏病有效。
多巴胺 脂质体 经鼻给药 帕金森氏病
帕金森氏病(Parkinson's disease, PD) 是一种神经退行性运动功能障碍性疾病。PD的病理改变主要是中脑黑质的多巴胺能神经元进行性凋亡。因此,PD的治疗策略之一是补充脑内多巴胺。然而,多巴胺不能通过血脑屏障,因此目前尚不能用多巴胺治疗PD。鼻脑通路可以让药物绕过血脑屏障进入中枢,其机制可能有:嗅上皮毛细血管吸收小分子脂溶性药物后穿过血脑屏障进入中枢,通过伸入颅内嗅觉壶腹的嗅觉感受细胞间的细胞轴突转运,也可能通过鼻粘膜嗅上皮细胞之间的裂孔进行细胞旁转运。有文献报道,脂质体等药物载体经鼻给药可让其携带的药物绕过血脑屏障进入中枢[1-3]。因此,我们制备了多巴胺脂质体,目的是通过经鼻给药治疗帕金森氏病。
1 仪器与材料
1.1 仪器
P200II型高效液相色谱附UV200II型紫外可变波长检测器(大连伊力特分析仪器有限公司);RE-52A旋转蒸发器附SHZ-CD型循环水真空泵 (上海亚荣生化仪器厂);TGL-16M台式高速冷冻离心机(湘仪离心机仪器有限公司);激激光粒度/Zeta 电位分析仪(ELS800,日本);JEM透射-扫描电镜(日本电子光学公司)。
1.2 药品与试剂
多巴胺(志望化工有限公司,批号:20140812), 大豆卵磷脂(Sigma) ,油酸(上海生物,批号:20140602) ,其他试剂均为国产分析纯。
1.3 实验动物
健康雌性昆明种小白鼠,体重18-22g(沈阳医学院实验动物中心,合格证号 SC XK(辽20010103)。
2 方法与结果
2.1 多巴胺脂质体的制备
将25mg盐酸多巴胺,0.25g油酸和大豆磷脂1.0g溶于热90%乙醇适量。采用旋转蒸发法,在氮气流中除乙醇,至形成黏稠的溶液,加入2%聚乙二醇400(PEG400)溶液,脂质体自发形成。采用0. 01%NaOH调节上述脂质体分散系pH至7.4,置高速匀浆机冰水中匀浆15分钟,200nm微孔滤膜滤过, 即得多巴胺脂质体。
2.2 包封率的测定
2.2.1 多巴胺HPLC分析条件
报道,结合我们的仪器,多巴胺的HPLC分析条件如下:层析柱:SinoChrom ODS-BP5m,4.6mm×200mm;流动相:磷酸盐缓冲液(磷酸二氢钾8.34 g与磷酸氢二钾0.87g加水使溶解成1000m l,pH5.8)-甲醇(98∶2);检测波长:280nm;流速:1.0 ml/ min。
2.2.2 多巴胺标准曲线
精密称取多巴胺对照品,配制成多巴胺溶液,浓度分别为:20、40、80、160、320(g/mL)。在上述色谱条件下,采用HPLC测定各样品峰面积,进样量50L。以各样品浓度为横坐标,峰面积积分值为纵坐标,绘制标准曲线。计算得回归方程:Y =17.814X -88.45, 结果表明在20-320 μg/mL范围内样品浓度和峰面积呈线性关系(r =0. 9987)。
2.2.3 包封率的测定
采用絮凝分离法测定多巴胺脂质体的包封率。精密量取多巴胺脂质体0.25ml用15%NaCl和50mL容量瓶稀释到50mL,静置过夜,转入10ml刻度试管5000rpm离心30分钟,取下清液,按上述色谱条件和标准曲线,测定下清液中多巴胺浓度。按下述公式计算包封率:
包封率(%)=1-(游离多巴胺浓度/多巴胺总浓度)×100%。
2.2.4 粒度和Zeta 电位测定
采用激光粒度/Zeta 电位分析仪,测定多巴胺脂质体在蒸馏水中的粒度分布和Zeta电位。
2.3 抗帕金森病作用
2.3.1 小鼠帕金森氏病模型的制备
取昆明种雌性小白鼠50只,体重18-22g,按体重差最小原则分成5组(10只/组):空白对照组,多巴胺对照,模型对照组,多巴胺组,多巴胺脂质体组。除空白对照组和多巴胺对照,其它各组鼻腔给药5天后,腹腔注射MPTP(20mg/kg)连续12天,同时继续鼻腔给药。空白对照,不给任何药物。多巴胺组,鼻腔给药,但是腹腔不注射MPTP。经鼻给药剂量为5μL/10g动物。
2.3.2 爬杆试验
分别在在给予MPTP之后第6天和第10天,将小鼠置放于一根长50cm直径1cm的木杆顶端,木杆上缠上纱布以防打滑,然后将受试小鼠放到杆顶,并记录以下几个时间:小鼠爬完杆长的全长所需要的时间;小鼠爬完杆长的上半部分所用的时间;小鼠爬完杆长下半部分所用的时间。将这3个时间相加作为本次被测小鼠爬杆实验的总时间,并作统计学分析。
2.3.3 悬挂实验
分别在在给予MPTP之后第6天和第10天,将受试小鼠双前肢悬挂于一水平电线上,如小鼠用两后肢抓住电线则记3分,如用一后肢抓住电线则记2分,如果小鼠两后肢均抓不住电线则记1分,最后计算得分情况,并作统计学分析。
2.4 统计学方法
所有实验均至少重复3次,采用Microsoft Office Excel计算实验结果的平均值(均数±标准差),利用t检验分析统计学差异,P<0. 05,定为有统计学意义。

表1 多巴胺纳米脂质体经鼻给药的小白鼠悬挂实验
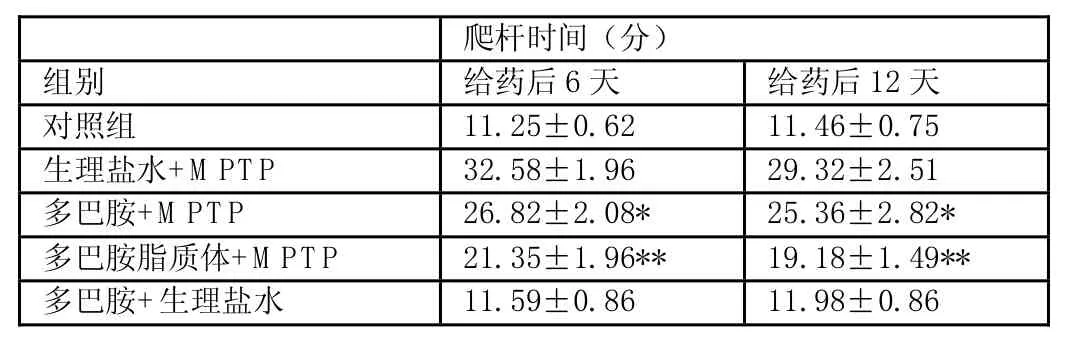
表2 多巴胺纳米脂质体经鼻给药的小白鼠爬杆实验
3 实验结果
3.1 多巴胺脂质体的理化性质
在蒸馏水中,多巴胺脂质体的平均粒径为20-120(nm), Zeta电位为-25.6 mV,对多巴胺的包封率为(98.2±1.6)%(n =3)。
3.2 多巴胺纳米脂质体的抗帕金森氏病效应
经鼻给药,在爬杆实验和悬挂实验中,多巴胺纳米脂质体对MPTP引起的帕金森氏症状的对抗作用如表1-2所示。
结果表明,多巴胺经鼻给药有一定的抗帕金森氏病作用,而且用脂质体运载多巴胺,可以显著提高多巴胺的抗帕金森氏病作用。但是,尚不能使动物恢复正常。
4 讨论
本实验研究多巴胺脂质体治疗帕金森氏病的疗效。实验结果表明,多巴胺经鼻给药有一定的抗帕金森氏病作用,而且用脂质体运载多巴胺,可以显著提高多巴胺的抗帕金森氏病作用。但是尚不能使动物恢复正常。
多巴胺难以通过血脑屏障,因此,目前帕金森氏病的治疗无法采用多巴胺。增加血脑屏障通透性,有可能促进多巴胺进入中枢,但是破坏血脑屏障中枢神经系统难以维持正常的功能。因此,要想采用多巴胺直接治疗帕金森氏病,必须让药物绕过血脑屏障进入中枢。
鞘内注射和鼻粘膜给药可以绕过血脑屏障[4]。鞘内注射不方便,因此我们选择了鼻粘膜给药治疗帕金森氏病。鼻腔给药后药物分子通过嗅粘膜,进入脑脊液,可绕过血脑屏障的途径。鼻粘膜壁薄,血管丰富,利于药物渗和吸收。经鼻给药的转运途径包括嗅神经通路,粘膜上皮通路(载体转运,胞饮或被动扩散方式)以及细胞旁通路,即透过细胞间隙或周围裂隙进入细胞间液,从而转运进入脑脊液)。还有其它通路,如淋巴系统,视神经,三叉神经等。之前有报道,脂质体能够促进蛋白质和肽类药物绕过血脑屏障进入中枢[2]。本试验表明,脂质体还能够促进其携带的小分子、极性强的药物绕过血脑屏障进入中枢。多巴胺是携带正电荷的小分子极性很强的药物,只能通过细胞旁路通道进入脑脊液,吸收很有限。脂质体携带多巴胺改变了电学性质,同时可以通过胞饮、穿过鼻粘膜或细胞旁路进入脑脊液,不过其具体机制尚待进一步研究。
5 结论
多巴胺脂质体能够提高多巴胺经鼻给药治疗帕金森氏病的疗效,但是尚不能达到完全消除帕金森病症状的程度。脂质体如何促进多巴胺进入中枢,以及如何提高多巴胺脂质体抗帕金森氏病的疗效尚待进一步研究。
参考文献
[1] Marianecci C, Rinaldi F, Hanieh PN, Paolino D, Marzio LD,Carafa M. Nose?to?Brain?Delivery: New Trends in Amphiphile-Based "Soft" Nanocarriers. Curr Pharm Des. 2015;21(36):5225-5232.
[2] Zheng X, Shao X, Zhang C, Tan Y, Liu Q, Wan X, Zhang Q, Xu S,Jiang X. Intranasal H102 Peptide-Loaded?Liposomes?for?Brain?Delivery to Treat Alzheimer's Disease. Pharm Res. 2015 Dec;32(12):3837-3849.
[3]Wavikar PR, Vavia PR. Rivastigmine-loaded in situ gelling nanostructured lipid carriers for?nose?to?brain?delivery. J?Liposome?Res. 2015;25(2):141-149.
[4]?Mistry A, Stolnik S, Illum L. Nanoparticles for direct noseto-brain delivery of drugs.?Int J Pharm.2009;379(1):146 157.
[5]Alam S, Khan ZI, Mustafa G, et al. Development and evaluation of thymoquinone-encapsulated chitosan nanoparticles for nose-to-brain targeting: a pharmacoscintigraphic study.?Int J Nanomedicine.?2012;7:5705-5718.
R453
A
1674-2060(2016)02-0214-02
