生态毒理数据筛查与评价准则研究
2016-10-27刘娜金小伟王业耀王子健
刘娜,金小伟,王业耀,2,王子健
1.中国地质大学(北京)水资源与环境学院,北京100083
2.中国环境监测总站,北京100012
3.中国科学院生态环境研究中心,北京100085
生态毒理数据筛查与评价准则研究
刘娜1,金小伟2,*,王业耀1,2,王子健3
1.中国地质大学(北京)水资源与环境学院,北京100083
2.中国环境监测总站,北京100012
3.中国科学院生态环境研究中心,北京100085
化学品生态风险评价和水质基准研究需要大量生态毒理数据,由于目前关于化学品毒性效应的研究较多,不同文献对同一测试终点的报道常常存在一定的差异,数据选择不当会直接影响最终评价结果。为了降低专业人员在数据筛选过程中的主观影响,有必要制定一套科学合理、操作性强的数据筛查与评价准则。本文整理比较了美国、荷兰、德国和澳大利亚等4个国家的5个毒理数据筛查与评价方法,并以荷兰的CRED方法为主,结合另外4个筛选方法以及现有的水质基准推导指南和生态风险评价技术导则,从可靠性、相关性、精确性三个方面详细阐述了数据质量评价标准与使用规范。其中数据质量评价包括五个方面:(1)实验设计,包括测试标准、操作规程、数据有效性、对照组设置;(2)实验试剂的纯度及其杂质的物理化学性质;(3)受试生物的基本信息和来源;(4)暴露条件,包括试验系统、暴露浓度设置及变化、暴露时间、生物负荷;(5)数据分析,包括平行样、统计分析方法、浓度-效应关系、原始数据;数据使用规范主要考虑受试生物、测试终点和暴露场景与评价目标的相关性,以及生态风险评价和水质基准推导对数据精确性的要求。这些均可为我国从事生态风险评价和水质基准研究的工作人员提供有益借鉴,使数据筛选过程更加客观、统一,同时还可以作为毒理实验论文撰写依据,提高数据报道质量。
生态毒理数据;筛查与评价;可靠性;相关性;生态风险评价;水质基准
刘娜,金小伟,王业耀,等.生态毒理数据筛查与评价准则研究[J].生态毒理学报,2016,11(3):1-10
Liu N,Jin X W,Wang Y Y,et al.Review of criteria for screening and evaluating ecotoxicity data[J].Asian Journal of Ecotoxicology,2016,11(3):1-10 (in Chinese)
制定化学品水质基准、推导预测无观察效应浓度(predicted no effect concentrations,PNECs)以及开展生态风险评价时往往需要大量的生态毒理数据,数据质量直接影响最终的结论,不好的数据无法正确解释参数的自然变异性,可能会产生不正确的评价结果[1]。因此,污染物毒理数据是水质基准及风险评价研究的基础和关键,在生态风险评价和水质基准推导过程中,首先要保证毒理数据的质量[2-3]。毒理数据一般通过数据库或文献检索获得,虽然目前关于化学品生态毒性效应的研究较多,由于毒性试验由不同试验人员分别在其各自的试验室独立完成,试验结果可能受到各种因素的影响。为了保证所用数据的准确性、可靠性、可比性,需要在筛选过程中对毒性试验的质量控制与质量保证措施做出严格要求[4-5]。
在水环境生态风险管理研究中,环境暴露、效应识别和风险评估是三个重要内容[6],目前我国关于水质基准和生态风险评价研究较多的是统计模型和推导方法的比较[7-8]、最少毒性数据需求(minimum toxicity data requirement,MTDR)以及生物效应比(biology-effect ratio,BER)[7-8],对于毒理数据筛查与评价准则,基本参照国外发达国家的方法,如Klimisch法则[9-10],无论在数据的质量评价,还是在方法的适应性方面,仍有一些科学问题不明确,缺乏统一的认识。同时,随着研究的深入,数据筛查与评价方法不断更新和细化。因此,在比较、总结国外的先进经验和最新成果的基础上,提出适合我国目前生态毒理学研究水平的科学、完善的毒理数据筛查与评价方法,有助于提高我国水质基准推导和化学品生态风险评价的质量。
1 生态毒理数据筛查与评价准则概述(General introduction to screening and evaluating criteria)
欧盟“环境质量标准推导技术指南”[11]采用Klimisch等[12]建立的数据评价方法体系,从可靠性和相关性两个方面对毒理数据进行筛查。可靠性是指试验所采用的方法是否按照标准的实验方法,试验过程和试验结果的描述是否清楚、合理;相关性是指所得试验数据的效应和终点是否与特定的风险评价相一致。该体系将毒理数据的可靠性分为可靠(完全符合标准)、限制性可靠(部分信息缺失)、不可靠(不符合标准)和不确定(数据来自摘要或二次引用文献,缺乏相关信息)4个等级,判断依据主要包括:是否使用国际或国家标准测试方法,操作过程是否遵循药物非临床研究质量管理规范(Good Laboratory Practices,GLP)[13];对于非标准测试方法的试验,所用实验方法是否科学合理;试验过程和试验结果的描述是否详细;文献有没有提供原始数据。数据相关性主要考虑试验生物及暴露场景与评价区域的一致性,非标准模式生物的适用性,以及试验设计是否充分考虑测试药品的物理化学性质。类似地,Durda等[14]提出了30个判断依据,将数据质量分为高、中、低、不可靠、不确定5个等级;Hobbs等[15]对20个赋予不同权重的问题进行评分,根据评价总分占总可能分值(取决于数据类型)的百分比,将数据分为可接受、不可接受、高质量3种情况(表1)。目前Klimisch方法在国内外应用最为广泛[16],但该方法缺少一些重要的评价指标,对已有的评价指标尤其是数据相关性评价,缺乏必要的解释说明,专业人员在使用过程中容易产生分歧[17-18]。
在Klimisch评价方法体系的基础上,荷兰国家公共卫生与环境研究院(RIVM)于2016年总结发表了生态毒理数据报道与评价标准(Criteria for reporting and evaluating ecotoxicity data,CRED)[19],包括20个可靠性标准和13个相关性标准。其中可靠性评价标准内容及分级方法与Klimisch基本一致,但对试验设计、试验试剂、受试生物、暴露条件、试验数据统计分析等进行了更详细的描述。此外,CRED充分考虑了毒理数据对生态风险评价案例的适用性,丰富了受试生物及暴露场景与生态风险评价的相关性评价标准,并按照可靠性分级方法,将数据相关性分为相关、限制性相关、不相关、不确定4个等级。实验证明,CRED评价标准比常用的Klimisch方法描述更精确、通俗易懂,不同人员利用该方法得出的评价结果具有高度一致性[19]。
此外,美国环保署(United States Environmental Protection Agency,USEPA)于2011年颁布了修订版“开放文献的生态毒性数据评估指南”[20],用于指导识别、选择和获取公开发表的生态毒理数据,包括数据筛选、数据评估与分类、数据应用三个部分。第一部分为ECOTOX数据库和农药项目办公室(the Office of Pesticide Programs,OPP)各自认可的文献筛查标准,要求所用数据必须来自已公开的英文文献,文献中必须提供足够的佐证资料证明试验过程和结果的可靠性,列出了14条接受标准和26条不可接受标准;第二部分详细阐述了数据评估与分类标准,包括15条试验内容、28条与水生生物相关的无效数据判断标准、4条定量数据判断标准,将ECOTOX或OPP接受的数据分为定量、定性、无效3种类型(表1);第三部分分别阐述了定量数据、定性数据、混合物和以亚致死效应为测试终点的敏感数据在生态风险评价过程中的使用原则。
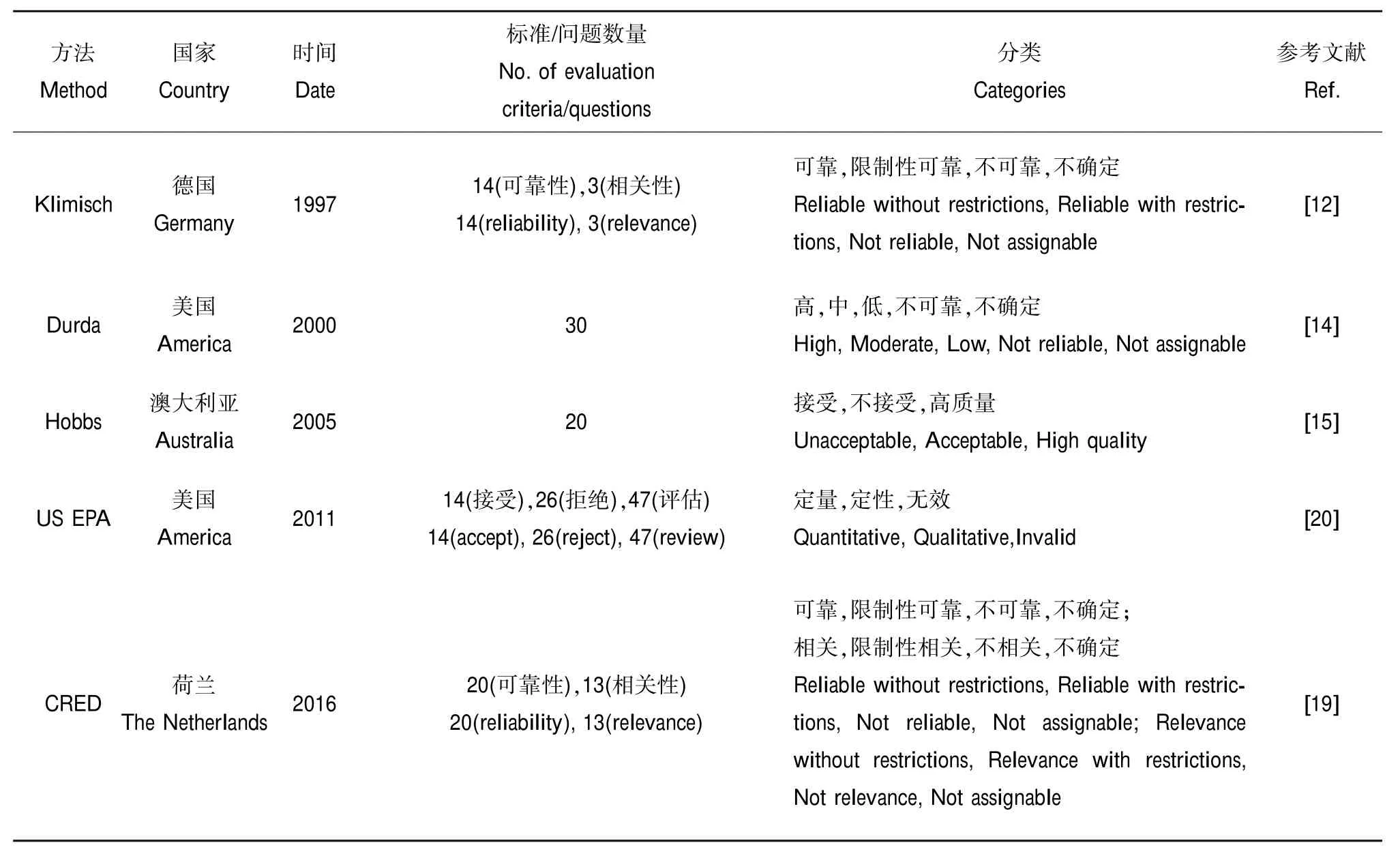
表1 生态毒理数据筛查与评价准则概述Table 1 Review of criteria for screening and evaluating ecotoxicity data
2 生态毒理数据质量评价标准(Evaluation criteria for the quality of ecotoxicity data)
一般认为,严格按照OECD、ISO等标准测试方法和GLP操作规程得到的毒理数据质量较高,可直接采用。反之,对于没有按照标准测试方法或GLP操作规程所进行的试验,则需要对其数据质量的可靠性进行评价。下面以CRED方法为主,结合另外4种数据评价标准,以及美国[21-22]、加拿大[23]、澳大利亚和新西兰[24]等国家及欧盟[11,25]的水质基准推导和生态风险评价指南,从试验设计、试验试剂、受试生物、暴露条件、数据分析5个方面介绍生态毒理数据质量评价准则。
2.1 试验设计
a.试验方法。毒理试验应按照国际或国家标准测试方法进行,否则应对试验设计及结果进行详细说明;若试验设计有缺陷或试验数据无统计学意义,即使按照标准测试方法得到的数据也不可靠。
b.试验过程。一般情况下,试验过程遵循GLP规范的数据可靠性较高,但GLP只是一种通过试验记录和操作过程控制来确保数据质量的管理体系[13,26],不是评价数据可靠性的严格标准。
c.数据有效性。为保证试验数据合理有效,对照组(包括空白对照组和溶剂对照组)与试验组生物应来自同一个种群,且对照组的参数变化范围与历史数据一致。例如,OECD指南要求藻类毒理试验开始的72 h内对照组的藻细胞呈指数增长[27],溞类急性活动抑制试验要求试验结束时对照组的溞类受抑制率不超过10%,对照组和试验组的溶解氧浓度不小于3 mg·L-1[28]。当受试生物为非模式生物时,应判断其与模式生物的相似性,对照组的死亡率、生长率是否在该物种的正常范围内。
d.对照组。试验必须设置空白对照组,如果使用助溶剂还需设置溶剂对照组,无对照组以及对照组中生物死亡过多或显示出压力、疾病迹象的数据禁止使用[20-21];当溶剂对照组的死亡率高于空白对照组时,应以溶剂对照组为基础进行数据统计分析,若溶剂对照组的死亡率过高,数据可靠性需进行专家判断[19];当测试指南要求设置阳性对照组时,缺乏阳性对照组会降低该毒理数据的可靠性[14-15]。
2.2 试验试剂
a.受试物。首先应明确受试物的准确名称及化学品登记号(CAS)。对于在大多数自然水体中以离子形式存在的化学品,其在化学平衡中的所有形式通常被认为是一种物质[21,29],因此,当受试物为无机盐时,若测试结果以质量浓度表示,应说明试验试剂的化学形式(盐单质、正/负离子、是否含结合水)。
b.试剂纯度。一般来说试剂纯度应大于80%。欧盟规定当试剂纯度<90%时,名义测试结果应根据试剂纯度进行纠正[11];OECD测试指南规定试验试剂使用“合适的纯度”,纯度越低数据可靠性越差(以实测浓度表示的数据除外);US EPA规定在适当的情况下可以使用工业级化学品的试验数据,配方混合物和乳状浓缩物的试验数据只能提供辅助信息,不能用于基准推导[21]。
c.配方混合物与杂质。当试验试剂为配方混合物或含有杂质时,应确定混合物中对生物体产生暴露的每一种化学组分的含量及其生态毒性效应,因为助溶剂等惰性成分可能会显著提高或降低受试物的毒性效应[19]。如果试剂含有碱性和酸性物质,还应提供测试样品的中和反应数据[12]。
2.3 受试生物
a.基本信息。包括受试生物的科学名称、年龄或所处生命阶段(幼年、青年、成年),当受试物为激素类物质时,还应说明受试生物的性别。
b.受试生物来源。为保证受试生物健康可靠,应说明受试生物的来源(试验室、野外),野外收集的还应说明具体地理位置;试验前应在试验条件下驯养,避免因生存条件的改变而受到影响。由于野生物种可能在试验前已经暴露于受试物或其他污染物,因此受试生物来自野外的试验数据可靠性偏低[19]。
2.4 暴露条件
a.试验系统与试验试剂。必须根据试验试剂的物理化学性质选择适宜的试验系统,并提供pH值、硬度、碱度等水质参数。例如:针对疏水性物质的试验应选择玻璃容器,不应使用塑料或其他具有吸附作用的材质;静态试验系统适用于稳定化学品的短期暴露,不适用于长期暴露;大部分试验为开放型试验系统,但挥发性物质应使用密闭式试验系统;对于易挥发、易水解或易降解的物质,只采用流水系统的试验数据,且试验过程中对受试物浓度进行监控,否则视为不可靠数据[19,21]。
b.试验系统与受试生物。试验系统应根据受试生物的生存特点进行选择。例如:淡水生物不应用于咸水试验系统;对于可光降解化学品,鱼类和大型溞试验在避光条件下进行,但藻类生长需要光照条件;温度、pH值、溶解氧等试验条件应根据受试生物的生存要求稳定在一定范围内;急性毒性试验不允许喂食,慢性毒性试验需定期喂食,但应说明食物类型[20]并及时清理食物残渣;对于需要基质的昆虫类水生生物试验,应选择石英砂、玻璃珠等惰性材料做基质[30]。
c.暴露浓度的有效性。如果暴露浓度不是实测浓度,当暴露浓度高于溶解度时需要对其有效性进行专家判断,高于溶解度10倍的名义浓度通常认为是不可靠数据[31];试验过程中出现沉淀物,说明试验实际浓度低于名义浓度,数据不可靠。如果试验需要助溶剂,其浓度不应大于0.01%。
d.浓度间隔。试验组浓度间隔不宜过大,尤其是用于推导无观察效应浓度(NOEC)的试验数据。毒理试验常用的浓度间隔系数为3.2,最大不超过10。
e.暴露时间。一般情况下,暴露时间指受试生物实际暴露时间,而非试验持续时间。对于有延迟效应的试验,应说明观察时间与暴露结束的时间间隔。
f.浓度变化。首先应明确用于计算效应浓度的数据是试验初始/终止浓度,还是算数平均/几何平均浓度。稳定化学品的急性毒性试验或半静态慢性毒性试验可直接使用名义浓度,其他其他情况则需要考虑试验过程中的浓度变化,至少需要提供试验初始浓度和终止浓度。正常情况下,实测浓度为名义浓度的80%~120%,否则应分析浓度变化原因,并说明分析方法。
g.生物负荷。生态毒理试验应控制容器内单位体积的生物量,例如,OECD推荐静态和半静态鱼类急性毒性试验的最大负荷为1.0 g·L-1,流水试验的生物负荷可以适度提高,但当试剂的logKOW>3时,需考虑生物吸附性,避免试剂浓度因生物负荷的提高而降低。
2.5 数据分析
a.平行样。试验应按照测试标准要求设置一定数量的平行样,每个平行对照组和测试组中应有足够数量的受试生物。对于未按照试验标准设定平行样的试验数据,需评价其是否具有统计学意义。
b.统计分析方法。试验数据应针对不同测试终点(ECX/LCX/NOEC/LOEC)选择相应的统计分析方法,并详细说明统计学参数。例如,计算ECX应使用内插法而非外推法,计算结果不应低于或高于试验浓度,当EC10比最低试验浓度低3倍以上时,数据可靠性较低;NOEC应根据统计学显著性的计算结果获得,通过观察图/表得到的为不可靠数据[19]。
c.浓度-效应关系。OECD评价指南规定,用于生态风险评价的毒理数据必须具有明显的浓度-效应关系[32],当缺少浓度-效应关系时,通过统计分析计算出的测试终点值为限制性可靠[19]。
d.原始数据。文献中应提供详细的原始数据,用于检查试验数据的统计学意义和对照组的有效性,验证文献给出的计算结果,还可以用于计算评价需要但文献中未给出的测试终点(如NOEC)。缺少原始数据的毒理数据为限制性可靠[12,19]。
比较5种数据筛查与评价方法(表2),尽管评价标准的细节描述存在差异,但基本包含了所有关键因素,其中CRED方法考虑的最全面,并对各评价因素进行了详细的解释,具有较强的实用性和可操作性。US EPA在“开放文献的生态毒理数据评估指南”数据评估与分类部分阐述的数据质量评价标准内容与另外4种方法大致相同,但根据ECOTOX数据库接受标准,其数据筛选仅致力于文献中试验方法和结果的充分性,对数据质量评价因素考虑的较少,因此来自ECOTOX数据库[33]的资料应与原始文献进行核对,判断其是否满足风险评价所要求的质量水平[29]。
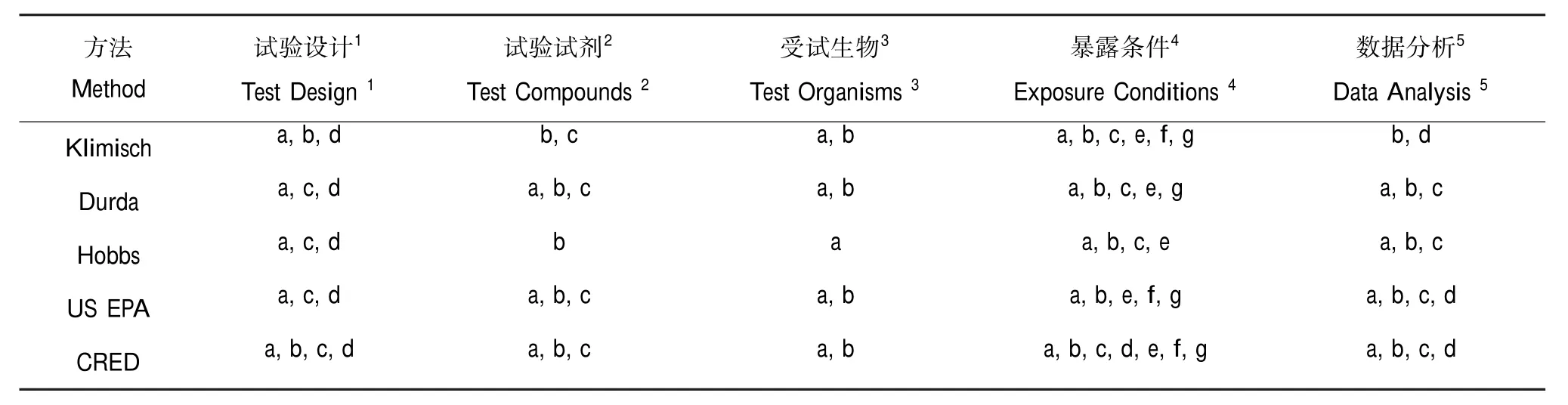
表2 数据筛查与评价方法所涉及的数据质量评价因素∗Table 2 Elements used for evaluating data quality in different methods*
3 生态毒理数据使用规范(Guideline for using ecotoxicity data)
对某一个特定化学品,当有多个测试终点的数据可用时,应根据具体的生态风险评价目标及评价模型筛选出最相关的数据,即评价数据的相关性与适用性;当相关测试终点存在多个可靠数据时,需要对数据进一步整理,得到最精确的数据,用于生态风险评价或水质基准推导。
3.1 数据的相关性
Klimisch提出了3个相关性评价标准:受试生物及试验暴露场景的设计是否与评价区域的污染情况一致,非标准模式生物的毒理数据是否有意义,试验设计是否充分考虑了受试物的物理化学性质。CRED从13个方面对受试生物和暴露场景的相关性评价进行了更详细的阐述。
a.受试生物与评价目标的空间一致性。例如,陆生植物对某一化学品的敏感性与水生态风险评价相关性不大;海水生物毒性数据是否适用于淡水生态系统,取决于所依据的生态风险评价或水质基准推导指南[19]。对于非本地种是否可以用来推导区域水生态基准目前尚存在争议[34],US EPA规定必须以北美地区物种的毒理数据计算水质基准值[21],澳大利亚也建议只用澳大利亚本地或区域水生态毒理数据[24,34]。然而,研究表明,地理分布区域对于构建物种敏感度分布曲线(species sensitivity distribution, SSD)没有显著性影响,而物种的种类则影响其敏感度分布[10,35];Jin等[36]通过整理38种化学物质的HC5(对5%生物产生危害的浓度),比较和验证了本土物种与非本土物种的敏感性差异。结果显示在不使用安全系数的条件下,使用非本土物种的数据推导74%的化合物可以为本土物种提供足够的保护,如果使用10作为安全系数,不确定的化合物的比例可以下降到10%。
b.受试生物与化学品的相关性。不同类型化学品的毒性效应机理存在显著差异,敏感性生物类群也不同[34-35];对于内分泌干扰物类化学品,雄性和雌性生物的毒性效应也存在差异,因此,应根据评价目的与评价方法选择相关生物的毒理数据。当评价化学品对某一个特定物种的潜在风险时,应同时关注敏感生物的毒性效应,例如,研究杀虫剂对某生物的毒性效应时,应同时关注昆虫的毒理数据[19];而对于繁殖/生殖毒性类化合物,鱼类的繁殖损伤毒性数据相比无脊椎水生动物更为敏感[37-38]。对于水质基准推导,US EPA规定在8个科中分别选择1种最敏感生物的毒性数据[21];而构建SSD曲线则需要大量毒理数据,非敏感物种也具有相关性[38]。
c.测试终点与管理目标的相关性。在水质基准和风险评价研究中,应针对不同的环境保护目标,选取恰当的毒性测试终点。例如,对于偶发的环境污染事故,通常采用急性毒理数据;对于长期持续暴露的污染物风险评价,主要采用慢性毒理数据[5]。US EPA规定在推导短期水质基准时,枝角类和蚊类以48 h EC50来表示,其他水生物种以96 h EC50表示,当缺乏EC50时用LC50代替;推导长期水质基准时,优先采用NOEC作为评价终点,当未搜索到NOEC时,用LOEC替代[21]。
d.测试终点与作用模式的相关性。环境中污染物种类繁多,包括有毒有机污染物、重金属、营养元素等,不同类别的污染物其作用位点和作用机制存在很大差异[6]。当对有特殊作用模式的化学品进行风险评价时,以该特殊作用模式或有害结局路径(adverse outcome pathway,AOP)为测试终点的数据相关性最大。例如,内分泌类干扰物(endocrine disrupting chemicals,EDCs)对鱼类繁殖毒性影响最大[37-38],研究其对鱼类雌激素、雄激素、类固醇生合成机制的干扰时,相关测试终点分别为卵黄蛋白原浓度、第二性征、性别比[39]。
e.测试指标与种群水平的相关性。一般认为只有生存、生长、繁殖等传统测试终点具有种群相关性,然而研究表明某些非传统测试指标(如过滤速度和动物行为)也具有种群相关性[19]。因此,推导水质基准时,除了US EPA使用的传统测试终点[21],OECD还考虑了生化测试终点[32],荷兰在采用传统测试终点的同时将生殖器官的病变、产卵量、受精率、孵化率等归纳为“繁殖效应”[40],加拿大将病理学、行为学、生理学的效应作为次等数据用于推导临时基准[23]。
f.效应量级的统计学显著性与生物学的相关性。当试验控制变量相对较小时,微小的变化也具有统计学显著性,但不一定具有生态相关性,此时应由专家判断该现象是否由受试物引起。推导慢性风险值时,优先考虑EC10和NOEC,缺乏EC10和NOEC时可以用EC50替代;欧盟规定推导急性风险值时EC50优于NOEC/EC10,当数据库中的某个急性EC50低于最小的慢性NOEC时,在风险评价过程中应根据该信息调整评价因子(assessment factor,AF)。
g.受试生物的生命阶段。基于测试终点和暴露时间,毒理试验分为全生命周期、部分生命周期以及早期生命阶段3类,受试生物的生命阶段应与研究目的一致。例如,一般认为早期生命阶段的试验与发育效应相关,与传统的繁殖效应不相关[19];US EPA规定,计算慢性毒性值时优先选择全生命周期和部分生命周期的试验数据,缺乏这两类数据时,可以用早期生命阶段试验数据对其进行预测[21,41]。
h.试验条件与受试生物的相关性。试验过程中暴露途径与暴露条件应与受试生物的自然生存条件一致,例如,淡水生物必须在淡水中进行试验,咸水生物在咸水中进行试验。当受试生物(如,摇蚊)通过水相暴露时,作为栖身之地或产卵基质的沉积物,应选择玻璃珠、石英砂、棉布等惰性材料,以避免对水相中的受试物造成干扰。
i.试验周期与测试终点及受试物种的相关性。一般情况下,藻类暴露试验不超过3~4 d,如果试验所用藻种生长较慢,可延长至7 d;大部分测试标准建议鱼类急性试验周期为96 h,但5 d或10 d的暴露数据依然具有相关性[21]。
j.生物恢复性。除了欧盟对植物保护产品的风险评价,大部分水质基准推导和风险评价指南未考虑生物恢复性。
k.试验试剂与目标化学品的相关性。对于配方混合物、盐类或代谢产物类,应考虑试验试剂是否与待评价的化学品相关。对药物类进行风险评价时,其代谢产物也许比药物本身的毒理数据相关性更大;对于不稳定化学品,应考虑试验过程中是否有代谢产物产生,如果引起毒性效应的不是受试物本身而是其代谢产物,其数据相关性应进行专家判断[19]。
l.试验暴露场景与化学品的相关性。生态风险评价应选择试验暴露场景(包括试验周期、暴露浓度、投药量、给药途径、暴露方式等)与污染物实际暴露情况一致的毒理数据。例如,对于农药或兽药类污染物,如果环境预测浓度为瞬时峰值,该污染物的鱼类慢性毒理数据的相关性较小;反之,当污染物持久存在时,鱼类慢性毒理数据的相关性较大[19]。对于没有环境浓度/剂量或施用率报道的化学品,美国ECOTOX数据库拒绝收录相关毒理数据[20]。
m.试验暴露场景与受试生物的相关性。根据生态风险评价框架与评价目的,某些暴露场景不一定适合受试生物。例如,持续时间为几分钟的短期暴露试验适用于以鱼卵为研究对象的繁殖毒性试验,而不一定适用于成年鱼的急性或慢性毒性效应研究。
3.2 数据的精确性
由于目前存在大量生态毒理试验相关的文献报道,毒理数据在经过可靠性和相关性筛选之后,还需要根据不同的情况对数据进一步整理,使用最精确的数据来推导水质基准值或进行生态风险评价。
当一个测试物种有多个测试终点或生命阶段的毒性数据可用时,一般选择最敏感测试终点或最敏感生命阶段的毒性数据[21,25,42];当某一物种在特定测试终点有多个毒性数据时,根据其相对质量的评价或不确定性分析的分布值,可能适用于这些值的几何平均数[11,24,32,42]、加权平均数或算术平均值[43],也可以直接选择最小值[20];如果试验参数(如,水的硬度或pH)的变化导致不同的效应值,可以将这些变量作为函数参数建立毒性效应模型,例如,US EPA关于硬度函数的金属毒性对水生生物作用模型[44];US EPA规定在将急性值与同一物种以及同一属中的其他物种的急性和慢性数据进行比较的过程中出现疑问时(例如,某一物种或属的急性值的差异大于10倍),某些数值或全部相关数值均不得用于计算[21]。
此外,对于试剂纯度、测试指标、受试物种等方面不符合要求的数据或定性数据,如果是由重要物种获得、已测定试验浓度或测试终点在生物学上非常重要,这类数据可以作为辅助信息,用于说明可能发生毒性效应的浓度范围[19,21]。
4 展望(Perspective)
开展污染物生态风险评价以及推导科学合理的水生态基准值依赖于有足够数量且高质量的不同生物类群的生态毒理和理化数据。目前国外对生态毒理数据筛查方法的研究已经相对成熟。数据质量可靠性评价主要以文献中对试验信息的描述为基础,关于试验方法、测试过程和统计分析的描述越详细,数据筛查结果的精确性越高。一套完善的数据筛查与评价方法不仅为生态风险评价与水质基准推导提供技术支撑,还可以用于指导生态毒理试验报告编写,使试验报告信息表述更加完整。然而,建立一套科学、完善的生态毒理数据筛查与评价方法还需要解决以下关键问题:
(1)由于不同生物类群的敏感性差异,物种的种类明显影响物种敏感度分布曲线。敏感物种的生态毒性数据结果决定生态风险评价的结果。建立一个模式生物需要充分的生物学背景资料,以及充分的毒性和毒理测试数据条件,标准化过程通常需要多年的时间。同样,任何一中标准化的测试方法需要从大量备选方法中筛选,并经过质量认证和大量应用性检验,以保证方法能够获得具有代表性的毒性数据。
(2)有毒化学品的种类繁多,不同类别的污染物其作用位点和作用机制存在很大差异。选择污染物特殊作用模式或AOP特殊测试终点为研究对象的数据相关性最大。准确评估污染物的生态风险需要建立在深入研究其毒性作用模式的基础之上。同时,如何利用生化指标,分子生物学指标,行为学以及其他一些非传统的测试终点来实现对整个群落、生态系统水平影响的预测需要我们进一步的研究。
(3)污染物的生态风险评价和化学品水质基准研究需要大量的生态毒理数据,不可避免的会牺牲大量实验生物。未来毒性测试的方法将尽可能少用甚至不用活体动物实验,而代之以构效关系模型预测、高通量体外毒性测试和应用环境组学等预测毒理学手段,如何对这些预测毒理学数据的有效性进行评价同样是我们面临的难题。
(References):
[1] Wheeler J,Grist E,Leung K,et al.Species sensitivity distributions:Data and model choice[J].Marine Pollution Bulletin,2002,45(1):192-202
[2] 金小伟,王业耀,王子健.淡水水生态基准方法学研究:数据筛选与模型计算[J].生态毒理学报,2014,9(1):1-13
Jin X W,Wang Y Y,Wang Z J.Methodologies for deriving aquatic life criteria(ALC):Data screening and model calculating[J].Asian Jounal of Ecotoxicology,2014,9(1): 1-13(in Chinese)
[3] Jin X W,Wang Y Y,Giesy J P.Development of aquatic life criteria in China:Viewpoint on the challenge[J].Environmental Science and Pollution Research International, 2014,21(1):61-66
[4] 张铃松,王业耀,孟凡生,等.水生生物基准推导中物种选择方法研究[J].环境科学,2014,35(10):3959-3969
Zhang L S,Wang Y Y,Meng F S,et al.Species selection methods in deriving water quality criteria for aquaticlife [J].Environmental Science,2014,35(10):3959-3969(in Chinese)
[5] 金小伟,雷炳莉,许宜平,等.水生态基准方法学概述及建立我国水生态基准的探讨[J].生态毒理学报, 2009,4(5):609-616
Jin X W,Lei B L,Xu Y P,et al.Methodologies for deriving water quality criteria to protect aquatic life(ALC) and proposal for development of ALC in China:A review [J].Asian Jounal of Ecotoxicology,2009,4(5):609-616 (in Chinese)
[6] 冯承莲,吴丰昌,赵晓丽,等.水质基准研究与进展[M].中国科学:地球科学,2012,42(5):646-656
[7] 闫振广,余若祯,焦聪颖,等.水质基准方法学中若干关键技术探讨[J].环境科学研究,2012,25(4):397-403
Yan Z G,Yu R Z,Jiao C Y,et al.Research on several critical methodological techniques for development of water quality criteria[J].Reserach of Environmemal Sciences,2012,25(4):397-403(in Chinese)
[8] 王业耀,张铃松,孟凡生,等.水生生物水质基准研究进展及建立我国氨氮水质基准的探讨[J].南水北调与水利科技,2012(5):108-113
Wang Y Y,Zhang S L,Meng F S,et al.Research progress on water quality criteria for aquatic life and establishment of water quality criteria of ammonia nitrogen in China[J].South-to-North Water Transfers and Water Science&Technology,2012(5):108-113(in Chinese)
[9] 金小伟,王子健,王业耀,等.淡水水生态基准方法学研究:繁殖/生殖毒性类化合物水生态基准探讨[J].生态毒理学报,2015,10(1):31-39
Jin X W,Wang Z J,Wang Y Y,et al.Methodologies for deriving aquatic life criteria(ALC):Discussion of ACL for chemicals causing reproductive toxicity[J].Asian Joumal of Ecotoxicology,2015,10(1):31-39(in Chinese)
[10] Jin X W,Zha J M,Xu Y,et al.Derivation of aquatic predicted no-effect concentration(PNEC)for 2,4-dichlorophenol:Comparing native species data with non-native species data[J].Chemosphere,2011,84(10):1506-1511
[11] European Commission.Common implementation strategy for the water framework directive(2000/60/EC).Guidance document No.27.Technical guidance for deriving environmental quality standards[R].Ispra,Italy:European Communities,2011
[12] Klimisch H J,Andreae M,Tillmann U.A systematic approach for evaluating the quality of experimental toxicological and ecotoxicological data[J].Regulatory Toxicology and Pharmacology,1997,25(1):1-5
[13] OECD.OECD Principles of good laboratory practice[R]. Paris,France:OECD,1998
[14] Durda J L,Preziosi D V.Data quality evaluation of toxicological studies used to derive ecotoxicological benchmarks[J].Human and Ecological Risk Assessment,2000, 6(5):747-765
[15] Hobbs D A,Warne M S J,Markich S J.Evaluation of criteria used to assess the quality of aquatic toxicity data[J]. Integrated Environmental Assessment and Management, 2005,1(3):174-180
[16] Caldwell D J,Mastrocco F,Hutchinson T H,et al.Derivation of an aquatic predicted no-effect concentration for the synthetic hormone,17α-ethinyl estradiol[J].Environment Science&Technology,2008,42(19):7046-7054
[17] Ågerstrand M,Breitholtz M,Rudén C.Comparison of four different methods for reliability evaluation of ecotoxicity data:A case study of non-standard test data used in environmental risk assessments of pharmaceutical substances[J].Environmental Sciences Europe,2011,23(1): 1-15
[18] Tweedale T L A,Muilerman H.Missed and dismissed. Pesticide regulators ignore the legal obligation to use independent science for deriving safe exposure levels[R]. Brussels,Belgium:PAN Europe,2014
[19] Moermond C T A,Kase R,Korkaric M,et al.CRED:Criteria for reporting and evaluating ecotoxicity data[J].Environmental Toxicology and Chemistry,2016,35(5):1297 -1309
[20] US EPA.Evaluation guidelines for ecological toxicity data in the open literature[R].Washington DC:US EPA,2011
[21] US EPA.Guidelines for deriving numerical national water quality criteria for the protection of aquatic organisms and their uses.National technical information service accession number PB85-227049[R].Washington DC:US EPA, Springfield VA:NTIS,1985:1-54
[22] US EPA.Guidelines for deriving numerical aquatic sitespecific water quality criteria by modifying National Criteria.EPA-600/3-84-099[R].Washington DC:US EPA, 1984
[23] CCME.A protocol for the derwation of water quality guidelines for the protection of aquatic life.Canadian Environmental Quality Guidelines[R].Ottawa:Canadiin Council of Ministers of the Environment,2007
[24] ANZECC,ARMCANZ.AustralianandNewZealand Guidelines for fresh and marine water quality[R].Canbena:Australian and New Zealand Environmentent and Conservation Council,Agriculture and Resource Management Council of Australian and New Zealand,2000
[25] ECB.Technical Guidance Document on Risk Assessment in Support of Conunission Directive 93/67/EEC on Risk Assessment for New Notified Substances,Commission Regulation(EC)No.1488/94 on Risk Assessment for Existing Substances and Directive 98/8/EC of the European Parliament and of the Council Concerning the Placing of Biocidal Products on the Market.PartⅡ:Environmental Risk Assessment[R].Ispra,Italy:European Chemicals Bureau,European Commission Joint Research Center,European Communities,2003
[26] 国家食品药品监督管理局.药物非临床研究质量管理规范[S].北京:国家食品药品监督管理局,2003
[27] OECD.Test No.201:Freshwater Alga and Cyanobacteria, Growth Inhibition Test[S].Paris,France:OECD,2011
[28] OECD.Test No.202:Daphniasp.Acute Immobilisation Test[S].Paris,France:OECD,2004
[29] 陈艳卿,韩梅,王红梅,等.美国水质基准方法学概论[M].北京:中国环境出版社,2014
[30] OECD.Test No.201:Sediment-water chironomid life-cycle toxicity test using spiked water or spiked sediment[S]. Paris,France:OECD,2010
[31] Mensink B,Smit C,Montforts M.Manual for summarizing and evaluating aspects of plant protection products [R].Bilthoven,The Netherlands,2008
[32] OECD.Guidance Document for Aquatic Effect Assessment[R].Paris,France:OECD,1995
[33] US EPA.Environmental Protection Agency,ECOTOX Database[EB/OL].http://cfpub.epa.gov/ecotox/
[34] Hose G,Van B P.Confirming the species-sensitivity distribution concept for endosulfan using laboratory,mesocosm,and field data[J].Archives of Environmental Contamination and Toxicology,2004,47(4):511-520
[35] Maltby L,Blake N,Brock T,et al.Insecticide species sensitivity distributions:Importance of test species selection and relevance to aquatic ecosystems[J].Environmental Toxicology and Chemistry,2005,24(2):379-388
[36] Jin X W,Wang Z J,Wang Y Y,et al.Do water quality criteria based on nonnative species provide appropriate protection for native species[J].Environmental Toxicolo-gy and Chemistry,2015,34(8):1793-1798
[37] Liu N,Wang Y Y,Yang Q,et al.Probabilistic assessment of risks of diethylhexyl phthalate(DEHP)in surface waters of China on reproduction of fish[J].Environment Pollution,2016,213:482-488
[38] Jin X W,Wang Y Y,Jin W,et al.Ecological risk of nonylphenol in China surface waters based on reproductive fitness[J].Environmental Science&Technology,2014, 48(2):1256-1262
[39] OECD.Information on OECD work related to endocrine disrupters[R].Paris,France:OECD,2012
[40] Slooff W.Ecotoxicological effect assessment:Deriving maximum tolerable concentrations(MTC)from singlespecies toxicity data:RIVM guidance document[R]. Bilthoven,The Netherlands:RIVM,1992
[41] 孟伟,闫振广,刘征涛.美国水质基准技术分析与我国相关基准的构建[J].环境科学研究,2009(7):757-761 Meng W,Yan Z G,Liu Z T.Analysis of guidelines for deriving water quality criteria in the United States and construction of related criteria in China[J].Research of Environmental Science,2009(7):757-761(in Chinese)
[42] RIVM.Guidance document on deriving environmental risk limits in the Netherlands[R].Bilthoven,The Netherlands:National Institute of Public Health and the Environment,2001
[43] Parkhurst D F.Peer reviewed:Arithmetic versus geometric means for environmental concentration data[J].Environmental Science&Technology,1998,32(3):92-98
[44] (美)Glenn W.Suter著.尹大强等译.生态风险评价[M].北京:高等教育出版社,2011:110-112◆
Review of Criteria for Screening and Evaluating Ecotoxicity Data
Liu Na1,Jin Xiaowei2,*,Wang Yeyao1,2,Wang Zijian3
1.School of Water Resources and Environment,China University of Geosciences(Beijing),Beijing 100083,China
2.China National Environmental Monitoring Center,Beijing 100012,China
3.Research Center for Eco-Environmental Sciences,Chinese Academy of Sciences,Beijing 100085,China
3 May 2016 accepted 9 May 2016
A large number of ecotoxicity data for various species taxon were needed in the research of ecological risk assessments(ERAs)and water quality criteria(WQC)for chemicals.Inevitably,there exist certain differences for ecotoxicity data due to abundant studies even for the same endpoint.Incorrect data will directly affect the final evaluation result.So,it is necessary to formulate a set of scientific,reasonable and strong operational criteria for da-ta screening and evaluation,in order to reduce the subjective effect of professionals in the process of data screening and evaluating.Five existing methodologies for data screening and evaluation from different countries and organizations are discussed in present study.Criteria for screening and evaluating ecotoxicity data were described from reliability,relevance and accuracy mainly based on the CRED method as well as the other 4 methods or guidelines for WQC and ERAs.More specifically,there are five evaluation criteria for the quality of ecotoxicity data as follow:(1)test design,including guideline method,experimental process,the validity of the test results and quality controls;(2)the purity of the test substances and other ingredients in formulation;(3)general information and source of test organisms;(4)exposure conditions,including the experimental system appropriate for the test substance,the experimental system appropriate for the test organisms,the reliability of nominal concentration,the spacing between test concentrations,exposure duration,verifing concentration and biomass loading;(5)data analysis, including replicate,statistical method,concentration-response curve and raw data.The correlation between assessment objective and test organisms,test endpoint and exposure scenarios as well as the requirement of data accuracy in ERAs and WQC derivation are mainly considered in guideline for using ecotoxicity data.With the review of these methods,it is hoped to provide reference in the process of data screening and evaluation,and make the results more objective and unitive.
ecotoxicity data;screening and evaluating;reliability;relevance;ecological risk assessment;water quality criteria
2016-05-03 录用日期:2016-05-09
1673-5897(2016)3-001-10
X171.5
A
10.7524/AJE.1673-5897.20160503005
简介:金小伟(1985—),男,博士,中国环境监测总站高级工程师,主要从事生态毒理以及生态风险评价的研究,已发表论文30余篇。
国家自然科学青年基金(21307165);国家水体污染控制与治理科技重大专项(2013ZX07502001);环境模拟与污染控制国家重点联合试验室(中国科学院生态环境研究中心)开放基金(14K02ESPCR)
刘娜(1985-),女,博士研究生,研究方向为生态毒理及风险评价,E-mail:liuna_1231@163.com
*通讯作者(Corresponding author),E-mail:jxw85@126.com
