尼可地尔骨架型缓释片的处方优化及体外释药研究
2016-10-26金桂兰谭建玲邢翔飞三峡大学人民医院宜昌市第一人民医院药学部湖北宜昌443000湖北中医药大学药学院武汉430064
金桂兰,罗 平,杜 娟,林 宁,谭建玲,邢翔飞#(.三峡大学人民医院/宜昌市第一人民医院药学部,湖北宜昌 443000;.湖北中医药大学药学院,武汉 430064)
尼可地尔骨架型缓释片的处方优化及体外释药研究
金桂兰1*,罗 平2,杜 娟2,林 宁2,谭建玲1,邢翔飞1#(1.三峡大学人民医院/宜昌市第一人民医院药学部,湖北宜昌 443000;2.湖北中医药大学药学院,武汉 430064)
目的:优化尼可地尔骨架型缓释片的处方,评价其体外释药特性。方法:采用粉末直接压片法,在单因素考察的基础上,以1、4、8、12 h尼可地尔的累积释放度(Q)为评价指标,用星点设计-响应面法优化制剂辅料中羟丙甲基纤维素(HPMC)、乙基纤维素(EC)的用量;比较所制缓释片在不同pH(1.0、5.0、6.8、7.4)介质中12 h内的Q值。结果:最优处方(每片量)为尼可地尔10 mg、HPMC 150 mg、EC 90 mg、微晶纤维素80 mg、乳糖60 mg、硬脂酸镁2%;所制缓释片的Q1 h、Q4 h、Q8 h、Q12 h分别为23.6%、51.3%、83.7%、96.9%,与预测值的偏差分别为2.1%、1.6%、1.0%、0.2%;缓释片在pH 1.0~7.4的介质中各时间点的Q值相近。结论:优化处方所制的尼可地尔骨架型缓释片具有缓释作用,pH在1.0~7.4范围内变化对其主药的释放无干扰。
尼可地尔;骨架型缓释片;处方优化;星点设计-响应面法;体外释药
尼可地尔(Nicorandil,又名烟浪丁),化学名N-[2-(硝基氧基)乙基]-3-吡啶羧酰胺,属硝酸酯类化合物,具有硝酸酯类和钾离子通道开放的双重作用[1-2],在临床上适用于高血压、冠心病及各类心绞痛的治疗,为较理想的抗心绞痛药。目前,尼可地尔上市制剂有片剂、注射剂等。实际应用中,该药物的水溶性较差,存在口服生物利用度低等问题。
近年来,结合缓控释制剂的优点,并根据心脑血管疾病的发病规律,研究可以长时间平稳起效的缓控释制剂已成为心脑血管药物研究的趋势之一。本研究以羟丙甲基纤维素(HPMC)和乙基纤维素(EC)为缓释材料,应用星点设计-响应面法[3]优化处方,并对其体外释药进行初步探讨,旨在研究制备一种服用方便且血药浓度持续稳定的尼可地尔缓释片。
1 材料
1.1 仪器
UV-2550紫外-可见分光光度计(日本岛津公司);BP211D十万分之一电子天平(德国Satorius公司);TDP单冲压片机(上海天祥健台制药机械有限公司);ZRS-8G溶出仪(天津市天大天发科技有限公司)。
1.2 药品与试剂
尼可地尔对照品和原料药(西安立邦制药厂提供,批号:20130307、120917,纯度:>99%);尼可地尔片(河南天方药业有限公司,批号:130709107,规格:5 mg/片);EC(黏度:0.01 Pa·s)、HPMC K4M和微晶纤维素(MCC)均购自安徽山河药用辅料股份有限公司;乳糖(天津市博迪化工有限公司);硬脂酸镁(天津市标准科技有限公司,化学纯);水为二次蒸馏水。
2 方法与结果
2.1 释放度的测定
2.1.1 含量测定方法的建立 精密称定尼可地尔对照品适量,用pH 6.8磷酸盐缓冲液(PBS)溶解定容至100 ml,备用。精密量取上述溶液,制备成质量浓度分别为1.01、3.03、6.06、9.09、12.12 μg/ml的对照品溶液,在262 nm波长处测定吸光度。以质量浓度(c)为横坐标、吸光度(A)为纵坐标,进行线性回归分析,得回归方程为A=0.017 6c-0.003 9(r2=0.999 7),尼可地尔检测质量浓度的线性范围为1.01~12.12 μg/ml。按相关方法考察,50%、100%、150%的加样回收率分别为101.98%、99.99%、98.53%,RSD分别为1.12%、0.39%、0.27%(n=3);精密度试验RSD为0.41%(n=6)。
2.1.2 篮法测定累积释放度 按2015年版《中国药典》(四部)释放度测定法中通则0931第一法(篮法)操作,以900 ml经脱气处理的pH 6.8的PBS为释放介质,转速50 r/min,温度(37± 0.5)℃ 。分别于0、0.5、1、2、3、4、6、8、10、12 h取样5 ml,并及时补加等体积同温新鲜介质。样品液用0.45µm微孔滤膜过滤,测定吸光度,并根据回归方程计算累积释放度(Q)。
2.2 星点设计-响应面法优化制剂处方
2.2.1 试验设计与结果 经过单因素试验的初步考察表明,HPMC和EC的用量是影响药物释放的主要因素。本研究设定每片制剂中HPMC(X1)的用量范围为100~160 mg、EC(X2)的用量范围为60~120 mg,响应值为Q1 h、Q4 h、Q8 h、Q12 h,以星点设计-响应面法进行2因素5水平的处方优化试验[4-5]。因素与水平见表1,星点设计与结果见表2。

表1 因素与水平Tab 1 Factors and levels
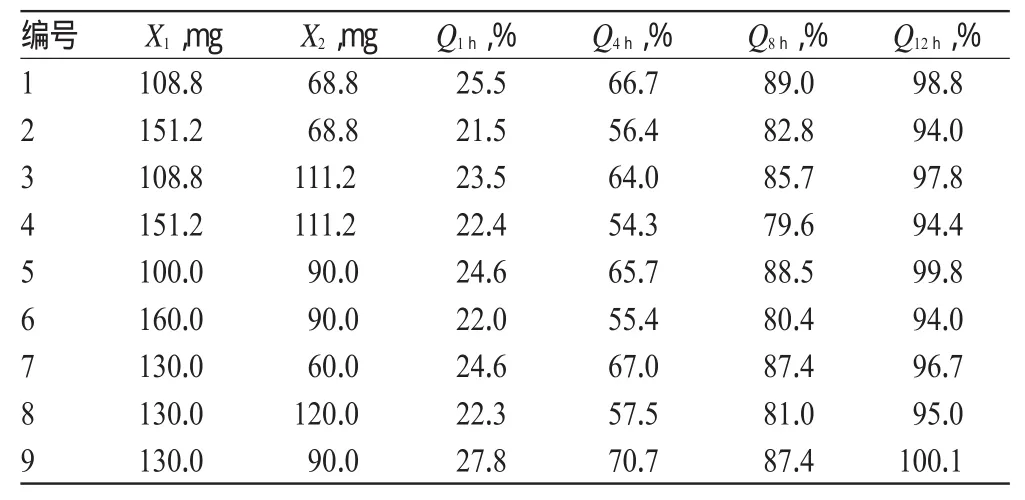
表2 星点设计与试验结果Tab 2 Central composite design and test results
2.2.2 模型拟合 以X1和X2为自变量,Q1 h、Q4 h、Q8 h、Q12 h为因变量,使用Design Expert软件处理数据,进行模型拟合,以模型拟合相关系数(r2)和置信度(P)判断最佳模型[6-7]。分别采用多元线性模型和二次多项式模型对不同时间点各自变量和因变量进行回归分析,二次多项式模型拟合相关系数明显高于多元线性模型,且置信度也优于多元线性模型。因此,本研究选择二次多项式模型拟合方程优化制剂处方,其方程为Q1 h= -70.052+1.125X1+0.650X2+0.001 6X1X2-0.005 1X-0.004 9X(r2=0.973 4,P=0.010 0);Q4 h=-170.48+2.85X1+1.64X2+0.000 33X1X2-0.011 2X-0.010X(r2=0.948 4,P=0.056 0);Q8 h=29.605+0.714X1+0.546X2+0.000 056X1X2-0.003 3X-0.003 6X(r2=0.991 8,P=0.029 5);Q12 h=23.283+0.776X1+0.744X2+0.000 78X1X2-0.003 6X-0.004 8X(r2=0.991 2,P= 0.005 4)。根据上述选用的二次多项式模型,分别绘制X1和X2对Q的响应面图和等高线图,见图1和图2。
2.2.3 处方优化与验证 设定响应值Q1 h为10%~30%、Q4 h为40%~60%、Q8 h为70%~90%、Q12 h>90%,将各个响应面优化区域进行重叠[8],得到X1较优用量范围为150~157 mg,X2较优用量范围为85~98 mg。综合考虑,最终确定尼可地尔骨架型缓释片的处方(每片量)为尼可地尔原料药10 mg、HPMC 150 mg、EC 90 mg、MCC 80 mg、乳糖60 mg、硬脂酸镁2%。对其进行验证试验,结果见表3。

图1 X1和X2对Q值影响的三维响应面图Fig 1 Three-dimensional response surface map of the effects of X1and X2on Q values

图2 X1和X2对Q值影响的等高线图Fig 2 Contour map of the effects of X1and X2on Q values

表3 验证试验结果Tab 3 Results of verification test
由表3可知,Q1 h、Q4 h、Q8 h、Q12 h的实测值与预测值的偏差均小于3%,表明优化结果良好,试验设计和模型的拟合均有较高的可信度和预测性。最终确定,每片尼可地尔骨架型缓释片中HPMC用量为150 mg、EC用量为90 mg。
2.3 尼可地尔骨架型缓释片的制备[9]
按“2.2.3”项下优化后处方量称取主药与辅料分别过120目筛,将尼可地尔与其他辅料等量递加法逐步混匀,再加入润滑剂混匀,采用直接压片法,于单冲压片机上压制成直径为12mm、片质量约为400 mg的尼可地尔骨架型缓释片,每片含尼可地尔10 mg。
2.4 体外释药特性评价
2.4.1 体外释药特性 按最优处方制备尼可地尔骨架型缓释片6片(批号:201456),测定其Q12 h,并与尼可地尔普通片进行比较。结果表明,与尼可地尔普通片比较,尼可地尔骨架型缓释片具有良好的缓释特性。2种制剂的累积释放曲线见图3。

图3 2种制剂的累积释放曲线(n=6)Fig 3 Cumulative release curves of 2preparations(n=6)
2.4.2 pH对Q值的影响 取同一批号尼可地尔骨架型缓释片(批号:201458),分别以0.1 mol/L的盐酸溶液(pH 1.0)和pH 5.0、6.8、7.4的PBS为释放介质,按“2.1.2”项下方法测定Q12 h,绘制累积释放曲线和Q-pH-时间(t)的三维图,具体见图4和图5。

图4 尼可地尔骨架型缓释片在不同pH介质中的累积释放曲线Fig 4 Cumulative release curves of Nicorandil sustained-release matrix tablet in different pH media
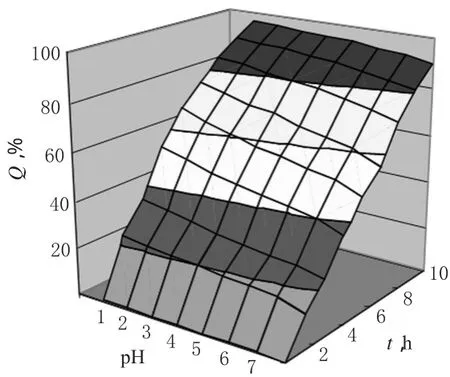
图5 尼可地尔骨架型缓释片Q-pH-t的三维图Fig 5 Three-dimensional map of Q-pH-t of Nicorandil sustained-release matrix tablet
由图4和图5可知,尼可地尔骨架型缓释片在pH 1.0~7.4的释放介质中各时间点的Q值相近,介质pH在1.0~7.4范围内变化对其主药的释放无干扰。
3 讨论
尼可地尔骨架型缓释片为混合型骨架片,系由亲水性高分子材料和不溶性骨架材料以及其他辅料混合制成。在制备工艺上,该制剂采用粉末直接压片法,制备工艺简单、便于工业化生产;在制剂处方上,笔者基于前期对HPMC黏度和用量,EC、MCC、乳糖用量进行单因素考察的基础上,采用星点设计-响应面法对制剂处方组成进行了筛选优化。
缓释、控释制剂长时间在体内释药,经过pH约为1.0的胃液到pH约7.4的小肠远端。为能反映制剂体内吸收特征,一般应对缓控释制剂的pH依赖性进行研究。药物释放介质的pH可能会影响某些控制药物释放关键辅料的特性[10-11],对缓释片的释放有一定影响。本试验通过对尼可地尔骨架型缓释片“Q-pH-t”释放特性的研究,发现缓释片在pH 1.0~7.4的释放介质中均能较好地释放,说明pH的变化对其主药的释放无干扰,符合剂型设计要求,同时也表明尼可地尔可制备成缓释制剂。
星点设计-响应面法是通过试验拟合因变量对自变量的响应面,从响应面上选择最优响应域的方法,其试验设计可靠性较高、偏差较小。笔者对星点设计-响应面法优化得到的处方进行验证,制备的尼可地尔骨架型缓释片体外释药平稳持久,达到缓释制剂的要求,为尼可地尔新剂型的开发提供了参考依据并奠定了基础。另外,其体内释药研究及体内外相关性研究仍在进行中,将另文报道。
[1]朱文玲.具有独特双重作用机制的抗心绞痛新药:尼可地尔[J].临床药物治疗杂志,2012,10(6):1.
[2]司延斌,赵志刚.KATP通道开放剂的药理作用及临床应用研究进展[J].中国药房,2007,18(34):2 704.
[3]刘艳杰,项荣武.星点设计效应面法在药学试验设计中的应用[J].中国现代应用药学杂志,2007,24(6):455.
[4]黄健,高春生,单利,等.星点设计-效应面法在酒石酸美托洛尔缓释微丸处方优化中的应用[J].中国药学杂志,2007,42(7):512.
[5]郝贵周,赵利枝,韩忠丽,等.星点设计-效应面法优化阿昔莫司控释片处方研究[J].齐鲁药事,2012,31(5):258.
[6]周绚,傅超美,黄逸维,等.星点设计-效应面法优化三七总皂苷生物黏附型缓释片处方[J].华西药学杂志,2010,25(4):406.
[7]肖婷婷,郭倩,田成旺,等.星点设计-效应面法优化五参分散片的处方研究[J].现代药物与临床,2013,28(6):861.
[8]陆兵,徐国杰,张汝华.纳曲酮植入剂体外处方优化[J].中国药学杂志,2000,35(7):452.
[9]崔福德.药剂学[M].6版.北京:人民卫生出版社,2008:134-135.
[10]张建国,郭银玉,陈文宜,等.不同厂家的茶碱缓释片三维释放特性及释放机制考察[J].中国药业,2010,19(3):7.
[11]徐翔,田国祥,许东航,等.不同pH的溶出介质对HPMC骨架片释药的影响[J].中国现代应用药学,2004,21(2):108.
(编辑:邹丽娟)
Study on Formulation Optimization of Nicorandil Sustained-release Matrix Tablet and Drug Release in vitro
JIN Guilan1,LUO Ping2,DU Juan2,LIN Ning2,TAN Jianling1,XING Xiangfei1(1.Dept.of Pharmacy,Three Gorges University People’s Hospital/the First People’s Hospital of Yichang,Hubei Yichang 443000,China;2.College of Pharmacy,Hubei University of Chinese Medicine,Wuhan 430064,China)
OBJECTIVE:To optimize the formulation optimization of Nicorandil sustained-release matrix tablet,and evaluate its drug release properties in vitro.METHODS:Based on single factor test,powder direct compression method was used,using nicorandil cumulative release rate(Q)in 1,4,8,12 h as evaluation indexes,central composite design-response surface method was adopted to optimize the amount of hydroxypropyl methylcellulose(HPMC)and ethyl cellulose(EC);Q values within 12 h in different pH(1.0,5.0,6.8,7.4)media were compared.RESULTS:The optimized formulation(every tablet)was nicorandil 10 mg,HPMC 150 mg,EC 90 mg,microcrystalline cellulose 80 mg,lactose 60 mg,magnesium stearate 2%.Q1 h,Q4 h,Q8 hand Q12 hof the obtained formulation were 23.6%,51.3%,83.7%and 96.9%,respectively;deviation from the predicted values were 2.1%,1.6%,1.0%,0.2%.Q values were similar in pH 1.0-7.4 at different time points.CONCLUSIONS:The obtained Nicorandil sustained-release matrix tablet by optimal formulation shows sustained-release effect,and the change of pH 1.0-7.4 has no interference in the release characteristics of main drug.
Nicorandil;Sustained-release matrix tablet;Formulation optimization;Central composite design-response surface method;Drug release in vitro
·综述讲座·
R943
A
1001-0408(2016)25-3564-03
10.6039/j.issn.1001-0408.2016.25.33
2015-11-27
2016-02-01)
*主任药师,硕士。研究方向:医院药学、药事管理。电话:0717-6228045。E-mail:jin_gl@163.com
主任药师,硕士。研究方向:药物制剂、临床药学。电话:0717-6227798。E-mail:xingxfemail@163.com
