盐酸苯海索-Ce(IV)荧光法检测虾中亚硫酸盐含量
2016-10-21张静马占玲汪莹李宁宁陈思励建荣
张静,马占玲,汪莹,李宁宁,陈思,励建荣
(渤海大学 化学化工与食品安全学院,辽宁省食品安全重点实验室,辽宁 锦州,121013)
盐酸苯海索-Ce(IV)荧光法检测虾中亚硫酸盐含量
张静,马占玲*,汪莹,李宁宁,陈思,励建荣
(渤海大学 化学化工与食品安全学院,辽宁省食品安全重点实验室,辽宁 锦州,121013)
基于盐酸苯海索-Ce(IV)-亚硫酸盐在弱酸或中性条件下反应生成强烈的荧光物质,建立了检测食品中亚硫酸盐含量的新方法。确定了测定亚硫酸盐的最佳条件。在最佳条件下,亚硫酸盐含量在0.02~1mg/mL呈现良好的线性,线性方程为:y=8 031.7x-203.31,相关系数为0.996 8,方法的检出限为0.001μg/mL,远低于国家标准方法——盐酸副玫瑰苯胺法。方法的相对标准偏差为6.08%,回收率在82.4%~92.8%之间。该方法操作简单、灵敏度高、污染小;用于测定虾中亚硫酸盐含量,与国标法无显著性差异。
盐酸苯海索;Ce(IV);亚硫酸盐;荧光法;虾
亚硫酸盐是一种常用的食品添加剂,具有漂白、防腐、抗氧化、防止褐变等作用[1-2]。虾类制品(海捕鲜虾,冻虾仁,速冻小虾,冻对虾,烤虾等)是亚硫酸盐的一大应用领域。此类制品中,亚硫酸盐能有效防止虾体在冷冻(藏)贮存和加工过程中的褐变,防腐保鲜,保护制品的品质和色泽,延长制品的保质期[1]。但是,亚硫酸盐具有一定的毒性,WHO规定每人每日摄入亚硫酸盐的量应低于0.7mg[3]。摄入过量亚硫酸盐将会导致呼吸困难、荨麻疹、哮喘、胃肠不适等问题,尤其是对哮喘患者尤为严重[4-5],过量的亚硫酸盐还会对人体的神经系统、生殖系统、循环系统、免疫系统等带来一定的危害[6-8]。基于对亚硫酸盐毒性的认识,各国均对食品中SO2残留量做出了严格的限定,国际食品法典委员会(CAC)明确规定了冷冻虾中SO2残留量,在生品可食性部分≤100mg/kg,熟食可食性部分≤30mg/kg[9]。目前我国检测食品中亚硫酸含量的方法主要有国标法中采用的盐酸副玫瑰苯胺比色法和蒸馏滴定法[10],其他方法如色谱法[11]、化学发光法[12]、电化学法[13]、传感器法[14]等,但均有各自的不足。如盐酸副玫瑰苯胺比色法使用大量剧毒试剂四氯汞钠,对环境和人体造成损害,同时食品中含量较高的离子如Cl-对方法的干扰较大,蒸馏滴定法操作复杂,不适合大批量样品的检测。
基于盐酸苯海索能显著增强Ce(IV)与亚硫酸盐之间化学发光反应[15],本文建立了一种检测水产品中亚硫酸盐含量的新的荧光法,与盐酸副玫瑰苯胺比色法相比,该方法污染性小,干扰低,检测限低,与蒸馏滴定法相比,操作简单、检测速度快、适合大批量样品检测。
1 实验部分
1.1仪器与试剂
KQ-250DB型数控超声波清洗器,昆山市超声仪器有限公司;PL303电子天平,梅特勒-托利多仪器(上海)有限公司;970CRT荧光分光光度计,上海仪电分析仪器有限公司;电热恒温水槽,上海精宏实验设备有限公司;RRHP-100型万能高速粉碎机,欧凯莱芙实业公司;UV-1801紫外可见分光光度计,北京瑞利分析仪器有限公司。
硫酸铈、盐酸苯海索、NaOH、Na2SO3均为分析纯,购自国药集团。
1.2样品处理与检测
1.2.1样品处理
样品经粉碎机粉碎均匀后,准确称取2.5g样品粉末,置于50mL容量瓶中,加入2.5mLNaOH溶液,再加入适量蒸馏水,超声1.5h后定容,取滤液备用。
1.2.2样品检测
向比色管中加入2mLCe(SO4)2(0.01mol/L),2mL盐酸苯海索(0.020mg/mL)、1mL样液,去离子水定容到20mL。摇匀,35℃条件下反应15min,在激发波长为265nm,发射波长为350nm,狭缝为10nm条件下进行荧光测定。
2 结果与讨论
2.1单因素实验条件的选择
2.1.1最大发射波长的确定
在最佳条件下,盐酸苯海索-亚硫酸根-硫酸铈进行反应,在200~800nm内进行发射光谱扫描,结果见图1,从而确定该反应体系的荧光发射波长为350nm。

图1 EM扫描荧光光谱 Fig.1 Chart of EM scanning fluorescence spectra
2.1.2盐酸苯海索用量的影响
当其他条件一定时,考察了20mg/L盐酸苯海索的用量对实验结果的影响,结果见图2。由图2可见,荧光强度随着盐酸苯海索用量的增加先变小后变大,盐酸苯海索用量为2.0mL时,荧光强度较大且比较稳定。本实验选择盐酸苯海索用量为2.0mL。

图2 盐酸苯海索用量对反应体系的影响Fig.2 Effect of trihexyphenidyl hydrochloride dosage on chemical reaction system
2.1.3硫酸铈用量的影响
探讨了0.01mol/L硫酸铈的用量对实验结果的影响,结果如图3所示。当其他条件一定时,随着硫酸铈用量的增加,荧光强度不断变大。可见在该反应体系中,荧光强度与硫酸铈和亚硫酸盐均有关,但在硫酸铈用量一定的条件下反应体系的荧光强度与亚硫酸盐成正比,考虑到实验条件,本实验确定Ce(SO4)2用量为2.0mL。

图3 Ce(SO4)2用量对反应体系的影响Fig.3 Effect of Ce(SO4)2 dosage on chemical reaction system
2.1.4反应温度的影响
当其他条件一定时,考察了温度对实验结果的影响,结果如图4所示。由图可见,荧光强度随着温度的升高先变小后变大,当反应温度为35 ℃时,荧光强度达到最大值。本文确定反应最佳温度为35 ℃。

图4 反应温度对反应体系的影响Fig.4 Effect of reaction temperature on chemical reaction system
2.1.5反应时间的影响
考察了时间对实验结果的影响,结果如图5所示。当其他条件一定时,反应时间对实验结果的影响不大。综合考虑,本文选择反应时间为15min。

图5 反应时间对反应体系的影响Fig.5 Effect of reaction time on chemical reaction system
2.2反应条件的正交实验
在单因素的基础上,对盐酸苯海索用量、Ce(SO4)2用量、反应温度、反应时间进行4因素4水平正交实验L16(45)。表1为正交实验因素水平表。表2和表3为正交实验结果表。
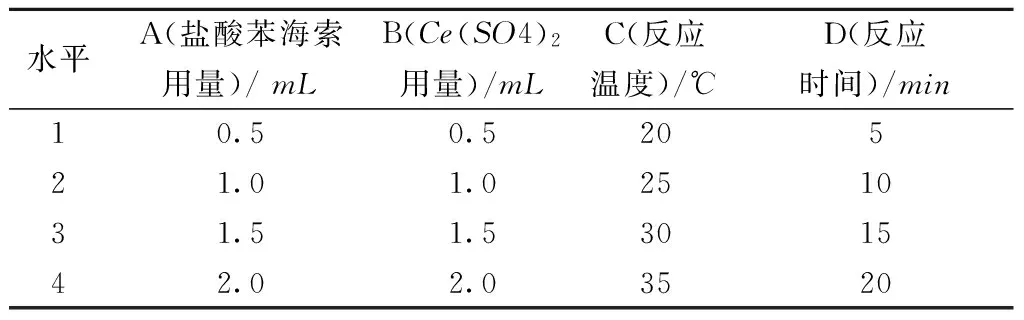
表1 正交实验因素水平表L16(45)

表2 正交实验结果及计算表L16(45)
通过极差分析可知,各因素对荧光强度(I)的影响顺序为:Ce(SO4)2用量B>反应温度C>盐酸苯海索用量A>反应时间D。荧光法检测食品中亚硫酸盐含量的最佳条件为:A4B4C4D3,即盐酸苯海索用量为2.0mL,Ce(SO4)2用量为2.0mL,反应温度为35 ℃,反应时间为15min。
方差分析结果表明,Ce(SO4)2(B)达到极显著水平,对荧光强度影响较大。其他因素对盐酸苯海索用量、反应温度、反应时间均未达到显著水平,对实验结果影响不大。
2.3共存离子的影响
在亚硫酸盐浓度为0.8g/L,相对偏差小于±5.0%时,干扰离子所允许的共存倍数为Na+(200倍)、Cl-(200倍) 、K+(200倍)、NO22-(100倍)、Zn2+(100倍)、蛋白质(100倍)、Vc(5倍)、PO43-(100倍),由此可见,该体系对亚硫酸盐的选择性较好。

表3 方差分析表
2.4方法评价
2.4.1工作曲线
取系列亚硫酸盐标准溶液,在最佳条件下反应15min后,在激发波长为265nm,发射波长为350nm下测定荧光强度,绘制工作曲线。实验结果表明,亚硫酸盐含量在0.02~1mg/mL荧光强度与浓度成正比,其线性回归方程为y=8031.7x-203.31,相关系数R为0.996 8,呈很好的线性关系。
2.4.2方法的检出限
使用空白溶液连续测量15次,利用公式(1)计算出本方法的最低检出限:
DL=3σ/k
(1)
式中:σ,标准偏差;k,工作曲线斜率。
经15次测量空白溶液,其标准偏差为3.48,工作曲线的斜率为8 031.7,计算方法检出限为0.001μg/mL,低于国标法盐酸副玫瑰苯胺的检测限0.1μg/mL(即1mg/kg,按10g样品定容100mL计)。可见该方法的检出限低,灵敏度高,能较好地适应虾中亚硫酸盐的检测。
2.4.3方法的精密度和回收率
取冻虾用粉碎机搅碎,准确称取5.00g,移入容量瓶中,加入2.5mLNaOH溶液,再加入少量水将样品浸没,超声90min之后,测定其中亚硝酸盐含量,平行测定5次,计算其相对标准偏差。然后分别加入不同量的亚硫酸盐,测定回收率。结果如表4所示,由实验结果可见,相对标准偏差为6.08%,平均回收率在82.4%~92.8%之间。精密度和准确度均能达到实验要求。

表4 方法精密度和回收率
2.4.4与国标法差异性检验
分别用本法与国标法检测冻虾中亚硫酸盐的含量,平行测定5次,结果如表5所示。
用F检验法和t检验法对国标法和荧光法测得的冻虾中亚硫酸盐含量的平均值显著性差异进行检验。通过计算F为1.05,小于F0.95,4(6.39),说明二者的方差不存在显著性差异(P<0.05);t值为1.27,小于t0.95,8(2.31),说明2种方法测得的平均值,即2种方法无显著性差异(P<0.05)。

表5 荧光法与国标法显著性差异比较
2.5样品检测
在市场买取5份不同的冻虾进行测量,测得结果见表6。结果表明5种冻虾中亚硫酸盐的含量在82.33~121.35mg/kg。其中有一种样品中亚硫酸盐含量超过中华人民共和国水产行业标准SC/T3113—2002规定的冷冻虾中SO2残留量≤100mg/kg的限量,其他4种样品合格。

表6 样品测定
3 结论
建立了盐酸苯海索荧光光度法检测食品中亚硫酸盐含量的新方法。与国标法中的盐酸副玫瑰苯胺比色法相比较,该方法未使用剧毒试剂,环境污染小,海产品中含量较大的离子如Cl-对方法的干扰较小,检测更快速;检出限低,适合大批量样品的检测。该方法用于冻虾中亚硫酸盐含量的检测,效果较好。
[1]张双灵, 赵奎浩, 周德庆,等. 水产品中亚硫酸盐的安全性及残留状况检测[J]. 现代食品科技, 2007, 23(3):60-62.
[2]AMATATONGCHAIM,SROYSEEW,CHAIRAMS,etal.Simpleflowinjectionfordeterminationofsulfitebyamperometricdetectionusingglassycarbonelectrodemodifiedwithcarbonnanotubes-PDDA-goldnanoparticles.[J].Talanta, 2015, 133:134-141.
[3]KOCHM,KOPPENR,SIEGELD.Determinationoftotalsulfiteinwinebyionchromatographyafterin-sampleoxidation[J].JournalofAgricultural&FoodChemistry, 2010, 58(17):9 463-9 467.
[4]RANGUELOVAK,RICEAB,LARDINOISOM,etal.Sulfite-mediatedoxidationofmyeloperoxidasetoafreeradical:immuno-spintrappingdetectioninhumanneutrophils[J].FreeRadicBiolMed, 2013, 60(10):98-106.
[5]WUMY,HET,LIK,etal.Areal-timecolorimetricandratiometricfluorescentprobeforsulfite[J].Analyst, 2013, 138(10):3 018-3 025.
[6]SANGN,YUNY,LIH,etal.SO2inhalationcontributestothedevelopmentandprogressionofischemicstrokeinthebrain[J].ToxicologicalSciences, 2010, 114(2):226-236(11).
[7]刘东奇, 陈华成, 杨雪丽. 二氧化硫对机体各组织器官毒性作用的研究进展[J]. 畜牧兽医杂志, 2008, 27(1):37-39.
[8]李雪莲, 杨丽, 陈鸿平,等. 食品中亚硫酸盐研究进展[J]. 亚太传统医药, 2015, 11(3):34-37.
[9]高平, 黄国方, 胡琼予,等. 浅议虾类产品标准中亚硫酸盐限量问题[J]. 当代水产, 2009(11):31-32.
[10]GB/T5009.34-2003.食品中亚硫酸盐的测定[S].
[11]ABERLA,COELHANM.Determinationofsulfurdioxideinwineusingheadspacegaschromatographyandelectroncapturedetection.[J].FoodAdditContamPartAChemAnalControlExpoRiskAssess, 2013, 30(2):226-233.
[12]NAVARRROMV,MARARAMOSPAYN,MIGUELANGELBELLOLPEZ,etal.Rapidflowinjectionmethodforthedeterminationofsulfiteinwineusingthepermanganate-luminolluminescencesystem.[J].Talanta, 2010, 82(5):2 003-2 006.
[13]FULM,JUWJ,LIUCC,etal.IntegratedmicrofluidicarraychipandLEDphotometersystemforsulfurdioxideandmethanolconcentrationdetection[J].ChemicalEngineeringJournal, 2014, 243(5):421-427.
[14]SARTORIER,VICENTINIFC,FATIBELLO-FILHOO.Indirectdeterminationofsulfiteusingapolyphenoloxidasebiosensorbasedonaglassycarbonelectrodemodifiedwithmulti-walledcarbonnanotubesandgoldnanoparticleswithinapoly(allylaminehydrochloride)film[J].Talanta, 2011, 87(2):235-242.
[15]张泾凯,李建国,屠一锋. 铈(Ⅳ)-亚硫酸盐体系流动注射化学发光法测定苯海索新方法研究[J]. 苏州大学学报:自然科学版, 2009, 25(3):68-71.
Fluorescencedeterminationofsulfiteinshrimpwithtrihexyphenidylhydrochloride-Ce(IV)systym
ZHANGJing,MAZhan-ling*,WANGYing,LINingning,CHENSi,LIJian-rong*
(CollegeofChemistry,ChemicalEngineeringandFoodSafety,BohaiUniversity,FoodSafetyKeyLabofLiaoningProvince,Jinzhou121013,China)
Strongfluorescentsubstancesweregeneratedbasedontrihexyphenidylhydrochloride-Ce(IV) -sulfiteundertheconditionsofweakacidorneutral.Anewdeterminationmethodofsulfitesinshrimpwasestablished.Thefluorescenceintensityandtheconcentrationofsulfite(SO2)showedgoodlinearityintherangeof0.02~1mg/mL,theregressionequationisy=8 031.7x~203.31.Thecorrelationcoefficientis0.999 6.Themethoddetectionlimitis0.001μg/mL.Itisfarlowerthanthatofthenationalstandard.Therelativedeviationofthesampleis6.08%andtherecoveryrateisbetween96%and107%.Themethodissimple,sensitive,andenvironmentallyfriendlyandtheresultwassatisfying.Theresultcomparingwiththestandardmethodisbasicallythesame.
trihexyphenidylhydrochloride;Ce(IV);sulfite;fluorescencespectrometry;shrimp
10.13995/j.cnki.11-1802/ts.201608032
硕士研究生(马占玲教授,励建荣教授为通讯作者,E-mail分别为:13898355801@sina.com和lijr6491@163.com)。
“十二五”国家支撑计划项目课题“水产品加工过程质量安全控制关键技术集成与示范”(No. 2012BAD29B06)
2015-12-30,改回日期:2016-02-22
